Lệch hoặc trật IOL
Chẩn đoán và chỉ định phẫu thuật cho IOL rơi do đứt dây chằng Zinn. Lựa chọn cố định trong củng mạc (phương pháp flange hoặc kẹp).

Thấu kính nội nhãn (IOL) là một thấu kính nhân tạo được cấy vĩnh viễn vào bên trong mắt sau khi loại bỏ thủy tinh thể tự nhiên bị đục trong quá trình phẫu thuật đục thủy tinh thể. Mắt có IOL được gọi là mắt giả thủy tinh thể (pseudophakia). Khác với điều chỉnh bằng kính đeo mắt hoặc kính áp tròng, IOL được tích hợp trực tiếp vào hệ thống quang học của mắt, không gây phóng đại hay thu nhỏ hình ảnh, mang lại chức năng thị giác tự nhiên và sinh lý nhất.
Loại IOL phổ biến nhất hiện nay là IOL có thể gấp lại (foldable IOL), bao gồm phần quang học (optic) và phần đỡ (haptic). Đường kính quang học tiêu chuẩn là 6,0 mm, có thể được đưa vào qua một vết mổ nhỏ (2,4–2,8 mm) bằng dụng cụ tiêm trong quá trình tán nhuyễn thủy tinh thể bằng siêu âm (PEA). Trong một số trường hợp khó, IOL có đường kính quang học lớn 7,0 mm được sử dụng để cải thiện khả năng quan sát khi khám đáy mắt và cải thiện độ ổn định cố định trung tâm khi cố định ngoài bao.
Phân loại theo vật liệu như sau:
| Vật liệu | Đặc điểm | Chỉ định chính |
|---|---|---|
| Acrylic kỵ nước | Ít đục thủy tinh thể thứ phát. Cần chú ý hiện tượng lấp lánh (glistenings) | Lựa chọn tiêu chuẩn hiện tại |
| Acrylic ưa nước | Tương thích sinh học cao. Nguy cơ lắng đọng canxi (đục IOL) khi sử dụng lâu dài | IOL thiết kế đặc biệt |
| Silicone | Khả năng gập tốt. Không phù hợp với mắt đã được chèn dầu silicone nội nhãn | Một số PIOL |
| PMMA | Vật liệu cứng. Cần mở rộng vết mổ lên 5-7 mm | IOL cố định đặc biệt và cấy ghép thứ phát |
Về cấu trúc, có loại thấu kính một mảnh (1-piece) trong đó phần quang học và phần đỡ được làm từ cùng một chất liệu, và loại ba mảnh (3-piece) từ các chất liệu khác nhau. Thấu kính một mảnh thường được dùng để cố định trong bao (bag-in-the-lens), trong khi thấu kính ba mảnh phù hợp cho cố định ngoài bao, cố định củng mạc và khâu. Cần thận trọng nếu vô tình cố định thấu kính một mảnh ngoài bao (rãnh thể mi), vì phần đỡ có thể cọ xát vào mống mắt, gây phân tán sắc tố mống mắt và viêm kéo dài.
Ở IOL cầu (spherical IOL), xảy ra quang sai cầu (spherical aberration) khi tiêu điểm của tia paraxial gần trục quang học khác với tia ngoại vi. Ngược lại, IOL phi cầu (aspheric IOL) giảm quang sai cầu bằng cách thay đổi độ nghiêng của mỗi bề mặt khúc xạ để hội tụ tia ngoại vi và tia paraxial vào cùng một tiêu điểm. Hiện nay, hầu hết các IOL đều áp dụng thiết kế phi cầu, cải thiện độ nhạy tương phản. Tuy nhiên, thiết kế phi cầu làm tăng quang sai dạng sao chổi (coma) khi bị lệch tâm hoặc nghiêng, do đó trong các trường hợp dây chằng Zinn yếu và cố định IOL không ổn định, có thể chọn IOL cầu.
IOL màu (bộ lọc vàng) làm giảm độ truyền qua của ánh sáng bước sóng ngắn (ánh sáng xanh), được thiết kế để gần với độ truyền quang phổ của thủy tinh thể người trưởng thành, và được kỳ vọng giảm nguy cơ tổn thương võng mạc do ánh sáng.
Năm 1981, Sanders và cộng sự đã đề xuất công thức SRK (Sanders-Retzlaff-Kraff), hệ thống hóa việc tính toán công suất IOL1). Năm 1984, Mazzocco đã phát triển IOL silicone có thể gấp lại, mở đường cho phẫu thuật đường rạch nhỏ. Nhật Bản là quốc gia đầu tiên trên thế giới phê duyệt IOL có thể gấp lại, và sau đó đóng vai trò tiên phong quốc tế trong việc phát triển dụng cụ tiêm (injector). Năm 1953, Strampelli đã thực hiện cấy IOL tiền phòng, nhưng gây ra bệnh lý giác mạc bọng nước (bullous keratopathy) ở 70-80% trường hợp sau vài năm, dẫn đến thất bại, nhưng điều này đã trở thành động lực cho những cải tiến thiết kế IOL sau này.
Loại IOL phổ biến nhất, được thiết kế để hội tụ tại một điểm duy nhất. Đây là lựa chọn tiêu chuẩn được thực hiện theo bảo hiểm (điều trị lựa chọn) và nếu mục tiêu là đạt được thị lực chính thị sau phẫu thuật, thì thị lực xa sẽ tốt khi không đeo kính, nhưng thị lực gần cần kính đọc sách. Ưu điểm là độ nhạy tương phản cao nhất và giảm thiểu chói và quầng sáng ban đêm.
Có các lựa chọn sau để xử lý lão thị sau phẫu thuật:
→ Xem Thấu kính nội nhãn đơn tiêu để biết chi tiết.
Cung cấp thị lực tốt ở nhiều khoảng cách tiêu cự, là IOL giá trị gia tăng nhằm giảm sự phụ thuộc vào kính (độc lập với kính). Do hiệu suất sử dụng ánh sáng bị phân tán, có thể xảy ra giảm độ nhạy tương phản và chói/lóa, cần giải thích đầy đủ trước phẫu thuật. Chi phí do bệnh nhân tự chi trả như điều trị tự chọn.
Tập trung vào hai điểm: xa và gần. Hơi không phù hợp cho khoảng cách trung gian (ví dụ làm việc máy tính ở 50-80 cm). Có loại nhiễu xạ (AcrySof IQ ReSTOR, TECNIS Multifocal) và khúc xạ.
Ở loại nhiễu xạ, ánh sáng nhiễu xạ bậc 0 cho tiêu điểm xa, bậc 1 cho tiêu điểm gần, và ánh sáng nhiễu xạ bậc 2 trở lên (khoảng 18%) là yếu tố làm giảm độ nhạy tương phản tần số cao. Loại apodized cải thiện chức năng thị lực xa lúc chạng vạng bằng cách giảm độ chênh ở vùng ngoại vi đồng tử.
Trong một phân tích tổng hợp bao gồm 8 RCT, IOL đa tiêu vượt trội hơn IOL đơn tiêu về thị lực gần không điều chỉnh (UCNVA, tỷ lệ 6/6 hoặc thấp hơn: RR 0,20; KTC 95% 0,07-0,58; 782 mắt) và tỷ lệ không phụ thuộc kính (RR 0,63; KTC 95% 0,55-0,73; 1.000 mắt). Mặt khác, tần suất quầng sáng (RR 3,58; KTC 95% 1,99-6,46; 662 mắt) cao hơn đáng kể ở IOL đa tiêu. 3)
Thấu kính ba tiêu cự hội tụ tại ba điểm: xa, trung gian và gần, hiện là loại thấu kính đa tiêu cự chủ đạo. Thấu kính ba tiêu cự đầu tiên được đưa vào lâm sàng năm 20104), và các sản phẩm đại diện hiện nay bao gồm AcrySof IQ PanOptix (Alcon), AT LISA tri (Carl Zeiss), FineVision (PhysIOL) và TECNIS Synergy (J&J Vision).
Trong một phân tích tổng hợp từ 22 nghiên cứu với 2.200 mắt, thấu kính ba tiêu cự vượt trội hơn thấu kính EDOF về thị lực gần không chỉnh (UCNVA: MD = 0,12 logMAR, p < 0,00001) và tỷ lệ không phụ thuộc kính (OR = 0,26, p = 0,02). Trong khi đó, không có sự khác biệt đáng kể giữa hai nhóm về thị lực xa không chỉnh (UDVA) và thị lực trung gian không chỉnh (UIVA), và điểm Chất lượng Thị giác cao hơn đáng kể ở thấu kính ba tiêu cự (MD = 1,24, p = 0,03).5)
Trong một đánh giá có hệ thống về thấu kính ba tiêu cự, thị lực trung gian tốt hơn đáng kể ở thấu kính ba tiêu cự so với thấu kính hai tiêu cự (DCIVA: MD −0,16 logMAR, KTC 95% −0,22 đến −0,10), nhưng không có sự khác biệt đáng kể về CDVA, thị lực xa, thị lực gần, độ nhạy tương phản hoặc sự hài lòng của bệnh nhân.4)
Thấu kính mở rộng độ sâu tiêu cự (EDOF) phân tán ánh sáng thành một dải tiêu cự liên tục thay vì một điểm tiêu cự duy nhất, cung cấp độ sâu tiêu cự rộng từ xa đến trung gian. Sản phẩm đầu tiên đạt chứng nhận CE xuất hiện vào năm 20144). Các sản phẩm đại diện bao gồm TECNIS Symfony (J&J Vision), TECNIS Eyhance và AcrySof IQ Vivity (Alcon).
Trong phân tích tổng hợp nêu trên (22 nghiên cứu), IOL EDOF vượt trội hơn một chút về thị lực nhìn xa đã chỉnh (CDVA: MD = −0,01 logMAR, p = 0,01) so với IOL ba tiêu cự, và không có sự khác biệt đáng kể về tần suất chói và quầng sáng giữa hai nhóm. 5) Hướng dẫn của ESCRS khuyến nghị IOL EDOF như một lựa chọn cho bệnh nhân ưu tiên thị lực trung gian đồng thời giảm thiểu tác dụng phụ quang học. 4) Trong thử nghiệm đăng ký tại Hoa Kỳ đánh giá IOL EDOF (AcrySof IQ Vivity), thị lực nhìn xa tốt nhất đã chỉnh (BCVA) tương đương với nhóm đối chứng đơn tiêu cự (CDVA một mắt 0,00 logMAR), và mức giảm độ nhạy tương phản trong điều kiện ánh sáng trung bình chỉ ở mức trung bình. 17)
→ Để biết chi tiết, xem Thấu kính nội nhãn đa tiêu cự.
IOL được thiết kế để điều chỉnh loạn thị giác mạc đều, có đánh dấu trên kinh tuyến yếu của phần quang học, và được cố định trong bao thể thủy tinh sao cho dấu này trùng với kinh tuyến mạnh của giác mạc. Mỗi độ lệch trục 1° làm giảm hiệu quả điều chỉnh khoảng 3,3%, và lệch trục 30° không chỉ làm mất hiệu quả điều chỉnh mà còn có thể làm suy giảm chức năng thị giác so với IOL không toric.
Tiêu chí chỉ định IOL Toric ước tính (tùy theo cơ sở):
Hướng dẫn ESCRS (2024) khuyến nghị cân nhắc IOL toric cho mắt có loạn thị giác mạc ≥ 1,0 D, và có bằng chứng mạnh (GRADE ++) cho ≥ 2,0 D. 4) Một phân tích tổng hợp 13 thử nghiệm cho thấy IOL toric vượt trội hơn IOL không toric (có hoặc không có rạch thư giãn) về thị lực không chỉnh sau phẫu thuật (MD −0,07 logMAR, KTC 95% −0,10 đến −0,04) và tỷ lệ không đạt 20/25 (RR 0,59, KTC 95% 0,50 đến 0,70). 14)
Các trường hợp dây chằng Zinn yếu, vỡ bao sau hoặc giãn đồng tử không đủ thường không phù hợp do khó căn chỉnh trục chính xác. Để tính toán, sử dụng máy tính trực tuyến của từng nhà sản xuất hoặc công thức Barrett Toric hoặc Haigis-T tích hợp trong thiết bị.
→ Xem Thấu kính nội nhãn Toric để biết chi tiết.
Là IOL được cố định sau mống mắt hoặc trong rãnh thể mi, giữ lại thể thủy tinh, là một dạng phẫu thuật khúc xạ. Ví dụ điển hình là ICL (Implantable Collamer Lens; EVO+ ICL), một PIOL hậu phòng làm từ chất liệu collamer có tính tương thích sinh học cao. Không cần cắt bỏ giác mạc, có thể đảo ngược và phù hợp với cận thị trung bình đến cao.
Hướng dẫn phẫu thuật khúc xạ của Hiệp hội Nhãn khoa Nhật Bản (phiên bản thứ 8) quy định độ tuổi thích hợp cho phẫu thuật thủy tinh thể nội nhãn còn thể thủy tinh (Phakic IOL) là từ 21 đến 45 tuổi, và lượng khúc xạ thích hợp là cận thị từ 6 D trở lên. Cận thị trung bình (3 đến dưới 6 D) và cận thị nặng (trên 15 D) cần được xử lý thận trọng. Ngoài các chống chỉ định tương tự như phẫu thuật laser excimer (như viêm mắt ngoài hoạt động, đục thủy tinh thể, viêm màng bồ đào), các chống chỉ định bổ sung bao gồm tiền phòng nông, rối loạn nội mô giác mạc và giác mạc hình chóp tiến triển. 6)
Các đánh giá trước phẫu thuật bắt buộc bao gồm kiểm tra mật độ tế bào nội mô giác mạc, phân tích hình ảnh đoạn trước (bao gồm độ sâu tiền phòng) và đo đường kính giác mạc (đường kính ngang). 6)
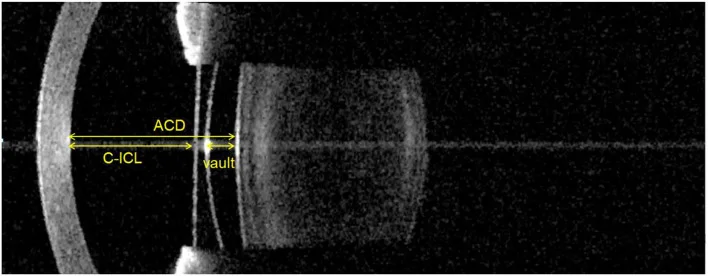
→ Để biết chi tiết, hãy tham khảo Thủy tinh thể hậu phòng còn thể thủy tinh (ICL).
Thấu kính phụ trợ được cố định vào rãnh thể mi bên trên thấu kính đơn tiêu hiện có. Cho phép điều chỉnh lão thị, loạn thị và cận thị sau này ngay cả ở những mắt đã được cấy thấu kính đơn tiêu trước đó. Khoảng cách từ thấu kính trong bao tương đối ổn định, và độ ổn định lâu dài được cho là tốt.
→ Xem Thấu kính nội nhãn bổ sung để biết chi tiết.
| Loại | Vùng tiêu cự | Độ nhạy tương phản | Chói và quầng sáng | Điều chỉnh loạn thị | Bảo hiểm chi trả | Chi phí bổ sung ước tính (cả hai mắt) |
|---|---|---|---|---|---|---|
| Một tiêu cự | 1 điểm (xa hoặc gần) | ◎ | Không có | △ (toric riêng) | ○ (chăm sóc được lựa chọn) | 0 đến vài chục nghìn yên |
| Hai tiêu cự (nhiễu xạ) | Xa + Gần | ○ | ++ (trung bình) | △〜○ | × | 300.000〜500.000 yên |
| Ba tiêu cự | Xa + Trung gian + Gần | ○ | ++ (Trung bình) | △~○ | × | 40-60 nghìn yên |
| EDOF | Xa đến Trung (Liên tục) | ◎~○ | + (Nhẹ) | △~○ | × | 35~55 nghìn yên |
| Kính toric (đơn tiêu) | 1 điểm (ưu tiên nhìn xa) | ◎ | không có | ◎ | × (điều trị được chọn) | 100.000-150.000 yên |
| Thể thủy tinh nhân tạo (PIOL/ICL) | Xa (không cần chỉnh giác mạc) | ◎ | Không | EVO+ △~○ | × | 500.000~700.000 yên |
| Kính nội nhãn bổ sung | IOL hiện có + điều chỉnh lão thị | ○ | + | ○ | × | 30-45 nghìn yên |
Chi phí là ước tính gần đúng cho cả hai mắt khi tự túc. Khác biệt đáng kể tùy theo cơ sở và loại kính được chọn.
Việc lựa chọn IOL ảnh hưởng trực tiếp đến thị lực sau phẫu thuật, do đó việc xác nhận kỹ lưỡng mong muốn của bệnh nhân trước phẫu thuật là không thể thiếu. Hướng dẫn về đục thủy tinh thể của ESCRS nêu rõ: “Đánh giá kỳ vọng của bệnh nhân và sự đồng ý có hiểu biết chi tiết là tiền đề quan trọng nhất để lựa chọn IOL phù hợp”. 4) Thông tin cần nắm bắt:
Các điều kiện phù hợp cho IOL đa tiêu (ba tiêu/EDOF):
Phân tích tổng hợp cho thấy tỷ lệ thay IOL trong vòng một năm tăng nếu sự phụ thuộc vào kính không được giải quyết hoặc tác dụng phụ quang học không cải thiện sau khi cấy IOL đa tiêu.3)
IOL Toric có hiệu quả trong điều chỉnh loạn giác mạc đều, nhưng có một số điều kiện tiên quyết.
Để xem xét ảnh hưởng của loạn thị giác mạc sau, nên sử dụng công thức Barrett Toric hoặc công thức Haigis-T tích hợp trong máy đo chiều dài trục quang học. 7) Ngoài ra, xoay nhãn cầu (cyclotorsion) giữa tư thế ngồi và nằm trung bình 4-5°, do đó đánh dấu bằng ảnh hoặc hệ thống hướng dẫn hình ảnh (CALLISTO eye, VERION) để căn chỉnh trục tự động hữu ích để cải thiện độ chính xác. Trong một thử nghiệm tiến cứu so sánh hệ thống hướng dẫn hình ảnh với đánh dấu thủ công, loạn thị tồn dư sau mổ thấp hơn đáng kể ở nhóm hướng dẫn hình ảnh (0,33 D so với 0,51 D, p = 0,003). 19)
Đối với những người lái xe ban đêm nhiều hoặc làm công việc thị giác chính xác, thấu kính đơn tiêu có thể phù hợp hơn. Ngược lại, những người muốn thực hiện các khoảng cách khác nhau như dùng điện thoại thông minh, máy tính và đọc sách mà không cần kính, thấu kính đa tiêu là ứng cử viên. Tuy nhiên, một số tình trạng mắt (như bệnh hoàng điểm, glôcôm, khô mắt) có thể không phù hợp với thấu kính đa tiêu. Tư vấn trước phẫu thuật với bác sĩ điều trị là quan trọng nhất.
Để tính toán công suất IOL chính xác, việc đo đồng thời nhiều thông số bằng thiết bị đo chiều dài trục quang học đã trở thành tiêu chuẩn. Phương pháp quang học có sai số đo nhỏ hơn so với phương pháp siêu âm A-mode. Tại Nhật Bản, sau khi được bảo hiểm chi trả vào năm 2010 với tên gọi “đo chiều dài trục quang học”, phương pháp này đã lan rộng nhanh chóng. Nhờ áp dụng phương pháp FD (Miền Fourier), tỷ lệ thành công đo tăng từ khoảng 90% lên 98%, và độ lệch chuẩn của các phép đo nằm trong khoảng 0,02 mm. 7)
| Thiết bị | Phương pháp đo | Các chức năng chính được tích hợp |
|---|---|---|
| IOLMaster 700 (Carl Zeiss) | SS-OCT (nguồn quét) | Chiều dài trục, công suất khúc xạ giác mạc, độ sâu tiền phòng, độ dày thủy tinh thể, đường kính giác mạc, tiêu chuẩn vàng |
| ARGOS (Santen/Santek) | FD-OCT (phương pháp phân đoạn) | Đo chỉ số khúc xạ riêng của từng mô. Có xu hướng đo chiều dài trục ngắn hơn IOLMaster 700 |
| OA-2000 (Tomey) | FD-OCT | Hiển thị song song hình ảnh B-scan và dạng sóng A-scan |
| Phương pháp siêu âm chế độ A | Siêu âm (1.550 m/s) | Có thể áp dụng cho mọi trường hợp nhưng sai số lớn (được cho là nguyên nhân của phần lớn sai số khúc xạ sau phẫu thuật)7) |
Vì phương pháp quang học hiển thị chiều dài trục dài hơn 0,2–0,3 mm so với phương pháp siêu âm, bắt buộc phải sử dụng hằng số IOL (như hằng số A) dành riêng cho thiết bị đo. Vì ARGOS sử dụng phương pháp phân đoạn, cần tránh sử dụng tương thích hằng số IOL với IOLMaster 700. 7)
| Công thức | Thế hệ | Đặc điểm | Ứng dụng chính |
|---|---|---|---|
| Công thức SRK/T | Thế hệ thứ 3 | Hơn 90% sử dụng trong nước. Kinh nghiệm lâm sàng phong phú, hằng số A | Lựa chọn đầu tiên cho trục nhãn cầu tiêu chuẩn (22-25 mm) |
| Công thức Haigis | Thế hệ thứ 3 | Sử dụng độ sâu tiền phòng làm biến độc lập. Ba hằng số a0, a1, a2 (cần tối ưu hóa trên 200 mắt trở lên) | Mắt có tiền phòng nông/sâu |
| Công thức Barrett Universal II | Thế hệ thứ 4 | Dựa trên lý thuyết thấu kính dày. Độ chính xác tốt với IOL công suất thấp. Có thể tính miễn phí trên trang web APACRS | Trục dài, trục ngắn, IOL công suất thấp |
| Hill-RBF | AI (học máy) | Nhận dạng mẫu từ dữ liệu lớn. Không dựa trên công thức | Trục dài, cận thị nặng |
| Công thức Kane | AI (học máy + công thức lý thuyết) | Giới tính cũng được sử dụng như một biến số | Cận thị nặng cực độ (chiều dài trục ≥ 30 mm) |
Tại Nhật Bản, công thức SRK/T thế hệ thứ 3 được sử dụng rộng rãi, nhưng nên so sánh nhiều kết quả tính toán tùy theo chiều dài trục và giải phẫu tiền phòng (độ đồng đều của nhãn cầu). Vì khoảng 15% bệnh nhân phẫu thuật đục thủy tinh thể có nhãn cầu không đồng đều về chiều dài trục và công suất khúc xạ giác mạc, cần thận trọng khi chọn công thức sử dụng. 7)
Trong một nghiên cứu đa trung tâm trên 13.301 mắt, các công thức Barrett Universal II, Olsen và Haigis cho thấy độ chính xác cao hơn đáng kể so với SRK/T, Holladay 1 và Hoffer Q (Holladay 2 có độ chính xác gần tương đương), và các công thức thế hệ thứ 4 trở lên vượt trội cho cả trục dài và trục ngắn. 15) Trong một phân tích tổng hợp khác tập trung vào mắt trục ngắn (AL < 22 mm), Barrett Universal II có MAE nhỏ hơn đáng kể so với Haigis và SRK/T (p < 0,05). 18)
Trong một nghiên cứu trên 80 mắt cận thị nặng (chiều dài trục ≥ 30 mm), các công thức AI (Kane, Hill-RBF) có sai số tuyệt đối trung bình (MAE) nhỏ hơn đáng kể so với SRK/T (Kane: 0,51 D, Hill-RBF: 0,52 D, Barrett Universal II: 0,66 D, SRK/T: khác biệt có ý nghĩa, p < 0,05), và tỷ lệ sai số khúc xạ >1,0 D được kiểm soát ở mức 7,5% đối với Kane và Hill-RBF, trong khi SRK/T lên tới 42,5%. 8) Ở những mắt có chiều dài trục ≥ 32 mm, công thức Kane đạt MAE (0,44 D) và MedAE (0,40 D) thấp nhất. 8) Trong một báo cáo khác của Rong 2019 trên mắt có chiều dài trục ≥ 28 mm, MedAE của Barrett Universal II là 0,37 D, nhỏ hơn đáng kể so với 0,46 D của Haigis (p = 0,038). Ở mắt có chiều dài trục ≥ 30 mm, Barrett Universal II cho thấy độ chính xác tốt hơn Haigis. 16)
| Trường hợp | Công thức Khuyến nghị | Lưu ý |
|---|---|---|
| Mắt tiêu chuẩn (AL 22–25 mm) | SRK/T, Haigis, Barrett Universal II | So sánh nhiều công thức |
| Trục dài (AL > 26 mm) | Barrett Universal II, Hill-RBF, Kane | Chú ý sự khác biệt về độ chính xác khi dùng IOL công suất thấp15,16) |
| Trục ngắn (AL < 22 mm) | Barrett Universal II, Haigis, Holladay 2 | Nguy cơ sai số khúc xạ cao. Sai số dự đoán ELP lớn18) |
| Sau phẫu thuật khúc xạ giác mạc (sau LASIK) | Haigis-L, Shammas No-history, Barrett True-K, OKULIX | So sánh máy tính trực tuyến ASCRS với nhiều công thức9,20) |
| Cố định rãnh thể mi (ngoài bao) | Hiệu chỉnh −1,0 D sau khi tính bằng SRK/T v.v. | Hiệu chỉnh ít hơn cho công suất thấp ở trục dài, hiệu chỉnh −2,0 D cho công suất cao ở trục ngắn |
| Cố định trong củng mạc (phương pháp kẹp) | Hiệu chỉnh tương tự như cố định ngoài bao | Khác nhau tùy theo kỹ thuật phẫu thuật |
| Giác mạc hình chóp / sau ghép giác mạc | Công thức chuyên biệt (Seitz-Langenbucher v.v.) hoặc đánh giá của chuyên gia | Công thức tiêu chuẩn cho sai số lớn |
Sau phẫu thuật LASIK, giác mạc có hình dạng phẳng cục bộ, dẫn đến việc đo công suất khúc xạ trung tâm bằng máy đo độ cong giác mạc tự động bị đánh giá quá cao, gây ra tình trạng viễn thị hóa sau phẫu thuật (hyperopic shift). Các thiết bị đo chiều dài trục quang học được trang bị các công thức có thể sử dụng ngay cả khi không có dữ liệu trước LASIK (như Haigis-L, Shammas No-history, Barrett True-K), và máy tính trực tuyến miễn phí của ASCRS (Hiệp hội Phẫu thuật Đục thủy tinh thể và Khúc xạ Hoa Kỳ) có thể so sánh nhiều công thức như một biện pháp đối phó. 7,9) Trong một nghiên cứu trên 110 mắt sau LASIK, độ chính xác của Barrett True-K khi sử dụng riêng với máy đo sinh học tương đương với phương pháp trung bình nhiều công thức (MAE 0,41 D so với 0,42 D, p = 0,81), cho thấy độ tin cậy khi sử dụng riêng lẻ. 20)
Trước phẫu thuật, giá trị khúc xạ mục tiêu được thiết lập dựa trên lối sống, công việc và sở thích của bệnh nhân (giá trị dự đoán theo tương đương cầu).
| Lối sống | Giá trị khúc xạ mục tiêu khuyến nghị |
|---|---|
| Ưu tiên nhìn xa (lái xe, thể thao) | Chính thị (0,00 D) đến −0,25 D |
| Loại cân bằng | −0,25 đến −0,50 D (hơi cận thị nhẹ) |
| Ưu tiên nhìn gần (đọc sách, công việc chi tiết) | −1,50 đến −2,00 D (ứng cử viên cho monovision) |
| Monovision (mắt không trội) | −1,50 đến −2,00 D |
| Thấu kính đa tiêu (hầu hết các sản phẩm) | Chính thị (phải trong khoảng ±0,25 D) |
Để tính toán IOL điều chỉnh loạn thị, hãy sử dụng công thức tích hợp trong máy đo chiều dài trục quang học (như công thức Haigis-T hoặc Barrett Toric) để tránh rắc rối khi nhập số đo và nguy cơ sai sót. Nguyên tắc cơ bản là sử dụng nhất quán chiều dài trục quang học, công suất giác mạc và hằng số IOL. 7)
Sai số khúc xạ nhẹ (trong ±0,5 D) có thể điều chỉnh bằng kính mắt. Sai số lớn (≥±1,5 D) cần thêm IOL phụ trợ hoặc thay IOL. Với IOL đa tiêu, ngay cả sai số dưới 0,5 D cũng có thể làm giảm đáng kể sự hài lòng của bệnh nhân, do đó việc đo đạc chính xác và lựa chọn công thức trước phẫu thuật đặc biệt quan trọng.
Sau khi đặt IOL, sự điều tiết tự nhiên của thể thủy tinh (thay đổi độ dày do co cơ thể mi) biến mất. Tuy nhiên, trên lâm sàng có thể xảy ra hiện tượng gọi là “điều tiết giả” (pseudoaccommodation), cho phép nhìn gần một chút. Điều tiết giả là do tính đa tiêu cự của giác mạc, loạn thị, hiệu ứng lỗ kim của đồng tử, quang sai cầu của IOL, và ngay cả với IOL đơn tiêu cũng có thể quan sát thấy điều tiết giả khoảng 0,5-1,0 D.
IOL đơn tiêu mang lại độ nhạy tương phản tương đương hoặc tốt hơn thể thủy tinh tự nhiên trẻ. Mặt khác, IOL đa tiêu làm giảm độ nhạy tương phản ở tần số cao do tán xạ ánh sáng. Trong đục thủy tinh thể nhẹ hoặc mắt có IOL, độ nhạy tương phản có thể giảm ngay cả khi thị lực không thay đổi. Trong một phân tích tổng hợp (22 nghiên cứu) về IOL ba tiêu và EDOF, không có sự khác biệt đáng kể về độ nhạy tương phản giữa hai nhóm.5) Nhìn chung, trong một phân tích tổng hợp Cochrane (bao gồm 8 RCT) về IOL đa tiêu, độ nhạy tương phản giảm nhẹ so với IOL đơn tiêu, nhưng ý nghĩa lâm sàng không rõ ràng.3)
Nếu đục bao sau (PCO) xảy ra trong vòng 5 năm sau phẫu thuật, độ nhạy tương phản có thể giảm đáng kể. IOL acrylic kỵ nước có tỷ lệ PCO thấp hơn so với acrylic ưa nước, và thiết kế cạnh vuông cũng có hiệu quả trong phòng ngừa.10)
Hào quang (halo) là vòng sáng nhìn thấy xung quanh nguồn sáng, chói lóa (glare) là sự chói mắt hoặc mờ tầm nhìn do nguồn sáng gây ra. Ở kính nội nhãn (IOL) đa tiêu, hào quang (RR 3,58; KTC 95% 1,99–6,46) và chói lóa tăng đáng kể so với IOL đơn tiêu. 3) IOL EDOF có ít tác dụng phụ quang học hơn so với IOL hai tiêu và ba tiêu truyền thống, nhưng không biến mất hoàn toàn. 5)
Xử trí:
Ngay sau khi đặt IOL không màu, bệnh nhân có thể phàn nàn về cảm giác nhìn xanh (xanh thị) do khả năng truyền ánh sáng bước sóng ngắn cao hơn so với thủy tinh thể tự nhiên. IOL có màu (bộ lọc vàng) làm giảm hiện tượng này. Sự thích nghi thần kinh xảy ra trong vài ngày đến vài tuần, và hầu hết bệnh nhân không còn nhận thấy.
Glistenings là những phản xạ dạng chấm xuất hiện ở phần quang học của IOL acrylic kỵ nước. Những chấm ở lớp sâu gọi là glistenings, còn ở bề mặt gọi là subsurface nano glistenings (SSNG). Cả hai đều do thủy dịch xâm nhập vào các khoảng nhỏ trong vật liệu quang học, không phải do thoái hóa vật liệu. Thông thường không ảnh hưởng đến chức năng thị giác, nhưng đã có báo cáo về suy giảm thị lực ở bệnh nhân có chức năng võng mạc kém. Các IOL hiện đang bán đã được cải tiến quy trình sản xuất, làm giảm các hiện tượng này. Ở IOL acrylic ưa nước, canxi photphat có thể lắng đọng trên bề mặt khi sử dụng lâu dài, gây đục nặng (lắng đọng canxi). 10)
Phẫu thuật đục thủy tinh thể hiện đại rất an toàn, nhưng đục thủy tinh thể thứ phát (có thể điều trị bằng laser) xảy ra ở khoảng 20-40% sau 5 năm. Các biến chứng nghiêm trọng (viêm nội nhãn, xuất huyết tống xuất) hiếm gặp (0,006-0,04%). Trật IOL tăng dần theo thời gian do lão hóa và yếu dây chằng Zinn, đặc biệt ở người già, cận thị nặng và hội chứng giả bong bao.
| Biến chứng | Tỷ lệ xảy ra (ước tính) | Tổng quan | Xử trí |
|---|---|---|---|
| Đục thủy tinh thể thứ phát (đục bao sau) | 20-40% sau 5 năm phẫu thuật | Tế bào biểu mô thủy tinh thể tăng sinh trên bao sau phía sau IOL, làm giảm chức năng thị giác | Mở bao sau bằng laser Nd:YAG |
| Lệch hoặc trật IOL | Vài % mỗi năm ở mắt có dây chằng Zinn yếu | Đứt dây chằng Zinn do lão hóa, chấn thương hoặc hội chứng giả bong bao, khiến IOL rơi vào dịch kính | Cố định trong củng mạc, khâu hoặc thay IOL11) |
| Kẹp đồng tử (kẹp mống mắt) | Một vài phần trăm sau cố định trong củng mạc | Tình trạng phần quang học của IOL lệch ra phía trước đồng tử. | Giãn đồng tử, thay đổi tư thế, thay IOL có đường kính quang học lớn hơn12) |
| Đục IOL | Lấp lánh kỵ nước vài %, lắng đọng canxi ưa nước sau vài năm | Suy giảm thị lực do biến chất vật liệu | Thay IOL10) |
| Glôcôm sau PIOL | Tăng nhãn áp sau phẫu thuật ICL 1-5% | Tăng nhãn áp do tắc góc hoặc block đồng tử | Đánh giá độ sâu tiền phòng trước phẫu thuật và quản lý định kỳ sau phẫu thuật13) |
Lệch hoặc trật IOL
Chẩn đoán và chỉ định phẫu thuật cho IOL rơi do đứt dây chằng Zinn. Lựa chọn cố định trong củng mạc (phương pháp flange hoặc kẹp).
Đục thủy tinh thể nhân tạo (IOL)
Cơ chế và quản lý glistening, SSNG, lắng đọng canxi và đục bao sau. Thông tin ảnh hưởng đến lựa chọn chất liệu IOL.
Đo sinh trắc (Tính công suất IOL)
Đo đồng thời chính xác chiều dài trục, công suất khúc xạ giác mạc và độ sâu tiền phòng bằng thiết bị đo chiều dài trục quang học. Đo sinh trắc để tính công suất IOL
Cố định trong củng mạc
Phương pháp mặt bích và kẹp để cấy phần đỡ IOL vào trong củng mạc mà không cần khâu. Tránh nguy cơ viêm nội nhãn và thoái hóa chỉ khâu. IOL cố định trong củng mạc
Sanders DR, Retzlaff J, Kraff MC. Comparison of the SRK II formula and other second generation formulas. J Cataract Refract Surg. 1988;14(2):136-141.1)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapter 4.6: patient selection for correcting presbyopia. https://www.escrs.org/escrs-guideline-for-cataract-surgery/2)
de Silva SR, Evans JR, Kirthi V, Ziaei M, Leyland M. Multifocal versus monofocal intraocular lenses after cataract extraction. Cochrane Database Syst Rev. 2016;12(12):CD003169. doi:10.1002/14651858.CD003169.pub4. PMID:27943250; PMCID:PMC6463930.3)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapters 4.6-4.7 and 6.1-6.3. https://www.escrs.org/escrs-guideline-for-cataract-surgery/4)
Karam M, Alkhowaiter N, et al. Extended Depth of Focus Versus Trifocal for Intraocular Lens Implantation: An Updated Systematic Review and Meta-Analysis. J Refract Surg. 2022. 22 studies, 2200 eyes.5)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 日眼会誌. 2024;128(2):135-142.6)
Werner L. Intraocular lenses: overview of designs, materials, and pathophysiologic features. Ophthalmology. 2021;128(11):e74-e93.7)
Suzuki Y, Kamoi K, Uramoto K, Ohno-Matsui K. Artificial intelligence driven intraocular lens power calculation in extreme axial myopia. Sci Rep. 2025. 80 eyes, axial length ≥30.0 mm, Institute of Science Tokyo.8)
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern®. AAO; 2021.9)
Grzybowski A, Markeviciute A, Zemaitiene R. A narrative review of intraocular lens opacifications: update 2020. Ann Transl Med. 2020;8(22):1547. doi:10.21037/atm-20-4207. PMID:33313292; PMCID:PMC7729367.10)
Tripathi M, Rao S, Sinha R. Scleral-fixated IOLs - A comprehensive review of current practices and emerging trends. Indian J Ophthalmol. 2025;73(7):933-945. doi:10.4103/IJO.IJO_2812_24. PMID:40586185; PMCID:PMC12356440.11)
Choi SR, Jeon JH, Kang JW, Heo JW. Risk factors for and management of pupillary intraocular lens capture after intraocular lens transscleral fixation. J Cataract Refract Surg. 2017;43(12):1557-1562. PMID: 29335100. doi:10.1016/j.jcrs.2017.08.021.12)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 有水晶体眼内レンズ手術の禁忌・慎重事項. 日眼会誌. 2024;128(2):135-142.13)
Kessel L, Andresen J, Tendal B, Erngaard D, Flesner P, Hjortdal J. Toric intraocular lenses in the correction of astigmatism during cataract surgery: a systematic review and meta-analysis. Ophthalmology. 2016;123(2):275-286. doi:10.1016/j.ophtha.2015.10.002. PMID:26601819.14)
Melles RB, Holladay JT, Chang WJ. Accuracy of intraocular lens calculation formulas. Ophthalmology. 2018;125(2):169-178. doi:10.1016/j.ophtha.2017.08.027. PMID:28951074.15)
Rong X, He W, Zhu Q, et al. Intraocular lens power calculation in eyes with extreme myopia: comparison of Barrett Universal II, Haigis, and Olsen formulas. J Cataract Refract Surg. 2019;45(6):732-737.16)
McCabe C, Berdahl J, Reiser H, et al. Clinical outcomes in a U.S. registration study of a new EDOF intraocular lens with a nondiffractive design. J Cataract Refract Surg. 2022;48(11):1297-1304. PMID: 35616507. PMCID: PMC9622364. doi:10.1097/j.jcrs.0000000000000978.17)
Wang Q, Jiang W, Lin T, Wu X, Lin H, Chen W. Meta-analysis of accuracy of intraocular lens power calculation formulas in short eyes. Clin Exp Ophthalmol. 2018;46(4):356-363. doi:10.1111/ceo.13058. PMID:28887901.18)
Webers VSC, Bauer NJC, Visser N, et al. Image-guided system versus manual marking for toric intraocular lens alignment in cataract surgery. J Cataract Refract Surg. 2017;43(6):781-788. doi:10.1016/j.jcrs.2017.03.041. PMID:28732612.19)
Ferguson TJ, Downes RA, Randleman JB. IOL power calculations after LASIK or PRK: Barrett True-K biometer-only calculation strategy yields equivalent outcomes as a multiple formula approach. J Cataract Refract Surg. 2022;48(7):784-789. doi:10.1097/j.jcrs.0000000000000883. PMID:35067661.20)