IOL-Dezentrierung und -Luxation
Diagnose und Operationsindikation bei IOL-Abfall durch Zonulafaserriss. Auswahl der intrakleralen Fixation (Flanschmethode/Pinzettmethode).

Eine Intraokularlinse (IOL) ist eine künstliche Linse, die nach der Entfernung der getrübten natürlichen Linse bei einer Kataraktoperation dauerhaft im Auge verbleibt. Ein Auge mit einer IOL wird als Pseudophakie bezeichnet. Im Gegensatz zur Korrektur durch Brille oder Kontaktlinsen wird die IOL direkt in das optische System des Auges integriert, sodass keine Bildvergrößerung oder -verkleinerung auftritt und die natürlichste und physiologischste Sehfunktion erreicht wird.
Die derzeit am weitesten verbreitete IOL ist die faltbare IOL, die aus einem optischen Teil und einem Haptikteil besteht. Der optische Durchmesser beträgt standardmäßig 6,0 mm, und sie kann über einen 2,4–2,8 mm kleinen Schnitt bei der Phakoemulsifikation (PEA) mit einem Injektor eingesetzt werden. In einigen schwierigen Fällen wird eine IOL mit einem großen optischen Durchmesser von 7,0 mm verwendet, was die Sichtbarkeit bei der Fundusuntersuchung und die zentrale Stabilität bei der extrakapsulären Fixation verbessert.
Die Klassifizierung nach Material ist unten aufgeführt.
| Material | Eigenschaften | Hauptindikationen |
|---|---|---|
| Hydrophobes Acryl | Weniger Nachstar. Achtung vor Glistenings | Aktuelle Standardwahl |
| Hydrophiles Acryl | Hohe Biokompatibilität. Risiko von Kalziumablagerungen (IOL-Trübung) bei Langzeitanwendung | Spezialdesign-IOL |
| Silikon | Gute Faltbarkeit. Nicht geeignet bei Silikonöl-Tamponade im Auge | Einige PIOL |
| PMMA | Hartes Material. Erfordert Erweiterung des Schnitts auf 5-7 mm | Spezialfixierte IOL, Sekundärimplantation |
Strukturell gibt es 1-Stück-Linsen, bei denen Optik und Haptik aus demselben Material bestehen, und 3-Stück-Linsen aus unterschiedlichen Materialien. 1-Stück-Linsen werden üblicherweise für die intrakapsuläre Fixation (Bag-in-the-Lens) verwendet, während 3-Stück-Linsen für die extrakapsuläre Fixation, Skleralfixation und Naht geeignet sind. Wird eine 1-Stück-Linse versehentlich extrakapsulär (im Ziliarsulkus) fixiert, können die Haptiken die Iris reiben, was zu Irispigmentdispersion und anhaltender Entzündung führen kann – Vorsicht ist geboten.
Sphärische IOL erzeugen eine sphärische Aberration, da der Brennpunkt der paraxialen Strahlen nahe der optischen Achse und der der peripheren Strahlen unterschiedlich ist. Asphärische IOLs hingegen verringern die sphärische Aberration, indem sie die Neigung jeder brechenden Fläche verändern und die peripheren und paraxialen Strahlen auf denselben Brennpunkt konvergieren lassen. Heutzutage verwenden fast alle IOLs ein asphärisches Design, was die Kontrastempfindlichkeit verbessert. Allerdings erhöht das asphärische Design die Koma-Aberration bei Dezentrierung oder Neigung. Daher wird bei Patienten mit schwachen Zonulafasern und instabiler IOL-Fixierung manchmal die Wahl einer sphärischen IOL getroffen.
Getönte (Gelbfilter-) IOL reduziert die Transmission von kurzwelligem Licht (blaues Licht), nähert sich der spektralen Transmission der menschlichen Erwachsenenlinse an und soll das Risiko einer Netzhautlichtschädigung verringern.
1981 schlugen Sanders et al. die SRK-Formel (Sanders-Retzlaff-Kraff-Formel) vor, die die IOL-Stärkenberechnung systematisierte1). 1984 entwickelte Mazzocco die faltbare Silikon-IOL und ebnete den Weg für die kleinschnittige Chirurgie. Japan war das erste Land der Welt, das faltbare IOLs zuließ, und spielte später eine führende Rolle bei der Entwicklung von Injektoren. Die 1953 von Strampelli durchgeführte Vorderkammer-IOL-Implantation scheiterte nach einigen Jahren, da sie bei 70–80 % der Fälle eine bullöse Keratopathie verursachte, was jedoch die treibende Kraft für spätere Verbesserungen des IOL-Designs war.
Die am weitesten verbreitete IOL, die nur auf einen Punkt fokussiert. Es ist die Standardoption unter der Krankenversicherung (selektive Behandlung). Wenn die postoperative Emmetropie angestrebt wird, ist das Fernsehen ohne Brille gut, aber für die Nahsicht ist eine Lesebrille erforderlich. Die Vorteile sind die höchste Kontrastempfindlichkeit und minimale Blendung und Halos in der Nacht.
Für die postoperative Presbyopie-Behandlung gibt es folgende Optionen:
→ Siehe Monofokale Intraokularlinse für Details.
Es handelt sich um eine Mehrwert-IOL, die auf mehreren Brennweiten eine gute Sehschärfe bietet und die Brillenunabhängigkeit zum Ziel hat. Da die Lichtausnutzungseffizienz verteilt ist, kann es zu einer verminderten Kontrastempfindlichkeit sowie Blendung und Halos kommen, was präoperativ ausreichend erklärt werden muss. Es handelt sich um eine Wahlleistung, die vom Patienten selbst zu tragen ist.
Sie fokussiert auf zwei Punkte: Ferne und Nähe. Mittlere Entfernungen (50–80 cm, z. B. Computerarbeit) waren weniger geeignet. Es gibt diffraktive (AcrySof IQ ReSTOR, TECNIS Multifocal) und refraktive Typen.
Beim diffraktiven Typ bildet das Licht nullter Beugungsordnung den Fernfokus und das erster Ordnung den Nahfokus; Licht höherer Beugungsordnungen (ca. 18 %) verringert die hochfrequente Kontrastempfindlichkeit. Der apodisierte Typ verbessert das Fernsehen in der Dämmerung, indem die Stufenhöhe in der Pupillenperipherie reduziert wird.
Eine Metaanalyse mit 8 RCTs zeigte, dass multifokale IOLs monofokalen IOLs in der unkorrigierten Nahvisus (UCNVA, Anteil ≤ 6/6: RR 0,20; 95 %-KI 0,07–0,58; 782 Augen) und der Brillenunabhängigkeit (RR 0,63; 95 %-KI 0,55–0,73; 1000 Augen) überlegen waren. Dagegen war die Häufigkeit von Halos (RR 3,58; 95 %-KI 1,99–6,46; 662 Augen) bei multifokalen IOLs signifikant höher. 3)
Es fokussiert auf drei Punkte: Ferne, mittlere Distanz und Nähe, und ist derzeit der vorherrschende Typ multifokaler IOLs. Die erste trifokale IOL wurde 2010 klinisch eingeführt4), und aktuelle repräsentative Produkte sind AcrySof IQ PanOptix (Alcon), AT LISA tri (Carl Zeiss), FineVision (PhysIOL), TECNIS Synergy (J&J Vision) usw.
In einer Metaanalyse von 22 Studien mit 2.200 Augen waren trifokale IOLs den EDOF-IOLs hinsichtlich der Nahvisus (UCNVA: MD = 0,12 logMAR, p < 0,00001) und der Brillenunabhängigkeitsrate (OR = 0,26, p = 0,02) überlegen. Dagegen gab es keine signifikanten Unterschiede zwischen den Gruppen beim Fernvisus (UDVA) und Intermediärvisus (UIVA), und der Quality-of-Vision-Score war bei trifokalen IOLs signifikant höher (MD = 1,24, p = 0,03). 5)
In einer systematischen Übersichtsarbeit zu trifokalen IOLs war die intermediäre Sehschärfe mit trifokalen IOLs signifikant besser als mit bifokalen (DCIVA: MD −0,16 logMAR, 95 % KI −0,22 bis −0,10), jedoch gab es keine signifikanten Unterschiede bei CDVA, Fernvisus, Nahvisus, Kontrastempfindlichkeit oder Patientenzufriedenheit. 4)
Extended Depth of Focus (EDOF) IOLs verteilen das Licht nicht auf einen einzelnen Brennpunkt, sondern auf einen kontinuierlichen Fokusbereich und bieten so eine große Tiefenschärfe (Depth of Focus) von der Ferne bis in den mittleren Bereich. Das erste Produkt mit CE-Kennzeichnung erschien 20144). Zu den repräsentativen Produkten gehören TECNIS Symfony (J&J Vision), TECNIS Eyhance und AcrySof IQ Vivity (Alcon).
上述のメタ解析(22 試験)では EDOF IOL は三焦点 IOL と比較して遠方矯正視力(CDVA: MD = −0.01 logMAR、p = 0.01)でわずかに優れ、グレア・ハローの頻度に両群間の有意差はなかった。5) ESCRS ガイドラインは、EDOF IOL を「中間視力を重視しつつ光学的副作用を最小化したい患者への選択肢」として推奨している。4) EDOF IOL(AcrySof IQ Vivity)を評価した米国登録試験では、最低矯正遠方視力(BCVA)は単焦点対照群と同等(モノキュラー CDVA 0.00 logMAR)であり、メソピックコントラスト感度の低下は中等度にとどまった。17)
→ 詳細は 多焦点眼内レンズ を参照。
角膜の正乱視を補正するために設計された IOL で、光学部の弱主経線にマーキングが施されており、このマークを角膜強主経線に一致させて囊内固定する。軸が 1° ずれるごとに矯正効果は約 3.3% 減少し、30° 軸がずれると矯正効果が消失するのみならず、非トーリック IOL と比較してかえって視機能が低下する可能性がある。
トーリック IOL の適応基準の目安(施設ごとに設定):
ESCRS ガイドライン(2024)は、角膜乱視 1.0 D 以上の眼でトーリック IOL を考慮することを推奨し、2.0 D 以上では強いエビデンス(GRADE ++)がある。4) 13 試験のメタ解析では、トーリック IOL は非トーリック IOL(弛緩切開あり/なし)と比較して術後 UDVA(MD −0.07 logMAR、95% CI −0.10〜−0.04)および 20/25 未達率(RR 0.59、95% CI 0.50〜0.70)で優れていた。14)
Zinn 小帯脆弱・後囊破損症例や散瞳不十分例は正確な軸合わせが困難なため適応外となる場合が多い。計算には各メーカー提供のオンラインカリキュレーター、または装置内蔵の Barrett Toric 式・Haigis-T 式を用いる。
→ 詳細は トーリック眼内レンズ を参照。
水晶体を保持したまま虹彩後面・毛様溝に固定する IOL で、屈折矯正手術の一形態である。代表的なものは ICL(Implantable Collamer Lens; EVO+ ICL)で、コラマー素材でできた後房型 PIOL であり、高い生体適合性を持つ。角膜を削らず可逆性があり、中等度から強度近視まで幅広く対応できる。
Gemäß den Leitlinien der Japanischen Ophthalmologischen Gesellschaft für refraktive Chirurgie (8. Auflage) liegt das empfohlene Alter für eine phake Intraokularlinsen-Operation grundsätzlich zwischen 21 und 45 Jahren, und die indizierte Refraktionsmenge ist eine Myopie von 6 D oder mehr. Bei mittlerer Myopie von 3 bis unter 6 D und hoher Myopie über 15 D ist Vorsicht geboten. Zusätzlich zu den Kontraindikationen, die denen der Excimer-Laser-Chirurgie ähneln (aktive äußere Augenentzündung, Katarakt, Uveitis usw.), sind flache Vorderkammer, Hornhautendothelstörungen und progressiver Keratokonus zusätzliche Kontraindikationen. 6)
Zu den obligatorischen präoperativen Untersuchungen gehören die Hornhautendothelzellendichtemessung, die Bildanalyse des vorderen Augenabschnitts (einschließlich Vorderkammertiefe) und die Messung des Hornhautdurchmessers (horizontaler Durchmesser). 6)
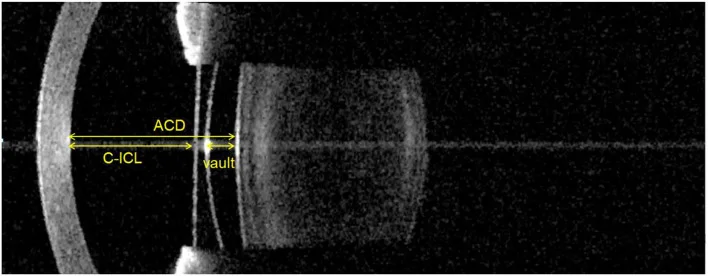
→ Einzelheiten finden Sie unter Phake Hinterkammerlinse (ICL).
Es handelt sich um eine zusätzliche IOL, die über einer bestehenden monofokalen IOL im Sulcus ciliaris fixiert wird. Auch bei Augen, die bereits eine monofokale IOL erhalten haben, kann damit nachträglich eine Presbyopie-, Astigmatismus- und Myopiekorrektur vorgenommen werden. Der Abstand zur intrakapsulären IOL ist relativ konstant, und die Langzeitstabilität gilt als gut.
→ Einzelheiten finden Sie unter Add-on Intraokularlinse.
| Typ | Fokusbereich | Kontrastempfindlichkeit | Blendung und Halos | Astigmatismuskorrektur | Versicherungsabdeckung | Zusätzliche Kosten (beide Augen) |
|---|---|---|---|---|---|---|
| Monofokal | 1 Punkt (Ferne oder Nähe) | ◎ | Keine | △ (torisch separat) | ○ (Wahlleistung) | 0 bis einige zehntausend Yen |
| Bifokal (Beugungstyp) | Fern + Nah | ○ | ++ (mäßig) | △〜○ | × | 300.000 bis 500.000 Yen |
| Trifokal | Fern+mittel+Nah | ○ | ++ (mäßig) | △〜○ | × | 40-60万 Yen |
| EDOF | Fern~Mittel (kontinuierlich) | ◎~○ | + (leicht) | △~○ | × | 35~55 Mio. Yen |
| Torisch (monofokal) | 1 Punkt (Fernpriorität) | ◎ | Keine | ◎ | × (ausgewählte Behandlung) | 10–150.000 Yen |
| Phake (PIOL/ICL) | Ferne (keine Hornhautkorrektur nötig) | ◎ | Keine | EVO+ : △~○ | × | 500.000 ~ 700.000 Yen |
| Add-on | Bestehende IOL + Alterssichtkorrektur | ○ | + | ○ | × | 300.000–450.000 ¥ |
Die Kosten sind eine grobe Schätzung für beide Augen bei Selbstzahlung. Sie variieren stark je nach Einrichtung und gewählter Linse.
Die IOL-Auswahl wirkt sich direkt auf das postoperative Sehen aus, daher ist eine sorgfältige präoperative Abklärung der Erwartungen unerlässlich. Die ESCRS-Leitlinien zum Grauen Star stellen klar: „Die Bewertung der Patientenerwartungen und eine detaillierte Einwilligung nach Aufklärung sind die wichtigsten Voraussetzungen für eine angemessene IOL-Auswahl.“ 4) Zu erfassende Informationen:
Geeignete Bedingungen für multifokale IOLs (trifokal, EDOF):
Eine Metaanalyse hat gezeigt, dass die Austauschrate von IOLs innerhalb eines Jahres steigt, wenn die Brillenabhängigkeit nach Implantation einer multifokalen IOL nicht behoben ist oder optische Nebenwirkungen nicht nachlassen. 3)
Torische IOLs sind wirksam zur Korrektur des regulären Hornhautastigmatismus, es gelten jedoch einige Voraussetzungen.
Um den Einfluss des hinteren Hornhautastigmatismus zu berücksichtigen, wird die Verwendung der Barrett-Toric-Formel oder der in optischen Achslängenmessgeräten integrierten Haigis-T-Formel empfohlen. 7) Da die okulare Zyklotorsion zwischen sitzender und liegender Position im Durchschnitt 4–5° beträgt, verbessern fotografische Markierungen oder die automatische Ausrichtung durch bildgeführte Systeme (CALLISTO eye, VERION) die Genauigkeit. Eine prospektive Studie, die bildgeführte Systeme mit manueller Markierung verglich, zeigte im bildgeführten System eine signifikant geringere postoperative Restastigmatismen (0,33 D vs. 0,51 D, p = 0,003). 19)
Für Personen, die nachts viel Auto fahren oder präzise Seharbeiten verrichten, ist eine monofokale IOL möglicherweise besser geeignet. Umgekehrt kommt für diejenigen, die ein breites Entfernungsspektrum (Smartphone, Computer, Lesen) ohne Brille bewältigen möchten, eine multifokale IOL in Frage. Allerdings können bestimmte Augenerkrankungen (Makulopathien, Glaukom, trockenes Auge usw.) eine multifokale IOL ausschließen. Die präoperative Beratung mit dem behandelnden Arzt ist von größter Bedeutung.
精密な IOL 度数計算には、光学式眼軸長測定装置による複数パラメータの同時計測が標準となっている。光学式は超音波 Aモード法と比較して測定誤差が小さく、国内では 2010年に「光学的眼軸長測定」として保険収載された後、急速に普及した。FD(フーリエドメイン)方式の採用により測定成功率が従来の約 90% から 98% 程度に向上し、測定値の標準偏差も 0.02 mm に収まるようになっている。7)
| 装置 | 測定方式 | 主な搭載機能 |
|---|---|---|
| IOLMaster 700 (Carl Zeiss) | SS-OCT (Swept-Source) | Axiale Länge, Hornhautbrechkraft, Vorderkammertiefe, Linsendicke, Hornhautdurchmesser, Goldstandard |
| ARGOS (Santen/Santek) | FD-OCT (Segmentverfahren) | Individuelle Messung des Brechungsindex jedes Gewebes. Tendenz zu kürzerer axialer Längenmessung als IOLMaster 700 |
| OA-2000 (Tomey) | FD-OCT | Parallele Anzeige von B-Scan-Bild und A-Scan-Wellenform |
| Ultraschall-A-Mode-Verfahren | Ultraschall (1.550 m/s) | Für alle Fälle anwendbar, aber mit großen Fehlern (gilt als Ursache der Mehrheit der postoperativen Refraktionsfehler)7) |
Optische Geräte zeigen die Achsenlänge um 0,2–0,3 mm länger an als die Ultraschallmethode, daher ist die Verwendung von IOL-Konstanten (z. B. A-Konstante) zwingend erforderlich, die für das jeweilige Messgerät spezifisch sind. Da ARGOS das Segmentverfahren verwendet, sollte eine austauschbare Verwendung der IOL-Konstanten mit dem IOLMaster 700 vermieden werden. 7)
| Formel | Generation | Merkmale | Hauptanwendung |
|---|---|---|---|
| SRK/T-Formel | 3. Generation | In Japan zu über 90% verwendet. Umfangreiche klinische Erfahrung, A-Konstante | Erste Wahl für Augen mit standardmäßiger Achsenlänge (22-25 mm) |
| Haigis-Formel | 3. Generation | Verwendet die Vorderkammertiefe als unabhängige Variable. Drei Konstanten a0, a1, a2 (Optimierung an mindestens 200 Augen erforderlich) | Augen mit flacher/tiefer Vorderkammer |
| Barrett Universal II Formel | 4. Generation | Basiert auf der Theorie dicker Linsen. Gute Genauigkeit bei IOL mit niedriger Brechkraft. Kostenlose Berechnung auf der APACRS-Website. | Langes Auge, kurzes Auge, IOL mit niedriger Brechkraft |
| Hill-RBF | KI (maschinelles Lernen) | Mustererkennung aus Big Data. Keine Formel. | Langes Auge, hohe Myopie |
| Kane-Formel | KI (maschinelles Lernen + theoretische Formel) | Geschlecht wird ebenfalls als Variable verwendet | Extreme hohe Myopie (Achsenlänge ≥ 30 mm) |
In Japan wird die SRK/T-Formel der dritten Generation häufig verwendet, aber es ist wünschenswert, mehrere Berechnungsergebnisse in Abhängigkeit von der Achsenlänge und der Anatomie des vorderen Augenabschnitts (okuläre Biometrie) zu vergleichen. Bei etwa 15 % der Kataraktoperationskandidaten liegt eine nicht harmonische okuläre Biometrie zwischen Achsenlänge und Hornhautbrechkraft vor, daher ist bei der verwendeten Formel Vorsicht geboten. 7)
Eine multizentrische Studie mit 13.301 Augen zeigte, dass die Barrett Universal II-, Olsen- und Haigis-Formeln signifikant genauer waren als SRK/T, Holladay 1 und Hoffer Q (Holladay 2 mit vergleichbarer Genauigkeit) und dass Formeln der vierten Generation und neuer sowohl für lange als auch für kurze Achsenlängen überlegen waren. 15) Eine weitere Metaanalyse mit kurzen Achsenlängen (AL < 22 mm) ergab ebenfalls, dass Barrett Universal II im Vergleich zu Haigis und SRK/T eine signifikant geringere MAE aufwies (p < 0,05). 18)
強度近視(眼軸長 ≥ 30 mm)の 80 眼を対象とした研究では、AI 式(Kane・Hill-RBF)は SRK/T と比較して平均絶対誤差(MAE)が有意に小さく(Kane: 0.51 D vs. Hill-RBF: 0.52 D vs. Barrett Universal II: 0.66 D vs. SRK/T: 有意差あり、p < 0.05)、1.0 D 超の屈折誤差率も Kane・Hill-RBF は 7.5% に抑えられたのに対し SRK/T では 42.5% に達した。8) 眼軸長 ≥ 32 mm の眼では Kane 式が最も低い MAE(0.44 D)と MedAE(0.40 D)を達成した。8) 眼軸長 ≥ 28 mm を対象としたRong 2019の別報でも、Barrett Universal IIのMedAEは0.37 Dであり、Haigisの0.46 Dより有意に小さかった(p = 0.038)。眼軸長 ≥ 30 mmの眼では、Barrett Universal IIがHaigisより良好な精度を示した。16)
| 症例 | 推奨計算式 | 注意点 |
|---|---|---|
| 標準眼(AL 22〜25 mm) | SRK/T、Haigis、Barrett Universal II | 複数式で比較 |
| Langes Auge (AL > 26 mm) | Barrett Universal II, Hill-RBF, Kane | Genauigkeitsunterschied bei Niedrig-Power-IOL beachten15,16) |
| Kurzes Auge (AL < 22 mm) | Barrett Universal II, Haigis, Holladay 2 | Risiko hoher Refraktionsfehler. Großer ELP-Vorhersagefehler18) |
| Nach Hornhautrefraktionschirurgie (nach LASIK) | Haigis-L, Shammas No-history, Barrett True-K, OKULIX | Vergleich mehrerer Formeln mit dem ASCRS Online-Rechner9,20) |
| Ziliarsulkus-Fixation (extrakapsulär) | Korrektur um −1,0 D nach Berechnung mit SRK/T usw. | Bei langer Achse geringe Korrektur, bei kurzer Achse hohe Leistung mit −2,0 D |
| Intrasklerale Fixation (Pinzettenmethode) | Gleiche Korrektur wie bei extrakapsulärer Fixation | Unterschiedlich je nach Operationsmethode |
| Keratoconus, nach Hornhauttransplantation | Spezielle Formel (Seitz-Langenbucher etc.) oder Expertenurteil | Großer Fehler bei Standardformeln |
Nach LASIK weist die Hornhaut lokal eine abgeflachte Form auf, was zu einer Überschätzung der zentralen Brechkraft durch das Autokeratometer führt und eine postoperative hyperope Verschiebung verursacht. Auch ohne präoperative LASIK-Daten verwendbare Formeln (Haigis-L, Shammas No-history, Barrett True-K usw.) sind in verschiedenen optischen Biometriegeräten integriert, und der Vergleich mehrerer Formeln mit dem kostenlosen Online-Rechner der ASCRS ist eine empfohlene Maßnahme. 7,9) Eine Studie an 110 Augen nach LASIK zeigte, dass die alleinige Verwendung von Barrett True-K mit einem Biometer eine ähnliche Genauigkeit wie der Mittelwertansatz mehrerer Formeln aufweist (MAE 0,41 D vs. 0,42 D, p = 0,81), was auf eine zuverlässige Einzelanwendung hinweist. 20)
Vor der Operation wird der Zielrefraktionswert basierend auf dem Lebensstil, der Arbeit und den Hobbys des Patienten festgelegt (vorhergesagter Wert als sphärisches Äquivalent).
| Lebensstil | Empfohlener Zielrefraktionswert |
|---|---|
| Bevorzugung des Fernsehens (Autofahren, Sport) | Emmetropie (0,00 D) bis −0,25 D |
| Ausgeglichener Typ | −0,25 bis −0,50 D (leichte Myopie) |
| Nahsehpriorität (Lesen, Feinarbeit) | −1,50 bis −2,00 D (Monovisionskandidat) |
| Monovision (nicht-dominantes Auge) | −1,50 bis −2,00 D |
| Multifokale IOL (die meisten Produkte) | Emmetropie (±0,25 D erforderlich) |
Für die Berechnung einer torischen IOL sollten Formeln verwendet werden, die in das optische Achslängenmessgerät integriert sind (z. B. Haigis-T- oder Barrett-Toric-Formel), um den Aufwand der manuellen Eingabe von Messwerten zu vermeiden und Eingabefehler zu reduzieren. Das Grundprinzip ist die konsistente Verwendung der optischen Achslänge, der Hornhautbrechkraft und der IOL-Konstante. 7)
Ein geringer Refraktionsfehler (bis ±0,5 D) kann mit einer Brille korrigiert werden. Bei größeren Fehlern (≥ ±1,5 D) wird die Implantation einer Add-on-IOL oder ein IOL-Austausch in Betracht gezogen. Bei multifokalen IOLs kann selbst ein Fehler von weniger als 0,5 D die Patientenzufriedenheit erheblich beeinträchtigen, weshalb eine präzise präoperative Messung und die Wahl der Berechnungsformel besonders wichtig sind.
IOL 挿入後は本来の水晶体調節(毛様体筋収縮による厚みの変化)は消失する。しかし臨床上は「偽調節(pseudoaccommodation)」と呼ばれる現象が生じ、わずかな近方視が可能になることがある。偽調節は角膜の多焦点性・乱視・瞳孔のピンホール効果・IOL の球面収差などによって生じ、単焦点 IOL でも 0.5〜1.0 D 程度の偽調節が認められる場合がある。
単焦点 IOL では若年者の正常水晶体と同等かそれ以上のコントラスト感度が得られる。一方、多焦点 IOL は光分散によって高周波領域のコントラスト感度が低下する。軽度の白内障や IOL 挿入眼では、視力に変化がなくてもコントラスト感度が低下していることがある。三焦点 IOL と EDOF IOL のメタ解析(22 試験)では、コントラスト感度に両群間の有意差は認められなかった。5) 多焦点 IOL 全般(8 RCT 含む Cochrane メタ解析)においても、単焦点と比較してコントラスト感度はわずかに低下するが、その臨床的意義は不明確とされている。3)
術後 5 年以内に後発白内障(posterior capsule opacification; PCO)が発生すると、コントラスト感度が著しく低下することがある。疎水性アクリル IOL は親水性アクリルと比較して PCO 発生率が低いことが示されており、Square edge 光学部設計もその予防に有効である。10)
Ein Halo ist ein Lichtring, der um eine Lichtquelle herum sichtbar ist, und Blendung (Glare) ist eine durch Licht verursachte Blendung oder Trübung des Sichtfelds. Bei multifokalen IOLs treten Halos (RR 3,58; 95 %-KI 1,99–6,46) und Blendung im Vergleich zu monofokalen IOLs signifikant häufiger auf. 3) EDOF-IOLs haben weniger optische Nebenwirkungen als herkömmliche bifokale oder trifokale IOLs, verschwinden aber nicht vollständig. 5)
Gegenmaßnahmen:
Direkt nach dem Einsetzen einer ungefärbten IOL kann aufgrund der höheren Transmission kurzwelliger Lichts im Vergleich zur menschlichen Linse ein bläuliches Farbsehen (Zyanopsie) auftreten. Bei gefärbten (Gelbfilter-)IOLs wird dieses Phänomen reduziert. Innerhalb weniger Tage bis Wochen kommt es zur neuronalen Adaptation, sodass die meisten Patienten es nicht mehr wahrnehmen.
Punktförmige Reflexionen im optischen Teil hydrophober Acryl-IOLs werden als Glistenings bezeichnet. Tiefe werden als Glistenings, oberflächliche als Subsurface Nano Glistenings (SSNG) bezeichnet. Beide entstehen durch das Eindringen von Kammerwasser in kleine Hohlräume des optischen Materials und sind keine Materialdegeneration. Sie beeinträchtigen die Sehfunktion in der Regel nicht, jedoch wurde bei Patienten mit eingeschränkter Netzhautfunktion eine Verschlechterung des Sehvermögens berichtet. Bei aktuell erhältlichen IOLs wurde das Herstellungsverfahren verbessert, sodass diese Phänomene seltener auftreten. Bei hydrophilen Acryl-IOLs kann es bei längerer Nutzung zu Kalziumphosphatablagerungen auf der Oberfläche kommen, die eine starke Trübung (Kalziumablagerung) verursachen. 10)
Die moderne Kataraktchirurgie ist sehr sicher, aber ein Nachstar (laserbehandelbar) tritt bei etwa 20–40 % der Patienten 5 Jahre postoperativ auf. Schwerwiegende Komplikationen (Endophthalmitis, expulsive Blutung) sind selten (0,006–0,04 %). IOL-Dislokationen nehmen langfristig aufgrund von Alterung und Schwächung der Zonulafasern zu, insbesondere bei älteren Menschen, starker Kurzsichtigkeit und Pseudoexfoliationssyndrom ist Vorsicht geboten.
| Komplikation | Inzidenz (Richtwert) | Beschreibung | Behandlung |
|---|---|---|---|
| Nachstar (Hinterkapseltrübung) | 20–40 % nach 5 Jahren postoperativ | Proliferation von Linsenepithelzellen auf der Hinterkapsel hinter der IOL, was zu einer Verschlechterung der Sehfunktion führt | Nd:YAG-Laser-Hinterkapsulotomie |
| IOL-Dezentrierung oder -Luxation | Einige % pro Jahr bei Augen mit Zonula-Zinn-Schwäche | Ruptur der Zonula Zinn durch Alterung, Trauma oder Pseudoexfoliationssyndrom, wodurch die IOL in den Glaskörper fällt | Sklerale Fixation, Naht oder IOL-Austausch11) |
| Pupilleneinklemmung (Iris-Einklemmung) | Einige Prozent nach intrascleraler Fixation usw. | Zustand, bei dem der optische Teil der IOL vor die Pupille verlagert ist. | Mydriasis, Positionswechsel, Austausch gegen eine IOL mit großem Optikdurchmesser12) |
| IOL-Trübung | Hydrophobes Glistening : wenige % · Hydrophile Kalziumablagerung : nach einigen Jahren | Sehverschlechterung durch Materialveränderung | IOL-Austausch10) |
| Glaukom nach PIOL | Augeninnendruckerhöhung nach ICL 1-5% | Augeninnendruckerhöhung durch Kammerwinkelblockade und Pupillarblock | Präoperative Beurteilung der Vorderkammertiefe und regelmäßige postoperative Nachsorge13) |
IOL-Dezentrierung und -Luxation
Diagnose und Operationsindikation bei IOL-Abfall durch Zonulafaserriss. Auswahl der intrakleralen Fixation (Flanschmethode/Pinzettmethode).
IOL-Trübung
Mechanismen und Management von Glistening, SSNG, Kalziumablagerungen und Nachstar. Informationen, die die Wahl des IOL-Materials beeinflussen.
Biometrie (IOL-Stärkenberechnung)
Gleichzeitige präzise Messung von Achslänge, Hornhautbrechkraft und Vorderkammertiefe mit einem optischen Achslängenmessgerät. Biometrie zur IOL-Stärkenberechnung
Sklerale Fixation
Flansch- und Pinzettenmethode zur Implantation des IOL-Stützteils in die Sklera ohne Naht. Vermeidet Risiken von Endophthalmitis und Nahtdegeneration. Skleral fixierte IOL
Sanders DR, Retzlaff J, Kraff MC. Comparison of the SRK II formula and other second generation formulas. J Cataract Refract Surg. 1988;14(2):136-141.1)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapter 4.6: patient selection for correcting presbyopia. https://www.escrs.org/escrs-guideline-for-cataract-surgery/2)
de Silva SR, Evans JR, Kirthi V, Ziaei M, Leyland M. Multifocal versus monofocal intraocular lenses after cataract extraction. Cochrane Database Syst Rev. 2016;12(12):CD003169. doi:10.1002/14651858.CD003169.pub4. PMID:27943250; PMCID:PMC6463930.3)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapters 4.6-4.7 and 6.1-6.3. https://www.escrs.org/escrs-guideline-for-cataract-surgery/4)
Karam M, Alkhowaiter N, et al. Extended Depth of Focus Versus Trifocal for Intraocular Lens Implantation: An Updated Systematic Review and Meta-Analysis. J Refract Surg. 2022. 22 studies, 2200 eyes.5)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 日眼会誌. 2024;128(2):135-142.6)
Werner L. Intraocular lenses: overview of designs, materials, and pathophysiologic features. Ophthalmology. 2021;128(11):e74-e93.7)
Suzuki Y, Kamoi K, Uramoto K, Ohno-Matsui K. Artificial intelligence driven intraocular lens power calculation in extreme axial myopia. Sci Rep. 2025. 80 eyes, axial length ≥30.0 mm, Institute of Science Tokyo.8)
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern®. AAO; 2021.9)
Grzybowski A, Markeviciute A, Zemaitiene R. A narrative review of intraocular lens opacifications: update 2020. Ann Transl Med. 2020;8(22):1547. doi:10.21037/atm-20-4207. PMID:33313292; PMCID:PMC7729367.10)
Tripathi M, Rao S, Sinha R. Scleral-fixated IOLs - A comprehensive review of current practices and emerging trends. Indian J Ophthalmol. 2025;73(7):933-945. doi:10.4103/IJO.IJO_2812_24. PMID:40586185; PMCID:PMC12356440.11)
Choi SR, Jeon JH, Kang JW, Heo JW. Risk factors for and management of pupillary intraocular lens capture after intraocular lens transscleral fixation. J Cataract Refract Surg. 2017;43(12):1557-1562. PMID: 29335100. doi:10.1016/j.jcrs.2017.08.021.12)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 有水晶体眼内レンズ手術の禁忌・慎重事項. 日眼会誌. 2024;128(2):135-142.13)
Kessel L, Andresen J, Tendal B, Erngaard D, Flesner P, Hjortdal J. Toric intraocular lenses in the correction of astigmatism during cataract surgery: a systematic review and meta-analysis. Ophthalmology. 2016;123(2):275-286. doi:10.1016/j.ophtha.2015.10.002. PMID:26601819.14)
Melles RB, Holladay JT, Chang WJ. Accuracy of intraocular lens calculation formulas. Ophthalmology. 2018;125(2):169-178. doi:10.1016/j.ophtha.2017.08.027. PMID:28951074.15)
Rong X, He W, Zhu Q, et al. Intraocular lens power calculation in eyes with extreme myopia: comparison of Barrett Universal II, Haigis, and Olsen formulas. J Cataract Refract Surg. 2019;45(6):732-737.16)
McCabe C, Berdahl J, Reiser H, et al. Clinical outcomes in a U.S. registration study of a new EDOF intraocular lens with a nondiffractive design. J Cataract Refract Surg. 2022;48(11):1297-1304. PMID: 35616507. PMCID: PMC9622364. doi:10.1097/j.jcrs.0000000000000978.17)
Wang Q, Jiang W, Lin T, Wu X, Lin H, Chen W. Meta-analysis of accuracy of intraocular lens power calculation formulas in short eyes. Clin Exp Ophthalmol. 2018;46(4):356-363. doi:10.1111/ceo.13058. PMID:28887901.18)
Webers VSC, Bauer NJC, Visser N, et al. Image-guided system versus manual marking for toric intraocular lens alignment in cataract surgery. J Cataract Refract Surg. 2017;43(6):781-788. doi:10.1016/j.jcrs.2017.03.041. PMID:28732612.19)
Ferguson TJ, Downes RA, Randleman JB. IOL power calculations after LASIK or PRK: Barrett True-K biometer-only calculation strategy yields equivalent outcomes as a multiple formula approach. J Cataract Refract Surg. 2022;48(7):784-789. doi:10.1097/j.jcrs.0000000000000883. PMID:35067661.20)