Desplazamiento y luxación del LIO
Diagnóstico e indicaciones quirúrgicas para la caída del LIO por rotura de la zónula de Zinn. Selección de fijación intraescleral (técnica de flange, técnica de pinzas).

El lente intraocular (LIO) es un lente artificial que se coloca permanentemente dentro del ojo después de extraer el cristalino opaco durante la cirugía de cataratas. Un ojo con un LIO se denomina pseudofaquia. A diferencia de la corrección con gafas o lentes de contacto, el LIO se integra directamente en el sistema óptico del ojo, por lo que no se produce magnificación o minimización de la imagen, proporcionando la función visual más natural y fisiológica.
El LIO más utilizado actualmente es el LIO plegable, que consta de una óptica y hápticos. El diámetro óptico estándar es de 6.0 mm y se puede insertar a través de una incisión pequeña de 2.4–2.8 mm en la facoemulsificación (PEA) utilizando un inyector. En algunos casos difíciles, se utiliza un LIO de óptica grande de 7.0 mm, que mejora la visibilidad durante el examen de fondo de ojo y la estabilidad de centración durante la fijación extracapsular.
La clasificación por material se muestra a continuación.
| Material | Características | Indicaciones principales |
|---|---|---|
| Acrílico hidrofóbico | Menos opacificación capsular posterior. Cuidado con los destellos (glistenings). | Elección estándar actual |
| Acrílico hidrofílico | Alta biocompatibilidad. Riesgo de depósitos de calcio (opacificación del LIO) con uso prolongado. | LIO de diseño especial |
| Silicón | Buena plegabilidad. No apto en ojos con taponamiento interno con aceite de silicona. | Algunos PIOL |
| PMMA | Material rígido. Requiere ampliar la incisión a 5–7 mm. | LIO de fijación especial, implante secundario |
En cuanto a la estructura, existen lentes de una pieza, donde la óptica y los hápticos son del mismo material, y lentes de tres piezas, donde son de diferentes materiales. La lente de una pieza se usa típicamente para fijación dentro del saco capsular, mientras que la de tres piezas es adecuada para fijación fuera del saco, fijación escleral y sutura. Se debe tener cuidado porque si una lente de una pieza se fija erróneamente fuera del saco (en el surco ciliar), los hápticos pueden rozar el iris, causando dispersión de pigmento del iris e inflamación prolongada.
Los LIO esféricos producen aberración esférica, donde los puntos focales de los rayos paraxiales que pasan cerca del eje óptico y los rayos periféricos están desalineados. En contraste, los LIO asféricos reducen la aberración esférica al variar la curvatura de cada superficie refractiva para converger los rayos periféricos y paraxiales en el mismo punto focal. Actualmente, casi todos los LIO adoptan diseños asféricos, mejorando la sensibilidad al contraste. Sin embargo, los diseños asféricos aumentan la aberración tipo coma con descentración o inclinación, por lo que en casos con zónulas de Zinn débiles y fijación inestable del LIO, se puede optar por un LIO esférico.
Los LIO teñidos (con filtro amarillo) reducen la transmitancia de la luz de onda corta (luz azul), aproximándose a la transmitancia espectral del cristalino humano adulto, y se espera que reduzcan el riesgo de fototoxicidad retiniana.
En 1981, Sanders y colaboradores propusieron la fórmula SRK (Sanders-Retzlaff-Kraff), sistematizando el cálculo de la potencia del LIO1). En 1984, Mazzocco desarrolló el LIO plegable de silicona, abriendo el camino para la cirugía de pequeña incisión. Japón fue el primer país en aprobar los LIO plegables y desde entonces ha desempeñado un papel pionero internacional en el desarrollo de inyectores. En 1953, Strampelli realizó la implantación de un LIO de cámara anterior, pero 70–80% de los casos desarrollaron queratopatía bullosa años después, lo que llevó al fracaso; sin embargo, esto se convirtió en un motor para las mejoras posteriores en el diseño de los LIO.
El LIO más utilizado, diseñado para enfocar en un solo punto. Es la opción estándar cubierta por el seguro (tratamiento selectivo). Si se busca la emetropía postoperatoria, la visión de lejos es buena sin gafas, pero se necesitan gafas para leer para la visión de cerca. Sus ventajas son la mayor sensibilidad al contraste y mínimos deslumbramientos y halos nocturnos.
Las siguientes opciones están disponibles para el manejo de la presbicia postoperatoria:
→ Para más detalles, consulte Lente Intraocular Monofocal.
Las LIO multifocales proporcionan buena visión a múltiples distancias y son LIO premium destinadas a reducir la dependencia de gafas (independencia de gafas). Debido a que la eficiencia de la luz se distribuye, la sensibilidad al contraste puede disminuir y pueden aparecer deslumbramientos y halos; esto debe explicarse completamente antes de la cirugía. Son tratamientos electivos y requieren pago de bolsillo por parte del paciente.
Enfoca en dos puntos: lejos y cerca. Era algo inadecuado para distancias intermedias (p. ej., trabajo en computadora a 50–80 cm). Existen tipos difractivos (AcrySof IQ ReSTOR, TECNIS Multifocal) y refractivos.
En los tipos difractivos, la luz difractada de orden 0 enfoca en lejos y la de primer orden en cerca, mientras que la luz difractada de órdenes superiores (aproximadamente 18%) causa una reducción en la sensibilidad al contraste de alta frecuencia. Los diseños apodizados mejoran la visión de lejos en condiciones de poca luz al reducir la altura de los escalones en la periferia pupilar.
Un metanálisis que incluyó 8 ECA mostró que las LIO multifocales eran superiores a las monofocales en agudeza visual de cerca sin corrección (UCNVA, proporción de 6/6 o mejor: RR 0.20, IC 95% 0.07–0.58, 782 ojos) y en tasa de independencia de gafas (RR 0.63, IC 95% 0.55–0.73, 1000 ojos). Sin embargo, la frecuencia de halos (RR 3.58, IC 95% 1.99–6.46, 662 ojos) fue significativamente mayor con las LIO multifocales. 3)
Los LIOs trifocales enfocan en tres puntos: lejos, intermedio y cerca, y son actualmente la corriente principal de los LIOs multifocales. El primer LIO trifocal se introdujo clínicamente en 20104), y los productos representativos actuales incluyen AcrySof IQ PanOptix (Alcon), AT LISA tri (Carl Zeiss), FineVision (PhysIOL) y TECNIS Synergy (J&J Vision).
En un metanálisis de 22 ensayos con 2200 ojos, los LIOs trifocales fueron superiores a los LIOs EDOF en agudeza visual de cerca (UCNVA: DM = 0.12 logMAR, p < 0.00001) y tasa de independencia de gafas (OR = 0.26, p = 0.02). Mientras tanto, no hubo diferencias significativas entre los dos grupos en agudeza visual de lejos (UDVA) y agudeza visual intermedia (UIVA), y la puntuación de Calidad de Visión fue significativamente mayor para los LIOs trifocales (DM = 1.24, p = 0.03).5)
En una revisión sistemática de LIOs trifocales, los LIOs trifocales mostraron una agudeza visual intermedia significativamente mejor en comparación con los LIOs bifocales (DCIVA: DM −0.16 logMAR, IC 95% −0.22 a −0.10), pero no hubo diferencias significativas en CDVA, agudeza visual de lejos, agudeza visual de cerca, sensibilidad al contraste o satisfacción del paciente.4)
Los LIOs de profundidad de foco extendida (EDOF) distribuyen la luz en un rango focal continuo en lugar de un solo foco, proporcionando una amplia profundidad de foco desde lejos hasta intermedio. El primer producto en recibir la marca CE apareció en 20144). Los productos representativos incluyen TECNIS Symfony (J&J Vision), TECNIS Eyhance y AcrySof IQ Vivity (Alcon).
En el metanálisis mencionado (22 ensayos), los LIO EDOF fueron ligeramente superiores a los LIO trifocales en la agudeza visual corregida de lejos (CDVA: DM = −0.01 logMAR, p = 0.01), y no hubo diferencias significativas en la frecuencia de deslumbramiento y halos entre ambos grupos. 5) Las guías ESCRS recomiendan los LIO EDOF como “una opción para pacientes que priorizan la visión intermedia mientras minimizan los efectos secundarios ópticos”. 4) En un ensayo de registro estadounidense que evaluó el LIO EDOF (AcrySof IQ Vivity), la mejor agudeza visual corregida de lejos (BCVA) fue equivalente a la del grupo control monofocal (CDVA monocular 0.00 logMAR), y la reducción en la sensibilidad al contraste mesópica fue moderada. 17)
→ Para más detalles, consulte Lente Intraocular Multifocal.
Los LIO tóricos están diseñados para corregir el astigmatismo corneal regular. La óptica tiene marcas a lo largo del meridiano plano, y estas marcas se alinean con el meridiano corneal curvo durante la fijación en el saco capsular. Por cada 1° de desviación del eje, el efecto correctivo disminuye aproximadamente un 3.3%. Una desviación de 30° no solo elimina el efecto correctivo, sino que también puede empeorar la función visual en comparación con un LIO no tórico.
Criterios de indicación general para LIO tórico (varían según la institución):
Las guías ESCRS (2024) recomiendan considerar un LIO tórico en ojos con astigmatismo corneal ≥1.0 D, y hay evidencia fuerte (GRADE ++) para ≥2.0 D. 4) Un metanálisis de 13 ensayos mostró que los LIO tóricos fueron superiores a los no tóricos (con o sin incisiones relajantes) en la AVCD postoperatoria (DM −0.07 logMAR, IC 95% −0.10 a −0.04) y en la tasa de no alcanzar 20/25 (RR 0.59, IC 95% 0.50 a 0.70). 14)
Los casos con debilidad zonular, rotura capsular posterior o midriasis insuficiente a menudo están contraindicados porque es difícil alinear el eje con precisión. Para el cálculo, use la calculadora en línea de cada fabricante o la fórmula Barrett Tórica o Haigis-T incorporada en el dispositivo.
→ Para más detalles, consulte Lente intraocular tórica.
Es un LIO fijado en la cara posterior del iris o surco ciliar mientras se conserva el cristalino natural, y es una forma de cirugía refractiva. Un ejemplo representativo es el ICL (Implantable Collamer Lens; EVO+ ICL), un PIOL de cámara posterior hecho de material colámero con alta biocompatibilidad. No ablaciona la córnea, es reversible y puede usarse para un amplio rango de miopía moderada a alta.
Las Guías de Cirugía Refractiva de la Sociedad Japonesa de Oftalmología (8.ª edición) establecen que la edad recomendada para la cirugía de lente intraocular fáquica es de 21 a 45 años, y el rango refractivo indicado es miopía de 6 D o más. Se requiere precaución en miopía moderada de 3 a menos de 6 D y miopía alta superior a 15 D. Además de las mismas contraindicaciones que la cirugía con láser excimer (inflamación ocular externa activa, catarata, uveítis, etc.), la cámara anterior poco profunda, el daño endotelial corneal y el queratocono progresivo son contraindicaciones adicionales. 6)
Las evaluaciones preoperatorias esenciales incluyen la medición de la densidad de células endoteliales corneales, la imagenología del segmento anterior (incluyendo la profundidad de la cámara anterior) y la medición del diámetro corneal (horizontal). 6)
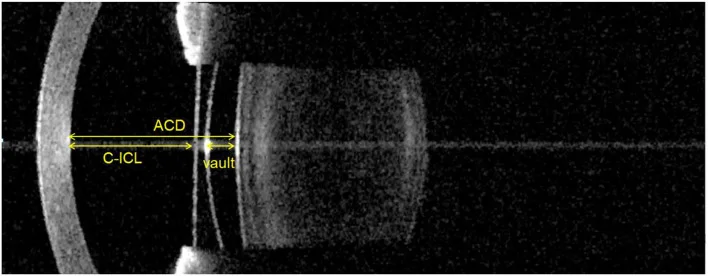
→ Para más detalles, consulte Lente fáquica de cámara posterior (ICL).
Es un LIO auxiliar que se coloca adicionalmente sobre un LIO monofocal existente, fijado en el surco ciliar. Incluso en ojos que han recibido previamente un LIO monofocal, permite la corrección de la presbicia, el astigmatismo y la miopía de forma retroactiva. La distancia con el LIO fijado en el saco capsular es relativamente constante y se considera que tiene una buena estabilidad a largo plazo.
→ Para más detalles, consulte LIO adicional.
| Tipo | Rango focal | Sensibilidad al contraste | Deslumbramiento/halo | Corrección del astigmatismo | Cobertura del seguro | Costo adicional estimado (ambos ojos) |
|---|---|---|---|---|---|---|
| Monofocal | 1 punto (lejos o cerca) | ◎ | Ninguno | △ (tórico por separado) | ○ (atención médica seleccionada) | 0 a decenas de miles de yenes |
| Bifocal (difractivo) | Lejos + Cerca | ○ | ++ (moderado) | △〜○ | × | 300,000–500,000 yenes |
| Trifocal | Lejos + Intermedio + Cerca | ○ | ++ (Moderado) | △〜○ | × | 40–60 mil yenes |
| EDOF | Lejos a intermedio (continuo) | ◎〜○ | + (leve) | △〜○ | × | 35–55 mil yenes |
| Tórica (monofocal) | 1 punto (prioridad de lejos) | ◎ | Ninguno | ◎ | × (tratamiento seleccionado) | 10–15 mil yenes |
| LIO fáquico (PIOL/ICL) | Lejos (sin corrección corneal) | ◎ | Ninguno | △~○ con EVO+ | × | 500,000–700,000 yenes |
| Adicional | LIO existente + corrección de presbicia | ○ | + | ○ | × | 300,000–450,000 yenes |
Los costos son estimaciones aproximadas para el tratamiento bilateral privado. Varían mucho según la instalación y el lente seleccionado.
La selección del LIO afecta directamente la visión postoperatoria, por lo que es esencial una cuidadosa confirmación de las expectativas del paciente antes de la cirugía. Las guías de cataratas de la ESCRS establecen que “la evaluación de las expectativas del paciente y el consentimiento informado detallado son los requisitos previos más importantes para una selección adecuada del LIO”. 4) Información a recopilar:
Condiciones adecuadas para LIO multifocales (trifocales/EDOF):
Los metanálisis han demostrado que la tasa de intercambio de LIO en el primer año aumenta cuando no se logra la independencia de gafas o los efectos secundarios ópticos no mejoran después de la implantación de una LIO multifocal. 3)
Las LIO tóricas son efectivas para corregir el astigmatismo corneal regular, pero existen varios requisitos previos.
Para considerar el efecto del astigmatismo corneal posterior, se recomienda utilizar la fórmula de Barrett Toric o la fórmula Haigis-T integrada en los biómetros ópticos. 7) Además, la ciclotorsión ocular entre la posición sentada y supina tiene un promedio de 4–5°, por lo que el marcado basado en fotografías o los sistemas de guía por imagen (CALLISTO eye, VERION) para la alineación automática del eje son útiles para mejorar la precisión. En un estudio prospectivo que comparó los sistemas de guía por imagen con el marcado manual, el grupo de guía por imagen tuvo un astigmatismo residual postoperatorio significativamente menor (0.33 D vs. 0.51 D, p = 0.003). 19)
Para quienes conducen con frecuencia de noche o realizan principalmente trabajos visuales de precisión, un LIO monofocal puede ser más adecuado. Por el contrario, para quienes desean manejar una amplia gama de distancias—como teléfonos inteligentes, computadoras y lectura—sin gafas, un LIO multifocal puede ser un candidato. Sin embargo, dependiendo de la condición ocular (enfermedad macular, glaucoma, ojo seco, etc.), los LIO multifocales pueden no ser apropiados. La consulta preoperatoria con el médico tratante es lo más importante.
Para un cálculo preciso de la potencia del LIO, la medición simultánea de múltiples parámetros con un biómetro óptico es el estándar. En comparación con el método de ultrasonido modo A, el biómetro óptico tiene un menor error de medición. En Japón, fue cubierto por el seguro como “medición óptica de la longitud axial” en 2010 y se difundió rápidamente. La adopción de la tecnología FD (dominio de Fourier) ha mejorado la tasa de éxito de la medición de aproximadamente 90% a 98%, y la desviación estándar de las mediciones ahora se encuentra dentro de 0.02 mm. 7)
| Dispositivo | Método de medición | Funciones principales |
|---|---|---|
| IOLMaster 700 (Carl Zeiss) | SS-OCT (fuente de barrido) | Longitud axial, poder refractivo corneal, profundidad de la cámara anterior, grosor del cristalino, diámetro corneal, estándar de oro |
| ARGOS (Santen/Santek) | FD-OCT (método de segmentos) | Mide el índice de refracción de cada tejido individualmente. Tiende a medir la longitud axial más corta que el IOLMaster 700 |
| OA-2000 (Tomey) | FD-OCT | Muestra la imagen de B-scan y la forma de onda de A-scan en paralelo |
| Método de modo A por ultrasonido | Ultrasonido (1,550 m/s) | Aplicable a todos los casos pero con gran error (considerado la causa de la mayoría de los errores refractivos postoperatorios)7) |
La biometría óptica muestra la longitud axial 0.2–0.3 mm más larga que la ecografía, por lo que es esencial usar constantes de IOL (como la constante A) específicas del dispositivo de medición. Dado que ARGOS utiliza un enfoque segmentado, se debe evitar el uso intercambiable de constantes de IOL con IOLMaster 700. 7)
| Fórmula | Generación | Características | Uso principal |
|---|---|---|---|
| Fórmula SRK/T | 3.ª generación | Utilizada en más del 90% de los casos en Japón. Amplia experiencia clínica, constante A | Primera línea para eje axial estándar (22–25 mm) |
| Fórmula de Haigis | 3.ª generación | Utiliza la profundidad de la cámara anterior como variable independiente. Tres constantes a0, a1, a2 (requiere optimización con ≥200 ojos) | Para cámaras anteriores poco profundas/profundas |
| Fórmula Barrett Universal II | 4.ª generación | Basada en la teoría de lentes gruesas. Buena precisión para LIO de baja potencia. Cálculo gratuito disponible en el sitio web de APACRS. | Eje largo, eje corto, LIO de baja potencia |
| Hill-RBF | IA (aprendizaje automático) | Reconocimiento de patrones a partir de grandes datos. No basada en fórmulas. | Eje largo, miopía alta |
| Fórmula de Kane | IA (aprendizaje automático + fórmula teórica) | El sexo también se utiliza como variable | Miopía alta extrema (longitud axial ≥ 30 mm) |
En Japón, la fórmula SRK/T de tercera generación se usa ampliamente, pero es recomendable comparar múltiples resultados de cálculo según la longitud axial y la anatomía del segmento anterior (biometría ocular). Aproximadamente el 15% de los pacientes que solicitan cirugía de cataratas presentan ojos con biometría irregular en cuanto a longitud axial y poder refractivo corneal, por lo que se debe tener precaución al seleccionar la fórmula de cálculo. 7)
Un estudio multicéntrico de 13,301 ojos mostró que las fórmulas Barrett Universal II, Olsen y Haigis eran significativamente más precisas que SRK/T, Holladay 1 y Hoffer Q (Holladay 2 tenía una precisión casi equivalente), y las fórmulas de cuarta generación en adelante fueron superiores tanto para longitudes axiales largas como cortas. 15) Otro metanálisis centrado en la longitud axial corta (AL < 22 mm) también encontró que Barrett Universal II tenía un MAE significativamente menor que Haigis y SRK/T (p < 0.05). 18)
En un estudio de 80 ojos con miopía alta (longitud axial ≥ 30 mm), las fórmulas de IA (Kane, Hill-RBF) mostraron un error absoluto medio (MAE) significativamente menor en comparación con SRK/T (Kane: 0.51 D, Hill-RBF: 0.52 D, Barrett Universal II: 0.66 D, SRK/T: diferencia significativa, p < 0.05). La tasa de error refractivo > 1.0 D se suprimió al 7.5% con Kane y Hill-RBF, mientras que alcanzó el 42.5% con SRK/T. 8) En ojos con longitud axial ≥ 32 mm, la fórmula Kane logró el MAE más bajo (0.44 D) y MedAE (0.40 D). 8) En otro informe de Rong 2019 dirigido a ojos con longitud axial ≥ 28 mm, el MedAE de Barrett Universal II fue de 0.37 D, significativamente menor que el de Haigis (0.46 D, p = 0.038). En ojos con longitud axial ≥ 30 mm, Barrett Universal II mostró mejor precisión que Haigis. 16)
| Caso | Fórmula recomendada | Notas |
|---|---|---|
| Ojo estándar (AL 22–25 mm) | SRK/T, Haigis, Barrett Universal II | Comparar múltiples fórmulas |
| Eje axial largo (AL > 26 mm) | Barrett Universal II, Hill-RBF, Kane | Tenga en cuenta las diferencias de precisión con LIO de baja potencia15,16) |
| Eje axial corto (AL < 22 mm) | Barrett Universal II, Haigis, Holladay 2 | Riesgo de error refractivo alto. Gran error de predicción de ELP18) |
| Después de cirugía refractiva corneal (post-LASIK) | Haigis-L, Shammas No-history, Barrett True-K, OKULIX | Comparar múltiples fórmulas con la calculadora en línea de ASCRS9,20) |
| Fijación en surco ciliar (extracapsular) | Calcular con SRK/T etc., luego ajustar −1.0 D | Para eje largo, baja potencia requiere menos ajuste; para eje corto, alta potencia requiere −2.0 D |
| Fijación intraescleral (método de pinzas) | Misma corrección que la fijación extracapsular | Varía según la técnica quirúrgica |
| Queratocono / postrasplante de córnea | Fórmula dedicada (Seitz-Langenbucher, etc.) o juicio de experto | Las fórmulas estándar tienen errores grandes |
Después de LASIK, la córnea presenta un aplanamiento local, por lo que la autoqueratometría tiende a sobreestimar el poder refractivo central, lo que provoca un desplazamiento hipermétrope postoperatorio. Incluso sin datos preoperatorios de LASIK, los biómetros ópticos incluyen fórmulas como Haigis-L, Shammas No-history y Barrett True-K, y comparar múltiples fórmulas mediante la calculadora en línea gratuita de la ASCRS (Sociedad Americana de Catarata y Cirugía Refractiva) es una estrategia útil. 7,9) En un estudio de 110 ojos post-LASIK, la precisión de Barrett True-K solo fue comparable al promedio de múltiples fórmulas (MAE 0.41 D vs. 0.42 D, p = 0.81), lo que demuestra su fiabilidad incluso en uso aislado. 20)
Antes de la cirugía, establezca la refracción objetivo basándose en el estilo de vida, trabajo y pasatiempos del paciente (valor predicho como equivalente esférico).
| Estilo de vida | Refracción objetivo recomendada |
|---|---|
| Prioridad de visión lejana (conducir, deportes) | Emmetropía (0.00 D) a −0.25 D |
| Tipo equilibrado | −0.25 a −0.50 D (ligera miopización) |
| Prioridad de visión cercana (lectura, trabajo detallado) | −1.50 a −2.00 D (candidato a monovisión) |
| Monovisión (ojo no dominante) | −1.50 a −2.00 D |
| LIO multifocal (la mayoría de los productos) | Emmetropía (debe estar dentro de ±0.25 D) |
Para el cálculo de LIO tórica, el uso de fórmulas integradas en los biómetros ópticos (como la fórmula Haigis-T o la fórmula Barrett Toric) elimina la necesidad de ingresar manualmente los valores de medición y reduce el riesgo de errores de entrada. El principio básico es utilizar de manera consistente la longitud axial óptica, la potencia corneal y las constantes de la LIO. 7)
Los errores refractivos leves (dentro de ±0.5 D) pueden corregirse con gafas. Para errores mayores (≥±1.5 D), considere agregar un IOL adicional o realizar un intercambio de IOL. Con los IOL multifocales, incluso errores menores de 0.5 D pueden reducir significativamente la satisfacción del paciente, por lo que las mediciones preoperatorias precisas y la selección cuidadosa de las fórmulas de cálculo son especialmente importantes.
Después de la implantación del LIO, se pierde la acomodación natural del cristalino (cambio de grosor por contracción del músculo ciliar). Sin embargo, clínicamente puede ocurrir un fenómeno llamado “pseudoacomodación”, que permite una ligera visión de cerca. La pseudoacomodación es causada por la multifocalidad corneal, el astigmatismo, el efecto estenopeico de la pupila y la aberración esférica del LIO. Incluso con LIOs monofocales, se puede observar una pseudoacomodación de aproximadamente 0.5 a 1.0 D.
Los LIOs monofocales proporcionan una sensibilidad al contraste igual o mejor que la de un cristalino joven normal. Por otro lado, los LIOs multifocales reducen la sensibilidad al contraste en el rango de alta frecuencia espacial debido a la dispersión de la luz. En ojos con catarata leve o implante de LIO, la sensibilidad al contraste puede estar reducida incluso si la agudeza visual no ha cambiado. Un metaanálisis de LIOs trifocales y LIOs EDOF (22 estudios) no encontró diferencias significativas en la sensibilidad al contraste entre ambos grupos. 5) En los LIOs multifocales en general (metaanálisis de Cochrane que incluye 8 ECA), la sensibilidad al contraste está ligeramente reducida en comparación con los monofocales, pero su significado clínico no está claro. 3)
Si se desarrolla opacificación de la cápsula posterior (OCP) dentro de los 5 años posteriores a la cirugía, la sensibilidad al contraste puede disminuir significativamente. Se ha demostrado que los LIOs acrílicos hidrofóbicos tienen una menor incidencia de OCP en comparación con los acrílicos hidrofílicos, y el diseño de borde cuadrado también es efectivo para prevenirla. 10)
El halo es un anillo de luz que se ve alrededor de una fuente de luz, y el deslumbramiento (glare) es el deslumbramiento o la opacidad visual causada por una fuente de luz. Con los LIO multifocales, los halos (RR 3.58; IC 95%: 1.99–6.46) y el deslumbramiento aumentan significativamente en comparación con los LIO monofocales. 3) Los LIO EDOF tienen menos efectos secundarios ópticos que los LIO bifocales o trifocales tradicionales, pero no desaparecen por completo. 5)
Estrategias de manejo:
Inmediatamente después de la inserción de un LIO no teñido, los pacientes pueden notar una tonalidad azulada en la visión (cianopsia) porque el LIO transmite más luz de onda corta que el cristalino humano natural. Los LIO teñidos (filtro amarillo) reducen este fenómeno. La adaptación neural ocurre en días o semanas, y la mayoría de los pacientes dejan de notarlo.
Los glistenings son reflejos puntiformes que se observan en la óptica de los LIO acrílicos hidrofóbicos. Los que ocurren en capas profundas se denominan glistenings, y los de la superficie, nano glistenings subsuperficiales (SSNG). Ambos se deben a la entrada de humor acuoso en pequeños espacios dentro del material óptico y no representan degradación del material. Por lo general, no afectan la función visual, aunque se ha informado disminución visual en pacientes con función retiniana reducida. Los LIO actualmente disponibles tienen procesos de fabricación mejorados que reducen estos fenómenos. En los LIO acrílicos hidrofílicos, puede depositarse fosfato de calcio en la superficie con el uso prolongado, causando opacificación severa (depósito de calcio). 10)
La cirugía moderna de cataratas es muy segura, pero la opacificación de la cápsula posterior (tratable con láser) ocurre en aproximadamente el 20–40% de los pacientes a los 5 años. Las complicaciones graves (endoftalmitis, hemorragia expulsiva) son raras, con una incidencia del 0.006–0.04%. El desplazamiento del LIO tiende a aumentar con el tiempo debido al envejecimiento y debilitamiento de las zónulas, especialmente en pacientes de edad avanzada, con miopía alta o síndrome de pseudoexfoliación.
| Complicación | Incidencia (aproximada) | Descripción general | Manejo |
|---|---|---|---|
| Opacificación de la cápsula posterior (catarata secundaria) | 20–40% a los 5 años postoperatorios | Las células epiteliales del cristalino proliferan en la cápsula posterior detrás del LIO, reduciendo la función visual | Capsulotomía posterior con láser Nd:YAG |
| Descentración o luxación del LIO | Varios por ciento por año en ojos con zónula debilitada | La rotura zonular por envejecimiento, traumatismo o síndrome de pseudoexfoliación provoca la caída del LIO en la cavidad vítrea | Fijación intraescleral, sutura o intercambio del LIO11) |
| Captura pupilar (captura del iris) | Unos pocos por ciento después de fijación intraescleral, etc. | Estado en el que la óptica del LIO se desplaza por delante de la pupila. | Midriasis, cambio postural, intercambio por LIO con diámetro óptico mayor12) |
| Opacificación del LIO | Glistening hidrofóbico: unos pocos %; depósito de calcio hidrofílico: varios años después | Disminución de la función visual debido a la degradación del material | Intercambio del LIO10) |
| Glaucoma después de PIOL | Elevación de la presión intraocular después de la cirugía ICL 1–5% | Cierre angular y bloqueo pupilar que causan elevación de la presión intraocular | Evaluación preoperatoria de la profundidad de la cámara anterior y manejo postoperatorio regular13) |
Desplazamiento y luxación del LIO
Diagnóstico e indicaciones quirúrgicas para la caída del LIO por rotura de la zónula de Zinn. Selección de fijación intraescleral (técnica de flange, técnica de pinzas).
Opacificación del LIO
Mecanismos y manejo de glistening, SSNG, depósitos de calcio y opacificación de la cápsula posterior. Información que influye en la selección del material del LIO.
Biometría (cálculo de potencia del LIO)
Medición simultánea precisa de la longitud axial, potencia corneal y profundidad de la cámara anterior mediante un biómetro óptico. Biometría para el cálculo de potencia del LIO
Fijación intraescleral
Técnica de flange y técnica con fórceps para implantar los hápticos del IOL en la esclera sin suturas. Evita riesgos de endoftalmitis y degradación de la sutura. IOL de fijación intraescleral
Sanders DR, Retzlaff J, Kraff MC. Comparison of the SRK II formula and other second generation formulas. J Cataract Refract Surg. 1988;14(2):136-141.1)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapter 4.6: patient selection for correcting presbyopia. https://www.escrs.org/escrs-guideline-for-cataract-surgery/2)
de Silva SR, Evans JR, Kirthi V, Ziaei M, Leyland M. Multifocal versus monofocal intraocular lenses after cataract extraction. Cochrane Database Syst Rev. 2016;12(12):CD003169. doi:10.1002/14651858.CD003169.pub4. PMID:27943250; PMCID:PMC6463930.3)
European Society of Cataract and Refractive Surgeons. ESCRS recommendations for cataract surgery. Draft version September 2024. Chapters 4.6-4.7 and 6.1-6.3. https://www.escrs.org/escrs-guideline-for-cataract-surgery/4)
Karam M, Alkhowaiter N, et al. Extended Depth of Focus Versus Trifocal for Intraocular Lens Implantation: An Updated Systematic Review and Meta-Analysis. J Refract Surg. 2022. 22 studies, 2200 eyes.5)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 日眼会誌. 2024;128(2):135-142.6)
Werner L. Intraocular lenses: overview of designs, materials, and pathophysiologic features. Ophthalmology. 2021;128(11):e74-e93.7)
Suzuki Y, Kamoi K, Uramoto K, Ohno-Matsui K. Artificial intelligence driven intraocular lens power calculation in extreme axial myopia. Sci Rep. 2025. 80 eyes, axial length ≥30.0 mm, Institute of Science Tokyo.8)
American Academy of Ophthalmology. Cataract in the Adult Eye Preferred Practice Pattern®. AAO; 2021.9)
Grzybowski A, Markeviciute A, Zemaitiene R. A narrative review of intraocular lens opacifications: update 2020. Ann Transl Med. 2020;8(22):1547. doi:10.21037/atm-20-4207. PMID:33313292; PMCID:PMC7729367.10)
Tripathi M, Rao S, Sinha R. Scleral-fixated IOLs - A comprehensive review of current practices and emerging trends. Indian J Ophthalmol. 2025;73(7):933-945. doi:10.4103/IJO.IJO_2812_24. PMID:40586185; PMCID:PMC12356440.11)
Choi SR, Jeon JH, Kang JW, Heo JW. Risk factors for and management of pupillary intraocular lens capture after intraocular lens transscleral fixation. J Cataract Refract Surg. 2017;43(12):1557-1562. PMID: 29335100. doi:10.1016/j.jcrs.2017.08.021.12)
日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第 8 版). 有水晶体眼内レンズ手術の禁忌・慎重事項. 日眼会誌. 2024;128(2):135-142.13)
Kessel L, Andresen J, Tendal B, Erngaard D, Flesner P, Hjortdal J. Toric intraocular lenses in the correction of astigmatism during cataract surgery: a systematic review and meta-analysis. Ophthalmology. 2016;123(2):275-286. doi:10.1016/j.ophtha.2015.10.002. PMID:26601819.14)
Melles RB, Holladay JT, Chang WJ. Accuracy of intraocular lens calculation formulas. Ophthalmology. 2018;125(2):169-178. doi:10.1016/j.ophtha.2017.08.027. PMID:28951074.15)
Rong X, He W, Zhu Q, et al. Intraocular lens power calculation in eyes with extreme myopia: comparison of Barrett Universal II, Haigis, and Olsen formulas. J Cataract Refract Surg. 2019;45(6):732-737.16)
McCabe C, Berdahl J, Reiser H, et al. Clinical outcomes in a U.S. registration study of a new EDOF intraocular lens with a nondiffractive design. J Cataract Refract Surg. 2022;48(11):1297-1304. PMID: 35616507. PMCID: PMC9622364. doi:10.1097/j.jcrs.0000000000000978.17)
Wang Q, Jiang W, Lin T, Wu X, Lin H, Chen W. Meta-analysis of accuracy of intraocular lens power calculation formulas in short eyes. Clin Exp Ophthalmol. 2018;46(4):356-363. doi:10.1111/ceo.13058. PMID:28887901.18)
Webers VSC, Bauer NJC, Visser N, et al. Image-guided system versus manual marking for toric intraocular lens alignment in cataract surgery. J Cataract Refract Surg. 2017;43(6):781-788. doi:10.1016/j.jcrs.2017.03.041. PMID:28732612.19)
Ferguson TJ, Downes RA, Randleman JB. IOL power calculations after LASIK or PRK: Barrett True-K biometer-only calculation strategy yields equivalent outcomes as a multiple formula approach. J Cataract Refract Surg. 2022;48(7):784-789. doi:10.1097/j.jcrs.0000000000000883. PMID:35067661.20)