角膜所见
角膜基质水肿:呈磨玻璃样角膜混浊。角膜厚度显著增加,有时超过800 μm。
Descemet膜皱褶:因内皮功能不全,角膜后表面形成皱褶。这是内皮损伤的重要指标。
上皮下水疱:在进展期,形成巨大水疱,破裂导致上皮缺损和疼痛。
实质瘢痕和血管侵入:慢性化导致周边部血管侵入和瘢痕性混浊,成为视力下降的原因之一。

大疱性角膜病变(bullous keratopathy)是由于角膜内皮细胞损伤导致角膜基质和上皮发生不可逆性水肿,随着病情进展,上皮下形成水疱(bulla)的病理状态。视力下降的主要原因是基质水肿,而疼痛则因上皮水疱破裂引起。
角膜内皮通过泵功能和具有选择性通透性的屏障功能,维持角膜基质含水量和角膜厚度的恒定。当内皮细胞密度低于400~500个/mm²时,泵功能失代偿,出现基质水肿,进一步进展则形成上皮水肿和水疱。由于角膜内皮细胞在前房内不分裂,因此损伤是不可逆的。
| 分类 | 代表性病因 |
|---|---|
| 医源性 | 白内障术后(人工晶体眼/无晶体眼)、激光虹膜切开术后、角膜移植术后排斥反应 |
| 变性/营养不良 | Fuchs角膜内皮营养不良、后部多形性角膜营养不良(PPCD)、ICE综合征 |
| 炎症性 | 疱疹性角膜内皮炎、巨细胞病毒性角膜内皮炎、特发性角膜内皮炎 |
| 外伤性 | 产钳分娩导致的Descemet膜破裂、角膜裂伤、钝挫伤 |
| 药物性 | 金刚烷胺、氯丙嗪、部分ROCK抑制剂滴眼液(如奈他舒地尔等) |
| 代谢/全身性 | 糖尿病、黏多糖贮积症、家族性高脂血症(LCAT缺乏症、Tangier病)、Schnyder角膜营养不良 |
假性晶状体眼大疱性角膜病变(PBK)发生在1-2%的白内障手术患者中,通常在术后8个月至7年内显现1)。随着白内障手术技术的进步,发病率呈下降趋势,但它与Fuchs角膜内皮营养不良一样,仍是角膜移植的主要适应症4,8)。
角膜内皮细胞密度随年龄增长生理性下降。新生儿为3,500-4,000 cells/mm²,20多岁时约2,700 cells/mm²,70岁以上平均降至约2,200 cells/mm²。正常生理下降率为每年0.5%,但白内障术后加速至每年约2%,青光眼术后加速至每年约10%。
Fuchs角膜内皮营养不良具有常染色体显性遗传背景,男女比例约为1:4,女性更常见4)。与白种人和黑种人相比,日本人中较少见,但其前驱阶段滴状角膜(cornea guttata)在白内障术前患者中观察到1.2%,随着寿命延长,日本也有增加趋势。
大疱性角膜病变是角膜疾病导致视力障碍的主要原因之一,也是全球角膜移植的主要适应症。由于白内障手术是全球最常进行的眼科手术,假性晶状体眼大疱性角膜病变在公共卫生方面也很重要。随着手术方式的微创化、粘弹性物质的改进以及超声波能量减少技术的进步,发病率逐年下降,但并未完全消失。近年来,超高龄患者白内障手术的增加以及术前存在Fuchs角膜内皮营养不良携带者被重新认识为风险因素。
角膜移植的主要适应症在全球范围内以Fuchs角膜内皮营养不良和假性晶状体眼大疱性角膜病变为主8)。日本角膜供体长期不足,高度依赖海外供体是其特点。根据近年国内统计,角膜移植总数中约40-50%为大疱性角膜病变(包括假性晶状体眼和无晶状体眼)。随着白内障手术的微创化,绝对数量有所减少,但仍是角膜移植的主要适应症。激光虹膜切开术(LI)后的大疱性角膜病变曾一度在日本多见,但随着向预防性白内障手术的转变而减少。
不,大疱性角膜病变是由角膜内皮细胞不可逆损伤引起的疾病,不会自然痊愈。人类角膜内皮细胞分裂和再生能力极差,一旦丢失无法恢复。根治性治疗是角膜内皮移植术,近年来利用培养角膜内皮细胞的再生医学也在逐步实用化。
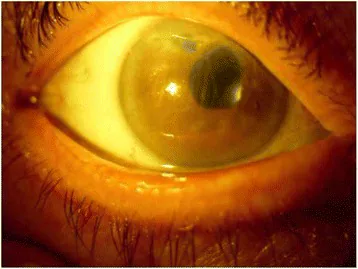
大疱性角膜病变的自觉症状因水肿程度和受累层次而异。
角膜所见
角膜基质水肿:呈磨玻璃样角膜混浊。角膜厚度显著增加,有时超过800 μm。
Descemet膜皱褶:因内皮功能不全,角膜后表面形成皱褶。这是内皮损伤的重要指标。
上皮下水疱:在进展期,形成巨大水疱,破裂导致上皮缺损和疼痛。
实质瘢痕和血管侵入:慢性化导致周边部血管侵入和瘢痕性混浊,成为视力下降的原因之一。
不同病因的特征性表现
Fuchs角膜内皮营养不良:从中央部滴状角膜(guttae)开始,进展后呈现锤击样外观。在镜面反射显微镜下观察为暗点。
假性晶状体眼性:确认人工晶状体的类型和位置。前房型IOL风险高,同时评估对侧眼的内皮状态。
盘状水肿:圆形局限的实质水肿和猪脂样角膜后沉着物提示疱疹性角膜内皮炎。
弥漫性水肿:从角膜缘到角膜缘的水肿提示中毒性前节综合征(TASS)或药物毒性7)。
裂隙灯检查中,如果观察到无炎症体征的实质水肿,首先考虑内皮功能不全。内眼手术后的实质水肿通常靠近切口部位,感染性角膜炎的浸润灶周围也可见实质水肿。荧光素染色时,上皮水疱部分表现为暗点。
提示角膜内皮异常的表现包括在角膜中央附近内皮面观察到的灰白色或褐色滴状物。滴状物扩大融合后呈现称为锤击样外观的特征性表现,在镜面反射法或内皮显微镜下表现为暗点。
大疱性角膜病变的进展大致可分为以下阶段。
各阶段的治疗策略不同。在实质水肿期之前,可以通过保守治疗和药物治疗进行观察,但进入水疱形成期后,需要疼痛管理和考虑内皮移植。
当角膜内皮功能下降时,闭眼(睡眠)期间泪液蒸发减少,角膜水肿容易积聚。白天,泪液蒸发从角膜中带走水分,减轻水肿,改善视力。这种模式是水疱性角膜病和早期Fuchs角膜内皮营养不良的典型症状。
角膜内皮细胞在体内不分裂或增殖。局部损伤通过邻近细胞的扩大和迁移来修复,但当密度降至一定水平以下时,会发生不可逆的代偿失调。水疱性角膜病的原因多种多样:医源性、退行性、外伤性、炎症性和药物性。最常见的是假性晶状体眼性水疱性角膜病(PBK)和Fuchs角膜内皮营养不良。
风险由白内障手术前后的因素决定。
前房型IOL(ACIOL)约14%合并PBK的报道,被认为比后房型IOL风险更高3)。术后内皮细胞减少率约为每年2.5%,是正常每年0.6%的约4倍,术后5年较术前减少约11%,10年以上减少约18.7%。
这是一种常染色体显性遗传的双侧进行性内皮疾病,角膜中央出现滴状角膜,并逐渐向周边扩展4)。通常50岁以下无症状,进展缓慢。随着病情进展,内皮的屏障功能和泵功能均下降,导致大疱性角膜病变。
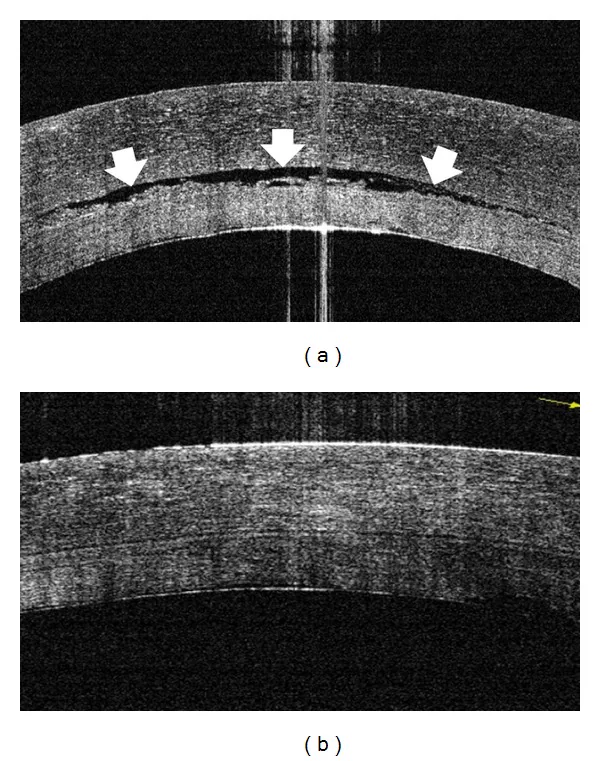
大疱性角膜病变的诊断基于临床发现,辅助检查评估内皮功能和水肿程度。
这是最基本的检查。通过后照法评估角膜混浊的范围和深度,通过巩膜散射法确认上皮水肿的扩散。使用镜面反射法,在Fuchs相关病例中可观察到内皮的锤击样外观。
水肿模式有助于推断病因。弥漫性水肿提示TASS或药物毒性,局部水肿提示Descemet膜脱离或器械接触,盘状水肿提示疱疹性角膜内皮炎。角膜移植眼中,扇形水肿和角膜后沉着物(Khodadoust线)提示排斥反应。
这是评估角膜内皮细胞密度和形态的核心检查。
| 指标 | 正常值 | 异常值 |
|---|---|---|
| 细胞密度 | 根据年龄为2,200–4,000 cells/mm² | 低于500 cells/mm²时难以维持透明性 |
| CV值(变异系数) | 0.2~0.3 | 0.35以上 |
| 六角形细胞出现率 | 60~70% | 50%以下 |
在轻症病例中,它对术前评估有用,但在严重水肿的病例中,成像变得困难。在这种情况下,接触型镜面显微镜或共聚焦显微镜是有用的。
它对水肿的定量评估至关重要。超声角膜测厚是一种快速且标准的检查,而眼前段OCT和Scheimpflug成像可以非接触地测量多个部位9)。
它可以高分辨率显示角膜各层,详细评估上皮下大疱的范围、基质增厚和Descemet膜异常。它有助于识别裂隙灯难以确认的结构异常9)。特别是,它可以广泛应用于术后评估、Descemet膜脱离的检测、上皮水肿范围的评估以及移植物粘附状态的确认。眼前段OCT是非接触式的,对患者负担小,也适合纵向观察。
在严重角膜水肿且镜面显微镜评估困难的病例中,共聚焦显微镜是有用的。它可以直接观察角膜内皮细胞形态,评估细胞密度和多形性。在研究用途中,它也用于观察神经丛、角膜细胞和免疫细胞。
在接受白内障手术的老年患者中,除了与年龄相关的自然减少外,并存的全身疾病和既往眼科手术或外伤史也会影响内皮细胞的状态。根据术前获得的镜面显微镜结果,估计手术预后和发生大疱性角膜病变的风险。特别是在内皮细胞密度≤1,000 cells/mm²、CV≥0.4、六角形细胞出现率<40%的病例中,术后失代偿的风险很高,需要手术方式的调整,如充分使用粘弹剂、最小化超声能量以及处理硬核。
怀疑大疱性角膜病变时,以下鉴别诊断很重要。
大疱性角膜病变的治疗根据内皮损伤的可逆性和视功能需求,结合内科治疗和外科治疗。
治疗以“去除病因”、“保护和恢复内皮功能”、“减轻水肿和疼痛”、“恢复视功能”为四大支柱。在内皮损伤可逆阶段(炎症性、药物性、术后一过性),消除病因有望减轻水肿。在不可逆阶段,以保守治疗的对症处理和外科治疗的根治为主。
作为内皮移植前的过渡,或手术困难病例的对症治疗进行。
Rho相关卷曲螺旋形成激酶(ROCK)抑制剂可促进角膜内皮细胞的增殖、迁移和粘附,并抑制凋亡。Erdinest等人报告,对常规保守治疗无效的3例PBK患者,使用利帕舒地尔0.4%滴眼液每日3次,持续3-11个月,所有病例均显示中央角膜厚度减少和矫正视力改善,避免了角膜移植10)。病例3在治疗11个月后,实质混浊完全消失,中央角膜厚度从582μm降至540μm,视力从0.3 logMAR改善至0.04 logMAR。
此外,有报道称,在高风险眼白内障术后12个月,围手术期使用利帕舒地尔的内皮细胞丢失率在利帕舒地尔组为4.5%,而对照组为12.8%,提示其可能具有预防性用途1)。
角膜内皮不可逆功能障碍的根治性治疗是角膜移植。
角膜内皮移植术(DSAEK·DMEK)
穿透性角膜移植术(PK)
适应证:适用于实质瘢痕或血管侵入严重,仅行内皮移植无法改善视力的病例。
特点:术后排斥反应风险高于内皮移植,需长期使用激素滴眼液管理。
注意事项:术后角膜强度降低,钝性外伤易导致创口裂开。
Sela等人的荟萃分析(8项研究,包括3项RCT、2项对侧眼研究和3项队列研究;376只眼:DMEK 187只,UT-DSAEK 189只)显示,12个月时logMAR BCVA在DMEK组显著更优(平均差−0.06,95%置信区间−0.10至−0.02)8)。然而,需要再次注气(rebubbling)的频率在DMEK组为19.79%,UT-DSAEK组为8.99%,DMEK组显著更高(OR 2.76,95%置信区间1.46–5.22)8)。有趣的是,当DSAEK植片厚度小于70 μm时,BCVA无显著差异,提示薄层化可能缩小两种术式的差距8)。
| 指标 | PK | DSAEK/UT-DSAEK | DMEK |
|---|---|---|---|
| 12个月BCVA | 恢复慢 | UT-DSAEK良好 | 最佳8) |
| 再次注气(空气再注入) | 不需要 | 约9% | 约20%8) |
| 5年排斥反应率 | 约22% | 约22% | 约2.8%9) |
| 植片脱离率 | 低 | 中等 | 相对较高3,9) |
| 术后抗外伤能力 | 低 | 良好 | 良好 |
术后6个月仍不改善的水肿病例被判断为内皮失代偿,适合进行角膜内皮移植9)。在小角膜或残留前房型人工晶体等复杂眼中也可实施DSAEK,有报告称无需更换人工晶体即可获得良好的视力恢复3)。
DMEK和DSAEK的选择基于患者是否存在复杂眼、术者经验、预期视力预后和术后管理体系。在复杂眼(广泛虹膜缺损、前房型人工晶体、玻璃体手术史、青光眼引流管植入眼、无晶体眼)中,移植片的展开和定位困难,因此DSAEK(或超薄DSAEK)更安全3,8)。另一方面,在无并发症的病例中,DMEK具有早期视力恢复和低排斥反应率的优点9)。
术后管理中,使用空气或气体(SF6、C3F8等)进行前房填塞,使移植片与后部基质紧密贴合。患者术后需保持仰卧位数天,若发生移植片脱离,则进行空气再注入(rebubbling)。术后类固醇滴眼液持续使用数月至一年以上以预防排斥,之后转为低剂量维持治疗。
Kinoshita等人开发了一种将培养的人角膜内皮细胞与ROCK抑制剂Y-27632一起注入前房的方法。据报道,在大疱性角膜病变的11只眼中,10只眼在5年后仍保持角膜透明,平均内皮细胞密度为1,257 cells/mm²14)。该疗法在日本经过II/III期临床试验后于2022年获得生产销售批准,作为弥补供体角膜不足的再生医疗而受到国际关注1,14)。
该疗法的步骤包括从供体角膜分离和培养内皮细胞,并将含有ROCK抑制剂Y-27632的细胞悬液注入前房。注入后,患者保持俯卧位(脸朝下)数小时,使细胞在重力作用下沉降并粘附于角膜内皮面。与传统的角膜内皮移植术相比,该疗法切口更小,且一个供体角膜可治疗多例患者,因此在有效利用供体角膜方面也具有重要意义。
治疗方案根据水肿进展程度、内皮细胞密度、视功能需求、合并症、全身状况和患者意愿综合判断决定。轻度和早期病例采用保守治疗或ROCK抑制剂滴眼液观察,中度和进展期病例考虑内皮移植。伴有实质混浊或血管侵入的进展期病例选择全层角膜移植。即使符合手术适应症的病例,若以疼痛为主诉且视力预后不佳,羊膜移植或治疗性PTK的对症治疗是有用的。
对于视力无改善希望且因水疱导致剧烈疼痛的病例,可选择前基质穿刺(ASP)、治疗性准分子激光角膜切除术(PTK)、羊膜移植等以缓解疼痛。
是的,2022年日本批准了培养角膜内皮细胞注射疗法的生产和销售。但可实施的设施有限,且有相应的适应症和标准。并非所有大疱性角膜病变患者都适用,需与主治医生商量判断是否可行。在角膜供体严重短缺的情况下,作为日本本土的再生医疗,其发展备受期待。
角膜通过维持约78%的含水量来保持透明性(脱水状态)。这种相对脱水状态由以下五个因素的平衡维持。
角膜内皮的水分调节由Maurice提出的泵漏机制解释。内皮细胞通过一级和二级主动转运机制驱动从角膜基质到前房的净离子流,形成渗透压梯度。这种泵功能主要依赖于HCO₃⁻和Cl⁻,Na⁺/K⁺-ATP酶起核心作用11)。
健康眼的吸水压IP表示为IP = IOP − SP,通常为约−35至−45 mmHg的负压。内皮功能障碍时,基质水分增加,SP下降;进一步进展时,SP低于IOP,IP转为正压。正压状态下,水分从基质被泵向上皮侧,形成上皮水肿和水疱。另一方面,高眼压(超过约50 mmHg)时,即使内皮健康,房水也可能被推入上皮层引起上皮水肿,但此时SP不变,不伴有基质水肿。
根据Tone等人的报告,Fuchs角膜内皮营养不良早期可见Na⁺/K⁺-ATP酶密度的代偿性增加,但随着病情进展逐渐下降11)。实时PCR检测到进展期病例中Na⁺/K⁺-ATP酶密度显著下调,同时MCT1和MCT4下调,证实内皮泵功能衰竭。角膜内皮通透性增加(屏障功能障碍)也被证明先于泵功能障碍发生11)。
白内障术后内皮细胞减少由多种机制引起。术中器械或IOL接触、超声波能量造成的机械性和物理性损伤是主要原因;虹膜损伤会升高前房内炎症细胞因子浓度,加速长期内皮细胞减少1,2)。
在IOL存在的情况下发生角膜水肿时,即使存在角膜内皮滴状物,也定义为PBK。与Fuchs角膜内皮营养不良不同,PBK的角膜水肿往往从周边开始并向中央进展。
当角膜内皮细胞密度低于约2,000 cells/mm²时,通透性逐渐增加,但通过代偿性泵机制,在约500–400 cells/mm²之前仍能维持去肿胀状态。低于此阈值时,很可能进展为大疱性角膜病变。但阈值存在个体差异,相同细胞密度下是否发生水肿取决于个体内皮功能。
角膜内皮细胞在前房环境中实际上不进行细胞分裂,当出现缺损时,通过周围细胞的扩大和迁移来覆盖。在此修复过程中,细胞面积增加,形状的异形性(pleomorphism)和大小不均(polymegethism)变得显著。通过镜面显微镜,这些变化被定量评估为CV值(变异系数)升高和六角形细胞出现率降低。在细胞密度较高时,泵功能得以维持,但一旦达到代偿极限,就会迅速转向水肿。内皮功能下降有时先于密度下降,仅凭密度的绝对值无法完全预测大疱性角膜病变的发生。
白内障手术及其他内眼手术后的慢性内皮细胞减少与前房内的炎症性细胞因子(TNF-α、IL-1、IL-6)有关。这些细胞因子诱导内皮细胞凋亡,降低屏障功能和泵功能。术后迁延性炎症是PBK的重要风险因素1)。
EndoArt(EyeYon Medical公司)是一种直径6.0毫米、厚度50微米的穹顶形人工内皮层,贴合角膜后表面曲率。由亲水性丙烯酸材料制成,采用类似DMEK的技术植入前房。由于是非生物材料,无需免疫抑制治疗,可长期保存。Auffarth等人报告了两例慢性角膜水肿患者移植EndoArt的情况,角膜厚度从病例1的730微米降至526微米,病例2的761微米降至457微米,并在17个月时保持稳定12)。已获得美国FDA突破性疗法认定,预计将应用于复杂眼(无虹膜、玻璃体切除术后、引流管植入眼)。
DSO是一种仅去除中央Descemet膜的手术方式,通过周边健康内皮细胞向中央迁移和再生来消退角膜水肿。早期Fuchs角膜内皮营养不良是其主要适应证,但近年来也有报道将其应用于MIGS管接触等局限性角膜水肿。Khan和Lin报告了一例因MIGS装置取出后Descemet膜剥离导致角膜水肿而行DSO的病例,偏心性descemetorrhexis后6周水肿消退,中央角膜内皮细胞密度从无法检测恢复到975 cells/mm²13)。ROCK抑制剂滴眼液(利帕舒地尔、奈他舒地尔)作为辅助治疗也在研究中。
针对Fuchs角膜内皮营养不良,靶向TCF4基因CTG重复扩增的反义寡核苷酸以及靶向氧化应激通路的分子治疗正处于基础研究阶段。氧化应激通路异常(Nrf2/NQO1信号下降、线粒体功能障碍)已被证明与细胞死亡有关,线粒体保护剂和抗氧化剂的应用正在研究中。
除了日本首创的培养角膜内皮细胞注射疗法外,其他国家也在推进使用iPS细胞和干细胞来源的角膜内皮细胞的研究。这种方法有可能用一只供体角膜治疗多只眼睛,有望解决全球角膜供体短缺问题1,14)。此外,关于ROCK抑制剂的长期疗效和安全性、内皮细胞迁移的定量评估以及最佳浓度和给药时间的临床试验正在进行中。
对于大疱性角膜病变的进展预测和治疗反应评估,正在研究中央角膜厚度的随时间变化、内皮细胞密度、前段OCT检测上皮水肿和微囊、泪液细胞因子浓度等。通过提高术前评估的准确性,有望早期为每位患者确定最佳治疗策略(继续保守治疗、ROCK抑制剂滴眼液、内皮移植、PK)。
大疱性角膜病变常双眼进展,对日常生活视功能的影响巨大。早晨视力下降会妨碍家务和通勤,进展后阅读、驾驶和精细工作变得困难。近年来,术前术后评估视功能相关患者报告结局(PROMs)的尝试正在推进,客观把握视功能相关生活质量的改善程度正被用作治疗选择的指标8)。内皮移植前后使用Visual Function Questionnaire-14和NEI VFQ-25进行的生活质量评估显示,DMEK组的改善程度更大8)。
大疱性角膜病变的治疗正从使用供体角膜的全层或内皮移植,向选择性细胞治疗、药物治疗和人工内皮装置多样化发展。日本首创的培养角膜内皮细胞前房内注射疗法是这一领域的先驱,作为解决全球供体角膜短缺问题的方案而备受关注。随着ROCK抑制剂滴眼液应用范围的扩大、EndoArt的临床普及、DSO适应症的扩展以及基因治疗的实用化,预计未来十年治疗选择将进一步扩大。通过早期诊断和分阶段治疗策略的建立,目标是减少角膜移植的需求,显著改善患者的视功能和生活质量。
Jukić A, Pavan J, Čapić Ivančić B, et al. RhoKinase (ROCK) Inhibition as a Therapeutic Strategy for Pseudophakic Bullous Keratopathy: A Comprehensive Review. J Clin Med. 2025;14(17):6093.
European Society of Cataract and Refractive Surgeons. ESCRS Clinical Guidelines for Cataract Surgery. 2024.
Singhal A, Kaushik J, Singh A, et al. Descemet Stripping Endothelial Keratoplasty in Microcornea for Pseudophakic Bullous Keratopathy With Anterior Chamber Intraocular Lens. Cureus. 2021;13(11):e19262.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Vandevenne MMS, Berendschot TTJM, Visser N, Dickman MM, Nuijts RMMA. Late-onset corneal edema after customized crosslinking for progressive keratoconus. Am J Ophthalmol Case Rep. 2024;35:102090.
Chu MJ, Song M, Palmares T, Song A, Song J. Rhopressa-induced corneal edema: a case report. J Med Case Rep. 2021;15:182.
Arici C, Mergen B, Kılıçarslan O, Ağaçhan A, Tülü Aygün B, Özdamar A. Diffuse corneal edema after uneventful pterygium surgery: toxic anterior segment syndrome or toxic keratopathy? Turk J Ophthalmol. 2022;52:69-71.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. BMJ Open Ophthalmol. 2023;8:e001397.
American Academy of Ophthalmology Cornea/External Disease PPP Panel. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2019.
Erdinest N, Shemesh N, Weill Y, et al. Managing pseudophakic bullous keratopathy with a topical rho kinase inhibitor: a case series. J Med Case Rep. 2025;19:214.
Tone SO, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: the vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Auffarth GU, Son HS, Koch M, et al. Implantation of an artificial endothelial layer for treatment of chronic corneal edema. Cornea. 2021;40:1633-1638.
Khan NC, Lin CC. Descemet stripping only for Descemet’s membrane detachment and sectoral corneal edema. Am J Ophthalmol Case Rep. 2023;29:101784.
Kinoshita S, Koizumi N, Okumura N, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.