
共聚焦显微镜(活体角膜共聚焦显微镜)
一目了然的要点
Section titled “一目了然的要点”1. 什么是共聚焦显微镜?
Section titled “1. 什么是共聚焦显微镜?”共聚焦显微镜是一种基于照明光和观察光共享同一焦面光学原理的高分辨率显微镜。在眼科领域,它应用于角膜的活体观察,也用于Fuchs角膜内皮营养不良等的评估 7)。
目前临床使用的主要设备有以下两种。
激光扫描型(HRT III-RCM):由Heidelberg Engineering公司制造。使用670 nm二极管激光作为光源,物镜63倍,观察视野400×400 μm。具有高分辨率,侧向分辨率1~2 μm,深度分辨率约4 μm 1)2)。通过PMA一次性帽(TomoCap)和眼科凝胶接触角膜使用。
裂隙扫描型(Confoscan 4):由Nidek公司制造。使用卤素光源,也可非接触使用。具备自动扫描功能,操作相对简单,但深度分辨率仅为25~27 μm。目前已停产。
IVCM具有三种成像模式。截面扫描获取单一深度的静态图像。体积扫描以2 μm间隔获取30~40张连续截面。序列扫描在同一深度获取最多100帧视频,适合观察动态变化。
IVCM需要专用设备和熟练的操作者,因此主要在大学医院和专科眼科机构引入。并非所有眼科都能进行,但在诊断角膜感染和角膜营养不良方面特别有用,必要时会转诊。
2. 主要所见和临床意义
Section titled “2. 主要所见和临床意义”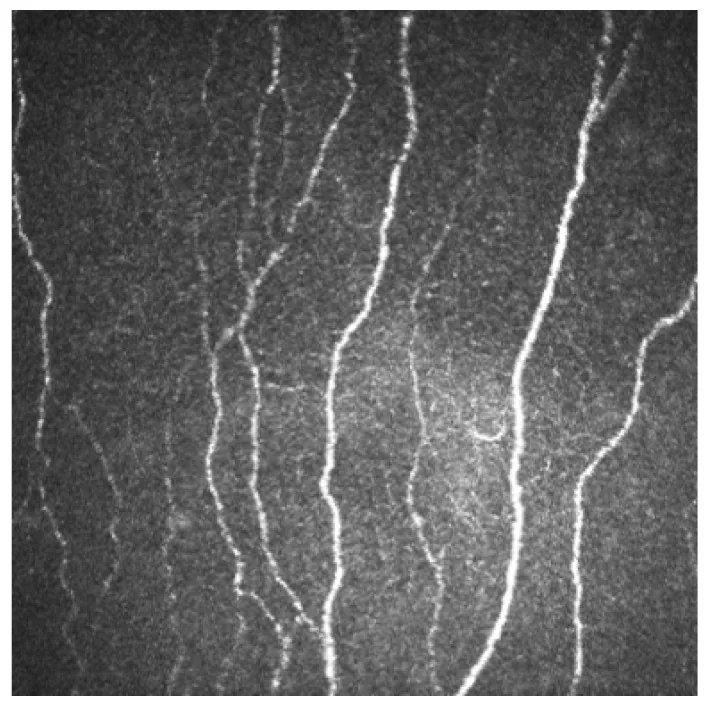
正常角膜所见
Section titled “正常角膜所见”IVCM可以分别观察角膜的各层。
角膜上皮:表层细胞呈多边形,40~50 μm。翼状细胞20~30 μm,细胞边界明亮,约5,000 cells/mm²。基底细胞8~10 μm,胞质暗,边界明亮(桥粒),呈蜂窝状。基底细胞密度为3,600~8,996 cells/mm²。
鲍曼层:观察为无结构的灰白色层,厚约10 μm。神经束穿行其中。
角膜基质:角膜基质细胞(角膜细胞)在非活跃状态时呈暗色,活跃状态时呈明亮的阿米巴样。前部基质细胞密度较高。
后弹力层:呈雾状层,厚6~10 μm。通常无法识别细胞结构。
角膜内皮:六角形细胞呈镶嵌排列。细胞直径约20 μm,密度2,550~2,720 cells/mm²,随年龄每年减少约0.6%。
角膜基底神经丛:在鲍曼层正下方观察为串珠状弯曲结构3)。在角膜中心鼻下方约1~2 mm处形成漩涡状图案。纤维直径0.52~4.6 μm。
树突状细胞(朗格汉斯细胞):角膜中央分布为34 ± 3 cells/mm²,周边为98 ± 8 cells/mm²。是免疫应答的指标。
角膜感染:真菌性角膜炎时,基质内可清晰观察到丝状菌丝8)。棘阿米巴以包囊(双层壁结构的球形)形式检出,但与炎症细胞的鉴别需要经验8)。细菌因菌体过小,直接可视化困难5)。
角膜营养不良:Avellino角膜营养不良(GCD2)中,基底上皮层可见高反射颗粒状沉积物,浅层至中层基质可见不规则高反射簇1)。格子状角膜营养不良I型以网状沉积物和分支纤维为特征1)。斑块状角膜营养不良可见边界不清的沉积物,Schnyder结晶状角膜营养不良可见针状结晶1)。
角膜扩张:圆锥角膜中可见角膜细胞密度降低,与严重程度相关。鲍曼层断裂也可见。PRK术后角膜扩张的特征是鲍曼层缺损和前部角膜细胞减少,与圆锥角膜的IVCM模式不同2)。
3. 检查技术与方法
Section titled “3. 检查技术与方法”IVCM检查步骤如下。
预处理:进行眼表麻醉(如奥布卡因)。将眼科凝胶涂抹于一次性TomoCap(PMMA材质)上,并安装到物镜前端。
检查实施:通过CCD摄像头监测镜头与角膜的接触情况,同时压平角膜。手动调整焦距,从角膜表层(0 μm)向深层依次观察。固视非常重要,需要患者的配合。检查时间约为5至15分钟。
并发症:偶有角膜上皮擦伤、感染(若存在已有上皮缺损则风险较高)发生。
| 项目 | HRT III-RCM | Confoscan 4 |
|---|---|---|
| 光源 | 二极管激光 | 卤素光 |
| 深度分辨率 | 4 μm | 25~27 μm |
| 接触 | 需要(TomoCap) | 可不需要 |
由于使用表面麻醉,检查过程中几乎没有疼痛。仅能感觉到角膜帽轻微接触。检查后可能出现短暂的异物感,但通常很快消退。
4. 光学原理与设备特点
Section titled “4. 光学原理与设备特点”共聚焦显微镜的基本原理是“共焦性”7)。照明系统和检测系统均具有针孔孔径,仅选择性检测来自物镜焦平面的反射光。焦平面外的散射光被针孔阻挡,从而获得高对比度和深度分辨率。
在激光扫描型(HRT III-RCM)中,670 nm二极管激光器作为点光源,逐点扫描角膜以构建图像。焦平面厚度(光学切片厚度)极薄,约4 μm,提供细胞水平的清晰横截面图像。
在裂隙扫描型(Confoscan 4)中,使用裂隙状光束进行扫描,因此仅在垂直于裂隙的方向上获得真正的共焦性。因此深度分辨率为25–27 μm,图像清晰度不如激光扫描型。
IVCM的局限性包括:仅灰度图像(无法彩色观察)、无法分辨细胞内结构、严重角膜混浊病例观察困难、难以精确定位观察部位、依赖检查者技能。
5. 主要临床应用
Section titled “5. 主要临床应用”IVCM的临床应用多种多样。
角膜感染的诊断辅助:作为培养检查的辅助手段有用。可检测真菌菌丝和棘阿米巴包囊,但判读结果需要专业知识8)。在疱疹性角膜炎中,可捕捉角膜神经的变化8)。在巨细胞病毒性角膜内皮炎中,有时可见猫头鹰眼样包涵体。
角膜营养不良的鉴别:每种营养不良具有特征性IVCM表现,可通过模式识别进行非侵入性鉴别1)。作为基因检测或活检前的筛查工具非常有用。也可用于评估治疗效果(PTK、DALK等)1)。
角膜缘干细胞缺乏症(LSCD)的评估:Vogt栅栏结构消失、结膜上皮替代角膜上皮、杯细胞出现是诊断依据6)。基底上皮细胞密度测量可定量评估LSCD严重程度6)。
角膜水肿和内皮疾病的评估:IVCM可通过中度角膜水肿观察内皮细胞,因此在镜面显微镜难以拍摄的病例中特别有用7)。在Fuchs角膜内皮营养不良(FECD)中,除评估内皮细胞外,还可捕捉神经密度降低和树突状细胞密度变化7)。
角膜神经评估:对基底下神经丛的定量评估用于神经营养性角膜病变的诊断和治疗效果判定3)。在角膜神经移植术后的神经再生评估中,IVCM可在术后6个月至1年确认再生表现3)。
全身性自身免疫性疾病的早期发现:在干燥综合征中,角膜中央神经纤维密度降低和活化树突状细胞增加可能在临床症状出现前被检测到4)。当中央角膜存在2个以上具有3个以上突起的活化树突状细胞时,对全身性免疫疾病的敏感性为60%,特异性为77%4)。
术后评估:用于LASIK、PRK术后角膜瓣边缘、鲍曼层变化及神经再生的随访观察2)。也应用于角膜移植术后排斥反应的早期检测。
6. 最新研究与未来展望
Section titled “6. 最新研究与未来展望”自动图像分析:已开发出如ACCMetrics软件等基底下神经纤维自动定量系统2)。可客观计算神经纤维密度、分支密度、弯曲度等参数,减少观察者间差异。
疾病临床前阶段的检测:有报道称,在干燥综合征病例中,IVCM异常可在抗体阳性或临床症状出现前数年检测到4)。这表明IVCM可能成为自身免疫性疾病的筛查工具。
干眼的亚型分类:通过分析树突状细胞的形态和分布模式,可能有助于区分免疫介导性干眼和蒸发过强型干眼4)。
术后神经再生的监测:利用IVCM对角膜神经移植术和角膜交联术后的神经再生过程进行纵向追踪的研究正在进展中3)。未来有望作为治疗效果的客观终点指标。
人工智能的整合:利用深度学习开发IVCM图像的自动分类和自动诊断系统的工作正在进行中,预计将应用于感染的快速诊断和角膜营养不良的自动鉴别。
7. 参考文献
Section titled “7. 参考文献”-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
