
กล้องจุลทรรศน์คอนโฟคอล (กล้องจุลทรรศน์คอนโฟคอลกระจกตาในร่างกาย)
ประเด็นสำคัญโดยสังเขป
หัวข้อที่มีชื่อว่า “ประเด็นสำคัญโดยสังเขป”1. กล้องจุลทรรศน์คอนโฟคอลคืออะไร?
หัวข้อที่มีชื่อว่า “1. กล้องจุลทรรศน์คอนโฟคอลคืออะไร?”กล้องจุลทรรศน์คอนโฟคอลเป็นกล้องจุลทรรศน์ความละเอียดสูงที่อาศัยหลักการทางแสงที่ว่าแสงส่องสว่างและแสงที่สังเกตร่วมกันมีระนาบโฟกัสเดียวกัน ในจักษุวิทยา ใช้สำหรับสังเกตกระจกตาในร่างกาย และยังใช้ในการประเมินกระจกตาเสื่อมชนิด Fuchs endothelial dystrophy 7)
อุปกรณ์หลักที่ใช้ในทางคลินิกปัจจุบันมีสองประเภทดังนี้:
ชนิดสแกนด้วยเลเซอร์ (HRT III-RCM): ผลิตโดย Heidelberg Engineering ใช้เลเซอร์ไดโอด 670 นาโนเมตรเป็นแหล่งกำเนิดแสง เลนส์วัตถุ 63 เท่า ขอบเขตการมองเห็น 400 × 400 ไมโครเมตร มีความละเอียดด้านข้าง 1-2 ไมโครเมตร และความละเอียดเชิงลึกประมาณ 4 ไมโครเมตร 1)2) ใช้ร่วมกับฝาครอบแบบใช้แล้วทิ้งที่ทำจาก PMMA (TomoCap) และเจลสำหรับจักษุ สัมผัสกับกระจกตา
ชนิดสแกนแบบกรีด (Confoscan 4): ผลิตโดย Nidek ใช้แหล่งกำเนิดแสงฮาโลเจน สามารถใช้แบบไม่สัมผัส มีฟังก์ชันสแกนอัตโนมัติ ใช้งานค่อนข้างง่าย แต่ความละเอียดเชิงลึกเพียง 25-27 ไมโครเมตร ปัจจุบันหยุดผลิตแล้ว
IVCM มีโหมดการถ่ายภาพสามโหมด การสแกนส่วน ถ่ายภาพนิ่งที่ความลึกเดียว การสแกนปริมาตร ถ่ายภาพต่อเนื่อง 30-40 ส่วนที่ระยะห่าง 2 ไมโครเมตร การสแกนลำดับ ถ่ายวิดีโอสูงสุด 100 เฟรมที่ความลึกเดียวกัน เหมาะสำหรับสังเกตการเปลี่ยนแปลงแบบไดนามิก
IVCM ต้องใช้อุปกรณ์เฉพาะและผู้ตรวจที่มีความชำนาญ ดังนั้นจึงติดตั้งเป็นหลักในโรงพยาบาลมหาวิทยาลัยและศูนย์จักษุวิทยาเฉพาะทาง ไม่มีให้บริการในคลินิกตาทุกแห่ง แต่มีประโยชน์อย่างยิ่งในการวินิจฉัยการติดเชื้อที่กระจกตาและกระจกตาเสื่อม และผู้ป่วยจะถูกส่งต่อเมื่อจำเป็น
2. ผลการตรวจหลักและความสำคัญทางคลินิก
หัวข้อที่มีชื่อว่า “2. ผลการตรวจหลักและความสำคัญทางคลินิก”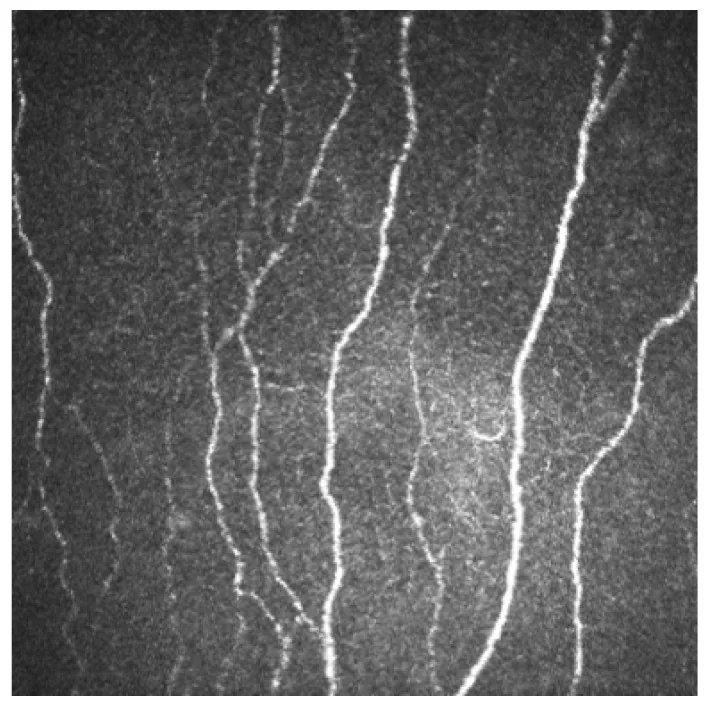
ผลการตรวจกระจกตาปกติ
หัวข้อที่มีชื่อว่า “ผลการตรวจกระจกตาปกติ”IVCM ช่วยให้สังเกตแต่ละชั้นของกระจกตาได้แยกกัน
เยื่อบุกระจกตา: เซลล์ผิวมีรูปหลายเหลี่ยม ขนาด 40–50 ไมโครเมตร เซลล์ปีกมีขนาด 20–30 ไมโครเมตร มีขอบเขตเซลล์ชัดเจน ประมาณ 5,000 เซลล์/ตร.มม. เซลล์ฐานมีขนาด 8–10 ไมโครเมตร มีไซโทพลาซึมสีเข้มและขอบสว่าง (เดสโมโซม) แสดงรูปแบบรังผึ้ง ความหนาแน่นของเซลล์ฐานคือ 3,600–8,996 เซลล์/ตร.มม.
เยื่อโบว์แมน: สังเกตเป็นชั้นสีเทาไม่มีโครงสร้างหนาประมาณ 10 ไมโครเมตร มีมัดประสาทวิ่งผ่าน
สโตรมาของกระจกตา: เซลล์สโตรมาของกระจกตา (เคอราโทไซต์) ปรากฏเป็นสีเข้มเมื่อไม่ทำงาน และสว่างเป็นรูปอะมีบาเมื่อถูกกระตุ้น ความหนาแน่นของเซลล์สูงกว่าในสโตรมาส่วนหน้า
เยื่อเดสเซเมต: สังเกตเป็นชั้นขุ่นมัวหนา 6–10 ไมโครเมตร โดยปกติไม่สามารถระบุโครงสร้างเซลล์ได้
เอ็นโดทีเลียมของกระจกตา: เซลล์รูปหกเหลี่ยมเรียงตัวแบบโมเสก เส้นผ่านศูนย์กลางเซลล์ประมาณ 20 ไมโครเมตร ความหนาแน่น 2,550–2,720 เซลล์/ตร.มม. ลดลงประมาณ 0.6% ต่อปีตามอายุ
ข่ายประสาทใต้ฐาน: สังเกตเป็นโครงสร้างโค้งคล้ายลูกปัดที่วิ่งอยู่ใต้เยื่อโบว์แมนโดยตรง 3) ก่อตัวเป็นรูปแบบก้นหอย (whorl pattern) ห่างจากศูนย์กลางกระจกตาประมาณ 1–2 มม. ทางด้านล่าง-จมูก เส้นผ่านศูนย์กลางเส้นใย 0.52–4.6 ไมโครเมตร
เซลล์เดนไดรต์ (เซลล์แลงเกอร์ฮานส์): กระจายตัว 34 ± 3 เซลล์/ตร.มม. ที่ศูนย์กลางกระจกตา และ 98 ± 8 เซลล์/ตร.มม. ที่รอบนอก เป็นตัวบ่งชี้การตอบสนองทางภูมิคุ้มกัน
ผลการตรวจที่ผิดปกติ
หัวข้อที่มีชื่อว่า “ผลการตรวจที่ผิดปกติ”การติดเชื้อที่กระจกตา: ในโรคกระจกตาอักเสบจากเชื้อรา จะสังเกตเห็นเส้นใยราแบบเส้นใยชัดเจนในสโตรมา 8) อะแคนทามีบาถูกตรวจพบเป็นซีสต์ (ทรงกลมผนังสองชั้น) แต่ต้องอาศัยประสบการณ์ในการแยกจากเซลล์อักเสบ 8) แบคทีเรียยากต่อการมองเห็นโดยตรงเนื่องจากเซลล์เดี่ยวมีขนาดเล็กเกินไป 5)
โรคกระจกตาเสื่อม: ในโรคกระจกตาเสื่อมชนิด Avellino (GCD2) มีการสะสมแบบเม็ดสะท้อนแสงสูงในชั้นเยื่อบุฐาน และกลุ่มก้อนสะท้อนแสงสูงรูปไม่สม่ำเสมอในสโตรมาชั้นตื้นถึงกลาง 1) โรคกระจกตาเสื่อมชนิดร่างแห type I มีลักษณะเฉพาะคือการสะสมแบบร่างแหและเส้นใยที่แตกแขนง 1) โรคกระจกตาเสื่อมชนิดจุดด่างแสดงการสะสมที่มีขอบเขตไม่ชัดเจน และโรคกระจกตาเสื่อมชนิดผลึก Schnyder แสดงผลึกรูปเข็ม 1)
ภาวะกระจกตาโป่งพอง: ในโรคกระจกตารูปกรวย มีความหนาแน่นของเคอราโทไซต์ลดลง ซึ่งสัมพันธ์กับความรุนแรง นอกจากนี้ยังพบการฉีกขาดของเยื่อโบว์แมน ในภาวะกระจกตาโป่งพองหลัง PRK มีลักษณะเฉพาะคือความบกพร่องของเยื่อโบว์แมนและการลดลงของเคอราโทไซต์ส่วนหน้า ซึ่งแสดงรูปแบบ IVCM ที่แตกต่างจากโรคกระจกตารูปกรวย 2)
3. เทคนิคและวิธีการตรวจ
หัวข้อที่มีชื่อว่า “3. เทคนิคและวิธีการตรวจ”ขั้นตอนการตรวจ IVCM มีดังนี้:
การเตรียมก่อน: หยอดยาชาเฉพาะที่ (เช่น ออกซิบูโปรเคน) ทาเจลสำหรับตาบน TomoCap แบบใช้แล้วทิ้ง (ทำจาก PMMA) และติดตั้งที่ปลายเลนส์วัตถุ
การตรวจ: กดกระจกตาแบบแอปพลาเนชันขณะตรวจสอบการสัมผัสระหว่างเลนส์กับกระจกตาด้วยกล้อง CCD ปรับโฟกัสด้วยมือ สังเกตตามลำดับจากชั้นผิวกระจกตา (0 ไมครอน) ไปยังชั้นลึก การจ้องตาคงที่สำคัญมาก ความร่วมมือของผู้รับการตรวจจำเป็น ระยะเวลาการตรวจประมาณ 5-15 นาที
ภาวะแทรกซ้อน: อาจเกิดการถลอกของเยื่อบุกระจกตา การติดเชื้อ (ความเสี่ยงสูงหากมีข้อบกพร่องของเยื่อบุอยู่ก่อน) ได้น้อยครั้ง
| รายการ | HRT III-RCM | Confoscan 4 |
|---|---|---|
| แหล่งกำเนิดแสง | เลเซอร์ไดโอด | แสงฮาโลเจน |
| ความละเอียดเชิงลึก | 4 ไมครอน | 25-27 ไมครอน |
| การสัมผัส | จำเป็น (TomoCap) | ไม่จำเป็นก็ได้ |
เนื่องจากใช้ยาชาหยอดตา จึงแทบไม่มีความเจ็บปวดระหว่างการตรวจ มีเพียงความรู้สึกสัมผัสเบาๆ ของฝาครอบกับกระจกตา อาจมีอาการระคายเคืองชั่วคราวหลังการตรวจ แต่โดยทั่วไปจะหายไปอย่างรวดเร็ว
4. หลักการทางแสงและลักษณะเฉพาะของอุปกรณ์
หัวข้อที่มีชื่อว่า “4. หลักการทางแสงและลักษณะเฉพาะของอุปกรณ์”หลักการพื้นฐานของกล้องจุลทรรศน์คอนโฟคอลคือ “การเป็นคอนโฟคอล” 7) ทั้งระบบให้แสงและระบบตรวจจับมีรูเข็ม ทำให้สามารถตรวจจับเฉพาะแสงที่สะท้อนจากระนาบโฟกัสของเลนส์ใกล้วัตถุได้อย่างเลือกสรร แสงกระเจิงจากภายนอกระนาบโฟกัสจะถูกกั้นโดยรูเข็ม ทำให้ได้คอนทราสต์สูงและความละเอียดเชิงลึกที่ดี
ในชนิดสแกนด้วยเลเซอร์ (HRT III-RCM) เลเซอร์ไดโอด 670 นาโนเมตรทำหน้าที่เป็นแหล่งกำเนิดแสงจุด สแกนกระจกตาทีละจุดเพื่อสร้างภาพ ความหนาของระนาบโฟกัส (ความหนาของภาพตัดขวางทางแสง) บางมากประมาณ 4 ไมโครเมตร ให้ภาพตัดขวางที่ชัดเจนในระดับเซลล์
ในชนิดสแกนด้วยช่องแสง (Confoscan 4) การสแกนทำด้วยลำแสงรูปช่อง ดังนั้นการเป็นคอนโฟคอลที่แท้จริงจะเกิดขึ้นเฉพาะในทิศทางตั้งฉากกับช่องแสงเท่านั้น ดังนั้นความละเอียดเชิงลึกคือ 25-27 ไมโครเมตร และความคมชัดของภาพด้อยกว่าชนิดสแกนด้วยเลเซอร์
ข้อจำกัดของ IVCM ได้แก่: ได้เฉพาะภาพระดับสีเทา (ไม่สามารถสังเกตสีได้), ไม่สามารถแยกแยะโครงสร้างภายในเซลล์, สังเกตได้ยากในกรณีกระจกตาขุ่นมัวรุนแรง, ยากต่อการระบุตำแหน่งที่สังเกตได้อย่างแม่นยำ, และขึ้นอยู่กับทักษะของผู้ตรวจ
5. การประยุกต์ใช้ทางคลินิกหลัก
หัวข้อที่มีชื่อว่า “5. การประยุกต์ใช้ทางคลินิกหลัก”การประยุกต์ใช้ทางคลินิกของ IVCM มีหลากหลาย
การช่วยวินิจฉัยการติดเชื้อที่กระจกตา: มีประโยชน์เป็นส่วนเสริมของการตรวจเพาะเชื้อ สามารถตรวจพบเส้นใยของเชื้อราและซีสต์ของอะแคนทามีบา แต่การแปลผลต้องอาศัยความรู้เฉพาะทาง 8) ในโรคเยื่อบุกระจกตาอักเสบจากเริม สามารถจับการเปลี่ยนแปลงของเส้นประสาทกระจกตาได้ 8) ในโรคเยื่อบุผนังกระจกตาอักเสบจากไซโตเมกาโลไวรัส อาจพบ owl’s eye inclusion body
การแยกโรคกระจกตาเสื่อม: โรคกระจกตาเสื่อมแต่ละชนิดมีลักษณะเฉพาะที่พบได้จาก IVCM ทำให้สามารถแยกโรคแบบไม่รุกล้ำโดยการจดจำรูปแบบ 1) มีประโยชน์สูงในการคัดกรองก่อนการตรวจทางพันธุกรรมหรือการตัดชิ้นเนื้อ นอกจากนี้ยังสามารถประยุกต์ใช้ในการประเมินผลหลังการรักษา (PTK, DALK ฯลฯ) 1)
การประเมินภาวะพร่องสเต็มเซลล์บริเวณลิมบัส (LSCD): การวินิจฉัยขึ้นอยู่กับการหายไปของโครงสร้างรั้ว Vogt, การแทนที่ของเยื่อบุกระจกตาด้วยเยื่อบุตาขาว, และการปรากฏของเซลล์กุณโฑ 6) สามารถวัดความหนาแน่นของเซลล์เยื่อบุฐานเพื่อประเมินความรุนแรงของ LSCD ในเชิงปริมาณ 6)
การประเมินอาการบวมน้ำที่กระจกตาและโรคเยื่อบุผนังกระจกตา: IVCM สามารถสังเกตเซลล์เยื่อบุผนังกระจกตาได้แม้ผ่านกระจกตาที่บวมน้ำระดับปานกลาง จึงมีประโยชน์อย่างยิ่งในกรณีที่กล้องจุลทรรศน์สเปคคูลาร์ถ่ายภาพได้ยาก 7) ในโรคกระจกตาเสื่อมฟุคส์ (FECD) นอกจากการประเมินเซลล์เยื่อบุผนังกระจกตาแล้ว ยังสามารถจับการลดลงของความหนาแน่นเส้นประสาทและการเปลี่ยนแปลงความหนาแน่นของเซลล์เดนไดรต์ 7)
การประเมินเส้นประสาทกระจกตา: การประเมินเชิงปริมาณของข่ายประสาทใต้ฐาน (subbasal nerve plexus) ใช้ในการวินิจฉัยโรคกระจกตาอักเสบจากเส้นประสาทเสื่อม (neurotrophic keratitis) และประเมินประสิทธิภาพการรักษา 3) หลังการผ่าตัดฟื้นฟูเส้นประสาทกระจกตา (surgical corneal neurotization) การตรวจ IVCM จะพบสัญญาณของการสร้างเส้นประสาทใหม่ในช่วง 6 เดือนถึง 1 ปีหลังผ่าตัด 3)
การตรวจพบโรคภูมิต้านตนเองทั่วร่างกายในระยะเริ่มต้น: ในกลุ่มอาการโจเกรน (Sjögren’s syndrome) การลดลงของความหนาแน่นเส้นใยประสาทบริเวณกลางกระจกตาและการเพิ่มขึ้นของเซลล์เดนไดรต์ที่ถูกกระตุ้นสามารถตรวจพบได้ก่อนการแสดงอาการทางคลินิก 4) หากพบเซลล์เดนไดรต์ที่ถูกกระตุ้นตั้งแต่ 2 เซลล์ขึ้นไปซึ่งมีส่วนยื่นตั้งแต่ 3 เส้นขึ้นไปบริเวณกลางกระจกตา มีรายงานความไว 60% และความจำเพาะ 77% สำหรับโรคภูมิคุ้มกันทั่วร่างกาย 4)
การประเมินหลังผ่าตัด: ใช้ในการติดตามการเปลี่ยนแปลงของขอบแผ่นปิดและเยื่อโบว์แมนหลังการทำ LASIK และ PRK รวมถึงการติดตามการสร้างเส้นประสาทใหม่ 2) นอกจากนี้ยังใช้ในการตรวจหาการปฏิเสธการปลูกถ่ายกระจกตาในระยะเริ่มต้น
6. งานวิจัยล่าสุดและแนวโน้มในอนาคต
หัวข้อที่มีชื่อว่า “6. งานวิจัยล่าสุดและแนวโน้มในอนาคต”การวิเคราะห์ภาพอัตโนมัติ: ได้มีการพัฒนาระบบวัดปริมาณเส้นใยประสาทใต้ฐานอัตโนมัติ เช่น ซอฟต์แวร์ ACCMetrics 2) ระบบจะคำนวณค่าพารามิเตอร์ต่างๆ เช่น ความหนาแน่นเส้นใยประสาท ความหนาแน่นของการแตกแขนง และความคดเคี้ยวอย่างเป็นกลาง ช่วยลดความแปรปรวนระหว่างผู้ตรวจ
การตรวจหาระยะก่อนแสดงอาการของโรค: ในผู้ป่วยกลุ่มอาการโจเกรน มีรายงานการตรวจพบความผิดปกติของ IVCM หลายปีก่อนที่แอนติบอดีจะเปลี่ยนเป็นบวกหรือมีอาการทางคลินิก 4) สิ่งนี้ชี้ให้เห็นว่า IVCM อาจเป็นเครื่องมือคัดกรองโรคภูมิต้านตนเอง
การจำแนกชนิดย่อยของโรคตาแห้ง: โดยการวิเคราะห์รูปร่างและรูปแบบการกระจายของเซลล์เดนไดรต์ อาจสามารถแยกความแตกต่างระหว่างตาแห้งที่เกิดจากภูมิคุ้มกันและตาแห้งชนิดระเหยเพิ่มขึ้น 4)
การติดตามการสร้างเส้นประสาทใหม่หลังผ่าตัด: กำลังมีการวิจัยเพื่อติดตามกระบวนการสร้างเส้นประสาทใหม่หลังการผ่าตัดฟื้นฟูเส้นประสาทกระจกตาหรือการเชื่อมขวางกระจกตาโดยใช้ IVCM ตามช่วงเวลา 3) ในอนาคต คาดว่าจะถูกใช้เป็นจุดสิ้นสุดเชิงวัตถุประสงค์สำหรับการประเมินประสิทธิภาพการรักษา
การบูรณาการปัญญาประดิษฐ์: กำลังมีการพัฒนาระบบจำแนกและวินิจฉัยภาพ IVCM อัตโนมัติโดยใช้การเรียนรู้เชิงลึก ซึ่งคาดว่าจะนำไปประยุกต์ใช้ในการวินิจฉัยการติดเชื้ออย่างรวดเร็วและการแยกแยะโรคกระจกตาเสื่อมโดยอัตโนมัติ
7. เอกสารอ้างอิง
หัวข้อที่มีชื่อว่า “7. เอกสารอ้างอิง”-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
