ภาวะพร่องสเต็มเซลล์ลิมบัส (LSCD ) เป็นโรคที่สเต็มเซลล์ของเยื่อบุกระจกตา หายไปหรือทำงานผิดปกติ
การบุกรุกของเยื่อบุตา ลงบนกระจกตา (conjunctivalization), หลอดเลือด新生ที่ผิว, และความขุ่นของกระจกตา ทำให้การมองเห็น บกพร่อง
สาเหตุหลักคือ แผลไหม้จากสารเคมี , ภาวะไม่มีม่านตา , คอนแทคเลนส์, และกลุ่มอาการสตีเวนส์-จอห์นสัน
การหายไปของ Palisades of Vogt (POV) เป็นกุญแจสำคัญในการวินิจฉัยทางคลินิก
การปลูกถ่ายกระจกตา เพียงอย่างเดียวไม่สามารถแก้ไขได้; การปลูกถ่ายสเต็มเซลล์ลิมบัส หรือการปลูกถ่ายเยื่อบุที่เพาะเลี้ยงเป็นหัวใจของการรักษา เยื่อบุกระจกตา เป็นเยื่อบุ squamous แบบชั้น (stratified squamous epithelium) ซึ่งจะถูกสร้างใหม่ทั้งหมดทุก 3 ถึง 10 วัน สเต็มเซลล์ที่สนับสนุนการสร้างใหม่ต่อเนื่องนี้อยู่ที่ลิมบัส ซึ่งเป็นรอยต่อระหว่างกระจกตา และเยื่อบุตา Palisades of Vogt (POV) ที่ Vogt บรรยายไว้ในปี 1921 คือ niche (สภาพแวดล้อมจุลภาค) ของสเต็มเซลล์เหล่านี้ 1)
ภาวะพร่องสเต็มเซลล์ลิมบัส (LSCD ) เป็นภาวะที่สเต็มเซลล์เหล่านี้หายไปหรือทำงานผิดปกติ ไม่ว่าจะเป็นมาแต่กำเนิดหรือเกิดขึ้นภายหลัง เมื่อความสามารถในการซ่อมแซมตัวเองของเยื่อบุกระจกตา หายไป จะเกิดการบุกรุกของเยื่อบุตา ลงบนกระจกตา (conjunctivalization) การ conjunctivalization มาพร้อมกับการพัฒนาของหลอดเลือด新生ที่ผิวและความขุ่นของกระจกตา นำไปสู่การบกพร่องทางการมองเห็น
ลิมบัส ยังทำหน้าที่เป็นเกราะป้องกันการบุกรุกของหลอดเลือดจากเยื่อบุตา เข้าสู่กระจกตา เมื่อเกราะนี้พังทลาย ความโปร่งใสของกระจกตา จะหายไป LSCD แสดงความรุนแรงตั้งแต่บางส่วน (conjunctivalization ไม่สมบูรณ์) ไปจนถึงรอบวง (conjunctivalization สมบูรณ์) 1) หากเหลือสเต็มเซลล์ลิมบัส เพียง 7% ก็สามารถสร้างเยื่อบุกระจกตา ขึ้นใหม่ได้ด้วยเทคนิคการผ่าตัดสมัยใหม่ 1)
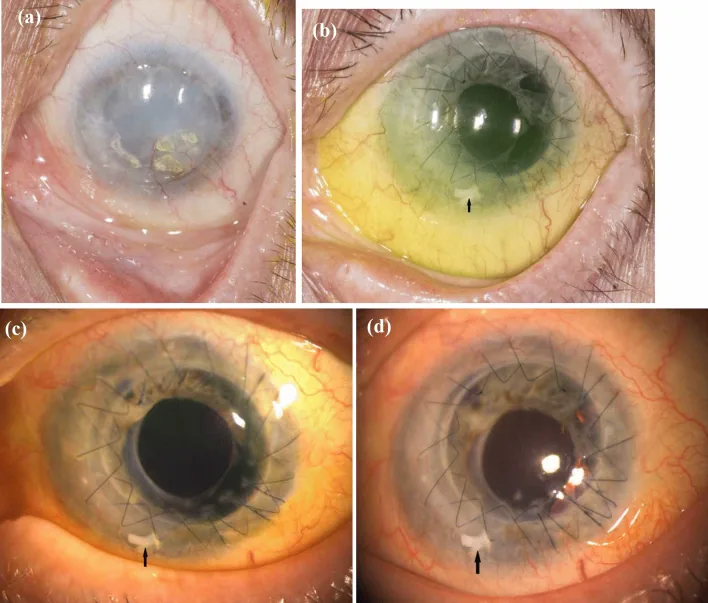
ภาพภาวะพร่องสเต็มเซลล์ลิมบัส Anja Viestenz, Christiane Kesper, Thomas Hammer, Joana Heinzelmann, et al. ALT (allogeneic limbal transplantation): a new surgical technique for limbal stem cell deficiency 2022 Aug 19 Int Ophthalmol. 2022 Aug 19; 42(12):3749-3762 Figure 3. PM
CI D: PMC9617846. License: CC BY.
a คือก่อนผ่าตัด กระจกตา ขุ่นมัวทั้งแผ่นและการบุกรุกของหลอดเลือดรุนแรง b ถึง d คือระยะหลังผ่าตัด ซึ่งการสร้างเยื่อบุผิวที่ผิวและการฟื้นคืนความใสดำเนินไป และสามารถเห็นรอยต่อของลิมบัส ที่ระบุด้วยลูกศร
ข้อร้องเรียนหลักคือปวดตา และการมองเห็น ลดลงเนื่องจากการสึกกร่อนของเยื่อบุผิวซ้ำๆ ความรู้สึกมีสิ่งแปลกปลอม การไม่ทนต่อคอนแทคเลนส์ กลัวแสง และน้ำตาไหลก็พบได้บ่อยเช่นกัน การแตกของสิ่งกีดขวางเยื่อบุผิวทำให้เกิดโรคกระจกตา อักเสบติดเชื้อได้ง่าย
การตรวจด้วยกล้องจุลทรรศน์ชีวภาพ (slit-lamp) พบอาการแสดงต่อไปนี้ตามลำดับขั้น 1)
เล็กน้อย : โรคเยื่อบุผิวแบบเกลียว (whorl-epitheliopathy) เมื่อย้อมด้วยฟลูออเรสซีน เยื่อบุผิวบางลงจากลิมบัส เข้าสู่ศูนย์กลางปานกลาง : การปรากฏของเส้นเลือดใหม่ที่ผิวและพานนัสบริเวณรอบนอกรุนแรง : การกลายเป็นเยื่อบุตา ของกระจกตา 360 องศา เส้นเลือดใหม่ในสโตรมา กระจกตา ขุ่นและเป็นแผลเป็น อาจนำไปสู่การทะลุของกระจกตา
ในฉันทามติระดับโลกที่เผยแพร่โดย Cornea Society ในปี 2019 ได้เสนอการจำแนกระยะทางคลินิกตามขอบเขตของความเสียหายของลิมบัส ขอบเขตของการเกี่ยวข้องของผิวกระจกตา และผลกระทบต่อแนวแกนการมองเห็น 1)
โดยปกติ POV จะมีอยู่รอบลิมบัส ทั้งหมด (สังเกตได้ง่ายที่ส่วนบนและส่วนล่าง) ใน LSCD POV จะหายไป อย่างไรก็ตาม ในเด็กอายุต่ำกว่า 10 ปีหรือผู้ที่มีอายุมากกว่า 70 ปี อาจสังเกต POV ได้ยากแม้ในภาวะปกติ
สาเหตุของ LSCD แบ่งเป็น กรรมพันธุ์ ภายหลังเกิด และไม่ทราบสาเหตุ 1)
ภายหลังเกิด (บาดเจ็บ, จากการรักษา, จากยา)
แผลไหม้จากสารเคมี LSCD ข้างเดียว การบาดเจ็บจากด่าง มักรุนแรงเป็นพิเศษ
คอนแทคเลนส์ : พบ LSCD ในผู้ใส่คอนแทคเลนส์ 2-5% 1) การกระตุ้นเชิงกลและสภาพแวดล้อมที่ขาดออกซิเจนทำลายเซลล์ต้นกำเนิดลิมบัส
เกิดจากยา : มีรายงานยา dupilumab3) , durvalumab5) , mitomycin C และ 5-FU (เมื่อใช้ร่วมกับการผ่าตัดต้อหิน ) และอื่นๆ
การผ่าตัดและการฉายรังสี : การผ่าตัดต้อเนื้อ การผ่าตัดต้อหิน การจี้เย็น การฉายรังสีภายนอก
การอักเสบ การติดเชื้อ พันธุกรรม
กลุ่มอาการสตีเวนส์-จอห์นสัน ลิมบัส ทั้งสองข้าง
ทางภูมิคุ้มกัน : โรคเพมฟิกอยด์ตา (MMP), โรคกราฟต์เวอร์ซัสโฮสต์ (GVHD)
การติดเชื้อ : เยื่อบุตาอักเสบ จากเริม โรคริดสีดวงตา อีสุกอีใส6)
พันธุกรรม : ภาวะไม่มีม่านตา (การกลายพันธุ์ PAX6) พบบ่อยที่สุด รวมถึงกลุ่มอาการ KID, ซีโรเดอร์มา พิกเมนโตซัม และอื่นๆ
ในการสำรวจทางระบาดวิทยาของ 738 ตาในระยะเวลา 14 ปีที่ศูนย์ตติยภูมิแห่งหนึ่ง สาเหตุของภาวะพร่องสเต็มเซลล์ลิมบัส ได้แก่ ภาวะไม่มีม่านตา 30.9%, สารเคมี/แผลไหม้จากความร้อน 20.6%, คอนแทคเลนส์ 16.8%, กลุ่มอาการสตีเวนส์-จอห์นสัน 10.4%1)
Mehta และคณะรายงานผู้ป่วยชายอายุ 56 ปีที่เกิดภาวะพร่องสเต็มเซลล์ลิมบัส ทั้งสองข้างและเยื่อตาติดลูกตาอย่างกว้างขวางหลังจากเริ่มใช้ dupilumab 57 เดือน เชื่อว่าการยับยั้งสัญญาณ IL-4/IL-13 ทำให้เซลล์กอบเล็ตลดลง กระตุ้นการอักเสบของผิวตา และการอักเสบเรื้อรังทำให้สเต็มเซลล์ลิมบัส หมดไป3)
Schumaier และคณะรายงานผู้ป่วยชายอายุ 65 ปีที่พบลักษณะคล้ายภาวะพร่องสเต็มเซลล์ลิมบัส ทั้งสองข้างและกระจกตา ทะลุตาซ้ายหลังจากเริ่มใช้ durvalumab 2 เดือนสำหรับมะเร็งปอดชนิดไม่ใช่เซลล์เล็ก กระจกตา แสดง PD-L1 สูง และการยับยั้งวิถี PD-1/PD-L1 อาจทำให้เกิดเยื่อบุตาอักเสบ จากภูมิคุ้มกันตนเอง การอักเสบของเยื่อบุตา หายไปหลังจากหยุด durvalumab5)
สวมแว่นตาป้องกันเมื่อจัดการกับสารเคมี
หลีกเลี่ยงการใส่คอนแทคเลนส์เป็นเวลานานหรือการดูแลที่ไม่เหมาะสม
แนะนำให้ตรวจตาโดยจักษุแพทย์ก่อนเริ่มใช้ยาใหม่ เช่น dupilumab
รักษาโรคอักเสบทั่วร่างกายอย่างเหมาะสมและป้องกันภาวะแทรกซ้อนทางตา
Q
คอนแทคเลนส์ทำให้เกิด LSCD ได้หรือไม่?
A
การใส่คอนแทคเลนส์เป็นเวลานานอาจเป็นสาเหตุของ LSCD โดยพบได้บ่อยในคอนแทคเลนส์ชนิดอ่อน มีรายงานว่าผู้ใส่คอนแทคเลนส์ประมาณ 2-5% มี LSCD ระยะเวลาใส่เฉลี่ยจนเกิด LSCD คือ 14-17 ปี เชื่อว่าการกระตุ้นเชิงกล ภาวะขาดออกซิเจน และสารกันเสียในน้ำยาล้างเลนส์ทำลายสเต็มเซลล์บริเวณลิมบัส
การวินิจฉัย LSCD อาศัยอาการทางคลินิกเป็นหลัก โดยใช้การตรวจต่างๆ เป็นเครื่องมือเสริม 1) .
วิธีการวินิจฉัย ข้อดี ข้อเสีย การตรวจเซลล์วิทยาแบบประทับ ตรวจพบเซลล์กุณโฑเพื่อยืนยันการเปลี่ยนเป็นเยื่อบุตา ขึ้นอยู่กับคุณภาพของตัวอย่าง กล้องจุลทรรศน์คอนโฟคัล สามารถประเมินเซลล์ทุกชั้นในเชิงปริมาณ ต้องให้ความร่วมมือ 5-15 นาที OCT ส่วนหน้าตาไม่สัมผัสและใช้เวลาสั้น ความละเอียดต่ำกว่ากล้องจุลทรรศน์คอนโฟคัล
ขั้นตอนการวินิจฉัย :
ยืนยันการหายไปของ POV ด้วยกล้องจุลทรรศน์ร่องกราด
ประเมินโรคเยื่อบุผิวแบบเกลียวหรือรูปแบบการเปลี่ยนเป็นเยื่อบุตา ด้วยการย้อมฟลูออเรสซีน
หากจำเป็น ทำการตรวจเซลล์วิทยาแบบประทับเพื่อตรวจหาเซลล์กุณโฑบนผิวกระจกตา (เครื่องหมายของการเปลี่ยนเป็นเยื่อบุตา )
ใช้กล้องจุลทรรศน์คอนโฟคอล เพื่อยืนยันความหนาแน่นของเซลล์เยื่อบุผิวฐานที่ลดลงและการมีเซลล์เปลี่ยนรูป
การวินิจฉัยแยกโรค ได้แก่ ต้อเนื้อ (มักจำกัดอยู่ด้านจมูก), เนื้องอกเยื่อบุผิวสความัสของผิวตา (OSSN ), และกระจกตา อักเสบติดเชื้อบริเวณรอบนอก
การรักษาจะดำเนินการเป็นขั้นตอนตั้งแต่การจัดการแบบประคับประคองไปจนถึงการผ่าตัด การปลูกถ่ายกระจกตา เพียงอย่างเดียวไม่มีข้อบ่งชี้ใน LSCD 2)
การรักษาแบบประคับประคอง
หยุดใช้คอนแทคเลนส์และกำจัดปัจจัยระคายเคือง : หาก “ความเครียดของเซลล์ต้นกำเนิดลิมบัส ” สามารถกลับคืนได้ อาจดีขึ้นด้วยการจัดการแบบประคับประคอง
น้ำตาเทียม : หล่อลื่นผิวตาด้วยยาหยอดบ่อยครั้งที่ปราศจากสารกันเสีย
ยาหยอดสเตียรอยด์ : ให้แบบพัลส์ระยะสั้นเพื่อควบคุมการอักเสบ
ยาหยอดไซโคลสปอรีน : ใช้เพื่อปรับภูมิคุ้มกันระยะยาว
ยาหยอดซีรั่มตนเอง : มีประโยชน์ในการส่งเสริมการหายของเยื่อบุกระจกตา
การรักษาโดยการผ่าตัด
การปลูกถ่ายเยื่อบุตา ขาวและลิมบัส ด้วยตนเอง (CLAu) : เก็บเนื้อเยื่อลิมบัส จากตาที่แข็งแรงใน LSCD ข้างเดียว อัตราความสำเร็จ 77-100%2)
การปลูกถ่ายเยื่อบุลิมบัส ที่เพาะเลี้ยง (CLET) : ชิ้นเนื้อเยื่อลิมบัส ขนาดเล็กถูกขยายในห้องปฏิบัติการและปลูกถ่าย
SLET (การปลูกถ่ายเยื่อบุลิมบัส แบบง่าย)
การปลูกถ่ายเยื่อบุช่องปากที่เพาะเลี้ยง (COMET) : สำหรับ LSCD สองข้าง ใช้เยื่อบุช่องปากของผู้ป่วยเองเป็นสิ่งทดแทน4)
อุปกรณ์เทียมกระจกตา (KPro) : ทางเลือกสุดท้ายสำหรับ LSCD รอบด้านอย่างรุนแรง
การปลูกถ่ายเยื่อบุกระจกตา ที่เพาะเลี้ยง (การแพทย์ฟื้นฟูของญี่ปุ่น) และการปลูกถ่ายเยื่อหุ้มน้ำคร่ำก็ทำเช่นกัน ในกรณีที่มีการอักเสบรุนแรงเช่น SJS อาจใช้ mitomycin C เพื่อยับยั้งไฟโบรบลาสต์
Booranapong และคณะทำการปลูกถ่ายแผ่นเยื่อบุช่องปากที่เพาะเลี้ยงในผู้ป่วยแผลไหม้จากสารเคมี 3 รายและกลุ่มอาการสตีเวนส์-จอห์นสัน 3 รายในประเทศไทย ผู้ป่วยแผลไหม้จากสารเคมี 2 รายได้ผลการประเมินดีเยี่ยมหลังจาก 1 ปี แต่ผู้ป่วยกลุ่มอาการสตีเวนส์-จอห์นสัน มีผลลัพธ์ไม่ดีเนื่องจากเยื่อบุช่องปากเสียหายและความมีชีวิตของเซลล์ต่ำ4)
การปลูกถ่ายกระจกตา (PKP ) เพียงอย่างเดียวเกือบเป็นข้อห้ามใน LSCD เนื่องจากกระจกตา ผู้บริจาคไม่มีเซลล์ต้นกำเนิดลิมบัส การปลูกถ่ายจะใสชั่วคราวแต่ในที่สุดปัญหาจะกลับมาอีก ต้องเติมเซลล์ต้นกำเนิดลิมบัส ก่อนและสร้างนิชของเยื่อบุกระจกตา ขึ้นใหม่ จากนั้นจึงทำการปลูกถ่ายกระจกตา แบบสองขั้นตอนหากจำเป็น
Q
รักษาให้หายได้ด้วยการปลูกถ่ายกระจกตาเพียงอย่างเดียวหรือไม่?
A
การปลูกถ่ายกระจกตา เพียงอย่างเดียวไม่สามารถรักษา LSCD ได้ สิ่งที่ให้ในการปลูกถ่ายกระจกตา คือสโตรมาและเอนโดทีเลียมของกระจกตา ไม่มีเซลล์ต้นกำเนิดเยื่อบุกระจกตา หลังปลูกถ่าย การขาดเซลล์ต้นกำเนิดยังคงอยู่ และการกลายเป็นเยื่อบุตา ขาวและความขุ่นของกระจกตา จะดำเนินต่อไป ทำให้การปลูกถ่ายล้มเหลว ขั้นแรกให้ทำการผ่าตัดเติมเซลล์ต้นกำเนิดลิมบัส เพื่อทำให้ผิวกระจกตา มั่นคง จากนั้นจึงทำการปลูกถ่ายกระจกตา แบบสองขั้นตอนหากจำเป็น
เซลล์ต้นกำเนิดเยื่อบุกระจกตา อยู่ในชั้นเซลล์ฐานภายใน POV การมีเม็ดสีของ POV ปกป้องเซลล์ต้นกำเนิดจากรังสีอัลตราไวโอเลต เซลล์ต้นกำเนิดเคลื่อนที่ในฐานะเซลล์ฐานเข้าสู่ศูนย์กลางกระจกตา แบบ centripetal มุ่งสู่ผิวขณะที่แยกความแตกต่าง และสุดท้ายหลุดลอก1)
สภาพแวดล้อมนิชของเซลล์ต้นกำเนิด : เซลล์ต้นกำเนิดลิมบัส ต้องการสารอาหารจากหลอดเลือดภายนอกกระจกตา ดังนั้นจึงอยู่บริเวณรอบนอกใกล้หลอดเลือด กระจกตา ไม่มีหลอดเลือดเพื่อรักษาความใส และเซลล์ต้นกำเนิดอยู่ในบริเวณรอยต่อนี้
กลไกการเกิด LSCD :
ความเสียหายของเยื่อบุลิมบัส (แผลไหม้จากสารเคมี การอักเสบ การกระตุ้นเชิงกล ฯลฯ)
การทำลายสภาพแวดล้อมจุลภาคของนิชสเต็มเซลล์ลิมบัส (ไซโตไคน์อักเสบ, เมทริกซ์เมทัลโลโปรตีเนส)
การลดลงของสเต็มเซลล์ → ความสามารถในการสร้างเยื่อบุกระจกตา ลดลง
เยื่อบุตา บุกรุกกระจกตา (conjunctivalization)การดำเนินไปของเส้นเลือด新生ชั้นผิว กระจกตา ขุ่น และแผลเป็น
สเต็มเซลล์ลิมบัส ไม่เพียงทำหน้าที่สร้างประชากรเยื่อบุกระจกตา ใหม่ แต่ยังทำหน้าที่เป็นเกราะป้องกันการบุกรุกของหลอดเลือดจากเยื่อบุตา เมื่อเกราะนี้สูญเสียไป จะเกิด conjunctivalization และเส้นเลือด新生 และความโปร่งใสของกระจกตา จะเสียหายอย่างถาวร
ใน LSCD บางส่วน เยื่อบุกระจกตา จะถูกส่งมาจากลิมบัส ที่แข็งแรงที่เหลืออยู่ ดังนั้นหากพื้นที่เสียหายจำกัด การพยากรณ์โรคค่อนข้างดี ใน LSCD รอบทั้งหมด การผ่าตัดเป็นสิ่งจำเป็น
รายงาน LSCD ที่เกิดจากยาใหม่ : มีรายงาน LSCD ที่เกิดจากสารยับยั้ง checkpoint ภูมิคุ้มกันและสารชีวภาพใหม่ เช่น dupilumab 3) 5) มีการเสนอว่า dupilumab ลดเซลล์กอบเล็ตผ่านการยับยั้ง IL-4/IL-13 ทำให้เกิดการอักเสบเรื้อรังของผิวตาและ LSCD 3) Durvalumab อาจทำลายเอกสิทธิ์ทางภูมิคุ้มกันของกระจกตา โดยการยับยั้ง PD-L1 ทำให้เกิด keratitis ภูมิต้านตนเอง 5)
รายงานสาเหตุใหม่ : Elmansouri และคณะรายงานกรณีแรกของเด็กอายุ 10 ปีที่พัฒนา LSCD หลังโรคอีสุกอีใส 6) ความตระหนักเกี่ยวกับ LSCD ที่เกิดจากการติดเชื้อไวรัสกำลังขยายตัว
เวชศาสตร์ฟื้นฟูโดยใช้เยื่อบุช่องปาก : การปลูกถ่ายแผ่นเยื่อบุช่องปากเพาะเลี้ยง (COMET) และ SOMET เป็นทางเลือกที่มีแนวโน้มสำหรับ LSCD สองตาเมื่อไม่มีผู้บริจาคลิมบัส 4) เนื่องจากเป็นเนื้อเยื่อตนเอง จึงไม่จำเป็นต้องกดภูมิคุ้มกัน และ SOMET ซึ่งไม่ต้องการโครงสร้างพื้นฐานการเพาะเลี้ยงเซลล์ สามารถทำได้ในสภาพแวดล้อมที่มีทรัพยากรจำกัด
การสร้างเยื่อบุกระจกตา ใหม่โดยใช้เซลล์ iPS : การใช้เซลล์ iPS (เซลล์ต้นกำเนิด pluripotent เหนี่ยวนำ) คาดหวังว่าจะเป็นวิธีการแก้ปัญหาการขาดแคลนผู้บริจาคและการปฏิเสธ นอกจากเซลล์ iPS 自体แล้ว ยังกำลังพิจารณาการใช้ธนาคารเซลล์ iPS ต่างบุคคลที่มีชนิด HLA พิเศษซึ่งมีภูมิคุ้มกันต่ำ มีรายงานการเหนี่ยวนำให้เซลล์ iPS ของมนุษย์แยกตัวเป็นเซลล์เยื่อบุกระจกตา และการผลิตแผ่นเซลล์ และการวิจัยกำลังก้าวหน้าไปสู่การประยุกต์ใช้ทางคลินิกในฐานะทางเลือกการรักษาใหม่สำหรับ LSCD สองตา
การบูรณาการกับการบำบัดด้วยยีน : การปลูกถ่ายเยื่อบุลิมบัส เพาะเลี้ยง (CLET) ช่วยให้สามารถนำยีนเข้าไประหว่างการเพาะเลี้ยงในหลอดทดลอง กำลังศึกษาการใช้ร่วมกับการบำบัดด้วยยีน สำหรับ LSCD แต่กำเนิด เช่น epidermolysis bullosa นี่เป็นกลยุทธ์การรักษาที่ไม่สามารถทำได้กับ CLAu หรือ SLET และถือเป็นความสำคัญทางคลินิกเฉพาะของ CLET
ความก้าวหน้าในการวินิจฉัยด้วยภาพ : ด้วยการปรับปรุงเทคนิคกล้องจุลทรรศน์คอนโฟคอล และ OCT ส่วนหน้า การวินิจฉัย早期และการติดตามประสิทธิภาพการรักษาของ LSCD มีความแม่นยำมากขึ้น 1)
การประยุกต์ใช้การวิเคราะห์ยีน : ใน LSCD ที่ถ่ายทอดทางพันธุกรรม เช่น ภาวะไม่มีม่านตา การวิเคราะห์ลำดับยีนสามารถใช้ทำนายพยากรณ์โรคและกำหนดแผนการรักษาได้ 1)
Q
ยายับยั้งจุดตรวจสอบภูมิคุ้มกันทำให้เกิดผลข้างเคียงทางตาหรือไม่?
A
ใช่ ยายับยั้งจุดตรวจสอบภูมิคุ้มกันอาจทำให้เกิดผลข้างเคียงทางตาได้ไม่บ่อยนัก ม่านตาอักเสบ และตาแห้ง พบได้ค่อนข้างบ่อย แต่ในกรณีรุนแรง มีรายงานที่นำไปสู่ LSCD หรือกระจกตา ทะลุ หากมีอาการทางตา (ตาแดง ปวด ตาพร่า มัว) หลังจากเริ่มการรักษามะเร็ง สิ่งสำคัญคือต้องไปพบจักษุแพทย์ทันที
บทความนี้มีวัตถุประสงค์เพื่อให้ข้อมูลแก่บุคลากรทางการแพทย์และผู้เรียน ไม่ใช่สิ่งทดแทนการวินิจฉัยหรือการรักษาเฉพาะบุคคล ในการปฏิบัติทางคลินิก โปรดอ้างอิงแนวทางปฏิบัติล่าสุดและปรึกษาผู้เชี่ยวชาญหากจำเป็น
Trief D, Rapuano CJ. Limbal stem cell deficiency: pathophysiology, clinical manifestations, diagnosis, and causes. Ann Eye Sci. 2023;8:13.
Basu S, Chodosh J. Conjunctival limbal autograft transplantation for limbal stem cell deficiency: a systematic review. Br J Ophthalmol. 2023 (247.full).
Mehta U, Farid M. Dupilumab Induced Limbal Stem Cell Deficiency. Int Med Case Rep J. 2021;14:275-278.
Booranapong W, Kosrirukvongs P, Duangsaard S, et al. Transplantation of autologous cultivated oral mucosal epithelial sheets for limbal stem cell deficiency at Siriraj Hospital: a case series. J Med Case Rep. 2022;16:298.
Schumaier NP, Heidemann DG, Gupta C. Durvalumab-associated limbal stem cell deficiency and secondary corneal perforation. Am J Ophthalmol Case Rep. 2024;35:102074.
Elmansouri O, Lemkhoudem A, Bezza H, et al. Limbal stem cell deficiency: a dreaded complication of chickenpox in children. Oxford Med Case Rep. 2025;5:334-335.