獲得性(外傷、醫源性、藥物性)

輪部幹細胞缺乏症(LSCD)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是輪部幹細胞缺乏症(LSCD)?
Section titled “1. 什麼是輪部幹細胞缺乏症(LSCD)?”角膜上皮是複層鱗狀上皮,每3至10天完全更新一次。支持這種持續再生的幹細胞存在於角膜和結膜交界處的輪部。1921年Vogt描述的輪部柵狀組織(POV)就是這些幹細胞的微環境(niche)1)。
輪部幹細胞缺乏症(LSCD)是指這些幹細胞先天或後天消失或功能不全的狀態。當角膜上皮的自我修復能力喪失時,結膜上皮會侵入角膜,即「結膜化」。結膜化伴隨表層新生血管和角膜混濁的進展,導致視力障礙。
輪部還起到防止結膜血管侵入角膜的屏障作用。一旦這個屏障被破壞,角膜的透明性就會喪失。LSCD呈現從部分性(不完全結膜化)到全周性(完全結膜化)的各種嚴重程度1)。據認為,只要殘留7%的輪部幹細胞,現代手術技術就能重建角膜上皮1)。
2. 主要症狀和臨床所見
Section titled “2. 主要症狀和臨床所見”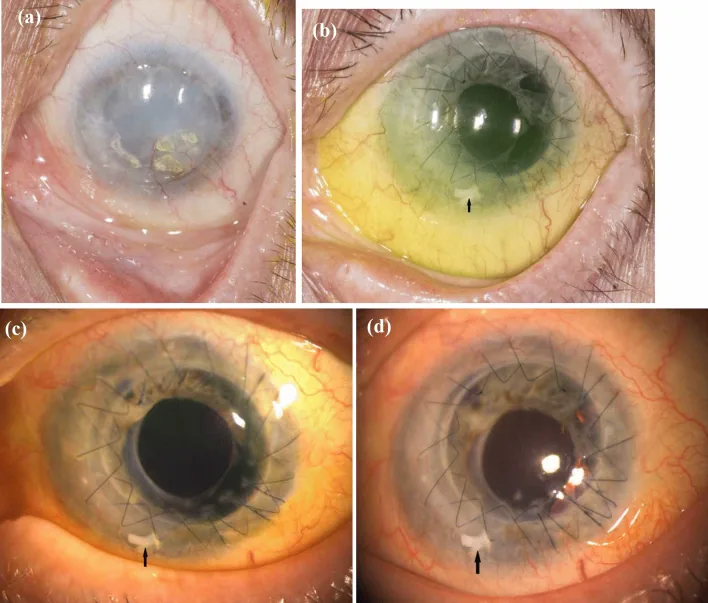
主要主訴為復發性上皮糜爛引起的眼痛和視力下降。異物感、隱形眼鏡不耐受、畏光和流淚也很常見。上皮屏障破壞易併發感染性角膜炎。
裂隙燈顯微鏡檢查可見以下階段性表現1)。
- 輕度:螢光素染色顯示漩渦狀上皮病變(whorl-epitheliopathy)。上皮變薄從角膜緣向中央進展。
- 中度:出現表層新生血管和周邊部角膜血管翳。
- 重度:360度角膜結膜化、基質新生血管、角膜混濁/瘢痕化。有時可導致角膜穿孔。
角膜學會2019年發布的全球共識提出了基於角膜緣受累範圍、角膜表面受累範圍及對視軸影響的臨床分期分類1)。
POV在正常情況下存在於角膜緣全周(尤其在上方和下方易於觀察)。LSCD時POV消失。但10歲以下或70歲以上正常人也可能難以觀察到POV。
3. 原因與風險因素
Section titled “3. 原因與風險因素”LSCD的原因分為遺傳性、獲得性和特發性1)。
發炎性、感染性、遺傳性
Stevens-Johnson症候群:嚴重的眼表發炎導致雙側LSCD。
免疫媒介性:眼黏膜類天皰瘡(MMP)、移植物抗宿主病(GVHD)。
感染性:皰疹性角膜炎、砂眼、水痘6)。
遺傳性:無虹膜症(PAX6突變)最常見。還包括KID症候群、著色性乾皮症等。
某三級醫院738隻眼14年的流行病學調查顯示,病因構成爲無虹膜症30.9%、化學/熱燒傷20.6%、CL 16.8%、Stevens-Johnson症候群10.4%1)。
Mehta等人報告了一例56歲男性在開始使用杜匹魯單抗57個月後出現雙側LSCD和廣泛眼瞼球粘連的病例。認爲IL-4/IL-13信號抑制導致杯狀細胞減少,引發眼表發炎,慢性發炎耗盡了角膜緣幹細胞。3)
Schumaier等人報告了一例65歲男性在開始使用德瓦魯單抗治療非小細胞肺癌2個月後出現雙側LSCD樣表現和左眼角膜穿孔的病例。角膜高表達PD-L1,PD-1/PD-L1路徑抑制可能誘發了自體免疫性角膜炎。停用德瓦魯單抗後結膜發炎消退。5)
長期佩戴隱形眼鏡可能導致LSCD。尤其常見於軟式隱形眼鏡,據報導約2%–5%的隱形眼鏡佩戴者出現LSCD。從開始佩戴到發病的平均時間為14–17年。機械刺激、低氧環境以及保養液中的防腐劑被認為會損傷角膜緣幹細胞。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”LSCD的診斷主要基於臨床表現,並輔以各種檢查1)。
| 診斷方法 | 優點 | 缺點 |
|---|---|---|
| 印跡細胞學 | 檢測杯狀細胞以確認結膜化 | 依賴檢體品質 |
| 共焦顯微鏡 | 可定量評估全層細胞 | 需要患者配合5–15分鐘 |
| 眼前段OCT | 非接觸、時間短 | 解析度低於共焦顯微鏡 |
診斷流程:
- 使用裂隙燈顯微鏡確認POV消失。
- 通過螢光素染色評估漩渦狀角膜病變或結膜化模式。
- 必要時進行印跡細胞學檢查,檢測角膜表面的杯狀細胞(結膜化的標誌)。
- 使用共聚焦顯微鏡確認基底上皮細胞密度降低和化生細胞的存在。
鑑別診斷包括翼狀胬肉(通常位於鼻側)、眼表鱗狀細胞腫瘤(OSSN)和周邊感染性角膜炎。
5. 標準治療方法
Section titled “5. 標準治療方法”治療從保守管理逐步進展,考慮手術介入。單獨角膜移植在LSCD中為禁忌症2)。
保守治療
停止佩戴隱形眼鏡並去除刺激因素:可逆的“角膜緣幹細胞應激”可通過保守管理改善。
人工淚液:頻繁滴用不含防腐劑的製劑以潤滑眼表。
類固醇滴眼液:短期脈衝給藥以控制炎症。
環孢素滴眼液:用於長期免疫調節。
自體血清滴眼液:有助於促進角膜上皮癒合。
手術治療
結膜輪部自體移植(CLAu):單眼LSCD從健康眼取輪部組織。成功率77~100%2)
培養輪部上皮移植(CLET):取小塊輪部組織在實驗室擴增培養後移植。
簡易輪部上皮移植(SLET):將供體幹細胞直接播種在羊膜上。無需實驗室。
培養口腔黏膜上皮移植(COMET):針對雙眼LSCD,用自體口腔黏膜替代。4)
人工角膜(KPro):嚴重全周性LSCD的最後手段。
培養角膜上皮移植(日本起源的再生醫療)和羊膜移植也常合併使用。對於SJS等發炎嚴重的病例,有時會合併使用絲裂黴素C抑制纖維母細胞。
Booranapong等在泰國對3例化學燒傷和3例Stevens-Johnson症候群患者進行了培養口腔黏膜上皮片移植。化學燒傷的2例在1年後達到優秀評價,但Stevens-Johnson症候群病例因口腔黏膜本身受損,細胞存活率低,結果不佳。4)
單純角膜移植不能治癒LSCD。角膜移植提供的是角膜基質和內皮,不含角膜上皮幹細胞。移植後幹細胞缺乏狀態未變,結膜化和角膜混濁會再次進展,導致移植失敗。應首先進行補充輪部幹細胞的手術,穩定角膜表面,然後根據需要二期進行角膜移植。
6. 病理生理學·詳細發病機轉
Section titled “6. 病理生理學·詳細發病機轉”角膜上皮幹細胞位於POV的基底細胞層。POV的色素沉著保護幹細胞免受紫外線傷害。幹細胞作為基底細胞向心性移向角膜中央,在分化過程中移向表層,最終脫落。1)
幹細胞微環境:輪部幹細胞需要角膜外基質血管系統的營養供應,因此位於靠近血管的周邊區域。角膜為維持透明性而無血管,幹細胞存在於這一過渡區域。
LSCD的發病機轉:
- 輪部上皮損傷(化學灼傷、發炎、機械刺激等)
- 幹細胞微環境破壞(發炎性細胞激素、基質金屬蛋白酶)
- 幹細胞減少 → 角膜上皮再生能力下降
- 結膜上皮侵入角膜(結膜化)
- 表層新生血管、角膜混濁、疤痕化進展
輪部幹細胞不僅負責角膜上皮的再群聚化,也扮演防止結膜血管侵入的屏障角色。一旦此屏障功能喪失,就會發生結膜化和新生血管,角膜透明度將不可逆地受損。
在部分性LSCD中,殘留的健康輪部可供應角膜上皮,因此若損傷範圍侷限,預後相對良好。在全周性LSCD中,外科介入必不可少。
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”新型藥物引起的LSCD:已有報導免疫檢查點抑制劑和杜匹魯單抗等新型生物製劑導致LSCD3)5)。提出杜匹魯單抗透過抑制IL-4/IL-13減少杯狀細胞,導致慢性眼表發炎進而發展為LSCD的機制3)。德瓦魯單抗可能透過抑制PD-L1破壞角膜免疫特權,引發自體免疫性角膜炎5)。
新病因的報導:Elmansouri等人報告了首例水痘後發生LSCD的10歲兒童病例6)。病毒感染導致LSCD的認識正在擴大。
口腔黏膜上皮再生醫學:培養口腔黏膜上皮片移植(COMET)和SOMET是雙側LSCD且無法獲得輪部供體時的有希望的選擇4)。由於使用自體組織,無需免疫抑制,且SOMET不需要細胞培養基礎設施,可在資源有限的環境中實施。
利用iPS細胞的角膜上皮再生:iPS細胞(誘導性多能幹細胞)有望解決供體不足和排斥反應的問題。除了自體iPS細胞,也正在考慮使用具有低免疫原性特定HLA類型的異體iPS細胞庫。已有報導將人類iPS細胞分化為角膜上皮細胞並製備細胞片,作為雙側LSCD的新治療選擇,臨床研究正在推進。
與基因治療的融合:培養輪部上皮移植(CLET)在體外培養過程中可以進行基因導入。對於先天性LSCD如大皰性表皮鬆解症,正在考慮與基因治療聯合使用。這是CLAu或SLET無法實現的治療策略,被認為是CLET獨特的臨床意義。
影像診斷的進步:共聚焦顯微鏡和前段OCT技術的改進使得LSCD的早期診斷和治療效果監測更加精確1)。
基因分析的應用:對於無虹膜症等遺傳性LSCD,基因序列分析可能用於預後預測和治療方針的決定1)。
8. 參考文獻
Section titled “8. 參考文獻”- Trief D, Rapuano CJ. Limbal stem cell deficiency: pathophysiology, clinical manifestations, diagnosis, and causes. Ann Eye Sci. 2023;8:13.
- Basu S, Chodosh J. Conjunctival limbal autograft transplantation for limbal stem cell deficiency: a systematic review. Br J Ophthalmol. 2023 (247.full).
- Mehta U, Farid M. Dupilumab Induced Limbal Stem Cell Deficiency. Int Med Case Rep J. 2021;14:275-278.
- Booranapong W, Kosrirukvongs P, Duangsaard S, et al. Transplantation of autologous cultivated oral mucosal epithelial sheets for limbal stem cell deficiency at Siriraj Hospital: a case series. J Med Case Rep. 2022;16:298.
- Schumaier NP, Heidemann DG, Gupta C. Durvalumab-associated limbal stem cell deficiency and secondary corneal perforation. Am J Ophthalmol Case Rep. 2024;35:102074.
- Elmansouri O, Lemkhoudem A, Bezza H, et al. Limbal stem cell deficiency: a dreaded complication of chickenpox in children. Oxford Med Case Rep. 2025;5:334-335.
