후천성 (외상, 의인성, 약물성)

윤부줄기세포결핍증 (LSCD)
한눈에 보는 포인트
섹션 제목: “한눈에 보는 포인트”1. 윤부줄기세포결핍증(LSCD)이란?
섹션 제목: “1. 윤부줄기세포결핍증(LSCD)이란?”각막 상피는 중층 편평 상피로, 3~10일마다 완전히 교체된다. 이 지속적인 재생을 지지하는 줄기세포는 각막과 결막의 경계인 윤부에 존재한다. 1921년 Vogt가 기술한 윤부의 울타리 조직(palisades of Vogt: POV)이 그 줄기세포의 니치(미세환경)이다1).
윤부줄기세포결핍증(LSCD)은 이러한 줄기세포가 선천적 또는 후천적으로 소실되거나 기능부전에 빠진 상태이다. 각막 상피의 자기 재생 능력이 상실되면 결막 상피가 각막 위로 침입하는 ‘결막화’가 발생한다. 결막화에 따라 표층 신생혈관, 각막 혼탁이 진행되어 시력 장애를 초래한다.
윤부는 결막에서 각막으로의 혈관 침입을 막는 장벽으로도 기능한다. 이 장벽이 무너지면 각막의 투명성이 상실된다. LSCD는 부분적(불완전한 결막화)부터 전주위성(완전한 결막화)까지 다양한 중증도를 나타낸다1). 단 7%의 윤부줄기세포만 남아 있어도 현대 수술 기술로 각막 상피 재건이 가능하다고 알려져 있다1).
2. 주요 증상과 임상 소견
섹션 제목: “2. 주요 증상과 임상 소견”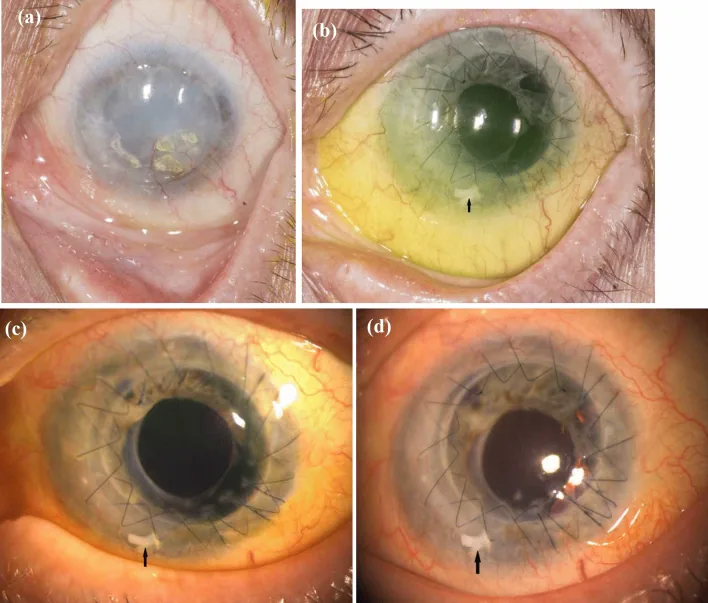
자각 증상
섹션 제목: “자각 증상”재발성 상피 미란으로 인한 안통과 시력 저하가 주된 호소입니다. 이물감, 콘택트렌즈 불내증, 눈부심, 눈물 흘림도 흔합니다. 상피 장벽의 파괴로 감염성 각막염이 합병되기 쉽습니다.
임상 소견
섹션 제목: “임상 소견”세극등 현미경 검사에서 다음과 같은 소견이 단계적으로 관찰됩니다1).
- 경도: 플루오레세인 염색에서 소용돌이 모양 상피병증(whorl-epitheliopathy). 상피가 윤부에서 중심부로 얇아짐.
- 중등도: 표층 신생혈관과 주변부 판누스 출현.
- 중증: 360도 각막 결막화, 실질 신생혈관, 각막 혼탁/반흔화. 각막 천공에 이르는 경우도 있음.
Cornea Society가 2019년에 발표한 글로벌 컨센서스에서는 윤부의 손상 범위, 각막 표면의 침범 범위, 시축에 대한 영향도에 기반한 임상적 병기 분류가 제안되었습니다1).
POV는 정상에서는 윤부 전주(특히 위쪽과 아래쪽에서 관찰하기 쉬움)에 존재합니다. LSCD에서는 POV가 소실됩니다. 단, 10세 이하나 70세 이상에서는 정상이어도 POV가 관찰되기 어려운 경우가 있습니다.
3. 원인과 위험 요인
섹션 제목: “3. 원인과 위험 요인”LSCD의 원인은 유전성, 후천성, 특발성으로 분류됩니다1).
염증성·감염성·유전성
스티븐스-존슨 증후군: 심한 안구 표면 염증으로 양안성 LSCD가 발생합니다.
면역 매개: 안 점막 유사천포창(MMP), 이식편대숙주병(GVHD).
감염성: 헤르페스 각막염, 트라코마, 수두6).
유전성: 무홍채증(PAX6 돌연변이)이 가장 흔합니다. KID 증후군, 색소성 건피증 등도 포함됩니다.
한 3차 의료기관의 738안, 14년 역학 조사에서 원인 분포는 무홍채증 30.9%, 화학/열 화상 20.6%, CL 16.8%, 스티븐스-존슨 증후군 10.4%였습니다1).
Mehta 등은 두필루맙 투여 시작 57개월 후 양안성 LSCD와 광범위한 안검구 유착이 발생한 56세 남성 증례를 보고했습니다. IL-4/IL-13 신호 억제로 인한 술잔세포 감소가 안구 표면 염증을 유발하고, 만성 염증이 윤부 줄기세포를 고갈시킨 것으로 생각됩니다.3)
Schumaier 등은 비소세포폐암에 대한 두르발루맙 투여 시작 2개월 후 양안성 LSCD 유사 소견과 좌안 각막 천공이 발생한 65세 남성 증례를 보고했습니다. 각막은 PD-L1을 고발현하며, PD-1/PD-L1 경로 억제가 자가면역 각막염을 유발했을 가능성이 있습니다. 두르발루맙 중단 후 결막 염증은 소실되었습니다.5)
장기간 콘택트렌즈 착용은 LSCD의 원인이 될 수 있습니다. 특히 소프트 콘택트렌즈에서 흔하며, 콘택트렌즈 착용자의 약 25%에서 LSCD가 발견된다는 보고가 있습니다. LSCD 발병까지의 평균 착용 기간은 1417년입니다. 기계적 자극, 저산소 환경, 렌즈액의 방부제가 윤부 줄기세포를 손상시키는 것으로 생각됩니다.
4. 진단 및 검사 방법
섹션 제목: “4. 진단 및 검사 방법”LSCD의 진단은 임상 소견을 기본으로 하며, 다양한 검사를 보조적으로 사용합니다1).
| 진단법 | 장점 | 단점 |
|---|---|---|
| 인상 세포검사 | 배상세포 검출로 결막화 확인 | 표본 품질에 의존 |
| 공초점 현미경 | 전층 세포 정량 평가 가능 | 5~15분의 검사 협조 필요 |
| 전안부 OCT | 비접촉, 단시간 | 공초점보다 해상도 낮음 |
진단 과정:
- 세극등 현미경으로 POV 소실을 확인합니다.
- 플루오레세인 염색으로 소용돌이 모양 각막병증 또는 결막화 패턴을 평가합니다.
- 필요시 인상 세포검사로 각막 표면의 배상세포(결막화의 지표)를 검출합니다.
- 공초점 현미경으로 기저 상피세포 밀도 감소와 화생세포 존재를 확인합니다.
감별 진단으로는 익상편(보통 비측 국한), 안표면 편평상피종양(OSSN), 주변부 감염성 각막염을 고려합니다.
5. 표준 치료법
섹션 제목: “5. 표준 치료법”치료는 보존적 관리에서 단계적으로 진행하며 수술적 개입을 고려합니다. 각막 이식 단독은 LSCD에서 금기입니다2).
보존적 치료
수술적 치료
배양 각막 상피 이식(일본 발 재생 의료) 및 양막 이식도 병용됩니다. SJS 등 염증이 심한 증례에서는 마이토마이신 C로 섬유아세포 억제를 병용하는 경우가 있습니다.
Booranapong 등은 태국에서 화학 화상 3예와 스티븐스-존슨 증후군 3예에 배양 구강 점막 상피 시트 이식을 시행했습니다. 화학 화상 2예는 1년 후 우수 평가를 달성했지만, 스티븐스-존슨 증후군 증례는 구강 점막 자체도 손상되어 세포 생존율이 낮아 결과가 불량했습니다.4)
각막 이식 단독으로는 LSCD가 낫지 않습니다. 각막 이식에서 제공되는 것은 각막 실질과 내피이며, 각막 상피 줄기세포는 포함되지 않습니다. 이식 후에도 줄기세포 부족 상태는 변하지 않으며, 다시 결막화와 각막 혼탁이 진행되어 이식편은 실패합니다. 먼저 윤부 줄기세포를 보충하는 수술을 시행하여 각막 표면을 안정화시킨 후, 필요에 따라 2단계로 각막 이식을 시행합니다.
6. 병태생리학·상세한 발병 기전
섹션 제목: “6. 병태생리학·상세한 발병 기전”각막 상피 줄기세포는 POV 내 기저 세포층에 위치합니다. POV의 색소 침착은 자외선으로부터 줄기세포를 보호합니다. 줄기세포는 기저 세포로서 구심적으로 각막 중앙 방향으로 이동하며, 분화하면서 표층으로 향하고 최종적으로 탈락합니다.1)
줄기세포 니치 환경 : 윤부 줄기세포는 각막 외부의 기질 혈관계로부터 영양 공급을 필요로 하므로 혈관에 가까운 주변부에 위치합니다. 각막은 투명성 유지를 위해 무혈관이며, 줄기세포는 이 이행 영역에 존재합니다.
LSCD의 발병 기전 :
- 윤부 상피 손상(화학 화상, 염증, 기계적 자극 등)
- 줄기세포 니치 미세환경 파괴(염증성 사이토카인, 기질 금속단백분해효소)
- 줄기세포 감소 → 각막 상피 재생 능력 저하
- 결막 상피가 각막으로 침입(결막화)
- 표층 신생혈관, 각막 혼탁, 반흔화 진행
윤부 줄기세포는 각막 상피를 재구성할 뿐만 아니라 결막으로부터의 혈관 침입을 막는 장벽으로도 기능합니다. 이 장벽 기능이 상실되면 결막화와 신생혈관이 발생하고 각막 투명성은 비가역적으로 손상됩니다.
부분 LSCD에서는 남아 있는 건강한 윤부가 각막 상피를 공급하므로 손상 범위가 제한적이면 예후가 비교적 좋습니다. 전주위 LSCD에서는 외과적 개입이 필수적입니다.
7. 최신 연구와 향후 전망
섹션 제목: “7. 최신 연구와 향후 전망”신약에 의한 LSCD 보고: 면역관문억제제 및 두필루맙과 같은 새로운 생물학적 제제에 의한 LSCD가 보고되었습니다3)5). 두필루맙은 IL-4/IL-13 억제를 통해 술잔세포를 감소시키고 만성 안구표면 염증을 유발하여 LSCD에 이르는 기전이 제안되었습니다3). 두르발루맙은 PD-L1 억제를 통해 각막 면역 특권을 파괴하여 자가면역 각막염을 유발할 가능성이 있습니다5).
새로운 원인 보고: Elmansouri 등은 수두 후 LSCD가 발생한 10세 소아의 첫 증례를 보고했습니다6). 바이러스 감염에 의한 LSCD에 대한 인식이 확대되고 있습니다.
구강 점막 상피를 이용한 재생 의학: 배양 구강 점막 상피 시트 이식(COMET) 및 SOMET은 양안 LSCD에서 윤부 공여자를 얻을 수 없는 경우 유망한 선택지입니다4). 자가 조직이므로 면역억제가 필요 없으며, 세포 배양 인프라가 필요 없는 SOMET은 자원이 제한된 환경에서도 시행 가능합니다.
iPS 세포를 이용한 각막 상피 재생: 공여자 부족과 거부 반응 문제를 해결하기 위해 iPS 세포(유도만능줄기세포)의 이용이 기대됩니다. 자가 iPS 세포 외에도 면역원성이 낮은 특정 HLA 유형을 가진 동종 iPS 세포 은행의 이용도 검토되고 있습니다. 인간 iPS 세포에서 각막 상피 세포로의 분화 유도와 세포 시트 제작이 보고되었으며, 양안 LSCD에 대한 새로운 치료 옵션으로서 임상 적용을 위한 연구가 진행 중입니다.
유전자 치료와의 융합: 배양 윤부 상피 이식(CLET)은 체외 배양 과정에서 유전자 도입이 가능합니다. 수포성 표피박리증과 같은 선천성 LSCD에 대해 유전자 치료와의 병용이 검토되고 있습니다. 이는 CLAu나 SLET로는 불가능한 치료 전략이며, CLET의 독특한 임상적 의의로 간주됩니다.
영상 진단의 발전: 공초점 현미경 및 전안부 OCT 기술의 향상으로 LSCD의 조기 진단 및 치료 효과 모니터링이 더욱 정밀해지고 있습니다1).
유전자 분석의 응용: 무홍채증과 같은 유전성 LSCD에서 유전자 서열 분석은 예후 예측 및 치료 방침 결정에 활용될 수 있습니다 1).
8. 참고 문헌
섹션 제목: “8. 참고 문헌”- Trief D, Rapuano CJ. Limbal stem cell deficiency: pathophysiology, clinical manifestations, diagnosis, and causes. Ann Eye Sci. 2023;8:13.
- Basu S, Chodosh J. Conjunctival limbal autograft transplantation for limbal stem cell deficiency: a systematic review. Br J Ophthalmol. 2023 (247.full).
- Mehta U, Farid M. Dupilumab Induced Limbal Stem Cell Deficiency. Int Med Case Rep J. 2021;14:275-278.
- Booranapong W, Kosrirukvongs P, Duangsaard S, et al. Transplantation of autologous cultivated oral mucosal epithelial sheets for limbal stem cell deficiency at Siriraj Hospital: a case series. J Med Case Rep. 2022;16:298.
- Schumaier NP, Heidemann DG, Gupta C. Durvalumab-associated limbal stem cell deficiency and secondary corneal perforation. Am J Ophthalmol Case Rep. 2024;35:102074.
- Elmansouri O, Lemkhoudem A, Bezza H, et al. Limbal stem cell deficiency: a dreaded complication of chickenpox in children. Oxford Med Case Rep. 2025;5:334-335.
