ต้อเนื้อเป็นโรคความเสื่อมของกระจกตา และเยื่อบุตา ที่ดำเนินไปเรื้อรัง โดยเนื้อเยื่อที่มีทั้งเส้นเลือดและพังผืดซึ่งมีต้นกำเนิดจากเยื่อบุตา รุกล้ำเข้ามาบนกระจกตา เป็นรูปสามเหลี่ยม
การได้รับรังสีอัลตราไวโอเลต (UV-B) เป็นปัจจัยเสี่ยงที่สำคัญที่สุด พบได้บ่อยในผู้ที่ทำงานกลางแจ้งและผู้ที่อาศัยอยู่ใกล้เส้นศูนย์สูตร
ส่วนใหญ่เกิดทางด้านหัวตา การเกิดทั้งด้านหัวตาและด้านหางตาพบร้อยละ 2–3 การเกิดเฉพาะด้านหางตาพบเพียงร้อยละ 1–2
เมื่อลุกลามเข้าสู่กลางกระจกตา จะทำให้เกิดสายตาเอียง ไม่สม่ำเสมอและการมองเห็น ลดลง หากลุกลามถึงแนวแกนสายตาจะเป็นข้อบ่งชี้ในการผ่าตัด
การรักษาด้วยยาเป็นเพียงการรักษาตามอาการ ไม่มีผลยับยั้งการดำเนินของโรค การรักษาหลักคือการผ่าตัดเอาเนื้อเยื่อออก
การตัดเนื้อเยื่อออกอย่างเดียว (วิธีเปิดเผยตาขาว ) มีอัตราการกลับเป็นซ้ำสูงถึงร้อยละ 30–89 ปัจจุบันไม่แนะนำให้ใช้
การปลูกถ่ายเยื่อบุตา ผู้ป่วยเอง (CAG) และการปลูกถ่ายเยื่อบุตา บริเวณลิมบัส ของผู้ป่วยเอง (LCAG) เป็นวิธีการผ่าตัดมาตรฐานในปัจจุบัน
การผ่าตัดครั้งแรกที่เหมาะสมสามารถควบคุมอัตราการกลับเป็นซ้ำได้ประมาณร้อยละ 1.5–5
ต้อเนื้อ (Pterygium) เป็นโรคความเสื่อมเรื้อรังที่เนื้อเยื่อที่มีทั้งเส้นเลือดและพังผืดซึ่งมีต้นกำเนิดจากเยื่อบุตา รุกล้ำเข้าไปในกระจกตา ส่วนใหญ่เกิดทางด้านหัวตาของกระจกตา เป็นรูปสามเหลี่ยมชี้เข้าสู่ศูนย์กลางกระจกตา 1) ชื่อ “pterygium” มาจากภาษากรีกแปลว่าปีก เนื่องจากมีลักษณะเป็นรูปสามเหลี่ยมคล้ายปีกที่กางออก ทางพยาธิวิทยาเนื้อเยื่อมีลักษณะเฉพาะคือการเพิ่มจำนวนของเนื้อเยื่อเกี่ยวพันใต้เยื่อบุตา การเสื่อมสภาพแบบยืดหยุ่น (elastoid degeneration) ของเส้นใยคอลลาเจน และการแทรกซึมของเซลล์อักเสบเรื้อรังซึ่งส่วนใหญ่เป็นลิมโฟไซต์ โรคนี้เกิดและดำเนินไปบนพื้นฐานของการเปลี่ยนแปลงตามวัย ร่วมกับการระคายเคืองจากรังสีอัลตราไวโอเลตเรื้อรังและการระคายเคืองจากความแห้งกร้าน
ต้อเนื้อไม่เพียงแต่มีการเคลื่อนย้ายและเพิ่มจำนวนของเซลล์เยื่อบุตา ขึ้นบนกระจกตา เท่านั้น แต่ยังมีการเพิ่มจำนวนของเนื้อเยื่อพังผืดและหลอดเลือดใต้เยื่อบุตา ร่วมด้วย จุดสำคัญที่แตกต่างจากต้อลม (pinguecula) ตามวัยคือ ต้อเนื้อไม่ใช่เพียงการยื่นยาวของเยื่อบุตา แต่เป็นรอยโรคที่มีการเพิ่มจำนวนอย่างมีกิจกรรม
ต้อเนื้อเกิดทางด้านหัวตาเป็นส่วนใหญ่ การเกิดทั้งด้านหัวตาและด้านหางตาพบร้อยละ 2–3 การเกิดเฉพาะด้านหางตาพบเพียงร้อยละ 1–2 มักเป็นข้างเดียว แต่ประมาณร้อยละ 10 เป็นทั้งสองข้าง1) ในกรณีที่เป็นทั้งสองข้าง มักไม่มีความแตกต่างอย่างมีนัยสำคัญของปริมาณรังสีอัลตราไวโอเลตที่ได้รับระหว่างสองตา
ต้อเนื้อสามารถแบ่งตามกายวิภาคได้เป็น 4 บริเวณดังนี้
cap (ปลาย) :เนื้อเยื่อสีขาวไร้หลอดเลือดที่ลุกลามบนกระจกตา ยึดติดแน่นกับเนื้อกระจกตา head (ศีรษะ) :ส่วนที่นูนออกมามากที่สุดบนกระจกตา neck (คอ) :เนื้อเยื่อเจริญที่นูนขึ้นบนกระจกตา body (ลำตัว) :เนื้อเยื่อเจริญบนตาขาว
ที่ด้านกระจกตา ของ cap อาจพบ Stocker’s line (เส้นสต็อกเกอร์) ซึ่งเป็นเส้นของการสะสมของเหล็กรูปโค้ง ซึ่งเป็นสิ่งสำคัญที่บ่งชี้ถึงการดำเนินโรคแบบเรื้อรัง บริเวณ cap ยึดติดแน่นกับเนื้อกระจกตา แต่ใกล้ลิมบัส จะยึดติดน้อยกว่า สามารถสอดหัววัดใต้รอยโรคได้ สิ่งนี้ช่วยแยกความแตกต่างจาก pterygium เทียม
Pterygium เป็นโรคผิวตาที่พบได้ทั่วไปทั่วโลก โดยเฉพาะในบริเวณใกล้เส้นศูนย์สูตรที่มีการได้รับรังสีอัลตราไวโอเลตสูง1) การศึกษาตามประชากรในภูมิภาคต่างๆ ทั่วโลกรายงานความชุกดังนี้1) :
ทิเบต (จีน) :ประมาณ 14.5%วิกตอเรีย ออสเตรเลีย :6.7%จีน Beijing Eye Study :10.1% (อัตราการเกิดโรคใน 10 ปี)ประชากรทั่วไปในสเปน :5.9%อินเดีย Andhra Pradesh Eye Disease Study :9.5%เมียนมาร์ตอนกลาง Meiktila Eye Study :19.6%
ผู้ชายมีความถี่ในการเกิดโรคประมาณ 2 เท่าของผู้หญิง และความชุกสูงขึ้นตามอายุ ผู้ป่วยส่วนใหญ่มารับการรักษาในช่วงอายุ 50–70 ปี การผ่าตัด pterygium เป็นหนึ่งในการผ่าตัดตาที่ทำบ่อยที่สุดในโลก1) 2) ในญี่ปุ่น pterygium เป็นหนึ่งในโรคเยื่อบุตา ที่พบได้บ่อย โดยเฉพาะในกลุ่มวัยกลางคนและสูงอายุที่ทำงานกลางแจ้ง เช่น เกษตรกรรม ประมง และป่าไม้ ความแตกต่างของปริมาณรังสียูวีในแต่ละภูมิภาคสะท้อนให้เห็น โดยในพื้นที่ที่มีรังสียูวีสูง เช่น จังหวัดโอกินาวะและตอนใต้ของคิวชู มีความชุกค่อนข้างสูง
ในแง่ระบาดวิทยา อายุ เพศ อาชีพ และละติจูดของที่อยู่อาศัยเป็นปัจจัยกำหนดหลัก ในบางพื้นที่ อัตราความชุกของโรคในผู้ชายวัยกลางคนและสูงอายุที่ทำงานกลางแจ้งสูงเกินกว่า 10% พบได้น้อยในคนหนุ่มสาว แต่บางครั้งพบผู้ป่วยอายุ 30 ปีในพื้นที่ที่มีรังสียูวีสูง เช่น โอกินาวะและคิวชูใต้ เป็นที่ทราบกันว่าผู้ป่วยที่อายุน้อยมีอัตราการกลับเป็นซ้ำสูง ดังนั้นการพิจารณาข้อบ่งชี้ในการผ่าตัดและการดูแลหลังผ่าตัดจึงมีความสำคัญเป็นพิเศษ
ในการศึกษาขนาดใหญ่ของ Oke และคณะโดยใช้ IRIS Registry ของสหรัฐอเมริกา (การผ่าตัดต้อเนื้อ 102,138 ราย) การปลูกถ่ายเนื้อเยื่อ (การปูกระจกตา เยื่อบุตา ด้วยตนเอง, การปลูกถ่ายเยื่อบุตา ลิมบัส ด้วยตนเอง, การปลูกถ่ายเยื่อหุ้มน้ำคร่ำ) ดำเนินการใน 83.0% และวิธีเปลือยตาขาว ใน 15.3% จักษุแพทย์กระจกตา ใช้อัตราการปลูกถ่ายเนื้อเยื่อที่สูงกว่า และมีการชี้ให้เห็นว่าการเผยแพร่การเลือกวิธีผ่าตัดตามหลักฐานยังคงเป็นความท้าทาย2) .
Q
ต้อเนื้อกับต้อเนื้อลิมบัสต่างกันอย่างไร?
A
ในขณะที่ต้อเนื้อเป็นเนื้อเยื่อเส้นใยหลอดเลือดจากเยื่อบุตา รุกล้ำเข้าไปบนกระจกตา ต้อเนื้อลิมบัส เป็นเพียงตุ่มนูนเล็กสีขาวเหลืองบนเยื่อบุตา ที่ติดกับลิมบัส และไม่รุกล้ำเข้าไปในกระจกตา ต้อเนื้อลิมบัส อาจพัฒนาไปเป็นต้อเนื้อได้หากมีการดำเนินโรค ดูรายละเอียดเพิ่มเติมได้ในหัวข้อ «สาเหตุและปัจจัยเสี่ยง»
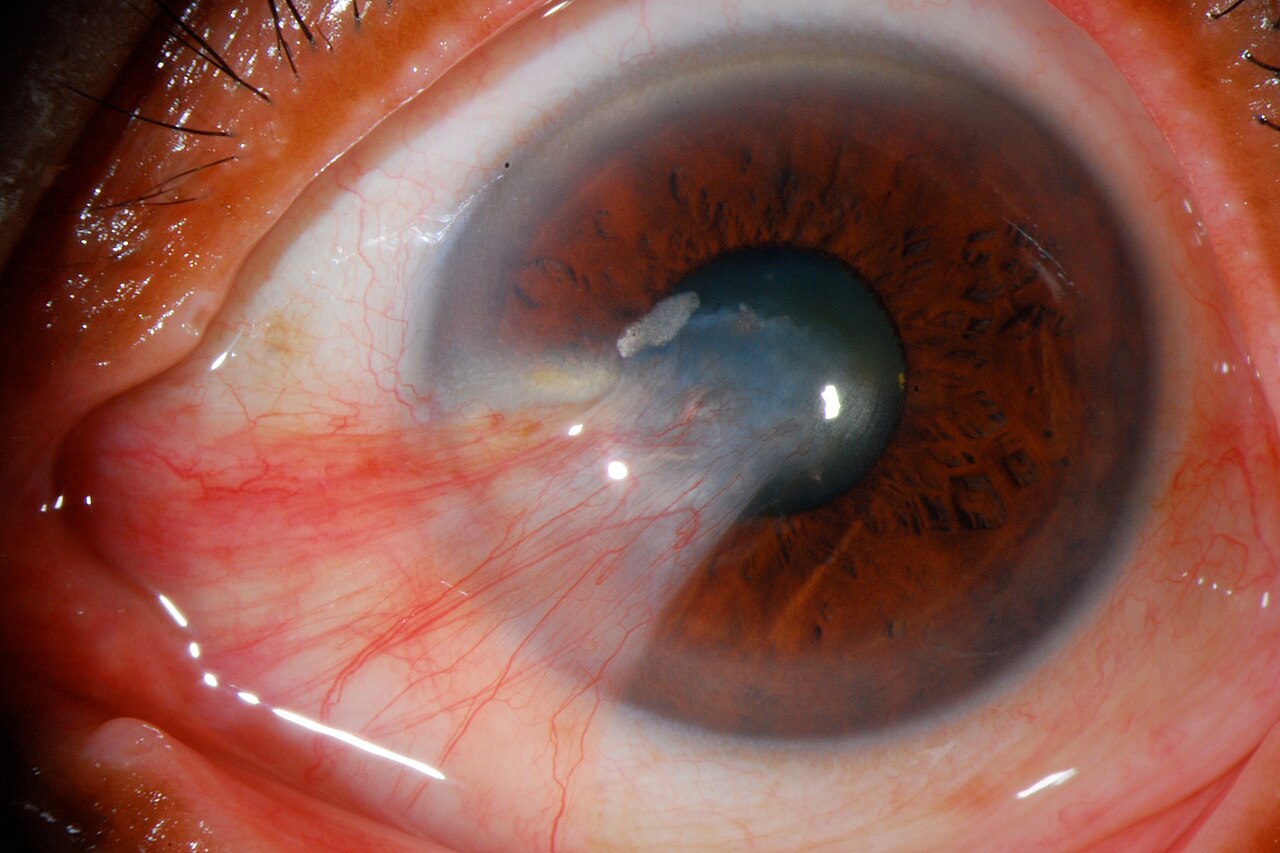
ภาพถ่ายด้วยหลอดกรีดของต้อเนื้อขั้นสูง Jmvaras José Miguel Varas, MD. Pterygium Slitlamp.jpg. Wikimedia Commons. License: CC BY 3.0.
เนื้อเยื่อเส้นใยสีขาวที่มีหลอดเลือดแผ่เป็นรูปสามเหลี่ยมจาก
เยื่อบุตา บริเวณกรีดตาไปยังศูนย์กลาง
กระจกตา เมื่อดำเนินไปจะเข้าใกล้บริเวณ
รูม่านตา ทำให้เกิด
สายตาเอียง ไม่ปกติและ
การมองเห็น ลดลง
ข้อร้องเรียนหลักของผู้ป่วยต้อเนื้อสามารถแบ่งออกเป็น 3 ประเภทใหญ่ ๆ
ความรู้สึกมีสิ่งแปลกปลอม : มักเกิดขึ้นเมื่อส่วนหัวของต้อเนื้อนูนสูง อาจมีอาการคล้ายตาแห้ง ร่วมด้วยเนื่องจากการกระจายตัวของน้ำตาที่ผิดปกติตาแดง ความบกพร่องทางการมองเห็น : เมื่อต้อเนื้อรุกล้ำเข้าไปในกระจกตา เกิน 2 มม. จะทำให้เกิดสายตาเอียง ปกติและสายตาเอียง ไม่ปกติ ซึ่งนำไปสู่การมองเห็น ลดลง
เมื่อส่วนหัวของต้อเนื้อนูนสูงอย่างรุนแรง อาจทำให้การกระจายตัวของน้ำตาผิดปกติ นำไปสู่การบาดเจ็บของเยื่อบุผิวและการเกิด dellen (รอยบุ๋ม) ในบริเวณรอบนอกกระจกตา ที่อยู่ติดกัน ในกรณีที่ดำเนินไปมาก อาจเกิดภาพซ้อน เนื่องจากการจำกัดการเคลื่อนไหวของลูกตา
ในระยะแรก มักสังเกตได้จากปัญหาทางความสวยงาม เช่น “ตาขาว ดูนูนขึ้นเล็กน้อย” หรือ “เมื่อส่องกระจกเห็นเส้นเลือดแดงชัดที่ตาขาว ด้านหัวตา” อาการตาแดง อาจกำเริบเป็นครั้งคราว และมักรุนแรงขึ้นเมื่อสัมผัสกับสิ่งกระตุ้น เช่น แสงแดดจ้า ละอองเกสรดอกไม้ อากาศแห้ง และควันบุหรี่
การตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (slit lamp) จะพบเนื้อเยื่อเยื่อสีขาวรูปสามเหลี่ยมที่มีหลอดเลือดมากมาย โดยมีฐานอยู่ที่หัวตาด้านในและลุกลามเข้าหากระจกตา ในกรณีทั่วไป การวินิจฉัยค่อนข้างง่ายและสามารถทำได้หลังจากตรวจสอบเพียงไม่กี่ราย ต้อเนื้อมักอธิบายด้วยชุดของอาการต่างๆ ได้แก่ ตาขาว ด้านหัวตาแดง ตัวต้อโป่งนูน หัวต้อรุกล้ำเข้าไปในกระจกตา และปลายสุดของหัวต้อมีสีเทาขาว ซึ่งอาการเหล่านี้ใช้ร่วมกันเพื่อประเมินระยะและกิจกรรมของโรค
หากตัวต้อมีอาการแดงมาก หลอดเลือดขยายตัวและมีลักษณะคดเคี้ยว แสดงว่าต้อมีกิจกรรมสูงและมีความเสี่ยงสูงต่อการลุกลามและการกลับเป็นซ้ำ ในทางกลับกัน ต้อ “ชนิดฝ่อ” ที่มีหลอดเลือดเล็ก ตัวต้อบางและโปร่งแสงเกือบใส และการลุกลามเกือบหยุดนิ่ง การเฝ้าสังเกตเพียงอย่างเดียวโดยไม่ต้องรีบผ่าตัดก็เป็นทางเลือกที่เหมาะสม
นอกจากนี้ยังมีกรณีที่ไม่ปกติ เช่น ปลายต้อไม่เป็นรูปสามเหลี่ยม หรือปลายต้อแยกเป็นสองหัว นอกจากนี้ แม้จะดูเหมือนต้อเนื้อ เมื่อสังเกตอย่างละเอียด อาจพบว่าเป็นเนื้องอก เช่น มะเร็งเซลล์สความัส (squamous cell carcinoma) ได้ในบางครั้ง ดังนั้นหากมีสิ่งผิดปกติ จำเป็นต้องวินิจฉัยแยกโรค
การตรวจทางพยาธิวิทยาของเนื้อเยื่อพบอาการแสดงดังต่อไปนี้
การเจริญเกินของเนื้อเยื่อเกี่ยวพันใต้เยื่อบุตา
การเสื่อมสภาพแบบอีลาสตอยด์ของเส้นใยคอลลาเจน (elastoid degeneration)
การแทรกซึมของเซลล์อักเสบเรื้อรังส่วนใหญ่เป็นลิมโฟไซต์
การเสื่อมสภาพแบบสเฟียรอยด์ใต้เยื่อบุผิว
ทางคลินิก การจำแนกตามระดับการลุกลามของรอยโรคใช้ในการตัดสินใจเกี่ยวกับข้อบ่งชี้ในการผ่าตัด
Grade ขอบเขตการลุกลาม Grade 1 จำกัดอยู่บริเวณใกล้ลิมบัส กระจกตา Grade 2 เจริญเกินเลยลิมบัส Grade 3 ถึงรูม่านตา Grade 4 เกินเลยรูม่านตา
การจำแนกแบบ Eguchi ใช้เป็นตัวบ่งชี้ขอบเขตและกิจกรรมของรอยโรค ในระดับสากล การจำแนกแบบ Tan ถูกใช้อย่างแพร่หลาย โดยประเมินความหนาของต้อเนื้อจากการมองเห็น หลอดเลือดเหนือตาขาว 11)
T1(atrophic) :ต้อเนื้อบาง มองเห็นหลอดเลือดเหนือตาขาว ได้ชัดเจนผ่านต้อเนื้อT2(intermediate) :ชนิดปานกลางT3(fleshy) :ต้อเนื้อหนา มองไม่เห็นหลอดเลือดเหนือตาขาว มีอัตราการกลับเป็นซ้ำสูง
ความหนาหรือไม่หนา รวมถึงอายุของผู้ป่วย เป็นข้อมูลสำคัญในการประเมินข้อบ่งชี้การผ่าตัดและความเสี่ยงในการกลับเป็นซ้ำ อัตราการกลับเป็นซ้ำสูงในผู้ป่วยอายุน้อย รอยโรคหนา และรอยโรคที่มีปานหรือรอยดำร่วมด้วย1) นอกจากการจำแนกแบบ Tan แล้ว ยังมีการประเมินความหนาแน่นของหลอดเลือดและระดับพังผืด เพื่อแบ่งระดับความเสี่ยงของการกลับเป็นซ้ำก่อนการผ่าตัด11)
ในทางคลินิก ระยะห่างของต้อเนื้อจากศูนย์กลางกระจกตา จะถูกบันทึกเป็นมิลลิเมตรในรูปแบบความยาวการลุกล้ำเข้าไปในกระจกตา (ระยะห่างจากยอดหัวถึงลิมบัส ) เชื่อกันว่าเมื่อความยาวการลุกล้ำเกิน 2 มิลลิเมตร จะเริ่มเกิดสายตาเอียง ไม่สม่ำเสมอ และเมื่อเกิน 3 มิลลิเมตร จะเริ่มกระทบกับแนวแกนการมองเห็น การตรวจภูมิประเทศกระจกตา จะแสดงเส้นเมอริเดียนที่แบนราบซึ่งแผ่รัศมีออกจากหัวต้อเนื้อ ซึ่งเป็นตัวชี้วัดการกลับคืนสู่รูปร่างปกติของกระจกตา หลังผ่าตัด
สาเหตุที่สำคัญที่สุดของการเกิดต้อเนื้อคือการได้รับรังสีอัลตราไวโอเลต (UV-B)1) การกระตุ้นรังสีอัลตราไวโอเลตเรื้อรังทำให้เซลล์ต้นกำเนิดลิมบัส กระจกตา เสียหาย เร่งการเจริญของเนื้อเยื่อใต้เยื่อบุตา ทะลุผ่านสิ่งกีดขวางของเยื่อ Bowman และบุกรุกระหว่างชั้นเซลล์ฐานเยื่อบุกระจกตา กับเยื่อ Bowman บริเวณใกล้ส่วนหัว จะทำลายเยื่อ Bowman และเกิดการยึดติดกับเนื้อเยื่อชั้นตื้นของสโตรมา
สมมติฐาน “albedo” อธิบายสาเหตุที่พบบริเวณหัวตาด้านจมูก รังสียูวีที่ส่องจากด้านจมูกของใบหน้าผ่านกระจกตา และรวมแสงที่ลิมบัส ด้านจมูกเนื่องจากเอฟเฟกต์เลนส์ของกระจกตา ทำให้เซลล์ต้นกำเนิดบริเวณลิมบัส ด้านจมูกได้รับความเสียหายมากขึ้น การจำลองด้วยคอมพิวเตอร์ยังแสดงให้เห็นว่ารังสียูวีที่ส่องจากด้านข้างรวมแสงที่ลิมบัส ฝั่งตรงข้าม (ด้านหัวตาด้านใน) นอกจากนี้ คารังเคิล รอยพับกึ่งจันทรา และเยื่อบุตา ด้านจมูกมีโครงสร้างทางกายวิภาคที่ได้รับการปกป้องจากเปลือกตาน้อยกว่า จึงสัมผัสรังสียูวีโดยตรงได้ง่ายกว่า
ปัจจัยที่ทำให้รุนแรงขึ้นนอกเหนือจากรังสียูวี ได้แก่ อายุที่มากขึ้น เพศชาย การทำงานกลางแจ้ง และการสัมผัสควันบุหรี่ อัตราความชุกที่สูงในบริเวณอาร์กติกและเส้นศูนย์สูตรยืนยันความสัมพันธ์ที่แน่นแฟ้นกับการสัมผัสรังสียูวี การมีส่วนร่วมของเชื้อ HPV และไวรัสเริมก็มีรายงานเช่นกัน
การสัมผัสรังสียูวี : ปัจจัยเสี่ยงสูงสุด พบมากในผู้ที่ทำงานกลางแจ้งและผู้อยู่อาศัยใกล้เส้นศูนย์สูตร1) อายุและเพศ : อัตราความชุกสูงขึ้นในผู้สูงอายุ เพศชายสูงกว่าเพศหญิงประมาณ 2 เท่าสภาพอากาศและสิ่งแวดล้อม : การสัมผัสกับความแห้ง ลม ฝุ่นทรายปัจจัยทางพันธุกรรม : มีรายงานประวัติครอบครัวการสูบบุหรี่และการสัมผัสควันบุหรี่ : มีการรายงานว่าการสัมผัสนิโคตินและโคตินินเปลี่ยนแปลงการเจริญเติบโตและการเคลื่อนที่ของเซลล์ต้อเนื้อ1) การติดเชื้อไวรัส : มีการเสนอว่า HPV และ HS V อาจเกี่ยวข้อง
ปัจจัยเสี่ยงต่อการกลับเป็นซ้ำ ได้แก่ อายุน้อย ต้อเนื้อหนาและไม่โปร่งแสง (Tan T3) และการอักเสบรุนแรง1) 11) โดยเฉพาะในผู้ป่วยอายุน้อยที่อายุต่ำกว่า 40 ปี ความสามารถในการเจริญเติบโตของเนื้อเยื่อสูงกว่าผู้สูงอายุ และอัตราการกลับเป็นซ้ำหลังผ่าตัดเพิ่มขึ้นหลายเท่า ในการพิจารณาผ่าตัด สิ่งสำคัญคือไม่ใช่ “รีบผ่าตัดเพราะผู้ป่วยอายุน้อย” แต่ต้อง “อธิบายความเสี่ยงในการกลับเป็นซ้ำและพิจารณาอย่างรอบคอบเพราะผู้ป่วยอายุน้อย”
ผู้ที่ทำงานกลางแจ้ง : อาชีพที่ต้องอยู่กลางแจ้งเป็นเวลานาน เช่น เกษตรกรรม ประมง ก่อสร้าง วนศาสตร์ มีปริมาณการได้รับรังสีอัลตราไวโอเลตสูงและโรคมีแนวโน้มดำเนินเร็ว แม้จะไม่สามารถใส่แว่นกันแดดเป็นประจำเนื่องจากลักษณะงาน ควรแนะนำให้สวมหมวกปีกกว้างหรือแว่นตาป้องกันชนิดป้องกันลมผู้สูงอายุ : มักมีภาวะน้ำตาลดลงตามวัยและต้อเนื้อร่วมด้วย ทำให้อาการระคายเคืองของต้อเนื้อแย่ลงได้ง่ายประวัติการผ่าตัดแก้ไขสายตา : เมื่อต้อเนื้อเกิดขึ้นบนกระจกตา หลังการทำ LASIK หรือ PRK การวางแผนผ่าตัดจะซับซ้อนมากขึ้น การประเมินรูปร่างกระจกตา ก่อนผ่าตัดมีความสำคัญเป็นพิเศษความเป็นไปได้ในการผ่าตัดต้อหิน ในอนาคต : การผ่าตัดที่ใช้เยื่อบุตา ขาวเป็นบริเวณกว้างอาจลดอัตราความสำเร็จของการผ่าตัดสร้างทางระบายน้ำในอนาคต ควรเลือกวิธีผ่าตัดที่สงวนเยื่อบุตา ขาวส่วนบนไว้
การป้องกันต้อเนื้อ สิ่งที่สำคัญที่สุดคือการปกป้องดวงตาจากรังสีอัลตราไวโอเลต เมื่อออกนอกบ้านควรใส่แว่นกันแดดหรือแว่นตาที่มีคุณสมบัติป้องกันรังสียูวี และสวมหมวกเพื่อหลีกเลี่ยงแสงแดดโดยตรง ผู้ที่ทำงานกลางแจ้งเป็นประจำควรระมัดระวังเป็นพิเศษ ในสภาพแวดล้อมที่แห้งหรือมีฝุ่นมาก การใช้แว่นตาป้องกันก็มีประสิทธิภาพเช่นกัน
Q
ต้อเนื้อเกิดขึ้นที่ตาทั้งสองข้างหรือไม่?
A
ต้อเนื้อมักเป็นที่ตาข้างเดียว แต่ประมาณ 10% เกิดขึ้นที่ตาทั้งสองข้าง กรณีที่เกิดทั้งด้านจมูกและด้านขมับพบได้ 2–3% เนื่องจากการได้รับรังสียูวีมีผลต่อทั้งสองตาเท่ากัน ดังนั้นหากเกิดที่ตาข้างเดียว การติดตามดูตาอีกข้างก็มีความสำคัญเช่นกัน
การวินิจฉัยต้อเนื้อสามารถทำได้ง่ายโดยการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีดแสง (slit lamp) การวินิจฉัยค่อนข้างง่ายจากลักษณะรูปร่างสามเหลี่ยมของเนื้อเยื่อเส้นเลือดและเนื้อเยื่อเส้นใยที่งอกเข้าสู่กระจกตา ทางด้านจมูก อย่างไรก็ตาม เมื่อพิจารณาการผ่าตัด จำเป็นต้องสังเกตรายละเอียดการกระจายของรอยโรคและการเสียหน้าที่ของลิมบัส สัญญาณจากกล้องจุลทรรศน์ชนิดกรีดแสงที่ควรบันทึก ได้แก่ ระดับการขยายของหลอดเลือดและเลือดคั่งในตัวต้อเนื้อ ความหนาของหัวต้อเนื้อ ตำแหน่งปลาย cap (ระยะห่างจากศูนย์กลางกระจกตา ) การมีหรือไม่มี Stocker’s line และการมีหรือไม่มี dellen
การตรวจสายตาและการหาค่าสายตา : การยืนยันค่าระดับสายตา เป็นสิ่งจำเป็นเนื่องจากต้อเนื้อเป็นโรคผิวตาที่ทำให้การมองเห็น บกพร่องการวิเคราะห์รูปทรงกระจกตา (topography)สายตาเอียง ที่ไม่สม่ำเสมอ มีประโยชน์ในการตัดสินใจผ่าตัดKeratometry (การวัดความโค้งกระจกตา ) : การประเมินการเปลี่ยนแปลงความโค้งของกระจกตา เครื่องตรวจวินิจฉัยคลื่นแสงส่วนหน้าของตา (Anterior segment OCT ) : การประเมินว่ากระจกตา บางลงหรือไม่ มีประโยชน์ในการแยกจากต้อเนื้อเทียมและการวางแผนผ่าตัดการตรวจการลอดผ่านของหัวตรวจ : การตรวจว่าหัวตรวจสามารถสอดใต้รอยโรคบริเวณใกล้ลิมบัส ได้หรือไม่ (ต้อเนื้อสามารถสอดได้, ต้อเนื้อเทียมไม่สามารถสอดได้)
ต้อเนื้อเทียม (Pseudopterygium) : เกิดภายหลังการบาดเจ็บทางเคมีของกระจกตา และเยื่อบุตา , การผ่าตัดตา, การบาดเจ็บ, แผลที่กระจกตา , การสึกกร่อนของเยื่อบุกระจกตา ที่ยืดเยื้อ, การติดเชื้อที่กระจกตา , โรคเยื่อบุตา ที่มีแผลเป็น เป็นต้น ต้อเนื้อมักเกิดทางด้านจมูก ในขณะที่ต้อเนื้อเทียมสามารถเกิดได้ทุกทิศทางไม่เฉพาะด้านจมูก นอกจากนี้เนื้อเยื่อเจริญยึดติดกับผิวกระจกตา ทั้งหมด ทำให้ไม่สามารถสอดหัวตรวจใต้รอยโรคได้ - ต้อลม (Pinguecula) : ตุ่มนูนเล็กสีขาวเหลืองติดกับลิมบัส ไม่ลุกลามเข้าไปในกระจกตา มะเร็งเยื่อบุผิวนอกระยะลุกลามของเยื่อบุตา (CIN ) และมะเร็งเซลล์สความัส : อาจเกิดร่วมกับต้อเนื้อได้ เมื่อพบลักษณะผิดปกติจำเป็นต้องวินิจฉัยแยกโรค - ไฝ เยื่อบุตา Pemphigoid ทางตา : มีแผลเป็นของเยื่อบุตา และการยึดติดระหว่างเยื่อบุตา กับลูกตา มักพบในสองตาโรคกระจกตา เสื่อมเทอร์เรียน (Terrien corneal degeneration) : โรคเสื่อมเรื้อรังที่ทำให้กระจกตา ส่วนปลายบางลง ในรายที่ดำเนินมากอาจมีเนื้อเยื่อเส้นใยและหลอดเลือดเจริญบนกระจกตา ทำให้มีลักษณะคล้ายต้อเนื้อได้ภาวะเยื่อบุตาอักเสบ บริเวณลิมบัส (Limbal conjunctivitis) : มีปุ่มอักเสบและเลือดคั่งที่ลิมบัส คล้ายกับเลือดคั่งของตัวต้อเนื้อ แยกโดยประวัติและการมีภาวะภูมิแพ้เยื่อบุตาหย่อน (Conjunctivochalasis)เยื่อบุตา ส่วนล่างเกินพอดี ทำให้เลือดคั่งและรู้สึกมีสิ่งแปลกปลอม สามารถเกิดขึ้นได้โดยไม่ขึ้นกับต้อเนื้อ ในกรณีที่เกิดร่วมกันต้องแยกและประเมินทั้งสองภาวะ
การทำความเข้าใจโรคที่เกิดร่วมและโรคที่ต้องวินิจฉัยแยกของต้อเนื้อมีความสำคัญในการวางแผนผ่าตัด ต้อเนื้อเทียมอาจทำให้กระจกตา บางลงอย่างมาก ซึ่งอาจนำไปสู่การทะลุของกระจกตา ในระหว่างและหลังผ่าตัด หาก OCT ส่วนหน้าพบว่ากระจกตา บางลง ควรพิจารณาผ่าตัดเปลี่ยนกระจกตา ชั้นผิวร่วมในคราวเดียวกันโดยใช้กระจกตา ที่เก็บรักษาไว้
เมื่อตรวจพบว่ารูปทรงของต้อเนื้อไม่ปกติจากการตรวจด้วย slit lamp (หัวแยกเป็นสองแฉก ปลายไม่เรียบ ผิวเป็นปุ่ม มีเลือดออก/เนื้อตาย) ควรคำนึงถึงมะเร็งเยื่อบุผิวชั้นในของเยื่อบุตา หรือมะเร็งเซลล์สความัส และต้องตรวจทางจุลพยาธิวิทยาของชิ้นเนื้อที่ตัดออกเสมอ แม้พบได้ยาก แต่มีรายงานผู้ป่วยที่มารับการรักษาด้วยลักษณะของต้อเนื้อ แต่แท้จริงแล้วเป็น OSSN
ต้อเนื้อที่ไม่มีอาการสามารถสังเกตอาการได้โดยไม่ต้องรักษา สำหรับภาวะเลือดคั่งและอาการรู้สึกมีสิ่งแปลกปลอม ให้รักษาตามอาการดังนี้
ยาหยอดตาสเตียรอยด์ ความเข้มข้นต่ำ : ลดอาการเลือดคั่งและการอักเสบยาหยอดตา NSAIDs : ลดอาการรู้สึกมีสิ่งแปลกปลอมและเลือดคั่งน้ำตาเทียม / ยาหยอดตากรดไฮยาลูโรนิก : จัดการอาการตาแห้ง จากการกระจายตัวของน้ำตาที่ผิดปกติ
อย่างไรก็ตาม การรักษาด้วยยาไม่สามารถหยุดการดำเนินโรคของรอยโรคได้ และกรณีที่ลุกลามจำเป็นต้องผ่าตัด การป้องกันรังสียูวีด้วยแว่นกันแดดและหมวกปีกกว้าง การทำให้น้ำตาคงที่ด้วยน้ำตาเทียม การหยอดกรดไฮยาลูโรนิกหรือไดควาโฟซอลโซเดียม 3% ในกรณีที่มีตาแห้ง ก็ใช้ร่วมด้วย การใช้ยาหยอดตาสเตียรอยด์ เป็นเวลานานมีความเสี่ยงต่อการเพิ่มความดันลูกตา ต้อกระจก ใต้แคปซูลด้านหลัง และการติดเชื้อ จึงไม่ควรใช้อย่างไม่ระมัดระวัง และควรประเมินความดันลูกตา และเลนส์แก้วตา เป็นระยะ
พิจารณาผ่าตัดในกรณีต่อไปนี้
เมื่อรอยโรคพาดผ่านแนวสายตา
เมื่อการลุกลามเข้าไปในกระจกตา ดำเนินไปจนทำให้เกิดสายตาเอียง ผิดปกติและการมองเห็น ลดลง
เมื่อเกิดข้อจำกัดของการเคลื่อนไหวลูกตา
เหตุผลด้านความสวยงาม
อธิบายข้อดีของการผ่าตัดและความเสี่ยงของการกลับเป็นซ้ำหลังผ่าตัดอย่างละเอียด และตัดสินใจข้อบ่งชี้ร่วมกับการปรึกษาผู้ป่วย ต้องอธิบายให้ผู้ป่วยทราบโดยคำนึงว่าผู้ป่วยอายุน้อยมีแนวโน้มกลับเป็นซ้ำได้ง่ายกว่า
การผ่าตัดต้อเนื้อประกอบด้วยการตัดเนื้อเยื่อเจริญผิดปกติออกและการสร้างพื้นผิวลูกตาขึ้นใหม่ วิธีการมาตรฐานในปัจจุบันคือการปลูกถ่ายเยื่อบุตา ชนิด autograft (conjunctival autograft; CAG) หรือการปลูกถ่ายเยื่อบุตา ร่วมกับลิมบัส ชนิด autograft (limbal-conjunctival autograft; LCAG)1) 11) การผสมผสานระหว่างการสร้างเยื่อบุตา ขึ้นใหม่และการยับยั้งเนื้อเยื่อเจริญผิดปกติเป็นหลักการป้องกันการกลับเป็นซ้ำ โดยเลือกใช้วิธีใดวิธีหนึ่งจาก: แผ่นเยื่อบุตา ชนิดมีก้าน, แผ่นเยื่อบุตา ชนิดอิสระ, หรือการคลุมด้วยเยื่อหุ้มครรภ์
ขั้นตอนการผ่าตัดทั่วไปมีดังนี้
หยอดยาชาและฉีดยาชาใต้เยื่อบุตา
ลอกหัวต้อเนื้อออกจากกระจกตา พร้อมกับเยื่อบุตา และถุง Tenon
กำจัดเนื้อเยื่อที่เหลือบนผิวกระจกตา ให้มากที่สุด และทำให้เรียบด้วยหัวกรอเพชรหรือคีมมีขอ
กำจัดถุง Tenon บริเวณลำตัวต้อเนื้อออกในวงกว้าง (ขั้นตอน “การดึงปุยฝ้าย”)
หากจำเป็น ทา mitomycin C (0.02–0.04%) นาน 1–3 นาที แล้วล้างออกด้วยน้ำเกลือให้สะอาด
นำแผ่นเยื่อบุตา หรือแผ่น LCAG จากเยื่อบุตา ลูกตาส่วนบน
ยึดแผ่นปลูกถ่ายเข้ากับบริเวณที่ตัดออกด้วยการเย็บหรือกาวไฟบริน
รอให้เยื่อบุตา บริเวณที่นำแผ่นออกสร้างเซลล์เยื่อบุผิวเอง หรือเย็บปิดหากชิ้นส่วนมีขนาดเล็ก
การปลูกถ่ายเยื่อบุตาชนิด autograft (CAG/LCAG)
แผ่นเยื่อบุตา ชนิดมีก้าน : เคลื่อนย้ายเยื่อบุตา ที่อยู่ติดกันมาคลุมบริเวณที่ตัดออก สามารถสร้างเนื้อเยื่อใหม่ได้ในขณะที่รักษาการไหลเวียนเลือดไว้ มีความปลอดภัยสูง
แผ่นเยื่อบุตา ชนิดอิสระ (CAG) : นำแผ่นเยื่อบุตา จากตำแหน่งอื่น (ส่วนใหญ่คือเยื่อบุตา ลูกตาส่วนบน-ด้านขมับ) มาปลูกถ่าย ข้อดีคือสามารถเย็บติดได้ทุกตำแหน่ง
การปลูกถ่ายเยื่อบุตา ร่วมกับลิมบัส ชนิด autograft (LCAG) : การปลูกถ่ายเยื่อบุตา ชนิด autograft ที่รวมเนื้อเยื่อลิมบัส ไว้ด้วย การฟื้นฟูการทำงานของลิมบัส ช่วยให้อัตราการกลับเป็นซ้ำลดลงยิ่งขึ้น1) 9)
วิธีการสร้างเนื้อเยื่อใหม่แบบอื่น
การปลูกถ่ายเยื่อหุ้มครรภ์ : สามารถคลุมเยื่อบุตา ที่ขาดหายไปในบริเวณกว้างได้ มีฤทธิ์ต้านการอักเสบ ยับยั้งการสร้างเส้นเลือดใหม่ และยับยั้งการเจริญของไฟโบรบลาสต์ มีประโยชน์ในต้อเนื้อที่กลับเป็นซ้ำและกรณีที่ต้องตัดเนื้อเยื่อออกในวงกว้าง10)
แผ่นเยื่อบุตา ชนิดหมุน : หมุนเยื่อบุตา ที่อยู่ติดกันมาคลุมบริเวณที่ตัดออก11)
กาวไฟบริน (Fibrin glue) : ใช้เป็นวิธีการยึดติดชิ้นเนื้อปลูกแทนที่การเย็บแผล มีรายงานว่าช่วยลดระยะเวลาการผ่าตัดและการอักเสบหลังผ่าตัด
อัตราการเกิดซ้ำของแต่ละวิธีในการผ่าตัดต้อเนื้อแสดงดังต่อไปนี้1) 9) 10)
วิธีการผ่าตัด อัตราการเกิดซ้ำ วิธีเปิดตาขาว (bare sclera) 30–89% การปลูกถ่ายเยื่อบุตา ด้วยตนเอง (CAG) 1.9–8% การปลูกถ่ายเยื่อบุตา ด้วยตนเองบริเวณลิมบัส (LCAG) 0–17% การปลูกถ่ายเยื่อหุ้มน้ำคร่ำ 3.7–40.9%
วิธีเปิดตาขาว มีอัตราการเกิดซ้ำสูงมากและปัจจุบันไม่แนะนำให้ใช้1) การปลูกถ่ายเยื่อบุตา ด้วยตนเองเป็นมาตรฐานทองคำในปัจจุบัน โดยเฉพาะ LCAG ที่มีอัตราการเกิดซ้ำต่ำที่สุด1) 9) ในการวิเคราะห์อภิมานของ Zheng และคณะ รายงานว่า LCAG มีอัตราการเกิดซ้ำต่ำกว่าอย่างมีนัยสำคัญเมื่อเทียบกับ bare sclera การปลูกถ่ายเยื่อบุตา ด้วยตนเอง และการรักษาด้วย MMC ระหว่างผ่าตัด (ความแตกต่างกับการปลูกถ่ายเยื่อหุ้มน้ำคร่ำไม่มีนัยสำคัญทางสถิติ)9)
อัตราการเกิดซ้ำของการปลูกถ่ายเยื่อหุ้มน้ำคร่ำในการวิเคราะห์อภิมานของ Li และคณะเท่ากับ 3.7–40.9% ซึ่งสูงกว่าการปลูกถ่ายเยื่อบุตา ด้วยตนเอง (2.6–17.7%) อย่างไรก็ตาม เป็นทางเลือกที่มีประโยชน์สำหรับผู้ป่วยที่มีแผลเป็นที่เยื่อบุตา อย่างกว้างขวาง หรือผู้ป่วยที่อาจต้องได้รับการผ่าตัดต้อหิน ในอนาคต10)
รายงานของ Oke และคณะที่วิเคราะห์ข้อมูล 102,138 รายจากทะเบียน IRIS ของสหรัฐอเมริกา พบว่าอัตราการผ่าตัดซ้ำใน 5 ปีของกลุ่มปลูกถ่ายเนื้อเยื่อเท่ากับ 7.7% และกลุ่ม bare sclera เท่ากับ 11.0% วิธี bare sclera ยังคงคิดเป็นประมาณ 15% ของการผ่าตัดต้อเนื้อในสหรัฐอเมริกา2)
ในการปลูกถ่ายแผ่นเยื่อบุตา อิสระ การแยกแยะด้านหน้าและด้านหลังของชิ้นเนื้อปลูกถ่ายอาจเป็นปัญหาได้ มีรายงานวิธีการพลิกสองครั้ง (double flip) เพื่อรักษาทิศทางที่ถูกต้องของชิ้นเนื้อปลูกถ่าย3)
Öztürk và cộng sự đã công bố kỹ thuật double flip trong ghép kết mạc tự thân, bằng cách cắt ba cạnh của mảnh ghép, sau đó lật ngược mảnh ghép ở cạnh chưa cắt và cố định bằng hai mũi khâu, rồi cắt cạnh thứ tư và lật lại lần nữa. Kỹ thuật này giúp duy trì chắc chắn hướng bề mặt biểu mô và hướng rìa–vòm của mảnh ghép3) .
เพื่อลดอัตราการกลับเป็นซ้ำให้ดียิ่งขึ้น จึงใช้การรักษาเสริมร่วมกับวิธีดังต่อไปนี้1) 11)
ไมโตมัยซิน ซี (MMC) : สารละลายความเข้มข้น 0.02–0.04% ชุ่มบนฟองน้ำและวางบนตาขาว นาน 1–5 นาที แล้วล้างออกด้วยน้ำปริมาณมาก ยับยั้งการเจริญของไฟโบรบลาสต์ใต้เยื่อบุตา ในประเทศญี่ปุ่น ไม่ครอบคลุมโดยประกันสุขภาพ และต้องได้รับคำอธิบายและความยินยอมอย่างเพียงพอก่อนใช้ ในการทดลองแบบสุ่มมีกลุ่มควบคุมของ Lam อัตราการกลับเป็นซ้ำในกลุ่มที่ใช้ MMC 0.02–0.04% นาน 5 นาทีอยู่ที่ 8.3–8.6% ส่วนกลุ่มที่ใช้นาน 3 นาทีอยู่ที่ 22.9–42.9% แสดงให้เห็นถึงผลกระทบของระยะเวลาในการวางยา8) ในการทดลองแบบสุ่มมีกลุ่มควบคุมระยะยาว 10 ปีของ Young อัตราการกลับเป็นซ้ำในกลุ่ม MMC อยู่ที่ 25.5% เทียบกับกลุ่ม LCAG อยู่ที่ 6.9% ซึ่ง LCAG เหนือกว่าในระยะยาว7) 5-ฟลูออโรยูราซิล (5-FU) : มีรายงานว่ามีภาวะแทรกซ้อนน้อยกว่า MMC และการฉายรังสีบีตา ในการศึกษาเปรียบเทียบของ Silva อัตราการกลับเป็นซ้ำในกลุ่ม 5-FU อยู่ที่ 5.83% เทียบกับ 25.5% ในกลุ่มที่ไม่ใช้15) การฉายรังสีบีตา : อัตราการกลับเป็นซ้ำ 0–11.8% แสดงให้เห็นถึงประสิทธิผล แต่มีรายงานภาวะแทรกซ้อนรุนแรง เช่น ตาขาว บางลง ตาขาว ละลาย ตาขาว ทะลุ เยื่อบุตาอักเสบ ติดเชื้อในลูกตา และต้อกระจก ที่แย่ลง ดังนั้นปัจจุบันจึงมีคำแนะนำในระดับต่ำ13) การรักษาด้วยยาต้าน VEGF (เบวาซิซูแมบ )เยื่อบุตา และยาหยอดตาหลังผ่าตัด ในการวิเคราะห์อภิมานปี 2018 ของ Sun รายงานว่าอัตราการกลับเป็นซ้ำลดลงเมื่อติดตามผล 12 เดือน แต่วิธีการให้ยาที่เหมาะสมที่สุดยังไม่ได้รับการกำหนด14) ยาหยอดตาไซโคลสปอรีน : การวิเคราะห์อภิมานแบบเครือข่ายปี 2017 โดย Fonseca และคณะ (14 การแทรกแซง, 24 RCT) พบว่าการปลูกถ่ายเยื่อบุตา ชนิดผู้ป่วยเองร่วมกับยาหยอดตาไซโคลสปอรีน 0.05% มีประสิทธิภาพสูงสุดในการป้องกันการกลับเป็นซ้ำ6)
เพื่อลดการอักเสบหลังผ่าตัดและยับยั้งการเจริญเพิ่มของเนื้อเยื่อใต้เยื่อบุตา มักใช้ตัวอย่างใบสั่งยาหยอดตาดังต่อไปนี้
ยาหยอดตาเลโวฟลอกซาซิน (Cravit®) 1.5% : วันละ 4 ครั้ง นาน 1 สัปดาห์ถึง 1 เดือนหลังผ่าตัดยาหยอดตาเบตาเมธาโซนโซเดียมฟอสเฟต (Rinderon®) 0.1% : วันละ 4 ครั้ง ต่อเนื่องประมาณ 6 เดือนหลังผ่าตัดยาหยอดตาทรานิลาสต์ (Rizaben®) 0.5% : วันละ 4 ครั้ง ต่อเนื่อง 6 เดือนหลังผ่าตัดเพื่อยับยั้งการเจริญเพิ่มของเนื้อเยื่อใต้เยื่อบุตา
ในบางสถานพยาบาล อาจใช้ยาหยอดตาflurometholone 0.1% แทนเบตาเมธาโซนเพื่อลดความเสี่ยงของความดันลูกตา สูง และใช้ยาหยอดตากรดไฮยาลูโรนิกร่วมด้วยเพื่อปกป้องเยื่อบุผิว การตัดไหมทำหลังจากประมาณ 2 สัปดาห์ หากปล่อยไว้ การอักเสบจะยืดเยื้อและกระตุ้นให้เกิดการกลับเป็นซ้ำ
การผ่าตัดครั้งแรกที่เหมาะสมช่วยควบคุมอัตราการกลับเป็นซ้ำให้อยู่ที่ 1.5–5% หากเกิดการกลับเป็นซ้ำ ไม่ควรผ่าซ้ำทันที แต่ให้ใช้ยาหยอดสเตียรอยด์ และทรานิลาสต์ต่อเนื่องประมาณ 6 เดือน ติดตามความคืบหน้าของการเจริญเพิ่มก่อนตัดสินใจว่าจำเป็นต้องผ่าซ้ำหรือไม่ การเจริญเพิ่มของเนื้อเยื่อที่กลับเป็นซ้ำอาจลดกิจกรรมลงเองในช่วง 6 เดือนถึง 1 ปีของการติดตาม ทำให้การผ่าซ้ำมีความยากลดลง
สำหรับข้อบกพร่องของเยื่อบุผิวที่หายช้าหลังผ่าตัด อาจใช้คอนแทคเลนส์นิ่มชนิดรักษา (ผลิตภัณฑ์ที่ได้รับอนุมัติในญี่ปุ่นคือ Air Optix® ของ Alcon) ซึ่งทำจากซิลิโคนไฮโดรเจลใส่ต่อเนื่องได้ 30 วัน ช่วยส่งเสริมการยึดติดของเยื่อบุผิวและบรรเทาอาการปวดตา ระหว่างใส่ หากเลนส์สกปรกหรือแห้งมาก ให้ล้างด้วยน้ำเกลือหรือเปลี่ยนเลนส์ใหม่ ห้ามใช้เมื่อมีการติดเชื้อที่มีกิจกรรม
มาตรฐานการติดตามผลหลังผ่าตัดคือ วันถัดไป, 1 สัปดาห์, 2 สัปดาห์ (ตัดไหม), 1 เดือน, 3 เดือน, 6 เดือน เนื่องจากการกลับเป็นซ้ำส่วนใหญ่ภายใน 6 เดือนเกิดขึ้นในช่วงเวลานี้ การมาติดตามผลอย่างสม่ำเสมอจึงมีความสำคัญอย่างยิ่ง สัญญาณเริ่มต้นของการกลับเป็นซ้ำ ได้แก่ การพบหลอดเลือดขนาดเล็กบุกรุกเข้าไปในกระจกตา จากขอบของพนังปลูกถ่ายหรือบริเวณที่ถูกตัดออก หากตรวจพบตั้งแต่ระยะแรก อาจสามารถควบคุมการดำเนินโรคได้โดยการเพิ่มความถี่ของยาหยอดตาสเตียรอยด์
เมื่อต้อเนื้อกลับเป็นซ้ำ เนื้อเยื่อเจริญที่มีฤทธิ์สูงจะยึดเกาะแน่นตั้งแต่กระจกตา จนถึงกล้ามเนื้อเรกตัสด้านใน ทำให้การผ่าตัดยากกว่าครั้งแรก มักจำเป็นต้องตัดรอยโรคออกอย่างกว้างขวางรวมถึงบริเวณรอบกล้ามเนื้อเรกตัสด้านใน และมักต้องใช้การปลูกถ่ายเยื่อหุ้มไข่ปลา การทาไมโตมัยซินซี และการปลูกถ่ายลิมบัส ตนเองร่วมกัน การผ่าตัดต้อเนื้อที่กลับเป็นซ้ำมักเป็นการผ่าตัดแบบซับซ้อนที่ผสมผสานหลายเทคนิค เช่น การลอกและยึดกล้ามเนื้อเรกตัสด้านในใหม่ การปิดเยื่อหุ้มไข่ปลาตามขนาดของรอยขาดของเยื่อบุตา และการปลูกถ่ายกระจกตา ชั้นตื้นร่วมหากจำเป็น
ในเรื่องการตัดสินใจระยะเวลาการผ่าตัดซ้ำสำหรับต้อเนื้อที่กลับเป็นซ้ำ เนื่องจากการผ่าตัดซ้ำโดยไม่เหมาะสมในระยะที่มีการอักเสบและการเจริญที่ active สูงอาจทำให้กลับเป็นซ้ำมากขึ้น จึงสมเหตุสมผลที่จะลดการอักเสบด้วยยาหยอดตาสเตียรอยด์ ก่อน แล้วจึงผ่าตัดซ้ำเมื่อกิจกรรมของโรคลดลง สิ่งสำคัญคือผู้ป่วยต้องเข้าใจนโยบายที่ว่า “ไม่ต้องผ่าตัดทันทีเมื่อกลับเป็นซ้ำ” แต่ “สังเกตอาการประมาณหกเดือนหลังจากกลับเป็นซ้ำ แล้วจึงค่อยพิจารณาผ่าตัดซ้ำ”
เมื่อทา MMC หรือฉายรังสี อาจเกิดการบางลงของตาขาว หรือตาขาว ทะลุ ซึ่งอาจต้องปลูกถ่ายตาขาว มีรายงานการติดเชื้อจากเชื้อก่อโรค เช่น Candida ด้วย ต้องระวังความดันลูกตา สูงจากการใช้สเตียรอยด์ เป็นเวลานานหลังผ่าตัด ภาวะแทรกซ้อนหลังผ่าตัดที่รายงาน ได้แก่ การติดเชื้อ การเกิด dellen แผลถลอกเยื่อบุผิวที่หายช้า แกรนูโลมา และตาขาว อักเสบชนิดเนื้อตาย การผ่าตัดต้อเนื้อที่กลับเป็นซ้ำยากกว่าการผ่าตัดครั้งแรก และเนื้อเยื่อเจริญที่ active สูงอาจยึดเกาะแน่นจนถึงกล้ามเนื้อเรกตัสด้านใน
Q
จะป้องกันการกลับเป็นซ้ำหลังผ่าตัดต้อเนื้อได้อย่างไร?
A
การปลูกถ่ายเยื่อบุตา ชนิด autograft (CAG หรือ LCAG) เป็นสิ่งสำคัญที่สุด การวิเคราะห์อภิมานแบบเครือข่ายพบว่าการใช้ CAG ร่วมกับ cyclosporine 0.05% ยาหยอดตามีประสิทธิภาพสูงสุดในการป้องกันการกลับเป็นซ้ำ การใช้ steroid และ tranilast ยาหยอดตาต่อเนื่องเป็นเวลา 6 เดือนหลังผ่าตัดก็ช่วยลดอัตราการกลับเป็นซ้ำได้เช่นกัน การผ่าตัดครั้งแรกที่เหมาะสมสามารถควบคุมอัตราการกลับเป็นซ้ำได้ประมาณ 1.5–5% การป้องกันรังสียูวียังมีประสิทธิภาพในการป้องกันการกลับเป็นซ้ำในระยะยาว
ความเสียหายของเซลล์ต้นกำเนิดบริเวณลิมบัส จากรังสียูวีมีบทบาทสำคัญในการเกิดต้อเนื้อ1) เนื้อเยื่อลิมบัส ปกติทำหน้าที่เป็นเกราะป้องกันเนื้อเยื่อใต้เยื่อบุตา รุกล้ำเข้าไปในกระจกตา แต่เมื่อการทำงานนี้ล้มเหลวจากการได้รับรังสี UV‑B เรื้อรัง จะเกิดต้อเนื้อขึ้น ปัจจุบันต้อเนื้อไม่ได้ถูกมองว่าเป็นเพียงการเสื่อมของเยื่อบุตา ตามวัย แต่เป็นพยาธิสภาพที่ซับซ้อนซึ่งประกอบด้วย “ความเสียหายของเซลล์ต้นกำเนิดเยื่อบุเฉพาะที่ + การ proliferative ของเนื้อเยื่อเส้นใยและหลอดเลือด + การอักเสบเรื้อรัง”
การกลายพันธุ์ของ p53 และ MDM2 : รังสียูวีทำให้เกิดความเสียหายต่อดีเอ็นเอ นำไปสู่การกลายพันธุ์ของยีน p53 ในเนื้อเยื่อต้อเนื้อพบว่าการแสดงออกของ p53 และ MDM2 (mouse double minute 2) เพิ่มขึ้นทั้งคู่ แต่ p53 อยู่ในไซโทพลาสซึมเป็นหลักและแทบไม่พบในนิวเคลียส12) ดังนั้นจึงไม่เกิด apoptosis และตรวจไม่พบ p21 ซึ่งเป็นเป้าหมายการถอดรหัสของ p53 ความผิดปกติของวิถี p53‑MDM2 เชื่อว่าสนับสนุนการอยู่รอดและการเพิ่มจำนวนของเซลล์ต้อเนื้อ1) 12) การกระตุ้น matrix metalloproteinase (MMP) : MMP‑1, MMP‑2, MMP‑9 และอื่นๆ ถูกกระตุ้น ย่อยสลาย Bowman membrane และ extracellular matrix ส่งเสริมการรุกล้ำของเนื้อเยื่อปัจจัยสร้างหลอดเลือด : VEGF, bFGF และอื่นๆ มีการแสดงออกมากเกินไป ส่งเสริมการสร้างหลอดเลือดใหม่จำนวนมากในต้อเนื้อ1) HIF‑1α : Hypoxia‑inducible factor มีการแสดงออกเพิ่มขึ้น ส่งเสริมการสร้างหลอดเลือดผ่านการตอบสนองต่อภาวะขาดออกซิเจนความเครียดออกซิเดชัน : มีรายงานการสะสมของ 8-OHdG (เครื่องหมายความเสียหายของดีเอ็นเอจากออกซิเดชัน) ซึ่งบ่งชี้ถึงการมีส่วนร่วมของความเครียดออกซิเดชัน1) การสะสมโปรตีนผิดปกติใต้เยื่อบุ : โปรตีนรวมตัวผิดปกติที่เสื่อมสภาพจากไกลเคชันและเรซีไมเซชันจะสะสมอยู่ใต้เยื่อบุผิว และมีความคิดว่าความผิดปกติของเนื้อเยื่อเกี่ยวพันใต้เยื่อบุผิวเป็นสาเหตุหลักของโรค - การเปลี่ยนสภาพเยื่อบุผิวเป็นมีเซนไคม์ (EMT) : ในเซลล์เยื่อบุผิวต้อเนื้อ มีรายงานการลดลงของเครื่องหมายเยื่อบุผิวเดิมของเยื่อบุตา ขาวและการเพิ่มขึ้นของเครื่องหมายมีเซนไคม์ เชื่อว่าเซลล์ที่ได้รับความสามารถในการเคลื่อนที่และการเพิ่มจำนวนผ่าน EMT จะเคลื่อนที่ไปบนกระจกตา ฤทธิ์เทโลเมอเรสและการยับยั้งอะพอพโทซิส : มีรายงานการเปลี่ยนแปลงของฤทธิ์เทโลเมอเรสในเซลล์เยื่อบุผิวต้อเนื้อ ทำให้เซลล์สามารถเพิ่มจำนวนอย่างต่อเนื่อง - การเกี่ยวข้องของไวรัส : มีรายงานการตรวจพบไวรัส เช่น HPV และ HS V ในเนื้อเยื่อต้อเนื้อ และมีการชี้ให้เห็นถึงความเป็นไปได้ที่การติดเชื้อไวรัสจะกระตุ้นให้เกิดการเสื่อมของเยื่อบุผิวและการตอบสนองทางภูมิคุ้มกัน ซึ่งมีส่วนร่วมในการเกิดโรค
การเพิ่มขึ้นของเนื้อเยื่อเกี่ยวพันใต้เยื่อบุตา และการเสื่อมสภาพแบบอีลาสตอยด์ (elastoid degeneration) ของเส้นใยคอลลาเจนเป็นลักษณะเด่น มีการแทรกซึมของเซลล์อักเสบเรื้อรังซึ่งส่วนใหญ่เป็นลิมโฟไซต์ เนื้อเยื่อต้อเนื้อจะข้ามสิ่งกีดขวางของเยื่อ Bowman ที่ลิมบัส ของกระจกตา แทรกซึมระหว่างชั้นเซลล์ฐานเยื่อบุผิวกระจกตา กับเยื่อ Bowman ทำลายเยื่อ Bowman บริเวณใกล้ปลายสุดและสร้างการยึดติดกับเนื้อเยื่อสโตรมาชั้นตื้น เมื่อดำเนินโรคไป โปรตีนรวมตัวผิดปกติที่เสื่อมสภาพจากไกลเคชันและเรซีไมเซชันจะสะสมใต้เยื่อบุผิว การเสื่อมของเส้นใยคอลลาเจนและการสร้างเส้นเลือดใหม่จะส่งเสริมการเปลี่ยนแปลงของเนื้อเยื่อเกี่ยวพันใต้เยื่อบุผิว การเปลี่ยนแปลงเนื้อเยื่อที่ซับซ้อนนี้เชื่อว่าอธิบายได้ว่าทำไมการตัดออกอย่างเดียวจึงทำให้เซลล์ที่ยังทำงานอยู่ที่เหลือสามารถเพิ่มจำนวนขึ้นมาใหม่ได้
เนื้อหาต่อไปนี้อยู่ในระยะการศึกษาวิจัยหรืออยู่ระหว่างการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
Oke vàคณะได้วิเคราะห์การผ่าตัดต้อเนื้อ 102,138 รายจากทะเบียน IRIS ของสหรัฐอเมริกา และรายงานว่าวิธีการเปลือยตาขาว (bare sclera) ยังคงถูกใช้ใน 15.3% ของกรณี เมื่อเทียบกับกลุ่มปลูกถ่ายเนื้อเยื่อ อัตราการผ่าซ้ำภายใน 5 ปีในกลุ่มเปลือยตาขาว สูงกว่าอย่างมีนัยสำคัญ (11.0% เทียบกับ 7.7%) และชี้ให้เห็นว่าการเผยแพร่การเลือกวิธีผ่าตัดตามหลักฐานยังคงเป็นความท้าทาย2)
Fonseca vàคณะได้ทำการวิเคราะห์อภิมานแบบเครือข่ายจาก RCT 24 ฉบับที่มีการแทรกแซง 14 รายการ และรายงานว่าการปลูกถ่ายเยื่อบุตา ด้วยตนเองร่วมกับยาหยอด cyclosporine 0.05% มีประสิทธิภาพสูงสุดในการป้องกันการกลับเป็นซ้ำ ในขณะที่การตัดออกอย่างเดียว (bare sclera) มีอัตราการกลับเป็นซ้ำสูงที่สุด อย่างไรก็ตาม การวิเคราะห์รวมเฉพาะการศึกษาที่มีระยะเวลาติดตามผลตั้งแต่ 3 เดือนขึ้นไป และชี้ให้เห็นว่าการขาดการติดตามระยะยาวเป็นข้อจำกัด6)
การศึกษาขั้นพื้นฐานรายงานว่า Nutlin ซึ่งยับยั้งปฏิสัมพันธ์ระหว่าง MDM2-p53 แสดงความเป็นพิษแบบเลือกสรรต่อเซลล์ต้อเนื้อ
ในการศึกษาในหลอดทดลองของ Cao vàคณะ การรักษาด้วย Nutlin ส่งเสริมการเคลื่อนย้าย p53 เข้านิวเคลียส เพิ่มการแสดงออกของ p21 และเหนี่ยวนำให้เกิด apoptosis ที่ความเข้มข้นของ Nutlin ที่ฆ่าเซลล์ต้อเนื้อได้ 50% อัตราการอยู่รอดของเซลล์เยื่อบุตา คือ 95% ในขณะที่ความเข้มข้นของ MMC ที่ให้ผลฆ่าเซลล์เทียบเท่ากัน อัตราการอยู่รอดของเซลล์เยื่อบุตา อยู่ที่เพียง 63%12)
ผลนี้ชี้ให้เห็นว่า Nutlin อาจมีความเลือกสรรต่อเซลล์ต้อเนื้อสูงกว่า MMC และคาดหวังให้พัฒนาเป็นการรักษาเสริมชนิดใหม่
การปลูกถ่ายโครงร่างคอลลาเจน (ย่อยสลายได้ทางชีวภาพใน 90–180 วัน) รายงานว่าทำให้เกิดการอักเสบของเยื่อบุตา และอาการปวดน้อยกว่า MMC และ LCAG1) นอกจากนี้ยังมีรายงานการใช้ร่วมกับการปลูกถ่ายเยื่อบุตา ด้วยตนเองในกรณีตาขาว บางจาก MMC
มีรายงานว่าสามารถเกิดโรคเริมที่กระจกตา (HS K) หลังการผ่าตัดต้อเนื้อได้
Cui และคณะรายงานผู้ป่วย HS K จำนวน 5 รายที่เกิดขึ้นประมาณ 30 วันหลังผ่าตัดต้อเนื้อ ผู้ป่วยทั้งหมดเป็นเพศชาย และ 4 ใน 5 รายเป็น HS K ชนิดเนื้อกระจกตา การตรวจ HS V-sIgA ในน้ำตา, PCR, และการหาลำดับพันธุกรรมยุคใหม่แบบเมทาจีโนมิกส์ (mNGS) มีประโยชน์ในการวินิจฉัย4)
โรคเยื่อบุตาอักเสบ จากเส้นเลือด (scleritis) หลังการตัดต้อเนื้อเป็นภาวะแทรกซ้อนที่พบได้ยากแต่รุนแรง และบางครั้งแยกยากระหว่างสาเหตุจากการติดเชื้อและจากภูมิต้านทานตนเอง
Mabrouki และคณะรายงานผู้ป่วยชายอายุ 70 ปีที่มีเยื่อบุตาอักเสบ จากเส้นเลือดชนิดรุนแรง 7 วันหลังตัดต้อเนื้อ ผลเพาะเชื้อเป็นลบ แต่ตอบสนองต่อยาปฏิชีวนะได้ไม่ดี และดีขึ้นอย่างมากหลังได้รับยาต้านเชื้อรา (voriconazole) มีการอภิปรายถึงความเป็นไปได้ที่การติดเชื้ออาจกระตุ้นปฏิกิริยาภูมิต้านทานตนเอง5)
ในการสร้างพื้นผิวลูกตาขึ้นใหม่หลังการตัดต้อเนื้อ การวิจัยประยุกต์เกี่ยวกับวัสดุทดแทนเยื่อบุตา ตนเอง เช่น แผ่นเยื่อบุผิวเยื่อบุตา ที่เพาะเลี้ยง แผ่นเยื่อบุผิวลิมบัส ที่เพาะเลี้ยง และเนื้อเยื่อที่เอาส่วนประกอบของเซลล์ออก กำลังดำเนินไปอย่างต่อเนื่อง ในประเทศญี่ปุ่น มีประสบการณ์สะสมเกี่ยวกับการใช้ทางคลินิกของผิวหนังเพาะเลี้ยงและเยื่อบุกระจกตา เพาะเลี้ยง และในอนาคตอาจถูกนำไปประยุกต์ใช้ในการสร้างต้อเนื้อที่ซับซ้อนหลังการตัดแบบกว้าง นอกจากนี้ จากมุมมองของเวชศาสตร์ฟื้นฟู การสร้างเซลล์ต้นกำเนิดลิมบัส ที่ใช้งานได้อาจนำไปสู่การรักษาต้อเนื้ออย่างถาวรได้
การปรับให้เหมาะสมของการรักษาด้วย anti-VEGF : จำเป็นต้องกำหนดวิธีการและช่วงเวลาที่เหมาะสมในการให้ bevacizumab14) การรักษาแบบจำเพาะต่อโมเลกุลเป้าหมาย : เส้นทาง MDM2-p53 กำลังถูกค้นพบ และการพัฒนายาเฉพาะทางเช่น Nutlin เป็นที่คาดหวัง12) การใช้ยาหยอดตา cyclosporine ร่วมกัน : การใช้ร่วมกับการปลูกถ่ายเยื่อบุตา ตนเองอาจลดอัตราการกลับเป็นซ้ำ และการนำไปใช้ทางคลินิกในอนาคตเป็นที่คาดหวัง6) ความก้าวหน้าของเครื่องมือผ่าตัดและวิธีการตรึง : วิธีการตรึงด้วยกาวไฟบรินและวิธี double-flip กำลังถูกพัฒนาขึ้นเพื่อลดระยะเวลาผ่าตัดและเพิ่มความสามารถในการทำซ้ำ3) การแบ่งระดับความเสี่ยงก่อนผ่าตัด : การวัดปริมาณความเสี่ยงของการกลับเป็นซ้ำโดยใช้การจำแนกประเภท Tan และความหนาแน่นของหลอดเลือดกำลังขยายวิธีการรักษาเฉพาะบุคคลที่ใช้การรักษาเสริมอย่างจริงจังในกรณีต้อเนื้อหนา11) การวิเคราะห์การแสดงออกของยีน : การวิเคราะห์ทรานสคริปโทมของเนื้อเยื่อต้อเนื้อบ่งชี้ถึงการมีส่วนร่วมของเส้นทาง VEGF, เส้นทางการอักเสบ, เส้นทางการเปลี่ยนผ่านเยื่อบุผิว-มีเซนไคม์ (EMT) และการระบุเป้าหมายการวินิจฉัยระดับโมเลกุลและการรักษากำลังก้าวหน้า1) 12)
Q
หากปล่อยต้อเนื้อไว้โดยไม่รักษาจะเกิดอะไรขึ้น?
A
ต้อเนื้อจะค่อย ๆ ลามเข้าสู่ใจกลางกระจกตา เมื่อการลุกลามเข้าสู่กระจกตา เกิน 2 มม. จะเริ่มเกิดสายตาเอียง ผิดปกติ และเมื่อกระทบกับแกนการมองเห็น จะทำให้การมองเห็น ลดลงอย่างชัดเจน ในกรณีที่ลุกลามมาก อาจเกิดข้อจำกัดของการเคลื่อนไหวลูกตาและการเห็นภาพซ้อน อย่างไรก็ตาม อัตราการดำเนินโรคแตกต่างกันมากในแต่ละบุคคล และบางกรณีอาจไม่เปลี่ยนแปลงเป็นระยะเวลานาน แม้อาการจะยังเล็กน้อย การป้องกันเช่นการป้องกันรังสียูวีก็มีความสำคัญ
Chu WK, Choi HL, Bhat AK, Jhanji V. Pterygium: new insights. Eye (Lond). 2020;34:1047-1050.
Oke I, Buxton IL, Golas L, et al. The prevalence and recurrence risk of bare sclera pterygium surgery in the United States. Ocul Surf. 2023;30:56-62.
Öztürk E, Gündüz A. Double Flip Technique for Graft Transfer in Autograft Pterygium Surgery. Turk J Ophthalmol. 2023;53:67-69.
Cui Y, Wei H, Hu Y, et al. Herpes Simplex Keratitis as a Complication of Pterygium Surgery. Am J Case Rep. 2024;25:e942828.
Mabrouki FZ, Sekhsoukh R. Scleritis Following Pterygium Excision: Infection, Autoimmunity, or Both? Cureus. 2021;13(9):e17736.
Fonseca EC, Rocha EM, Arruda GV. Comparison among adjuvant treatments for primary pterygium: a network meta-analysis. Br J Ophthalmol. 2018;102:748-756.
Young AL, Ho M, Jhanji V, Cheng LL. Ten-year results of a randomized controlled trial comparing 0.02% mitomycin C and limbal conjunctival autograft in pterygium surgery. Ophthalmology. 2013;120:2390-2395.
Lam DS, Wong AK, Fan DS, Chew S, Kwok PS, Tso MS . Intraoperative mitomycin C to prevent recurrence of pterygium after excision: a 30-month follow-up study. Ophthalmology. 1998;105:901-904.
Zheng K, Cai J, Jhanji V, Chen H. Comparison of pterygium recurrence rates after limbal conjunctival autograft transplantation and other techniques: meta-analysis. Cornea. 2012;31:1422-1427.
Li M, Zhu M, Yu Y, et al. Comparison of conjunctival autograft transplantation and amniotic membrane transplantation for pterygium: a meta-analysis. Graefes Arch Clin Exp Ophthalmol. 2012;250:375-381.
Kaufman SC, Jacobs DS, Lee WB, Deng SX, Rosenblatt MI, Shtein RM. Options and adjuvants in surgery for pterygium: a report by the American Academy of Ophthalmology. Ophthalmology. 2013;120(1):201-208. PMID: 23062647. doi:10.1016/j.ophtha.2012.06.066.
Cao D, Ng TK, Yip YWY, Young AL, Pang CP, Chu WK. p53 inhibition by MDM2 in human pterygium. Exp Eye Res. 2018;175:142-147.
Ali AM, Thariat J, Bensadoun RJ, Thyss A, Rostom Y, El-Haddad S, et al. The role of radiotherapy in the treatment of pterygium: a review of the literature including more than 6000 treated lesions. Cancer Radiother. 2011;15:140-147.
Sun Y, Zhang B, Jia X, Ling S, Deng J. Efficacy and safety of bevacizumab in the treatment of pterygium: an updated meta-analysis of randomized controlled trials. J Ophthalmol. 2018;2018:4598173.
Silva RSC, Avila MP, Rassi AR, Ximenes L, Silva DS Jr, Paula AC. Intra-operative use of 5-Fluorouracil in pterygium surgery: a comparative study. Semin Ophthalmol. 2013;28:34-36. PMID: 23305439. doi:10.3109/08820538.2012.730101.