โรคกระจกตาอักเสบจากเส้นประสาทเสื่อม (NK ) เป็นโรคเสื่อมที่เกิดจากความผิดปกติของการรับรู้ความรู้สึกของกระจกตา จากเส้นประสาทไทรเจมินัล ส่งผลให้สมดุลของกระจกตา ถูกรบกวน
เนื่องจากความรู้สึกของกระจกตา ลดลง อาการที่ผู้ป่วยรับรู้จึงมีน้อย มีความเสี่ยงที่โรคจะรุนแรงขึ้นโดยไม่รู้ตัว
สาเหตุที่พบบ่อยที่สุดคือกระจกตา อักเสบจากเชื้อเฮอร์ปีส์ (งูสวัดและเฮอร์ปีส์ซิมเพล็กซ์)
จำแนกตาม Mackie เป็นระดับ I (โรคเยื่อบุกระจกตา ชนิดจุดตื้น), ระดับ II (ข้อบกพร่องของเยื่อบุกระจกตา ที่ยาวนาน), และระดับ III (แผลและการทะลุ)
Senegermin (ปัจจัยการเจริญเติบโตของเส้นประสาทมนุษย์ชนิดรีคอมบิแนนท์) เป็นยาตัวแรกที่ได้รับการอนุมัติให้ใช้ได้การผ่าตัดฟื้นฟูเส้นประสาทกระจกตา เป็นการรักษาทางศัลยกรรมที่มุ่งฟื้นฟูการรับรู้เส้นประสาทพื้นฐาน และกำลังได้รับความสนใจ
ความชุกโดยประมาณน้อยกว่า 50 ต่อ 100,000 คน จัดเป็นโรคหายาก
โรคกระจกตาอักเสบจากเส้นประสาทเสื่อม (neurotrophic keratitis: NK ) เป็นโรคเสื่อมของกระจกตา ที่มีลักษณะเฉพาะคือความรู้สึกของกระจกตา ลดลงหรือหายไป เรียกอีกอย่างว่าโรคกระจกตา เสื่อมจากเส้นประสาท (neurotrophic keratopathy) หรือโรคกระจกตา อัมพาตจากเส้นประสาท (neuroparalytic keratopathy) เกิดจากความเสียหายต่อการรับรู้เส้นประสาทที่แยกจากแขนงแรกของเส้นประสาทไทรเจมินัล (เส้นประสาทสมองคู่ที่ 5) ซึ่งก็คือเส้นประสาทตา
ที่ปลายประสาทกระจกตา มีสารสื่อประสาทหลายชนิด เช่น สาร P, เปปไทด์ที่เกี่ยวข้องกับยีนแคลซิโทนิน (CGRP ), นิวโรเปปไทด์ Y (NPY), เปปไทด์ในลำไส้ที่ออกฤทธิ์ต่อหลอดเลือด (VIP), กาลานิน, เมไทโอนีนเอนเคฟาลิน, คาเทโคลามีน และอะเซทิลโคลีน ปัจจัยที่มาจากเส้นประสาทเหล่านี้ควบคุมการเผาผลาญ การหมุนเวียน และการสมานแผลของเยื่อบุกระจกตา และการลดลงของปัจจัยเหล่านี้เนื่องจากความเสียหายของเส้นประสาทไทรเจมินัล เป็นกลไกสำคัญของการรบกวนสมดุลของกระจกตา
การดำเนินโรคทางคลินิกดำเนินไปอย่างค่อยเป็นค่อยไป การสูญเสียความรู้สึกของกระจกตา บางส่วนหรือทั้งหมดนำไปสู่โรคเยื่อบุกระจกตา (โรคเยื่อบุกระจกตา ชนิดจุดตื้น: SPK ) จากนั้นเป็นข้อบกพร่องของเยื่อบุกระจกตา ที่ยาวนาน (PED ) แผลที่สโตรมาของกระจกตา และอาจดำเนินไปสู่การทะลุของกระจกตา 5) อย่างไรก็ตาม หากได้รับการจัดการอย่างเหมาะสมในระยะแรก ก็สามารถชะลอการดำเนินโรคได้
ความชุกโดยประมาณน้อยกว่า 50 ต่อ 100,000 คน จัดเป็นโรคหายาก 11) รหัส ICD-10 คือ H16.239 โรคนี้ไม่มีสาเหตุเดียว แต่สามารถเกิดจากภาวะใดก็ตามที่ทำลายเส้นทางของเส้นประสาทไทรเจมินัล ทำให้มีลักษณะเป็นกลุ่มอาการ
Q
โรคกระจกตาอักเสบจากเส้นประสาทเสื่อมและโรคกระจกตาอัมพาตจากเส้นประสาทเป็นโรคเดียวกันหรือไม่?
A
โรคกระจกตาอักเสบจากเส้นประสาทเสื่อม (neurotrophic keratitis), โรคกระจกตา เสื่อมจากเส้นประสาท (neurotrophic keratopathy) และโรคกระจกตา อัมพาตจากเส้นประสาท (neuroparalytic keratopathy) ล้วนหมายถึงภาวะเดียวกันที่เกิดจากความเสียหายของเส้นประสาทไทรเจมินัล ชื่อที่แตกต่างกันขึ้นอยู่กับการเน้นว่าความเสียหายของเยื่อบุกระจกตา เป็นแบบอักเสบหรือเสื่อม แต่มีความเท่าเทียมกันทางคลินิก
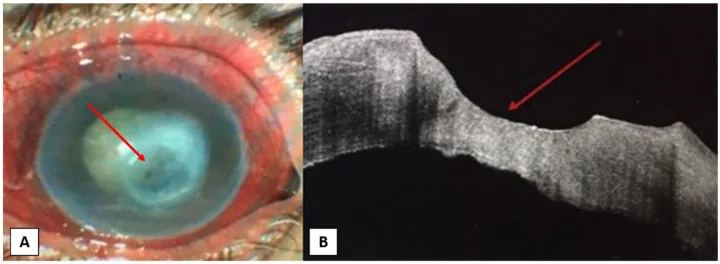
รอยขาดของเยื่อบุกระจกตาที่คงอยู่ (ย้อมฟลูออเรสซีน) ในโรคกระจกตาอักเสบจากเส้นประสาทเสื่อม (หลังงูสวัด) Inferrera A, et al. Real-World Cenegermin (Oxervate) Treatment of Neurotrophic Keratitis: A Multicenter Study. J Clin Med. 2022;11(6):1602. Figure 1. PM
CI D: PMC8955972. License: CC BY 4.0.
ภาพย้อม
ฟลูออเรสซีน ของผู้ป่วยโรค
กระจกตาอักเสบจากเส้นประสาทเสื่อม หลังงูสวัด แสดงรอยขาดของเยื่อบุ
กระจกตา ที่คงอยู่รูปไข่ขนาดใหญ่ขอบนูนก่อนการรักษา (i) แล้วลดขนาดลงหลังจาก 4 สัปดาห์ (ii) และ 8 สัปดาห์ (iii) สอดคล้องกับรอยขาดของเยื่อบุ
กระจกตา ที่คงอยู่ (
PED ) ระดับ II ตาม Mackie ที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
ใน NK เนื่องจากการควบคุมประสาทรับความรู้สึกของกระจกตา ถูกรบกวน ผู้ป่วยจึงไม่ค่อยมีอาการร้องเรียนเกี่ยวกับผิวตา ดังนั้นบางรายอาจมาพบแพทย์หลังจากเริ่มมีอาการหลายเดือนถึงหลายปี
ตามัวและการมองเห็น ลดลง : การทำงานของการมองเห็น ลดลงจากกระจกตา อักเสบแบบจุดตื้น รอยขาดของเยื่อบุ แผลเป็นที่กระจกตา และอาการบวมน้ำไม่มีอาการ : เนื่องจากไม่มีอาการปวดหรือความรู้สึกสิ่งแปลกปลอม ผู้ป่วยจึงไม่รู้ตัวจนกว่าอาการจะรุนแรงเยื่อบุตาอักเสบ และขี้ตาเยื่อบุตา แดงเล็กน้อยหรือมีสารคัดหลั่งในทารกและเด็กเล็ก : การกระพริบตาเฉพาะเมื่อมีการกระตุ้นด้วยภาพที่คุกคาม หรือการบาดเจ็บที่กระจกตา จากการทำร้ายตัวเองอาจเป็นเบาะแสกรณีที่มีความผิดปกติของเส้นประสาทใบหน้า : อาจมีภาวะหนังตาปิดไม่สนิท (ตากระต่าย) ทำให้ภาพทางคลินิกซับซ้อนขึ้น
ภาพทางคลินิกของ NK มีตั้งแต่ความผิดปกติเล็กน้อยของผิวกระจกตา ไปจนถึงการละลายและการทะลุของกระจกตา โดยทั่วไปการแบ่งระยะสามขั้นของ Mackie ถูกใช้อย่างแพร่หลาย 12,13)
ระดับ I (เล็กน้อย)
กระจกตา อักเสบแบบจุดตื้นกระจกตา โดยไม่มีรอยขาดของเยื่อบุ
ความผิดปกติเชิงคุณภาพของเยื่อบุ : ความขุ่นของเยื่อบุกระจกตา และความโปร่งใสลดลง
ความไม่เสถียรของชั้นน้ำตา : อาจร่วมกับการหลั่งน้ำตาลดลงหรือความหนาแน่นของเซลล์กุณโฑลดลง
ระดับ II (ปานกลาง)
ความบกพร่องของเยื่อบุผิวแบบถาวร (PED ) : มีลักษณะเป็นรูปไข่และขอบยกสูง (rolled margins) อาจร่วมกับความขุ่นหรือการสร้างเส้นเลือดใหม่
รอยพับของเยื่อเดสเซเมท : สัญญาณที่เกี่ยวข้องกับอาการบวมน้ำของกระจกตา
การอักเสบของช่องหน้าม่านตา เล็กน้อย : อาจพบการอักเสบเล็กน้อยในช่องหน้าม่านตา (cell/flare)
ระดับ III (รุนแรง)
แผลที่สโตรมาของกระจกตา : ความบกพร่องของสโตรมาร่วมกับการละลายของกระจกตา (melting)
การทะลุของกระจกตา : ภาวะแทรกซ้อนที่รุนแรงที่สุด จำเป็นต้องได้รับการผ่าตัดฉุกเฉิน
แผลเป็นที่กระจกตา : อาจทำให้การมองเห็น บกพร่องถาวรแม้หลังการหาย
การหลั่งน้ำตาลดลงเป็นสัญญาณร่วมที่พบบ่อยเกือบทุกครั้งในโรคกระจกตาอักเสบจากเส้นประสาทเสื่อม และในการประเมินควรใช้การทดสอบ Schirmer และ BUT ร่วมกับการตรวจกระจกตา เสมอ 11)
Q
ทำไมโรคถึงรุนแรงทั้งที่ไม่มีอาการ?
A
ในโรคกระจกตาอักเสบจากเส้นประสาทเสื่อม ความเสียหายของเส้นประสาทไทรเจมินัล ทำให้ความรู้สึกของกระจกตา ลดลงหรือหายไป โดยปกติ ความเสียหายของเยื่อบุผิวกระจกตา จะรับรู้เป็นความเจ็บปวดหรือความรู้สึกสิ่งแปลกปลอม แต่ในโรคนี้สัญญาณเตือนนี้ไม่ทำงาน นอกจากนี้ การหลั่งน้ำตาแบบรีเฟล็กซ์และการกระพริบตาก็ลดลง ทำให้ความบกพร่องของเยื่อบุผิวหรือแผลลุกลามโดยไม่มีอาการ主观 ส่งผลให้มาพบแพทย์ช้าและโรคมีความรุนแรง
โรคตาหรือโรคทางระบบใดๆ ที่ทำลายเส้นทางประสาทรับความรู้สึกจากกระจกตา ไปยังนิวเคลียสเส้นประสาทไทรเจมินัล ที่พอนส์สามารถทำให้เกิดโรคกระจกตาอักเสบจากเส้นประสาทเสื่อม ได้ จากมุมมองทางพยาธิสรีรวิทยา สาเหตุแบ่งออกเป็นส่วนปลาย (เฉพาะที่กระจกตา ถึงเบ้าตา ) ส่วนกลาง (ในกะโหลกศีรษะ) และเมแทบอลิก (เบาหวาน) 13)
โรคเยื่อบุตาอักเสบ จากเชื้อเฮอร์ปีส์ (Herpetic keratitis) : สาเหตุที่พบบ่อยที่สุด ความเสียหายของเส้นประสาทกระจกตา จากเชื้อไวรัสเฮอร์ปีส์ซิมเพล็กซ์ (HS V) และไวรัสวาริเซลลา-ซอสเตอร์ (VZV)โรคฮันเซน (เรื้อน) : ความผิดปกติทางความรู้สึกเนื่องจากการแทรกซึมโดยตรงของเส้นประสาทส่วนปลายการใช้ยาหยอดตาชาเฉพาะที่ในทางที่ผิด : ทำให้ความรู้สึกที่กระจกตา ลดลงโดยตรงและเกิดวงจรอุบาทว์ความเป็นพิษของยาหยอดตา : การใช้ยาหยอดตาที่มีเบนซาลโคเนียมคลอไรด์ (BAK) เป็นเวลานานทำให้ความรู้สึกที่กระจกตา ลดลงผ่านความเสียหายของเส้นประสาทยาหยอดตากลุ่มเบต้าบล็อกเกอร์ : การใช้ที่ไม่เหมาะสมเป็นเวลานานอาจทำให้ความรู้สึกที่กระจกตา ลดลงยาหยอดตากลุ่ม NSAID เฉพาะที่ (เช่น ไดโคลฟีแนค) : มีฤทธิ์ลดความรู้สึกที่กระจกตา ลงอีก จึงจำเป็นต้องจำกัดการใช้การบาดเจ็บจากสารเคมีและแผลไหม้ : ทำให้เกิดความเสียหายอย่างกว้างขวางต่อเส้นประสาทกระจกตา การใช้คอนแทคเลนส์ที่ไม่เหมาะสม : ผลกระทบต่อเส้นประสาทกระจกตา จากการใส่เป็นเวลานานการฉายรังสีที่ดวงตา : ทำลายเส้นประสาทรับความรู้สึกของกระจกตา โดยตรง
การผ่าตัดแก้ไขสายตา : LASIK ตัดข่ายประสาทใต้ฐานอย่างกว้างขวางระหว่างการสร้างแผ่นปิด ทำให้มีอุบัติการณ์ของความผิดปกติของเส้นประสาทชั่วคราวสูงกว่า PRK อย่างมีนัยสำคัญการปลูกถ่ายกระจกตา การปลูกถ่ายกระจกตา ทั้งชั้น (PK) และการปลูกถ่ายกระจกตา ชั้นลึก (DALK ) อาจทำให้ความรู้สึกที่กระจกตา ส่วนกลางลดลงนานถึง 12 เดือนหลังผ่าตัด การปลูกถ่ายเยื่อบุผิวดวงตา (DSAEK /DMEK ) จะรักษาเส้นประสาทในชั้นสโตรมาและเยื่อบุผิว ดังนั้นผลกระทบจึงน้อยกว่าการเชื่อมขวางคอลลาเจน : มีรายงานการลดลงของความรู้สึกที่กระจกตา หลังผ่าตัดในตาที่เป็นโรคกระจกตา โป่งพองการจี้แสงจอประสาทตา การจี้เย็น และการตัดน้ำวุ้นตา : ความเสียหายต่อเส้นประสาทซิลิอารีอาจส่งผลต่อการเลี้ยงเส้นประสาทกระจกตา ผ่านเส้นประสาทซิลิอารียาวการผ่าตัดต้อกระจก : อาจเกิดความรู้สึกลดลงชั่วคราวเนื่องจากแผลที่กระจกตา หรือการชะล้าง
เนื้องอกประสาทหู, ชวานโนมาของเส้นประสาทไทรเจมินัล , เยื่อหุ้มสมองอักเสบ : กดหรือบุกรุกเส้นประสาทไทรเจมินัล โดยตรงหลังการผ่าตัดประสาทศีรษะ : ความผิดปกติของเส้นประสาทไทรเจมินัล ที่เกิดจากแพทย์หลังการผ่าตัดคลายหลอดเลือดกดทับหรือตัดเนื้องอกหลอดเลือดโป่งพองในสมองและโรคหลอดเลือดสมอง : ผลต่อนิวเคลียสหรือทางเดินของเส้นประสาทไทรเจมินัล ในก้านสมองโรคปลอกประสาทเสื่อมแข็ง (MS ) : การทำลายปลอกไมอีลินส่วนกลางโรคความผิดปกติของระบบประสาทอัตโนมัติในครอบครัว (Riley-Day syndrome) และภาวะไม่รู้สึกเจ็บปวดแต่กำเนิดร่วมกับไม่มีเหงื่อ : ความผิดปกติทางประสาทสัมผัสแต่กำเนิดการขาดวิตามินเอ : เกี่ยวข้องกับการรักษาสมดุลของเยื่อบุกระจกตา ยาจิตเวชและยารักษาโรคจิต : ผลทางอ้อมต่อการทำงานของเส้นประสาทส่วนปลาย
ในผู้ป่วยเบาหวาน การเปลี่ยนแปลงทางสัณฐานวิทยาและการทำงานของเส้นประสาทรับความรู้สึกของกระจกตา จะดำเนินไป และความรู้สึกของกระจกตา จะลดลงตามความรุนแรงของจอประสาทตาเสื่อมจากเบาหวาน นี่เป็นแง่มุมหนึ่งของโรคเส้นประสาทส่วนปลายจากเบาหวาน และถือว่าคล้ายคลึงกับแผลที่ผิวหนังที่รักษายากและเนื้อตายเน่าที่เท้าจากเบาหวาน มีรายงานกรณีที่พบโรคกระจกตาอักเสบจากเส้นประสาทเสื่อม เป็นสัญญาณแรกของโรคเบาหวาน 11) .
ผู้ที่มีความรู้สึกที่กระจกตา ลดลงควรสังเกตการเปลี่ยนแปลง เช่น ตาแดง และตามัว เนื่องจากรู้สึกเจ็บปวดได้ยาก อาจไม่สังเกตเห็นความผิดปกติ แนะนำให้ตรวจตาเป็นประจำ ผู้ที่มีประวัติเริม หลังทำ LASIK หรือเป็นเบาหวานต้องระมัดระวังเป็นพิเศษ
Q
เป็นไปได้หรือไม่ที่จะเป็นโรคกระจกตาอักเสบจากเส้นประสาทเสื่อมหลังทำ LASIK?
A
ในการทำ LASIK เส้นประสาทกระจกตา จะถูกตัดในระหว่างการสร้างแผ่นปิด ส่งผลให้ความรู้สึกที่กระจกตา ลดลงชั่วคราวหลังการผ่าตัด ในกรณีส่วนใหญ่จะฟื้นตัวภายในไม่กี่เดือนถึงหนึ่งปี แต่ในบางกรณีอาจคงอยู่และนำไปสู่โรคกระจกตาอักเสบจากเส้นประสาทเสื่อม PRK ไม่สร้างแผ่นปิด ดังนั้นอุบัติการณ์ของโรคเส้นประสาทจึงต่ำกว่า ในกรณีที่มีภาวะตาแห้ง หรือความรู้สึกที่กระจกตา ลดลงก่อนการผ่าตัด จำเป็นต้องประเมินอย่างรอบคอบในขั้นตอนการเลือกเทคนิคการผ่าตัด
เป็นการทดสอบที่สำคัญที่สุดในการวินิจฉัย NK
เครื่องวัดความรู้สึกกระจกตา Cochet-Bonnet : วิธีการประเมินเชิงปริมาณมาตรฐานแบบสัมผัส ใช้เส้นใยไนลอนขนาด 0.12 มม. ยื่นออกมา 60 มม. สัมผัสกระจกตา ของผู้ป่วยในท่านั่ง หากไม่รู้สึก ให้ลดความยาวลงครั้งละ 5 มม. วัดความยาวสั้นที่สุดที่รู้สึกได้สามครั้ง ค่าเฉลี่ยแสดงเป็นความยาวเส้นใย (มม.) ค่าปกติคือ 50–60 มม. ต่ำกว่า 45 มม. บ่งชี้ว่าความรู้สึกกระจกตา ลดลง ต่ำกว่า 40 มม. บ่งชี้ว่าความรู้สึกลดลงอย่างชัดเจน1) ส่วนกลางกระจกตา ไวที่สุด ความรู้สึกลดลงไปทางส่วนปลาย ดังนั้นควรวัดในตำแหน่งเดิมเสมอการทดสอบด้วยสำลี : การประเมินเชิงคุณภาพโดยใช้สำลีสัมผัส ง่ายแต่ความสามารถในการทำซ้ำต่ำ ใช้ในการคัดกรองเครื่องวัดความรู้สึกแบบไม่สัมผัส CRCERT-Belmonte : วิธีการวัดแบบไม่สัมผัสโดยใช้การกระตุ้นด้วยอากาศ สามารถตรวจจับการเปลี่ยนแปลงความรู้สึกที่ละเอียดอ่อนซึ่งประเมินได้ยากด้วย Cochet-Bonnet13)
เนื่องจากยาหยอดตา (โดยเฉพาะยาชาหรือยาที่มีสารกันเสีย) ทำให้ค่าการวัดเปลี่ยนแปลง ควรทำการทดสอบความรู้สึกก่อนหยอดยา
การย้อมฟลูออเรสซีน กระจกตา ใช้ประเมินระยะเวลาการแตกตัวของฟิล์มน้ำตา (BUT ) ด้วยลิสซามีนกรีนและโรสเบงกอล : ประเมินความสมบูรณ์ของกระจกตา และเยื่อบุตา และเซลล์ที่เสื่อมสภาพการทดสอบ Schirmer NK มักพบการหลั่งน้ำตาลดลงเกือบทุกครั้งการตรวจด้วยกล้องจุลทรรศน์ชนิดกรีด (Slit Lamp)ม่านตา แบบพัด (บ่งชี้ประวัติเริม), และแผลเป็นที่กระจกตา
กล้องจุลทรรศน์คอนโฟคอล ในร่างกาย (IVCM)NK พบว่าความหนาแน่นของเส้นประสาทลดลงและความผิดปกติของรูปร่างเส้นประสาทได้รับการพิสูจน์เชิงปริมาณ1,10) มีประโยชน์ในการประเมินประสิทธิภาพการรักษาและการติดตามผลOCT ส่วนหน้า
เมื่อมีความผิดปกติของเยื่อบุกระจกตา อย่างรุนแรงโดยไม่มีอาการไม่สบายตาเนื่องจากกระจกตา ชา (corneal anesthesia) ควรสงสัย NK อย่างมาก จำเป็นต้องแยกโรคจากโรคต่อไปนี้
ตาแห้ง กระจกตา ชาได้บ้าง แต่โดยปกติผู้ป่วยจะรู้สึกมีสิ่งแปลกปลอมหรือปวดตา พิษต่อกระจกตา จากยาหยอดตา : แยกจากประวัติการใช้ยาโรคกระจกตา จากการเปิดเปลือกตาไม่สนิท : เกิดจากตาเหลือก (lagophthalmos) การประเมินตำแหน่งเปลือกตาสำคัญภาวะพร่องสเต็มเซลล์บริเวณลิมบัส ของกระจกตา : สาเหตุของความล้มเหลวในการสร้างเยื่อบุใหม่แตกต่างกันโรคกระจกตา อักเสบจากเชื้อเริมชนิด active : ทำให้กระจกตา ชา แต่ NK เป็นชนิดปราศจากเชื้อแผลที่กระจกตา จากการติดเชื้อช่องหน้าลูกตา
หลังจากยืนยันการวินิจฉัยแล้ว จำเป็นต้องค้นหาสาเหตุ ซักประวัติ (เริม เบาหวาน การผ่าตัดตา การบาดเจ็บ รอยโรคในกะโหลกศีรษะ ยาหยอดตา) และหากจำเป็น ให้ทำ MRI สมองและปรึกษาแพทย์ระบบประสาท/ศัลยกรรมประสาท
การรักษา NK ขึ้นอยู่กับการจัดการตามระยะของโรค ในทุกระยะ ให้ใช้ยาหยอดตาที่ไม่มีสารกันเสีย หากมีโรคผิวตาอื่นๆ (ตาแห้ง เปลือกตาอักเสบ โรคกระจกตา จากการเปิดเปลือกตาไม่สนิท ฯลฯ) ให้รักษาควบคู่กันไป รักษาโรคที่เป็นสาเหตุควบคู่กันไปด้วย
ระยะ เป้าหมายการรักษา การรักษาหลัก ระดับ I ปรับปรุงคุณภาพและความใสของเยื่อบุ ป้องกันการสูญเสียเยื่อบุ น้ำตาเทียม ไร้สารกันเสีย ยาหล่อลื่น อุดจุดน้ำตา ยาหยอดตาซีรั่มตนเอง ระดับ II ส่งเสริมการหายของรอยโรคเยื่อบุผิวที่คงอยู่ คอนแทคเลนส์รักษาโรค, การปลูกถ่ายเยื่อหุ้มน้ำคร่ำ, การเย็บเปลือกตา, เซเนเกอร์มิน ระดับ III การหายของแผลและการป้องกันการทะลุ NAC, เตตราไซคลินชนิดรับประทาน, กาวเนื้อเยื่อ, การปลูกถ่ายกระจกตา
เป้าหมายคือการปกป้องเยื่อบุผิวและทำให้ชั้นน้ำตาคงที่
น้ำตาเทียม และยาทาหล่อลื่นที่ปราศจากสารกันเสีย : การใช้บ่อยครั้ง (เช่น ยาหยอดโซเดียมไฮยาลูโรเนต 0.1% วันละ 5-6 ครั้ง ปรับตามความเหมาะสม) เป็นพื้นฐานยาทาตา : ทายาทาโอฟลอกซาซิน 0.3% วันละ 2-3 ครั้งเพื่อปกป้องเยื่อบุผิวกระจกตา ยาหยอดตาแขวนตะกอนรีบามิไพด์ (2%) : กระตุ้นการหลั่งเมือกเพื่อปกป้องเยื่อบุผิว หยอดวันละ 4 ครั้งการอุดรูน้ำตา : ในกรณีที่การหลั่งน้ำตาลดลงอย่างมาก ให้ใส่ปลั๊กอุดรูน้ำตาเพื่อเพิ่มการกักเก็บน้ำตายาหยอดตาซีรั่มตนเอง กระจกตา ที่คงอยู่ ให้ปัจจัยการเจริญเติบโต (EGF, FGF, TGF-β) เพื่อส่งเสริมการหายของแผล
นอกเหนือจากการรักษาระดับ I แล้ว ให้ใช้ดังต่อไปนี้:
คอนแทคเลนส์ชนิดอ่อนเพื่อการรักษา (TCL) : ปกป้องกระจกตา ในฐานะเลนส์ปิดแผลและส่งเสริมการหายของเยื่อบุผิวการปลูกถ่ายเยื่อหุ้มรก (AMT) : ปกคลุมและปกป้องเยื่อบุผิวกระจกตา ที่เปราะบาง ส่งเสริมการสร้างเยื่อบุผิวใหม่ผ่านฤทธิ์ต้านการอักเสบ ต้านการเกิดแผลเป็น และการให้ส่วนประกอบของเยื่อฐาน การขยายตัวของเยื่อบุผิวสังเกตได้ด้วยการย้อมฟลูออเรสซีน และนำเยื่อหุ้มออกหลังจากยืนยันการปกคลุมอีกครั้งการเย็บขอบตา (ชั่วคราว/ถาวร) : ลดการกระตุ้นเชิงกลและปรับปรุงการกักเก็บน้ำตา ในกรณีรุนแรง การเย็บขอบตาบางส่วนมีประสิทธิภาพการฉีดโบทูลินัมทอกซิน หนังตาตก แบบอัมพาตเพื่อส่งเสริมการปิดตายาหยอดตาต้านแบคทีเรีย : เพื่อป้องกันการติดเชื้อแทรกซ้อนเซเนเกอร์มิน (cenegermin / Oxervate™) : ยาหยอดตาปัจจัยการเจริญเติบโตของเส้นประสาทมนุษย์ชนิดรีคอมบิแนนท์ (rhNGF) ความเข้มข้น 20 ไมโครกรัม/มิลลิลิตร ได้รับการอนุมัติเป็นยาแรกสำหรับ NK ระดับ II และ III โดยสำนักงานยาแห่งยุโรป (EMA, 2017) และสำนักงานคณะกรรมการอาหารและยาสหรัฐอเมริกา (FDA, 2018)2) ขนาดยา คือ 6 ครั้งต่อวัน นาน 8 สัปดาห์2)
ในการทดลองทางคลินิกของเซเนเกอร์มิน ได้มีการศึกษาแบบสุ่มปกปิดสองทางที่มีกลุ่มควบคุมด้วยยาหลอก (REPARO ระยะที่ II, การศึกษาสำคัญของ Pflugfelder 2020) ในผู้ป่วย NK ระดับ II หรือ III8,9)
เมื่อรวมผลจากการทดลองแบบสุ่มที่มีกลุ่มควบคุมสองการศึกษา พบว่า 65-72% ของผู้ป่วยในกลุ่มยาหยอดตา rhNGF บรรลุการหายของกระจกตา อย่างสมบูรณ์หลังจาก 8 สัปดาห์ เทียบกับ 17-33% ในกลุ่มยาหลอก เหตุการณ์ไม่พึงประสงค์ที่พบบ่อยที่สุดคืออาการปวดบริเวณที่หยอดตา เกิดขึ้นประมาณ 16%3)
การทดลอง REPARO ระยะที่ I/II (NGF0212) แสดงให้เห็นการลดระยะเวลาการหายของข้อบกพร่องของเยื่อบุผิวและอัตราการกลับเป็นซ้ำที่ลดลง แต่ไม่แสดงการปรับปรุงที่สำคัญในการรับความรู้สึกของกระจกตา 2) ผู้ป่วยบางรายมีอาการ NK กลับเป็นซ้ำหลังจากหยุดการรักษา จึงจำเป็นต้องติดตามผลอย่างสม่ำเสมอ
ควรหลีกเลี่ยงสเตียรอยด์ ชนิดทาเฉพาะที่เนื่องจากอาจกระตุ้นให้เกิดการละลายของสโตรมา หากใช้เพื่อควบคุมการอักเสบ ต้องให้ด้วยความระมัดระวัง ควรหลีกเลี่ยง NSAIDs ชนิดทาเฉพาะที่เนื่องจากจะลดการรับความรู้สึกของกระจกตา ลงอีก ห้ามใช้ยาชาเฉพาะที่ชนิดหยอดตาอย่างต่อเนื่องโดยเด็ดขาด
นอกเหนือจากการรักษาระดับ I และ II หากมีการดำเนินไปของการละลายของสโตรมา ให้เพิ่มสิ่งต่อไปนี้:
ยาหยอดตา N-acetylcysteine (NAC) : ควบคุมการละลายของสโตรมาโดยการยับยั้งเอนไซม์ย่อยสลายคอลลาเจน (MMP)ยาเตตราไซคลินชนิดรับประทาน : ด็อกซีไซคลิน 100 มก. รับประทานวันละ 1-2 ครั้ง ยับยั้งการละลายของสโตรมาผ่านการยับยั้ง MMPยาหยอดตา medroxyprogesterone : การรักษาเสริมที่คาดว่าจะยับยั้งคอลลาจีเนสการเสริมวิตามินซี : ช่วยในการรักษาการสังเคราะห์คอลลาเจน
เมื่อเกิดการทะลุของกระจกตา การจัดการจะแบ่งตามขนาดเส้นผ่านศูนย์กลางของการทะลุ
การทะลุขนาดเล็ก (<2 มม.) : พยายามปิดด้วยกาวเนื้อเยื่อไซยาโนอะคริเลตและคอนแทคเลนส์ปิดแผล หรือการปลูกถ่ายเยื่อหุ้มน้ำคร่ำการทะลุขนาดใหญ่ : ทำการปลูกถ่ายกระจกตา ทั้งชั้นหรือการปลูกถ่ายกระจกตา ชั้นลึกเพื่อรักษาโครงสร้างแผ่นเยื่อบุตา (Gundersen flap) : พิจารณาเมื่อให้ความสำคัญกับการรักษาลูกตามากกว่าการฟื้นฟูการมองเห็น
ในญี่ปุ่น มีรายงานการรักษาต่อไปนี้ในระดับการวิจัยทางคลินิกเพื่อส่งเสริมการสมานแผลของเยื่อบุผิวกระจกตา ในกรณีที่ไม่ตอบสนองต่อการรักษามาตรฐาน จะพิจารณาปรึกษาไปยังสถานพยาบาลที่สามารถดำเนินการรักษาเหล่านี้ได้
ยาหยอดตาผสมสาร P และอินซูลินไลค์โกรทแฟคเตอร์-1 (IGF-1) : การรวมกันของลำดับขั้นต่ำที่จำเป็น FGLM-NH₂ และ SSSR รายงานว่าส่งเสริมการสมานแผลของเยื่อบุผิวยาหยอดตาไฟโบรเนกติน : ส่งเสริมการยึดเกาะของเซลล์และช่วยในการขยายตัวของเยื่อบุผิวยาหยอดตาเนิร์ฟโกรทแฟคเตอร์ (NGF) : ออกฤทธิ์โดยตรงต่อเซลล์เยื่อบุผิวกระจกตา (ในญี่ปุ่น มีการศึกษาวิจัยในรูปแบบยาที่แตกต่างจากเซเนเกอร์มิน)ยาหยอดตาซีรัมจากสายสะดือ : มีปัจจัยการเจริญเติบโตมากมายเช่นเดียวกับซีรัมตนเอง ใช้ในกรณีที่ยากต่อการเจาะเลือดตนเอง
การเย็บเปลือกตา (tarsorrhaphy) : การรักษาทันทีที่ได้ผลในกรณีที่มีการปิดเปลือกตาไม่สนิทการปลูกถ่ายเยื่อหุ้มน้ำคร่ำ : ปกป้องเยื่อบุผิวและส่งเสริมการสมานแผลการสร้างเส้นประสาทกระจกตาใหม่ (corneal neurotization: CN)กระจกตา โดยการย้ายเส้นประสาทรับความรู้สึกที่แข็งแรงไปยังบริเวณรอบกระจกตา 1,4)
ตามธรรมเนียมแล้ว การสร้างเส้นประสาทกระจกตา ขึ้นใหม่มีข้อบ่งชี้ในกรณีรุนแรงที่ไม่ตอบสนองต่อการรักษาแบบประคับประคอง แต่ด้วยความก้าวหน้าของเทคนิคการผ่าตัดแบบแผลเล็ก ข้อบ่งชี้จึงขยายออกไป 1) ข้อบ่งชี้รวมถึงผู้ป่วยที่มีความรู้สึกที่กระจกตา ลดลงหรือไม่มีเลยระดับปานกลางถึงรุนแรงที่ดื้อต่อการรักษาแบบประคับประคอง และมีเส้นประสาทผู้บริจาคที่แข็งแรงพร้อมใช้ 4) เส้นประสาทผู้บริจาคที่ใช้ ได้แก่ แขนงของเส้นประสาทไทรเจมินัล (เหนือเบ้าตา , เหนือโทรเคลียร์, ใต้เบ้าตา ) และเส้นประสาทหูใหญ่ที่คอ 1)
จำนวนแอกซอนของเส้นประสาทผู้บริจาคมีรายงานดังนี้: เส้นประสาทหูใหญ่เฉลี่ย 6,530, เส้นประสาทเหนือเบ้าตา ประมาณ 3,146 (ส่วนปลาย ที่ขอบเบ้าตา ประมาณ 6,000), เส้นประสาทเหนือโทรเคลียร์ 1,882 (ส่วนปลาย ที่ขอบเบ้าตา 2,534), และเส้นประสาทซูรัล 3,179–3,972 1) เชื่อว่ายิ่งจำนวนแอกซอนมากเท่าใด ผลการสร้างเส้นประสาทใหม่ก็จะยิ่งดีขึ้นเท่านั้น
เทคนิคการผ่าตัดแบ่งออกเป็นวิธีทางตรงและวิธีทางอ้อม 1,7)
วิธีทางตรง : เคลื่อนย้ายเส้นประสาทผู้บริจาคและปลูกถ่ายปลายเส้นประสาทโดยตรงรอบกระจกตา เนื่องจากความต่อเนื่องของเส้นประสาทยังคงอยู่ การฟื้นฟูความรู้สึกจึงเร็วขึ้น แต่มีข้อจำกัดในเรื่องระยะเอื้อมของเส้นประสาทผู้บริจาควิธีทางอ้อม : ใช้ชิ้นเนื้อเยื่อประสาท自体 (เส้นประสาทซูรัล, เส้นประสาทหูใหญ่) หรือชิ้นเนื้อเยื่อประสาท allograft ที่ไม่มีเซลล์ (AxoGen ยาวสูงสุด 70 มม.) เป็นชิ้นเนื้อเยื่อเชื่อมต่อระหว่างเส้นประสาทผู้บริจาคกับกระจกตา เวลาผ่าตัดสั้นกว่า แต่ระยะเวลาฟื้นตัวนานกว่าเนื่องจากแอกซอนต้องผ่านชิ้นเนื้อเยื่อ
วิธีการต่อเส้นประสาทมีทั้งแบบ end-to-end (ตัดเส้นประสาทผู้บริจาคทั้งหมดเพื่อเพิ่มภาระแอกซอนสูงสุด) และแบบ end-to-side (สร้างหน้าต่างที่ปลอกหุ้มเส้นประสาทผู้บริจาคเพื่อรักษาการทำงานที่เหลือ) วิธีหลังสามารถลดการสูญเสียความรู้สึกบริเวณผู้บริจาคได้ 1) ในการทดลองเปรียบเทียบแบบไปข้างหน้าหลายศูนย์ ไม่พบความแตกต่างอย่างมีนัยสำคัญในการปรับปรุงค่า Cochet-Bonnet ระหว่างวิธีทางตรงและทางอ้อมที่ 12 เดือน 7)
เส้นประสาทผู้บริจาคที่มาถึงกระจกตา จะถูกแบ่งออกเป็น 3–4 มัดเส้นประสาท จากนั้นสอดเข้าไปในอุโมงค์ตาขาว -กระจกตา รอบลิมบัส หรือยึดติดกับลิมบัส ด้วยกาวไฟบรินหรือไหมเย็บ 1) หลังผ่าตัด ใช้คอนแทคเลนส์ปิดแผลและการเย็บเปลือกตาชั่วคราวเพื่อป้องกัน ร่วมกับน้ำตาเทียม ไร้สารกันเสียและยาหยอดตาต้านแบคทีเรีย หลังจากหนึ่งเดือน การใช้ยาหยอดตาเซเนเกอร์มินอาจช่วยกระตุ้นการเจริญของเส้นประสาทกระจกตา 1)
Q
ยาเซเนเกอร์มิน (Oxervate) คืออะไร?
A
เซเนเกอร์มินเป็นยาหยอดตาที่ประกอบด้วยปัจจัยการเจริญเติบโตของเส้นประสาทมนุษย์ชนิดรีคอมบิแนนท์ (rhNGF) ความเข้มข้น 20 ไมโครกรัม/มิลลิลิตร และเป็นยารักษาแรกที่ได้รับการอนุมัติสำหรับ NK ในการทดลองทางคลินิก (REPARO ระยะที่ 2, การทดลองสำคัญระยะที่ 2) ที่มุ่งเป้าไปที่ NK ระดับ II และ III มีรายงานว่าผู้ป่วย 65-72% บรรลุการหายของกระจกตา อย่างสมบูรณ์หลังจากหยอดตา 6 ครั้งต่อวันเป็นเวลา 8 สัปดาห์ ในทางกลับกัน ไม่พบการปรับปรุงที่สำคัญในความรู้สึกของกระจกตา และมีกรณีกำเริบหลังจากหยุดการรักษา อาการปวดบริเวณที่หยอดตา (ประมาณ 16%) เป็นผลข้างเคียงหลัก
Q
การผ่าตัดฟื้นฟูเส้นประสาทกระจกตาคืออะไร?
A
การผ่าตัดฟื้นฟูเส้นประสาทกระจกตา เป็นขั้นตอนการย้ายเส้นประสาทรับความรู้สึกที่แข็งแรง (เช่น เส้นประสาทซูพราออร์บิทัล, ซูพราโทรเคลียร์, อินฟราออร์บิทัล, ออริคิวลาริสแมกนัส ฯลฯ) ไปยังบริเวณรอบกระจกตา เพื่อฟื้นฟูความรู้สึกในกระจกตา ที่ขาดสารอาหารทางประสาท มีทั้งวิธีการย้ายเส้นประสาทโดยตรงและการปลูกถ่ายเส้นประสาททางอ้อมผ่านเส้นประสาทซูราล เป็นต้น การฟื้นตัวของความรู้สึกกระจกตา เริ่มต้น 3-6 เดือนหลังการผ่าตัด และยังคงดีขึ้นต่อไปอีก 12-18 เดือนหรือมากกว่า ในการทบทวน 54 ตาโดย Park และคณะ มีรายงานว่าค่า Cochet-Bonnet เฉลี่ยฟื้นตัวจาก 2.18 มม. เป็น 40.1 มม. ผู้ป่วยที่อายุน้อยกว่า (อายุต่ำกว่า 18 ปี) มีแนวโน้มที่จะฟื้นตัวได้ดีกว่า
กระจกตา เป็นเนื้อเยื่อที่มีการเลี้ยงประสาทหนาแน่นที่สุดแห่งหนึ่งในร่างกายมนุษย์ เส้นประสาทซิลิอารียาวที่แยกจากแขนงแรกของเส้นประสาทไตรเจมินัล (เส้นประสาทตา ) ไปถึงกระจกตา เส้นใยประสาทเข้าสู่สโตรมาของกระจกตา ในแนวรัศมีจากลิมบัส ก่อตัวเป็นข่ายประสาทใต้เยื่อบุผิว (sub-epithelial plexus) ใต้เยื่อโบว์แมนโดยตรง จากนั้นเจาะทะลุเยื่อโบว์แมนเพื่อสร้างข่ายประสาทฐาน (sub-basal nerve plexus) และยื่นปลายประสาทอิสระระหว่างเซลล์เยื่อบุผิว เส้นใยประสาทประกอบด้วยเส้นใย Aδ ขนาดเล็กและเส้นใย C ที่ไม่มีปลอกไมอีลิน ซึ่งมีส่วนช่วยให้กระจกตา โปร่งใส
ข่ายประสาทฐานนี้ให้ปัจจัยเลี้ยงประสาทที่จำเป็นต่อการรักษาสมดุลของเยื่อบุผิวกระจกตา 1,8) เส้นใยประสาทประกอบด้วยสาร P ซึ่งช่วยเพิ่มผลของปัจจัยการเจริญเติบโตของผิวหนังชั้นนอก (EGF) และปัจจัยการเจริญเติบโตคล้ายอินซูลิน-1 (IGF-1) ต่อการเคลื่อนที่ของเซลล์เยื่อบุผิวกระจกตา จึงควบคุมการสมานแผลของเยื่อบุผิว เมื่อเส้นประสาทไตรเจมินัลเสียหาย กลไกการควบคุมนี้จะสูญเสียไป และการหลั่งน้ำตาสะท้อนและการกระพริบตาก็ลดลง ทำให้การบาดเจ็บของเยื่อบุผิวกระจกตา ดำเนินไปได้ง่ายและนำไปสู่ภาวะการสมานแผลที่ล่าช้า
เมื่อการส่งปัจจัยเลี้ยงประสาทหยุดชะงัก การเปลี่ยนแปลงทางเนื้อเยื่อวิทยาต่อไปนี้จะเกิดขึ้นทีละน้อย
การบางลงและการทำลายชั้นเยื่อบุผิว : ร่วมกับอาการบวมของไซโทพลาซึมของเซลล์เยื่อบุผิวการสูญเสียไมโครวิลไล : การเปลี่ยนแปลงการทำงานของผิวเยื่อบุผิวการฉีกขาดของเยื่อโบว์แมน : การลดลงของหน้าที่กั้นระหว่างเยื่อบุผิวและสโตรมาการสลายและการเกิดแผลเป็นของสโตรมา : ดำเนินไปโดยการกระตุ้นเอนไซม์ย่อยสลายคอลลาเจน (MMP)การสร้างเส้นเลือดใหม่ในกระจกตา : การเปลี่ยนแปลงที่เกี่ยวข้องกับการอักเสบเรื้อรังความหนาแน่นของเซลล์ก๊อบเล็ตลดลง : การทำงานของเยื่อบุตา ที่หลั่งลดลง
ในแบบจำลองสัตว์ หนูที่ถูกทำลายเส้นประสาทไทรเจมินัล แสดงการหายของข้อบกพร่องของเยื่อบุผิวกระจกตา เทียมที่ล่าช้าอย่างมีนัยสำคัญเมื่อเทียบกับกลุ่มควบคุม ซึ่งยืนยันจากการทดลองว่าการสูญเสียปัจจัยทางประสาทเป็นกลไกหลักของการหายของแผลที่ล่าช้า
NGF เป็นโมเลกุลตัวแทนของครอบครัวนิวโรโทรฟิน และจะทำงานหลังจากถูกตัดจากสารตั้งต้น pro-NGF รูปแบบที่ทำงานคือ β-NGF dimer (น้ำหนักโมเลกุล 26 kDa) ประกอบด้วยสองหน่วยย่อย β ที่จับกันแบบไม่ใช่โควาเลนต์2)
NGF จับกับตัวรับสองชนิดดังต่อไปนี้2) :
TrkA^NGFR^ : ตัวรับสัมพรรคภาพสูง การกระตุ้นจะขับเคลื่อนการส่งสัญญาณปลายน้ำผ่านวิถี MAPK, PI3K และ PLCp75^NTR^ : ตัวรับสัมพรรคภาพต่ำ ทำหน้าที่เสริม
ตัวรับเหล่านี้แสดงออกอย่างสม่ำเสมอบนเซลล์เยื่อบุผิวกระจกตา และเซลล์เยื่อบุผิวฐานของเยื่อบุตา NGF ส่งเสริมการเพิ่มจำนวนและการแยกตัวของเซลล์เยื่อบุผิวกระจกตา ซึ่งมีส่วนช่วยในการหายของแผล2) ในผู้ป่วย NK ปริมาณ NGF ที่ให้ลดลง ซึ่งมีส่วนทำให้สภาวะสมดุลของเยื่อบุผิวเสียหาย ผลทางคลินิกของยาหยอดตา rhNGF ในการทดลอง REPARO ถือเป็นการรักษาที่จำเพาะต่อสาเหตุของโรคโดยอาศัยกลไกระดับโมเลกุลนี้8,9)
การลดลงของความรู้สึกที่กระจกตา ในผู้ป่วยเบาหวานถือเป็นฟีโนไทป์หนึ่งของโรคปลายประสาทอักเสบจากเบาหวาน เป็นที่ทราบกันว่าความรู้สึกที่กระจกตา ลดลงตามความรุนแรงของจอประสาทตาเสื่อมจากเบาหวาน และการเปลี่ยนแปลงรูปร่างของเส้นประสาทกระจกตา ดำเนินไปสัมพันธ์กับการทำงานของไตที่ลดลง นี่คือการแสดงออกบนพื้นผิวตาของโรคปลายประสาทรับความรู้สึกส่วนปลายที่คล้ายกับเท้าเน่าจากเบาหวานและแผลที่ผิวหนังที่รักษายาก และเป็นหนึ่งในพื้นฐานทางพยาธิวิทยาที่สำคัญของโรคกระจกตา จากสาเหตุทางประสาท13)
ในการผ่าตัดฟื้นฟูเส้นประสาทกระจกตา หลังจากย้ายเส้นประสาทรับความรู้สึกที่แข็งแรงไปยังบริเวณรอบกระจกตา การงอกใหม่ของแอกซอนจะดำเนินไปตามกระบวนการ Wallerian degeneration 1)
ปฏิกิริยาการบาดเจ็บระยะแรก : แอกซอนที่ปลายเส้นประสาทผู้ให้เกิดการเสื่อมสลาย และมาโครฟาจจะกินและกำจัดไมอีลินที่เสื่อมสลายการเหนี่ยวนำเซลล์ชวานน์ : เซลล์ชวานน์จะแยกตัวและย้ายจากปลายใกล้เคียงที่ยังมีชีวิตของเส้นประสาทผู้ให้ เพื่อเป็นโครงสร้างสำหรับการงอกใหม่ของแอกซอนการแตกหน่อของแอกซอน : NGF และอินเตอร์ลิวคิน-1 (IL-1) ส่งเสริมการแตกหน่อของแอกซอน 1) การงอกใหม่แบบเลือกสรร : กระจกตา จะรับเฉพาะเส้นประสาทที่ไม่มีปลอกไมอีลินที่มีฟีโนไทป์เฉพาะเท่านั้น ดังนั้นมีเพียงบางส่วนของแอกซอนที่งอกใหม่เท่านั้นที่ไปถึงสโตรมาของกระจกตา และข่ายประสาทใต้ฐาน 1)
ที่น่าสนใจคือ การทดลองในสัตว์แสดงให้เห็นว่าเส้นประสาทกระจกตา ที่งอกใหม่ไม่จำเป็นต้องต่อเนื่องกับเส้นประสาทผู้ให้ ซึ่งบ่งชี้ว่าเส้นประสาทผู้ให้อาจทำหน้าที่ไม่เพียงแต่เป็นแหล่งของแอกซอน แต่ยังเป็นแหล่งของปัจจัยนิวโรโทรฟิกด้วย 1)
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
การผ่าตัดฟื้นฟูเส้นประสาทกระจกตา ได้พัฒนาจากขั้นตอนใหญ่ที่ต้องใช้แผลผ่าตัดแบบโคโรนัลไปเป็น แนวทางที่มีการบุกรุกน้อยที่สุด และเทคนิคการส่องกล้อง 1,14) ด้วยการนำกราฟต์เส้นประสาทจากผู้บริจาคที่ไม่มีเซลล์มาใช้ ทำให้สามารถหลีกเลี่ยงภาวะแทรกซ้อนที่เกี่ยวข้องกับการเก็บเส้นประสาทตนเองได้ และข้อบ่งชี้กำลังขยายออกไปด้วยการใช้เส้นประสาทผู้ให้ทางเลือก (เช่น เส้นประสาทหูใหญ่) 1)
ในด้านผลลัพธ์ การทบทวนของ Park ใน 54 ตารายงานว่าค่า Cochet-Bonnet ฟื้นตัวจากค่าเฉลี่ยก่อนผ่าตัด 2.18 มม. เป็น 40.1 มม. หลังผ่าตัด 1,6) ผู้ป่วยอายุน้อยที่อายุต่ำกว่า 18 ปีมีแนวโน้มที่จะฟื้นความรู้สึกได้เร็วและสมบูรณ์กว่า รวมถึงการมองเห็น ดีขึ้น ซึ่งเชื่อว่าเกิดจากความหนาแน่นของเส้นใยประสาทใต้ฐานกระจกตา ที่สูงกว่าในวัยหนุ่มสาว 1,6) การมองเห็น เส้นประสาทกระจกตา ด้วยกล้องจุลทรรศน์คอนโฟคอล ในร่างกายเริ่มต้น 3 เดือนหลังผ่าตัด และการปรับปรุงจะดำเนินต่อไปนาน 12-18 เดือน 1,14) หลังจากพื้นผิวตาคงที่ด้วยการผ่าตัดฟื้นฟูเส้นประสาทกระจกตา การฟื้นฟูการมองเห็น แบบเป็นขั้นตอนด้วยการปลูกถ่ายกระจกตา ทั้งชั้น (PK) หรือการปลูกถ่ายกระจกตา ชั้นหน้าส่วนลึก (DALK ) จะดำเนินการด้วยผลลัพธ์ที่ดี 1)
หลังจาก senegermin ได้รับการอนุมัติจาก FDA/EMA การสะสมข้อมูลทางคลินิกจริงยังคงดำเนินต่อไป เมื่อเร็ว ๆ นี้ มีรายงานการปรับปรุงอาการ การย้อมสีพื้นผิวตา และการหลั่งน้ำตาในการทดลองระยะที่ 2 สำหรับโรคตาแห้ง 2) การประยุกต์ใช้กับโรคพื้นผิวตาอื่น ๆ ก็อยู่ระหว่างการพิจารณาเช่นกัน
ยาหยอดตาที่มีไทโมซิน เบต้า-4 0.1% (RGN-259) ในการทดลองทางคลินิกระยะที่ 3 แบบสุ่ม ปกปิดสองด้าน ควบคุมด้วยยาหลอก ในผู้ป่วย NK แสดงให้เห็นว่าส่งเสริมการหายของกระจกตา และปรับปรุงอาการตามความรู้สึกของผู้ป่วย 3)
ไทโมซิน เบต้า-4 เป็นโปรตีนที่จับกับแอคติน ซึ่งเชื่อว่าส่งเสริมการซ่อมแซมเยื่อบุผิวผ่านการส่งเสริมการเคลื่อนที่ของเซลล์ ฤทธิ์ต้านการอักเสบ และต้านการตายของเซลล์ 15)
อินซูลินเฉพาะที่ได้รับการรายงานให้ใช้สำหรับโรคกระจกตา ตั้งแต่ปี ค.ศ. 1945 โดยส่งเสริมการสร้างเยื่อบุผิวกระจกตา ใหม่ ตัวรับอินซูลินและตัวรับ IGF-1 ได้รับการยืนยันว่ามีการแสดงออกบนพื้นผิวตาของมนุษย์ ยังไม่มีฉันทามติเกี่ยวกับขนาดยา แต่โดยทั่วไปจะหยอดวันละ 4 ครั้ง เนื่องจากมีราคาถูกและหาง่าย จึงคาดว่าจะมีประโยชน์ในพื้นที่กว้าง รวมถึงประเทศกำลังพัฒนา
RGTA (สารสร้างใหม่) ที่ให้เฉพาะที่เป็นสารเลียนแบบโปรตีโอไกลแคนเฮปารานซัลเฟต และได้รับการรายงานว่าส่งเสริมการหายของกระจกตา ในการศึกษาเชิงสังเกต ปัจจุบันมีเฉพาะในยุโรปเท่านั้น
ในประเทศ การวิจัยเกี่ยวกับยาหยอดตาผสมนิวโรเปปไทด์ที่ออกฤทธิ์โดยตรงต่อเซลล์เยื่อบุผิวกระจกตา ยังคงดำเนินต่อไป สารผสมของลำดับขั้นต่ำที่จำเป็น FGLM-NH₂ (จาก Substance P) และ SSSR (จาก IGF-1) ได้รับการแสดงว่าส่งเสริมการหายของแผลเยื่อบุผิว และคาดว่าจะนำไปใช้ในกรณีที่ดื้อต่อการรักษา
Hubschman S, Rosenblatt MI, Cortina MS . Corneal neurotization for the treatment of neurotrophic keratopathy. Curr Opin Ophthalmol. 2025;36(4):294-300.
Kanu LN, Ciolino JB. Nerve growth factor as an ocular therapy: applications, challenges, and future directions. Semin Ophthalmol. 2021;36(4):224-231.
TFOS DEWS III Management and Therapy Subcommittee. TFOS DEWS III Management and Therapy Report. Am J Ophthalmol. 2025;279:355-440.
Dragnea DC, Krolo I, Koppen C, et al. Corneal neurotization-indications, surgical techniques and outcomes. J Clin Med. 2023;12:2214.
Neurotrophic Keratopathy Study Group. Neurotrophic keratopathy: an updated understanding. Ocul Surf. 2023;30:129-138.
Park JK, Charlson ES, Leyngold I, Kossler AL. Corneal neurotization: a review of pathophysiology and outcomes. Ophthalmic Plast Reconstr Surg. 2020;36:431-437.
Fogagnolo P, Giannaccare G, Bolognesi F, et al. Direct versus indirect corneal neurotization for the treatment of neurotrophic keratopathy: a multicenter prospective comparative study. Am J Ophthalmol. 2020;220:203-214.
Bonini S, Lambiase A, Rama P, et al. Phase II randomized, double-masked, vehicle-controlled trial of recombinant human nerve growth factor for neurotrophic keratitis. Ophthalmology. 2018;125(9):1332-1343.
Pflugfelder SC, Massaro-Giordano M, Perez VL, et al. Topical recombinant human nerve growth factor (Cenegermin) for neurotrophic keratopathy: a multicenter randomized vehicle-controlled pivotal trial. Ophthalmology. 2020;127(1):14-26.
Mastropasqua L, Nubile M, Lanzini M, et al. Corneal subbasal nerve plexus changes in patients with neurotrophic keratitis: an in vivo confocal microscopy study. Clin Ther. 2020;42(2):291-302.
Sacchetti M, Lambiase A. Diagnosis and management of neurotrophic keratitis. Clin Ophthalmol. 2014;8:571-579.
Ruiz-Lozano RE, Hernandez-Camarena JC, Loya-Garcia D, Merayo-Lloves J, Rodriguez-Garcia A. The molecular basis of neurotrophic keratopathy: diagnostic and therapeutic implications. A review. Ocul Surf. 2021;19:224-240.
Dua HS , Said DG, Messmer EM, et al. Neurotrophic keratopathy: an updated understanding. Prog Retin Eye Res. 2018;66:107-131.
Catapano J, Fung SSM, Halliday W, et al. Treatment of neurotrophic keratopathy with minimally invasive corneal neurotisation: long-term clinical outcomes and evidence of corneal reinnervation. Br J Ophthalmol. 2019;103:1724-1731.
Sosne G, Kleinman HK. Primary mechanisms of thymosin β4 repair activity in dry eye disorders and other tissue injuries. Invest Ophthalmol Vis Sci. 2015;56(9):5110-5117.