I度(輕度)

神經營養性角膜炎(神經營養性角膜病變)
一目了然的要點
Section titled “一目了然的要點”1. 什麼是神經營養性角膜炎?
Section titled “1. 什麼是神經營養性角膜炎?”神經營養性角膜炎(NK)是一種以角膜感覺減退或消失為特徵的角膜變性疾病。也稱為神經營養性角膜病變或神經麻痺性角膜病變。由三叉神經(第V對腦神經)第一支眼神經分出的感覺神經支配受損引起。
角膜神經末梢含有多種神經傳導物質,如P物質、降鈣素基因相關胜肽(CGRP)、神經胜肽Y(NPY)、血管活性腸胜肽(VIP)、甘丙肽、甲硫胺酸腦啡肽、兒茶酚胺和乙醯膽鹼。這些神經源性因子調節角膜上皮的代謝、更新和傷口癒合。三叉神經損傷導致這些因子供應減少是角膜恆定性破壞的本質機制。
臨床病程呈階段性進展。角膜感覺部分或完全喪失始於上皮性角膜病變(點狀表層角膜病變,SPK),可進展為持續性上皮缺損(PED)、角膜基質潰瘍,甚至角膜穿孔5)。然而,如果在早期進行適當管理,可以阻止進展。
估計盛行率低於每10萬人50例,屬於罕見疾病11)。ICD-10編碼為H16.239。本病並非單一病因,而是任何損傷三叉神經通路的疾病均可引起的症候群。
神經營養性角膜炎、神經營養性角膜病變和神經麻痺性角膜病變均指由三叉神經損傷引起的同一疾病。這些術語在強調角膜上皮損傷是發炎性還是變性性方面有所不同,但臨床上視為等同。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”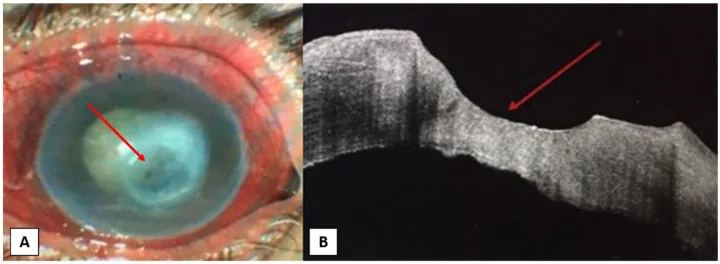
在NK中,由於角膜感覺神經支配受損,患者很少主訴眼表症狀。因此,有些病例在發病後數月至數年才首次就診。
- 霧視和視力下降:由於點狀角膜病變、上皮缺損、角膜疤痕和水腫導致的視功能下降
- 無自覺性:缺乏疼痛或異物感,因此直到病情嚴重才被察覺
- 結膜充血和分泌物:可能出現輕度充血或分泌物
- 嬰幼兒病例:僅在威脅性瞬目時眨眼,或自傷導致的角膜損傷可能成為線索
- 合併顏面神經麻痺的病例:可能伴有眼瞼閉合不全(兔眼),使病情複雜化
臨床所見與分期
Section titled “臨床所見與分期”NK的臨床表現從輕微的角膜表面不規則到角膜融解和穿孔不等。經典上,Mackie的三級分類被廣泛使用12,13)。
II度(中度)
III度(重度)
淚液分泌減少在NK中通常是幾乎必發的伴隨表現,評估時必須同時進行Schirmer試驗和淚膜破裂時間(BUT)檢查,而不僅僅是角膜表現11)。
在NK中,三叉神經損傷導致角膜感覺減退或消失。通常角膜上皮損傷會表現為疼痛或異物感,但在NK中這種警告信號不起作用。此外,反射性淚液分泌和眨眼也減少,因此上皮缺損和潰瘍在無症狀的情況下進展,導致就診延遲和病情加重。
3. 病因與危險因子
Section titled “3. 病因與危險因子”任何損害從角膜到橋腦三叉神經核的感覺神經通路的眼部或全身疾病都可能導致NK。從病理生理角度,可分為周邊性(角膜局部至眼眶)、中樞性(顱內)和代謝性(糖尿病)13)。
眼部病因(周邊性)
Section titled “眼部病因(周邊性)”- 疱疹性角膜炎:最常見的原因。單純疱疹病毒(HSV)及水痘-帶狀疱疹病毒(VZV)引起的角膜神經損傷。
- 痲瘋病:直接浸潤周邊神經導致知覺障礙。
- 濫用眼用麻醉藥:直接損害角膜知覺,形成惡性循環。
- 眼藥水的毒性:長期使用含苯扎氯銨(BAK)的藥物,經由神經損傷降低角膜知覺。
- β阻斷劑眼藥水:不當長期使用可能導致角膜知覺下降。
- 局部NSAID眼藥水(如雙氯芬酸):進一步降低角膜知覺,需限制使用。
- 化學傷或燒傷:廣泛損傷角膜神經。
- 隱形眼鏡使用不當:長期配戴影響角膜神經。
- 眼部放射照射:直接損傷角膜感覺神經。
與眼科手術相關的原因
Section titled “與眼科手術相關的原因”- 屈光手術:LASIK在製作角膜瓣時廣泛切斷基底下神經叢,因此比PRK更易引起暫時性神經損傷。
- 角膜移植術:穿透性角膜移植術(PK)和深層板層角膜移植術(DALK)術後12個月內可能導致中央角膜知覺下降。角膜內皮移植術(DSAEK/DMEK)保留基質-上皮神經,影響較小。
- 膠原交聯:圓錐角膜眼術後有角膜知覺下降的報告。
- 視網膜光凝、冷凍凝固和玻璃體手術:可能損傷睫狀神經,影響經長睫狀神經的角膜神經支配。
- 白內障手術:角膜切口和灌注可能導致一過性知覺下降。
全身性原因(中樞性)
Section titled “全身性原因(中樞性)”- 聽神經瘤、三叉神經鞘瘤、腦膜瘤:直接壓迫或浸潤三叉神經
- 神經外科手術後:三叉神經微血管減壓術、腫瘤切除術等醫源性三叉神經功能障礙
- 腦動脈瘤、腦中風:影響腦幹的三叉神經核或路徑
- 多發性硬化症(MS):中樞性脫髓鞘
- 家族性自主神經失調(Riley-Day症候群)、先天性無痛無汗症:先天性感覺神經異常
- 維生素A缺乏症:參與角膜上皮恆定維持
- 精神藥物、抗精神病藥:對周邊神經功能的間接影響
糖尿病患者中,角膜感覺神經的形態和功能變化逐漸進展,角膜感覺下降與糖尿病視網膜病變的嚴重程度相關。這是糖尿病周邊神經病變的一個面向,被認為與難治性皮膚潰瘍或糖尿病足壞疽類似。也有報告指出NK作為糖尿病的初發症狀被發現11)。
LASIK術中製作角膜瓣時會切斷角膜神經,導致術後暫時性角膜感覺下降。多數情況下在數月至一年內恢復,但少數會持續並發展為神經營養性角膜炎。PRK不製作角膜瓣,神經損傷發生率較低。術前已有乾眼或角膜感覺下降的病例,在選擇手術方式時需要仔細評估。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”角膜知覺檢查
Section titled “角膜知覺檢查”這是診斷NK最重要的檢查。
- Cochet-Bonnet角膜知覺計:標準的接觸式定量評估方法。將0.12 mm的尼龍線伸出60 mm,接觸坐位患者的角膜。如果患者感覺不到,則每次縮短5 mm。測量三次患者感覺到接觸的最短長度,取平均值,以尼龍線長度(mm)表示。正常值為50–60 mm,45 mm以下表示角膜知覺減退,40 mm以下表示明顯知覺減退1)。角膜中央最敏感,向周邊知覺減退,因此測量應始終在同一部位進行。
- 棉棒測試:用棉絮接觸進行定性評估。簡便但再現性差,用於篩查。
- CRCERT-Belmonte非接觸式知覺計:使用空氣刺激的非接觸測量方法。可檢測Cochet-Bonnet難以評估的細微知覺變化13)。
眼藥水(尤其是麻醉藥或含防腐劑的藥物)會改變測量值,因此知覺檢查應在點眼前進行。
角膜染色與淚液檢查
Section titled “角膜染色與淚液檢查”- 螢光素染色:使角膜上皮缺損可視化。也用於評估淚膜破裂時間(BUT)。
- 麗絲胺綠/玫瑰紅:評估角膜和結膜的完整性及變性細胞。
- Schirmer試驗:評估淚液分泌量。NK幾乎必然伴有淚液分泌減少。
- 裂隙燈顯微鏡檢查:檢查上皮缺損邊緣的捲邊、混濁、新生血管、扇形虹膜萎縮(提示既往皰疹)和角膜疤痕。
- 活體共聚焦顯微鏡(IVCM):直接可視化角膜基底下神經叢的結構。在NK中,可定量證明神經密度減少和神經形態異常1,10)。對評估療效和追蹤有用。
- 眼前段OCT:測量上皮缺損的厚度和基質融解的程度。
當角膜知覺麻痺導致眼部無不適症狀,但存在嚴重的角膜上皮損傷時,應高度懷疑NK。需要與以下疾病進行鑑別。
- 乾眼症:可能伴有某種程度的角膜知覺減退,但通常有異物感或眼痛。
- 眼藥水毒性角膜病變:透過用藥史鑑別。
- 暴露性角膜病變:由兔眼(眼瞼閉合不全)引起。眼瞼位置評估很重要。
- 角膜緣幹細胞缺乏症:上皮再生不全的原因不同。
- 活動性疱疹性角膜炎:可降低角膜知覺,但NK是無菌性的,這點不同。
- 感染性角膜潰瘍:透過潰瘍邊緣的浸潤表現和前房炎症鑑別。
確診後,必須查明原因。透過問診了解病史(疱疹、糖尿病、眼科手術、外傷、顱內病變、眼藥水),必要時進行頭部MRI或諮詢神經內科/神經外科。
5. 標準治療方法
Section titled “5. 標準治療方法”NK的治療基於分期管理。在所有分期中,使用不含防腐劑的眼藥水。如果合併其他眼表疾病(乾眼症、眼瞼炎、暴露性角膜病變等),應同時治療。同時治療原發病。
分期治療策略
Section titled “分期治療策略”| 分期 | 治療目標 | 主要治療方法 |
|---|---|---|
| I級 | 改善上皮品質和透明度,預防上皮缺損 | 不含防腐劑的人工淚液、潤滑眼膏、淚點栓塞、自體血清眼藥水 |
| II度 | 促進持續性上皮缺損癒合 | 治療性SCL、羊膜移植、瞼板縫合、塞奈吉明 |
| III度 | 潰瘍癒合與穿孔預防 | NAC、口服四環黴素、組織黏合劑、角膜移植 |
I度(SPK)的治療
Section titled “I度(SPK)的治療”旨在保護上皮和穩定淚膜。
- 無防腐劑人工淚液和潤滑軟膏:頻繁點眼(例如,0.1%玻尿酸鈉點眼液每日5-6次,視情況增減)是基本治療。
- 眼藥膏:每日塗抹0.3%氧氟沙星眼藥膏2-3次,保護角膜上皮。
- 瑞巴派特懸浮點眼液(2%):每日點眼4次,通過促進黏蛋白分泌發揮上皮保護作用。
- 淚點栓塞:當淚液分泌顯著減少時,插入淚點栓以促進淚液滯留。
- 自體血清點眼:對於持續性角膜上皮病變可考慮使用。通過提供生長因子(EGF、FGF、TGF-β)促進傷口癒合。
II度(持續性上皮缺損)的治療
Section titled “II度(持續性上皮缺損)的治療”在I度治療的基礎上,使用以下方法。
- 治療用軟性隱形眼鏡(TCL):作為繃帶鏡保護角膜,促進上皮癒合
- 羊膜移植(AMT):覆蓋並保護脆弱的角膜上皮,透過抗發炎、抗疤痕作用及提供基底膜成分促進上皮再生。以螢光素染色觀察角膜上皮延伸,確認再覆蓋後移除
- 眼瞼縫合(暫時/永久):減少機械刺激,改善淚液保留。重症病例中部分眼瞼縫合有效
- 肉毒桿菌毒素注射:作為眼瞼縫合的替代方法,誘導提眼瞼肌麻痺性眼瞼下垂以促進眼瞼閉合
- 抗菌眼藥水:預防繼發感染
- 塞奈吉明(cenegermin / Oxervate™):基因重組人類神經生長因子(rhNGF)20 μg/mL眼藥水。作為II度及III度NK的首個核准藥物,已獲歐洲藥品管理局(EMA,2017年)及美國食品藥物管理局(FDA,2018年)核准2)。用法:每日6次,持續8週2)
塞奈吉明的臨床試驗中,針對II度或III度NK患者進行了隨機、載體對照、雙盲研究(REPARO II期,Pflugfelder 2020關鍵試驗)8,9)。
合併兩項隨機對照試驗,rhNGF眼藥水組65-72%的患者在8週後達到完全角膜癒合,而載體對照組為17-33%。最常見的不良事件是點藥部位疼痛,發生率約16%3)。
REPARO I/II期試驗(NGF0212)顯示上皮缺損癒合時間縮短及復發率降低,但未顯示角膜感覺本身有顯著改善2)。部分患者停藥後NK復發,需要定期追蹤。
局部類固醇可能誘發基質溶解,用於控制發炎時應謹慎使用。避免使用局部NSAID,因為它們會進一步降低角膜感覺。嚴禁持續使用局部麻醉劑。
III度(潰瘍/穿孔)的治療
Section titled “III度(潰瘍/穿孔)的治療”在I度及II度治療的基礎上,若基質溶解進展,則添加以下治療:
- N-乙醯半胱氨酸(NAC)眼藥水:透過抑制膠原酶(MMP)活性控制基質溶解
- 口服四環黴素:多西環素100 mg每日1-2次口服,透過抑制MMP來抑制溶解
- 甲羥孕酮眼藥水:預期抑制膠原酶的輔助治療
- 維生素C補充:維持膠原蛋白合成的輔助治療
發生角膜穿孔時,根據穿孔大小採取不同的處理方式。
- 小穿孔(<2 mm):嘗試使用氰基丙烯酸酯組織黏合劑和繃帶型角膜接觸鏡,或羊膜移植進行封閉
- 大穿孔:進行穿透性角膜移植術或深層板層角膜移植術以維持結構
- 結膜瓣成形術(Gundersen flap):在優先考慮保留眼球而非恢復視功能時考慮
日本報告的先進治療
Section titled “日本報告的先進治療”在日本,以下促進角膜上皮傷口癒合的治療方法已在臨床研究層級報告。對於標準治療無效的病例,可考慮轉診至能夠實施這些治療的機構。
- P物質+胰島素樣生長因子-1(IGF-1)複合點眼液:必需最小序列FGLM-NH₂和SSSR的複合物已被報告可促進上皮傷口癒合
- 纖維連接蛋白點眼液:促進細胞黏附並輔助上皮伸展
- 神經生長因子(NGF)點眼液:直接作用於角膜上皮細胞(在日本,曾以與塞奈吉明不同的劑型進行研究)
- 臍帶血清點眼液:與自體血清一樣富含生長因子,用於自體採血困難的病例
- 瞼緣縫合術:對合併眼瞼閉合不全的病例有效的即時治療
- 羊膜移植:保護上皮並促進傷口癒合
- 角膜神經移植術(corneal neurotization: CN):將健康的感覺神經轉移到角膜周邊,恢復角膜神經支配本身的根治性外科治療1,4)
角膜神經再生術傳統上適用於保守治療無效的重症病例,但近年來隨著微創技術的進步,適應症正在擴大1)。適應對象包括保守治療無效的中重度角膜感覺減退或感覺缺失,且能獲得健康捐贈神經的患者4)。捐贈神經包括三叉神經分支(眶上神經、滑車上神經、眶下神經)以及頸部的大耳神經(GAN)1)。
捐贈神經的軸突數量報告如下:GAN平均6,530條;眶上神經約3,146條(遠端,眶緣處約6,000條);滑車上神經1,882條(遠端,眶緣處2,534條);腓腸神經3,179~3,972條1)。一般認為軸突數量越多,神經再生效果越好。
手術方式大致分為直接法和間接法1,7)。
- 直接法:將捐贈神經游離後,將其末端直接移植到角膜周邊。由於連續性得以保持,感覺恢復較快,但捐贈神經的到達範圍有限。
- 間接法:使用自體神經(如腓腸神經、大耳神經)或無細胞同種異體神經移植物(Axogen公司,最長70 mm)作為橋接移植物,連接捐贈神經和角膜。手術時間較短,但軸突需要通過移植物,因此恢復時間較長。
吻合方法包括端端吻合(完全切斷捐贈神經以最大化軸突負荷)和端側吻合(在捐贈神經鞘上開窗以保留殘餘功能);後者可減輕捐贈區域的感覺減退1)。一項前瞻性多中心比較試驗顯示,在12個月時,直接法和間接法的Cochet-Bonnet改善無顯著差異7)。
到達角膜的捐贈神經被分成3~4個神經束,插入角膜緣周圍的鞏膜-角膜隧道,或用纖維蛋白膠或縫線固定在角膜緣1)。術後使用繃帶型隱形眼鏡和臨時瞼板縫合保護,並使用無防腐劑人工淚液和抗菌眼藥水。術後1個月起聯合使用塞奈吉明眼藥水,有望促進角膜神經生長1)。
塞內吉明是一種含有20 μg/mL重組人類神經生長因子(rhNGF)的點眼藥,是首個獲批用於NK的治療藥物。針對II度及III度NK的臨床試驗(REPARO II期、關鍵II期)報告,每日點眼6次、持續8週,65-72%的患者實現了完全角膜癒合。另一方面,尚未顯示能顯著改善角膜感覺本身,停藥後也有復發案例。主要副作用是點眼部位疼痛(約16%)。
角膜神經再生術是將健康的感覺神經(如眶上神經、滑車上神經、眶下神經、耳大神經等)轉移到角膜周邊部,以恢復神經營養性角膜感覺的手術。有直接神經轉移法和通過腓腸神經等的間接神經移植法。術後3-6個月開始恢復角膜感覺,並在12-18個月以上持續改善。Park等人對54隻眼的綜述報告,Cochet-Bonnet值平均從2.18 mm恢復到40.1 mm。18歲以下的年輕患者往往恢復更好。
6. 病理生理學·詳細發病機轉
Section titled “6. 病理生理學·詳細發病機轉”角膜的神經支配
Section titled “角膜的神經支配”角膜是人體中神經支配最密集的組織之一。從三叉神經第一支(眼神經)分出的長睫狀神經到達角膜。神經纖維從角膜緣呈放射狀進入角膜基質,在Bowman層正下方形成上皮下神經叢。進一步穿過Bowman層形成基底細胞下神經叢,並在上皮細胞間伸展游離神經末梢。神經纖維由細小的Aδ纖維和C纖維組成的無髓神經,有助於角膜的透明性。
這個基底細胞下神經叢提供維持角膜上皮恆定所必需的神經營養因子1,8)。神經纖維內含有P物質,通過增強表皮生長因子(EGF)和胰島素樣生長因子-1(IGF-1)對角膜上皮細胞遷移的作用,調節上皮傷口癒合。當三叉神經受損時,這種調節機制喪失,反射性淚液分泌和眨眼也減弱,導致角膜上皮損傷容易進展且癒合延遲。
角膜上皮的變性過程
Section titled “角膜上皮的變性過程”當神經營養因子的供應中斷時,會逐步發生以下組織學變化。
- 上皮層變薄與破壞:伴隨上皮細胞胞質腫脹
- 微絨毛消失:上皮表面的功能改變
- 鮑曼氏膜斷裂:上皮-基質間屏障功能下降
- 基質溶解與瘢痕化:由膠原酶(MMP)活化而進展
- 角膜新生血管:伴隨慢性發炎的變化
- 杯細胞密度減少:結膜分泌功能下降
動物模型顯示,破壞三叉神經的大鼠人工角膜上皮缺損的癒合與對照組相比顯著延遲,實驗證實神經因子的喪失是傷口癒合延遲的核心機制。
神經生長因子(NGF)的分子機制
Section titled “神經生長因子(NGF)的分子機制”NGF是神經營養因子家族的典型分子,經由從前驅物pro-NGF切割而成為活性形式。活性形式是β-NGF二聚體(分子量26 kDa),由兩個非共價結合的β亞基組成2)。
NGF與以下兩種受體結合2):
- TrkA^NGFR^:高親和力受體。活化後經由MAPK、PI3K和PLC路徑驅動下游信號傳導
- p75^NTR^:低親和力受體。扮演輔助角色
這些受體在角膜上皮細胞和結膜基底上皮細胞上組成性表現。NGF促進角膜上皮細胞的增生與分化,有助於傷口癒合2)。NK患者中NGF供應減少,導致上皮恆定破壞。REPARO試驗中rhNGF眼藥水的臨床效果被定位為基於該分子機制的病因特異性治療8,9)。
與糖尿病性角膜病變的關聯
Section titled “與糖尿病性角膜病變的關聯”糖尿病患者的角膜感覺減退被認為是糖尿病周邊神經病變的一種表現。已知角膜感覺隨糖尿病視網膜病變的嚴重度而降低,且角膜神經的形態變化與腎功能下降相關。這是類似於糖尿病足壞疽和難治性皮膚潰瘍的周邊感覺神經病變在眼表面的表現,是神經營養性角膜病變的重要病理基礎之一13)。
角膜神經再生術的神經再生機轉
Section titled “角膜神經再生術的神經再生機轉”在角膜神經再生術中,將健康的感覺神經轉移到角膜周邊後,軸突再生遵循Wallerian變性的過程進行1)。
- 初期損傷反應:供體神經末端的軸突變性,巨噬細胞吞噬並清除變性的髓鞘。
- Schwann細胞引導:Schwann細胞從供體神經存活的近端分化並遷移,為軸突再生提供支架。
- 軸突發芽:NGF和介白素-1(IL-1)促進軸突發芽1)。
- 選擇性再生:角膜僅選擇性地接受特定表現型的無髓神經,因此只有部分再生軸突到達角膜基質和基底下神經叢1)。
有趣的是,動物實驗顯示再生的角膜神經不一定與供體神經連續,提示供體神經不僅作為軸突來源,也可能作為神經營養因子的來源1)。
7. 最新研究與未來展望(研究階段報告)
Section titled “7. 最新研究與未來展望(研究階段報告)”角膜神經再生術的進展與適應症擴展
Section titled “角膜神經再生術的進展與適應症擴展”角膜神經再生術已從需要冠狀切口的大型手術發展為微創方法和內視鏡技術1,14)。無細胞同種異體神經移植物的引入避免了自體神經採集相關的併發症,而替代供體神經(如耳大神經)的使用擴大了適應症1)。
在結果方面,Park等人對54隻眼的回顧性研究報告顯示,Cochet-Bonnet值從術前平均2.18 mm恢復到術後平均40.1 mm1,6)。18歲以下的年輕患者往往能更早、更完全地恢復感覺和視力改善,這被認為與年輕人角膜基底下神經纖維密度較高有關1,6)。術後3個月,活體共聚焦顯微鏡開始顯示角膜神經,並在12至18個月內持續改善1,14)。角膜神經再生術穩定眼表後,通過穿透性角膜移植術(PK)或深板層角膜移植術(DALK)進行分階段視力康復,取得了良好效果1)。
Cenegermin適應症的擴展
Section titled “Cenegermin適應症的擴展”自獲得FDA/EMA批准以來,cenegermin的真實世界臨床數據不斷累積。最近,一項針對乾眼症候群的II期試驗報告了症狀、眼表染色和淚液分泌的改善2)。其在其他眼表疾病中的應用也在考慮之中。
胸腺素β4(RGN-259)
Section titled “胸腺素β4(RGN-259)”含有0.1%胸腺素β4的眼藥水(RGN-259)在一項針對神經營養性角膜病變患者的隨機、安慰劑對照、雙盲第三期臨床試驗中,顯示出促進角膜癒合和改善主觀症狀的效果3)。
胸腺素β4是一種肌動蛋白結合蛋白,被認為透過促進細胞遷移、抗發炎和抗凋亡作用來促進上皮修復15)。
局部胰島素滴眼液
Section titled “局部胰島素滴眼液”自1945年以來就有報導用於角膜疾病的局部胰島素,可促進角膜上皮的再上皮化。已證實胰島素受體和IGF-1受體在人眼表面表現。雖然尚未建立劑量共識,但通常每天滴眼四次。由於其價格低廉且易於獲得,預計在包括發展中國家在內的廣泛地區具有實用性。
RGTA(Cacicol®)
Section titled “RGTA(Cacicol®)”局部給藥的RGTA(再生劑)是一種硫酸乙醯肝素蛋白聚糖模擬物,觀察性研究報告其可促進角膜癒合。目前僅在歐洲可用。
作為先進醫療的P物質/IGF-1合劑
Section titled “作為先進醫療的P物質/IGF-1合劑”在日本,關於直接作用於角膜上皮細胞的神經肽合劑滴眼液的研究正在進行中。由最小必需序列FGLM-NH₂(源自P物質)和SSSR(源自IGF-1)組成的合劑已被證明可促進上皮傷口癒合,有望應用於難治性病例。
8. 參考文獻
Section titled “8. 參考文獻”- Hubschman S, Rosenblatt MI, Cortina MS. Corneal neurotization for the treatment of neurotrophic keratopathy. Curr Opin Ophthalmol. 2025;36(4):294-300.
- Kanu LN, Ciolino JB. Nerve growth factor as an ocular therapy: applications, challenges, and future directions. Semin Ophthalmol. 2021;36(4):224-231.
- TFOS DEWS III Management and Therapy Subcommittee. TFOS DEWS III Management and Therapy Report. Am J Ophthalmol. 2025;279:355-440.
- Dragnea DC, Krolo I, Koppen C, et al. Corneal neurotization-indications, surgical techniques and outcomes. J Clin Med. 2023;12:2214.
- Neurotrophic Keratopathy Study Group. Neurotrophic keratopathy: an updated understanding. Ocul Surf. 2023;30:129-138.
- Park JK, Charlson ES, Leyngold I, Kossler AL. Corneal neurotization: a review of pathophysiology and outcomes. Ophthalmic Plast Reconstr Surg. 2020;36:431-437.
- Fogagnolo P, Giannaccare G, Bolognesi F, et al. Direct versus indirect corneal neurotization for the treatment of neurotrophic keratopathy: a multicenter prospective comparative study. Am J Ophthalmol. 2020;220:203-214.
- Bonini S, Lambiase A, Rama P, et al. Phase II randomized, double-masked, vehicle-controlled trial of recombinant human nerve growth factor for neurotrophic keratitis. Ophthalmology. 2018;125(9):1332-1343.
- Pflugfelder SC, Massaro-Giordano M, Perez VL, et al. Topical recombinant human nerve growth factor (Cenegermin) for neurotrophic keratopathy: a multicenter randomized vehicle-controlled pivotal trial. Ophthalmology. 2020;127(1):14-26.
- Mastropasqua L, Nubile M, Lanzini M, et al. Corneal subbasal nerve plexus changes in patients with neurotrophic keratitis: an in vivo confocal microscopy study. Clin Ther. 2020;42(2):291-302.
- Sacchetti M, Lambiase A. Diagnosis and management of neurotrophic keratitis. Clin Ophthalmol. 2014;8:571-579.
- Ruiz-Lozano RE, Hernandez-Camarena JC, Loya-Garcia D, Merayo-Lloves J, Rodriguez-Garcia A. The molecular basis of neurotrophic keratopathy: diagnostic and therapeutic implications. A review. Ocul Surf. 2021;19:224-240.
- Dua HS, Said DG, Messmer EM, et al. Neurotrophic keratopathy: an updated understanding. Prog Retin Eye Res. 2018;66:107-131.
- Catapano J, Fung SSM, Halliday W, et al. Treatment of neurotrophic keratopathy with minimally invasive corneal neurotisation: long-term clinical outcomes and evidence of corneal reinnervation. Br J Ophthalmol. 2019;103:1724-1731.
- Sosne G, Kleinman HK. Primary mechanisms of thymosin β4 repair activity in dry eye disorders and other tissue injuries. Invest Ophthalmol Vis Sci. 2015;56(9):5110-5117.
