درجه I (خفیف)
کراتوپاتی سطحی نقطهای: عمدتاً ناهمواریهای نقطهای اپیتلیوم قرنیه بدون نقص اپیتلیال.
ناهنجاری کیفی اپیتلیوم: کدورت و کاهش شفافیت اپیتلیوم قرنیه.
بیثباتی لایه اشکی: ممکن است با کاهش ترشح اشک یا کاهش تراکم سلولهای جامی همراه باشد.

کراتیت نوروتروفیک (NK) یک بیماری دژنراتیو قرنیه است که با کاهش یا فقدان حس قرنیه مشخص میشود. به آن کراتوپاتی نوروتروفیک یا کراتوپاتی نوروپارالیتیک نیز گفته میشود. این بیماری در اثر آسیب به عصبدهی حسی ناشی از شاخه اول عصب سهقلو (عصب مغزی V) یعنی عصب چشمی ایجاد میشود.
پایانههای عصبی قرنیه حاوی بسیاری از انتقالدهندههای عصبی مانند ماده P، پپتید مرتبط با ژن کلسی تونین (CGRP)، نوروپپتید Y (NPY)، پپتید وازواکتیو رودهای (VIP)، گالانین، متیونین انکفالین، کاتکول آمینها و استیل کولین هستند. این عوامل مشتق از عصب، متابولیسم، چرخش و ترمیم زخم اپیتلیوم قرنیه را تنظیم میکنند و کاهش عرضه این عوامل به دلیل آسیب عصب سهقلو، مکانیسم اساسی اختلال هموستاز قرنیه است.
سیر بالینی به تدریج پیشرفت میکند. از دست دادن نسبی یا کامل حس قرنیه از کراتوپاتی اپیتلیال (کراتوپاتی سطحی نقطهای: SPK) شروع شده و میتواند به نقص اپیتلیال پایدار (PED)، زخم استرومای قرنیه و حتی سوراخ شدن قرنیه پیشرفت کند 5). با این حال، در صورت مدیریت مناسب در مراحل اولیه، میتوان از پیشرفت بیماری جلوگیری کرد.
شیوع تخمینی کمتر از 50 نفر در 100,000 نفر است و به عنوان یک بیماری نادر طبقهبندی میشود 11). کد ICD-10 آن H16.239 است. این بیماری به جای یک علت واحد، ماهیت سندرمی دارد و میتواند در اثر هر وضعیتی که مسیر عصب سهقلو را در هر نقطهای مختل کند، ایجاد شود.
کراتیت نوروتروفیک، کراتوپاتی نوروتروفیک و کراتوپاتی نوروپارالیتیک همگی به یک وضعیت ناشی از آسیب عصب سهقلو اشاره دارند. این نامها بر اساس تأکید بر التهابی یا دژنراتیو بودن آسیب اپیتلیال قرنیه متفاوت هستند، اما از نظر بالینی معادل در نظر گرفته میشوند.
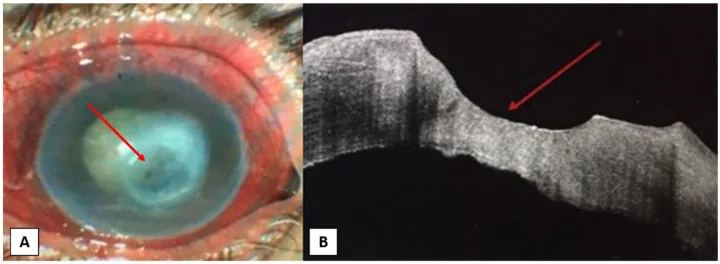
در NK به دلیل اختلال در عصبدهی حسی قرنیه، بیماران به ندرت از علائم سطح چشم شکایت میکنند. به همین دلیل، برخی موارد چند ماه تا چند سال پس از شروع بیماری برای اولین بار مراجعه میکنند.
تصویر بالینی NK از ناهمواریهای ظریف سطح قرنیه تا ذوب و سوراخ شدن قرنیه متغیر است. به طور کلاسیک، طبقهبندی سه مرحلهای Mackie به طور گسترده استفاده میشود 12,13).
درجه I (خفیف)
کراتوپاتی سطحی نقطهای: عمدتاً ناهمواریهای نقطهای اپیتلیوم قرنیه بدون نقص اپیتلیال.
ناهنجاری کیفی اپیتلیوم: کدورت و کاهش شفافیت اپیتلیوم قرنیه.
بیثباتی لایه اشکی: ممکن است با کاهش ترشح اشک یا کاهش تراکم سلولهای جامی همراه باشد.
درجه II (متوسط)
نقص اپیتلیال پایدار (PED): مشخصه آن شکل بیضی با لبههای برجسته (rolled margins) است. ممکن است با کدورت یا رگزایی همراه باشد.
چینهای غشای دسمه: یافتهای همراه با ادم قرنیه.
التهاب خفیف اتاق قدامی: ممکن است التهاب خفیف (cell/flare) در اتاق قدامی مشاهده شود.
درجه III (شدید)
زخم استرومای قرنیه: نقص استروما همراه با ذوب (melting) قرنیه.
سوراخ شدن قرنیه: شدیدترین عارضه که نیاز به مداخله جراحی فوری دارد.
اسکار قرنیه: ممکن است پس از بهبودی منجر به اختلال دائمی بینایی شود.
کاهش ترشح اشک اغلب یک یافته همراه و تقریباً همیشه در NK وجود دارد. در ارزیابی، علاوه بر یافتههای قرنیه، حتماً باید از تست شیرمر و BUT استفاده کرد 11).
در NK، به دلیل آسیب عصب سهقلو، حس قرنیه کاهش یافته یا از بین رفته است. معمولاً آسیب اپیتلیوم قرنیه به صورت درد یا احساس جسم خارجی احساس میشود، اما در NK این سیگنال هشدار عمل نمیکند. علاوه بر این، ترشح رفلکسی اشک و پلک زدن نیز کاهش مییابد، بنابراین حتی با پیشرفت نقص اپیتلیال یا زخم، علائم ذهنی وجود ندارد و به دلیل تأخیر در مراجعه، بیماری شدید میشود.
هر بیماری موضعی چشمی یا سیستمیک که مسیر عصبی حسی از قرنیه تا هسته عصب سهقو در پل مغزی را مختل کند، میتواند باعث NK شود. از نظر پاتوفیزیولوژی، به سه دسته محیطی (موضعی قرنیه تا حدقه)، مرکزی (داخل جمجمه) و متابولیک (دیابت) تقسیم میشود 13).
در بیماران دیابتی، تغییرات مورفولوژیک و عملکردی در اعصاب حسی قرنیه پیشرفت میکند و با شدت رتینوپاتی دیابتی، کاهش حس قرنیه مشاهده میشود. این یکی از جنبههای نوروپاتی محیطی دیابتی است و مشابه زخمهای پوستی مقاوم و گانگرن پای دیابتی در نظر گرفته میشود. مواردی از کشف NK به عنوان اولین علامت دیابت نیز گزارش شده است 11).
در LASIK، به دلیل برش اعصاب قرنیه هنگام ایجاد فلپ، کاهش موقت حس قرنیه پس از عمل رخ میدهد. در بیشتر موارد طی چند ماه تا یک سال بهبود مییابد، اما به ندرت طولانی شده و به کراتیت نوروتروفیک منجر میشود. PRK به دلیل عدم ایجاد فلپ، میزان بروز نوروپاتی کمتری دارد. در مواردی که قبل از عمل خشکی چشم یا کاهش حس قرنیه وجود دارد، ارزیابی دقیق در مرحله انتخاب روش جراحی ضروری است.
این مهمترین آزمایش برای تشخیص NK است.
از آنجایی که قطرههای چشمی (به ویژه داروهای بیحسکننده یا حاوی مواد نگهدارنده) مقادیر اندازهگیری را تغییر میدهند، آزمایش حساسیت باید قبل از استفاده از قطره انجام شود.
اگر با وجود عدم وجود علائم ناراحتی چشمی به دلیل بیحسی قرنیه، آسیب شدید اپیتلیوم قرنیه مشاهده شود، NK به شدت مشکوک است. افتراق از بیماریهای زیر ضروری است.
پس از تأیید تشخیص، بررسی علت ضروری است. با شرح حال (سابقه هرپس، دیابت، جراحی چشم، تروما، ضایعات داخل جمجمه، قطره چشم) و در صورت لزوم MRI مغز و مشاوره نورولوژی/جراحی مغز انجام میشود.
درمان NK بر اساس مدیریت مرحلهای با توجه به مرحله بیماری است. در تمام مراحل، از قطرههای چشمی بدون مواد نگهدارنده (preservative-free) استفاده میشود. در صورت وجود سایر بیماریهای سطح چشم (خشکی چشم، بلفاریت، کراتوپاتی ناشی از قرارگیری و …) به طور همزمان درمان میشوند. درمان بیماری زمینهای نیز همزمان انجام میشود.
| مرحله | هدف درمان | روشهای اصلی درمان |
|---|---|---|
| درجه I | بهبود کیفیت و شفافیت اپیتلیوم، پیشگیری از نقص اپیتلیال | اشک مصنوعی بدون مواد نگهدارنده، پماد روانکننده، بستن نقطه اشکی، قطره سرم خودی |
| درجه II | ترمیم نقص اپیتلیال پایدار | لنز تماسی درمانی، پیوند آمنیون، تارسورافی، سنگرمین |
| درجه III | ترمیم زخم و پیشگیری از سوراخ شدن | NAC، تتراسایکلین خوراکی، چسب بافتی، پیوند قرنیه |
هدف محافظت از اپیتلیوم و تثبیت لایه اشکی است.
علاوه بر درمان درجه I، موارد زیر استفاده میشود.
در کارآزماییهای بالینی سنگرمین، یک کارآزمایی تصادفیسازی شده دوسوکور با کنترل دارونما (فاز II REPARO، مطالعه محوری Pflugfelder 2020) روی بیماران مبتلا به NK درجه II یا III انجام شد8,9).
با تلفیق دو کارآزمایی تصادفیسازی شده، ۶۵ تا ۷۲٪ از بیماران گروه rhNGF پس از ۸ هفته بهبودی کامل قرنیه را به دست آوردند، در حالی که این میزان در گروه دارونما ۱۷ تا ۳۳٪ بود. شایعترین عارضه جانبی درد در محل مصرف قطره بود که در حدود ۱۶٪ از بیماران رخ داد3).
کارآزمایی فاز I/II REPARO (NGF0212) کاهش زمان بهبود نقص اپیتلیال و کاهش میزان عود را نشان داد، اما بهبود معنیداری در حس قرنیه مشاهده نشد2). برخی از بیماران پس از قطع درمان دچار عود NK میشوند و پیگیری منظم ضروری است.
استروئیدهای موضعی به دلیل خطر القای ذوب استروما باید در صورت استفاده برای کنترل التهاب با احتیاط تجویز شوند. NSAIDهای موضعی به دلیل کاهش بیشتر حس قرنیه باید اجتناب شوند. استفاده مداوم از قطرههای بیحسی موضعی اکیداً ممنوع است.
علاوه بر درمان درجه I و II، در صورت پیشرفت ذوب استروما، موارد زیر اضافه میشوند:
در صورت بروز سوراخ شدگی قرنیه، رویکرد درمانی بر اساس اندازه سوراخ متفاوت است.
در ژاپن، درمانهای زیر در سطح تحقیقات بالینی برای تسریع ترمیم زخم اپیتلیال قرنیه گزارش شدهاند. در مواردی که به درمان استاندارد پاسخ نمیدهند، مشاوره با مراکزی که این درمانها را انجام میدهند، در نظر گرفته میشود.
جراحی بازسازی عصب قرنیه به طور سنتی برای موارد شدید که به درمان محافظهکارانه پاسخ نمیدهند انجام میشد، اما با کمتهاجمیتر شدن روشها در سالهای اخیر، اندیکاسیون آن در حال گسترش است 1). موارد مناسب شامل بیماران با کاهش یا فقدان حس قرنیه متوسط تا شدید مقاوم به درمان محافظهکارانه است که بتوان از عصب سالم اهداکننده استفاده کرد 4). اعصاب اهداکننده شامل شاخههای عصب سهقلو (سوپرااوربیتال، سوپراتروکلئار، اینفرااوربیتال) و عصب بزرگ گوشی (GAN) از ناحیه گردن هستند 1).
تعداد آکسونهای عصب اهداکننده به طور متوسط برای GAN 6530، عصب سوپرااوربیتال حدود 3146 (در حاشیه حدقه حدود 6000)، عصب سوپراتروکلئار 1882 (در حاشیه حدقه 2534) و عصب سورال 3179 تا 3972 گزارش شده است 1). تصور میشود تعداد آکسون بیشتر با اثر بازسازی عصبی بهتر همراه باشد.
روشهای جراحی به دو دسته اصلی مستقیم و غیرمستقیم (پیوند عصب) تقسیم میشوند 1,7).
روشهای آناستوموز شامل end-to-end (قطع کامل عصب اهداکننده برای حداکثر بار آکسونی) و end-to-side (ایجاد پنجره در غلاف عصب اهداکننده برای حفظ عملکرد باقیمانده) است که روش دوم میتواند کاهش حس در ناحیه اهداکننده را کاهش دهد 1). در یک کارآزمایی مقایسهای چندمرکزی آیندهنگر، تفاوت معنیداری در بهبود Cochet-Bonnet بین روش مستقیم و غیرمستقیم در 12 ماه مشاهده نشد 7).
عصب اهداکننده که به قرنیه رسیده است به 3 تا 4 دسته عصبی تقسیم شده و در تونل اسکلرا-قرنیه در اطراف لیمبوس قرنیه قرار داده میشود، یا با چسب فیبرین یا بخیه به لیمبوس ثابت میشود 1). پس از عمل، با لنز تماسی بانداژ و تارسورافی موقت محافظت میشود و از اشک مصنوعی بدون مواد نگهدارنده و قطرههای آنتیبیوتیک استفاده میشود. از یک ماه پس از عمل، استفاده همزمان از قطره سنگرمین میتواند به رشد عصب قرنیه کمک کند 1).
سنگرمین یک قطره چشمی حاوی 20 میکروگرم در میلیلیتر فاکتور رشد عصبی انسانی نوترکیب (rhNGF) است و اولین داروی تأیید شده برای NK است. در کارآزماییهای بالینی (فاز II REPARO و فاز II pivotal) بر روی NK درجه II و III، با مصرف 6 بار در روز به مدت 8 هفته، بهبود کامل قرنیه در 65 تا 72٪ از بیماران گزارش شده است. از سوی دیگر، بهبود قابل توجهی در حس قرنیه نشان داده نشده است و موارد عود پس از قطع درمان وجود دارد. درد در محل مصرف قطره (حدود 16٪) عارضه جانبی اصلی است.
جراحی بازسازی عصب قرنیه، عملی است که در آن یک عصب حسی سالم (مانند عصب فوقاوربیتال، عصب تروکلئار فوقانی، عصب اینفرااوربیتال، عصب گوش بزرگ و غیره) به ناحیه اطراف قرنیه منتقل میشود تا حس قرنیه نوروتروفیک را بازگرداند. روشهای انتقال مستقیم عصب و پیوند غیرمستقیم عصب از طریق عصب سورال وجود دارد. بهبود حس قرنیه 3 تا 6 ماه پس از جراحی شروع میشود و تا 12 تا 18 ماه یا بیشتر ادامه مییابد. در مرور 54 چشم توسط Park و همکاران، مقدار Cochet-Bonnet به طور متوسط از 2.18 میلیمتر به 40.1 میلیمتر بهبود یافته است. بهبود در بیماران جوان زیر 18 سال تمایل به بهتر بودن دارد.
قرنیه یکی از متراکمترین بافتهای بدن از نظر عصبدهی است. اعصاب مژگانی بلند که از شاخه اول عصب سهقلو (عصب چشمی) منشعب میشوند، به قرنیه میرسند. رشتههای عصبی به صورت شعاعی از لیمبوس وارد استرومای قرنیه شده و در زیر غشای بومن شبکه عصبی زیراپیتلیال را تشکیل میدهند. سپس از غشای بومن عبور کرده و شبکه عصبی زیرپایهای را تشکیل میدهند و انتهای عصبی آزاد را بین سلولهای اپیتلیال گسترش میدهند. رشتههای عصبی از الیاف نازک Aδ و C تشکیل شدهاند که بدون میلین هستند و به شفافیت قرنیه کمک میکنند.
این شبکه عصبی زیرپایهای فاکتورهای نوروتروفیک ضروری برای حفظ هموستاز اپیتلیوم قرنیه را تأمین میکند 1,8). رشتههای عصبی حاوی ماده P هستند که اثر فاکتور رشد اپیدرمی (EGF) و فاکتور رشد شبهانسولین-1 (IGF-1) را بر مهاجرت سلولهای اپیتلیال قرنیه تقویت کرده و ترمیم زخم اپیتلیال را تنظیم میکنند. اگر عصب سهقله آسیب ببیند، این مکانیسم تنظیمی از بین میرود و ترشح اشک رفلکسی و پلک زدن نیز کاهش مییابد، بنابراین آسیب اپیتلیوم قرنیه به راحتی پیشرفت کرده و بهبودی به تأخیر میافتد.
هنگامی که تأمین فاکتورهای نوروتروفیک قطع میشود، تغییرات بافتشناسی زیر به تدریج رخ میدهد.
در مدلهای حیوانی، در موشهایی که عصب سهقلو تخریب شده است، بهبود نقص اپیتلیال قرنیه به طور قابل توجهی در مقایسه با گروه کنترل به تأخیر میافتد و این نشان میدهد که از دست دادن عوامل عصبی مکانیسم مرکزی تأخیر در ترمیم زخم است.
NGF یک مولکول شاخص از خانواده نوروتروفینها است که با برش از پیشساز pro-NGF به شکل فعال تبدیل میشود. شکل فعال دیمر β-NGF (وزن مولکولی 26 کیلودالتون) است که از دو زیرواحد β غیرکووالان تشکیل شده است2).
NGF به دو گیرنده زیر متصل میشود2):
این گیرندهها به طور ثابت در سلولهای اپیتلیال قرنیه و سلولهای اپیتلیال پایه ملتحمه بیان میشوند. NGF باعث افزایش تکثیر و تمایز سلولهای اپیتلیال قرنیه شده و به ترمیم زخم کمک میکند2). در بیماران NK، عرضه NGF کاهش مییابد که به اختلال هموستاز اپیتلیال کمک میکند. اثر بالینی قطره چشمی rhNGF در مطالعه REPARO به عنوان درمان اختصاصی بر اساس این مکانیسم مولکولی در نظر گرفته میشود8,9).
کاهش حس قرنیه در بیماران دیابتی به عنوان یک فنوتیپ از نوروپاتی محیطی دیابتی در نظر گرفته میشود. مشخص شده است که با شدت رتینوپاتی دیابتی، حس قرنیه کاهش مییابد و با کاهش عملکرد کلیه، تغییرات مورفولوژیک عصب قرنیه پیشرفت میکند. این تظاهر نوروپاتی حسی محیطی در سطح چشم، مشابه زخم پای دیابتی و زخمهای پوستی مقاوم به درمان است و یکی از پایههای مهم پاتولوژیک کراتوپاتی نوروتروفیک محسوب میشود13).
در جراحی بازسازی عصب قرنیه، پس از انتقال عصب حسی سالم به اطراف قرنیه، فرآیند بازسازی آکسون مطابق با مراحل دژنراسیون والرین پیش میرود 1).
جالب توجه است که مطالعات حیوانی نشان دادهاند اعصاب قرنیه بازسازی شده لزوماً با عصب دهنده پیوسته نیستند، که نشان میدهد عصب دهنده ممکن است نه تنها به عنوان منبع آکسون، بلکه به عنوان منبع فاکتورهای نوروتروفیک نیز عمل کند 1).
جراحی بازسازی عصب قرنیه از روشهای بزرگ با برش کرونر به رویکردهای کم تهاجمی و تکنیکهای آندوسکوپی تکامل یافته است 1,14). معرفی آلوگرافت عصبی بدون سلول، عوارض مرتبط با برداشت عصب خودی را قابل اجتناب کرده و استفاده از اعصاب دهنده جایگزین (مانند عصب گوش بزرگ) اندیکاسیونها را گسترش داده است 1).
از نظر پیامدها، در مرور 54 چشم توسط Park و همکاران، مقدار Cochet-Bonnet از میانگین 2.18 میلیمتر قبل از عمل به 40.1 میلیمتر پس از عمل بهبود یافته است 1,6). در بیماران جوان زیر 18 سال، تمایل به بهبود زودهنگام و کاملتر حس و بهبود بینایی وجود دارد که به تراکم بالای رشتههای عصبی زیر اپیتلیال قرنیه در سنین پایین نسبت داده میشود 1,6). از 3 ماه پس از عمل، با میکروسکوپ کانفوکال درونبدنی، اعصاب قرنیه قابل مشاهده میشوند و بهبود تا 12-18 ماه ادامه مییابد 1,14). پس از تثبیت سطح چشم با جراحی بازسازی عصب قرنیه، توانبخشی بینایی مرحلهای با پیوند کامل قرنیه (PK) یا پیوند لایهای قدامی عمیق (DALK) با نتایج خوب انجام میشود 1).
پس از تأیید سنگرمین توسط FDA/EMA، دادههای بالینی واقعی همچنان در حال جمعآوری است. اخیراً، یک مطالعه فاز II بر روی سندرم خشکی چشم، بهبود علائم، رنگپذیری سطح چشم و ترشح اشک را گزارش کرده است 2). کاربردهای دیگر در بیماریهای سطح چشم نیز در حال بررسی است.
قطره چشمی حاوی 0.1% تیموزین بتا 4 (RGN-259) در یک کارآزمایی بالینی فاز III تصادفی، دوسوکور و کنترلشده با دارونما در بیماران مبتلا به کراتیت نوروتروفیک، بهبود ترمیم قرنیه و کاهش علائم ذهنی را نشان داد3).
تیموزین بتا 4 یک پروتئین متصلشونده به اکتین است که تصور میشود از طریق تسهیل مهاجرت سلولی، ضدالتهاب و ضدآپوپتوز، ترمیم اپیتلیوم را تقویت میکند15).
انسولین موضعی که از سال 1945 برای استفاده در بیماریهای قرنیه گزارش شده است، بازسازی اپیتلیوم قرنیه را تسریع میکند. گیرندههای انسولین و گیرندههای IGF-1 در سطح چشم انسان بیان میشوند. اگرچه اجماعی در مورد دوز وجود ندارد، معمولاً چهار بار در روز استفاده میشود. به دلیل هزینه کم و در دسترس بودن بالا، انتظار میرود در مناطق وسیعی از جمله کشورهای در حال توسعه مفید باشد.
RGTA (عامل بازسازیکننده) که به صورت موضعی تجویز میشود، یک ماده تقلیدی از پروتئوگلیکان سولفات هپاران است و در مطالعات مشاهدهای تسریع ترمیم قرنیه گزارش شده است. در حال حاضر فقط در اروپا در دسترس است.
در داخل کشور، تحقیقات در مورد قطره چشمی ترکیبی از نوروپپتیدها که مستقیماً روی سلولهای اپیتلیال قرنیه اثر میکنند، ادامه دارد. ترکیبی از حداقل توالی ضروری FGLM-NH₂ (مشتق از سابستنس P) و SSSR (مشتق از IGF-1) نشان داده است که ترمیم زخم اپیتلیال را تسریع میکند و انتظار میرود در موارد مقاوم به درمان کاربرد داشته باشد.