
میکروسکوپ کانفوکال (میکروسکوپ کانفوکال قرنیه زنده)
نکات کلیدی در یک نگاه
Section titled “نکات کلیدی در یک نگاه”۱. میکروسکوپ کانفوکال چیست؟
Section titled “۱. میکروسکوپ کانفوکال چیست؟”میکروسکوپ کانفوکال یک میکروسکوپ با وضوح بالا است که بر اساس اصل نوری اشتراک صفحه کانونی نور روشنایی و نور مشاهده کار میکند. در چشمپزشکی برای مشاهده زنده قرنیه استفاده میشود و در ارزیابی دیستروفی اندوتلیال فوکس نیز کاربرد دارد 7).
دستگاههای اصلی که در حال حاضر در بالین استفاده میشوند دو نوع هستند:
نوع اسکن لیزری (HRT III-RCM): ساخت شرکت Heidelberg Engineering. از لیزر دیود ۶۷۰ نانومتر به عنوان منبع نور استفاده میکند، با لنز شیئی ۶۳ برابر و میدان دید ۴۰۰×۴۰۰ میکرومتر. قدرت تفکیک جانبی ۱-۲ میکرومتر و قدرت تفکیک عمقی حدود ۴ میکرومتر دارد 1)2). با استفاده از کلاهک یکبار مصرف PMMA (TomoCap) و ژل چشمی به قرنیه تماس داده میشود.
نوع اسکن شکاف (Confoscan 4): ساخت شرکت Nidek. از منبع نور هالوژن استفاده میکند و بدون تماس نیز قابل استفاده است. دارای عملکرد اسکن خودکار است و کار با آن نسبتاً آسان است، اما قدرت تفکیک عمقی آن به ۲۵-۲۷ میکرومتر محدود است. در حال حاضر تولید آن متوقف شده است.
IVCM دارای سه حالت تصویربرداری است. اسکن مقطعی تصاویر ثابت در یک عمق واحد میگیرد. اسکن حجمی ۳۰-۴۰ مقطع متوالی با فاصله ۲ میکرومتر میگیرد. اسکن دنبالهای تا ۱۰۰ فریم ویدئو در یک عمق واحد میگیرد و برای مشاهده تغییرات دینامیک مناسب است.
IVCM نیاز به دستگاه تخصصی و اپراتور ماهر دارد، بنابراین عمدتاً در بیمارستانهای دانشگاهی و مراکز تخصصی چشمپزشکی موجود است. این آزمایش در همه کلینیکهای چشم انجام نمیشود، اما برای تشخیص عفونتهای قرنیه و دیستروفیهای قرنیه بسیار مفید است و در صورت نیاز ارجاع داده میشود.
۲. یافتههای اصلی و اهمیت بالینی
Section titled “۲. یافتههای اصلی و اهمیت بالینی”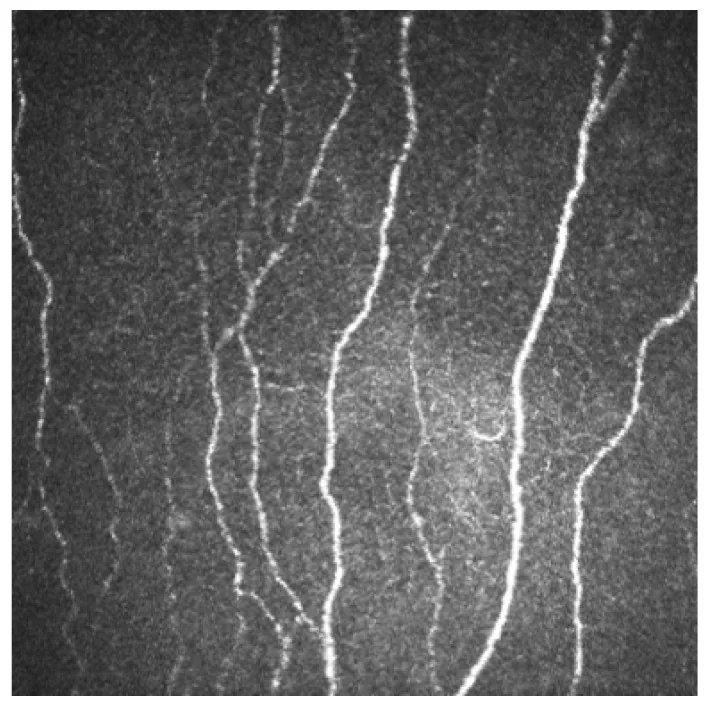
یافتههای قرنیه طبیعی
Section titled “یافتههای قرنیه طبیعی”در IVCM میتوان لایههای مختلف قرنیه را به صورت جداگانه مشاهده کرد.
اپیتلیوم قرنیه: سلولهای سطحی چندضلعی با اندازه ۴۰-۵۰ میکرومتر. سلولهای بالدار ۲۰-۳۰ میکرومتر با مرزهای سلولی روشن و حدود ۵۰۰۰ سلول در میلیمتر مربع. سلولهای پایه ۸-۱۰ میکرومتر با سیتوپلاسم تیره و مرزهای روشن (دسموزوم) و الگوی لانه زنبوری. تراکم سلولهای پایه ۳۶۰۰-۸۹۹۶ سلول در میلیمتر مربع است.
غشای بومن: به صورت لایهای بدون ساختار به رنگ خاکستری-سفید با ضخامت حدود ۱۰ میکرومتر مشاهده میشود. دستههای عصبی از آن عبور میکنند.
استرومای قرنیه: سلولهای استرومایی (کراتوسیتها) در حالت غیرفعال تیره و در حالت فعال به صورت آمیبی روشن دیده میشوند. تراکم سلولی در استرومای قدامی بیشتر است.
غشای دسمه: به صورت لایهای مهآلود با ضخامت ۶-۱۰ میکرومتر مشاهده میشود. ساختار سلولی معمولاً قابل تشخیص نیست.
اندوتلیوم قرنیه: سلولهای ششضلعی به صورت موزاییکی چیده شدهاند. قطر سلول حدود ۲۰ میکرومتر، تراکم ۲۵۵۰-۲۷۲۰ سلول در میلیمتر مربع که با افزایش سن سالانه حدود ۰.۶٪ کاهش مییابد.
شبکه عصبی زیر پایه: به صورت ساختارهای منحنی مهرهای شکل درست در زیر غشای بومن مشاهده میشود3). در حدود ۱-۲ میلیمتر پایین-داخلی از مرکز قرنیه، الگوی چرخشی (whorl pattern) تشکیل میدهد. قطر رشتهها ۰.۵۲-۴.۶ میکرومتر است.
سلولهای دندریتیک (سلولهای لانگرهانس): در مرکز قرنیه ۳۴ ± ۳ سلول در میلیمتر مربع و در محیط ۹۸ ± ۸ سلول در میلیمتر مربع توزیع میشوند. نشانگر پاسخ ایمنی هستند.
یافتههای غیرطبیعی
Section titled “یافتههای غیرطبیعی”عفونتهای قرنیه: در کراتیت قارچی، هیفهای رشتهای به وضوح در استروما مشاهده میشوند8). آکانتامبا به صورت کیست (کروی با دیواره دوگانه) تشخیص داده میشود، اما تمایز از سلولهای التهابی نیاز به تجربه دارد8). باکتریها به دلیل کوچکی بیش از حد سلولها، مستقیماً قابل مشاهده نیستند5).
دیستروفیهای قرنیه: در دیستروفی قرنیه آولینو (GCD2)، رسوبات دانهای با شدت بالا در لایه اپیتلیال پایه و خوشههای نامنظم با شدت بالا در استرومای سطحی تا میانی دیده میشود1). در دیستروفی قرنیه مشبک نوع I، رسوبات شبکهای و رشتههای منشعب مشخص است1). در دیستروفی قرنیه لکهای، رسوبات با مرز نامشخص دیده میشود و در دیستروفی قرنیه کریستالی اشنیدر، کریستالهای سوزنی شکل مشاهده میشود1).
اکتازی قرنیه: در قوز قرنیه، کاهش تراکم کراتوسیتها مشاهده میشود که با شدت بیماری همبستگی دارد. پارگی غشای بومن نیز دیده میشود. در اکتازی پس از PRK، نقص غشای بومن و کاهش کراتوسیتهای قدامی مشخص است و الگوی IVCM متفاوتی نسبت به قوز قرنیه نشان میدهد2).
۳. تکنیک و روش معاینه
Section titled “۳. تکنیک و روش معاینه”مراحل انجام IVCM به شرح زیر است.
آمادهسازی: بیحسی موضعی با قطره (مانند اکسیبوپروکائین) انجام میشود. ژل چشمی روی TomoCap یکبار مصرف (ساخته شده از PMMA) قرار داده شده و به نوک لنز شیئی متصل میشود.
انجام معاینه: در حالی که دوربین CCD تماس بین لنز و قرنیه را مانیتور میکند، قرنیه آپلانته میشود. فوکوس به صورت دستی تنظیم شده و از لایه سطحی قرنیه (0 میکرومتر) به سمت لایههای عمیقتر به ترتیب مشاهده میشود. تثبیت نگاه بسیار مهم است و همکاری بیمار ضروری میباشد. زمان معاینه حدود 5 تا 15 دقیقه است.
عوارض: به ندرت ممکن است خراشیدگی اپیتلیوم قرنیه یا عفونت (در صورت وجود نقص اپیتلیال قبلی، خطر بالاتر است) رخ دهد.
| ویژگی | HRT III-RCM | Confoscan 4 |
|---|---|---|
| منبع نور | لیزر دیودی | نور هالوژن |
| تفکیک عمقی | 4 میکرومتر | 25 تا 27 میکرومتر |
| تماس | نیاز دارد (TomoCap) | اختیاری |
به دلیل استفاده از بیحسی موضعی قطرهای، در حین معاینه تقریباً هیچ دردی وجود ندارد. فقط حس تماس خفیف کلاهک با قرنیه احساس میشود. ممکن است پس از معاینه احساس جسم خارجی موقتی ایجاد شود که معمولاً به سرعت برطرف میشود.
4. اصول نوری و ویژگیهای دستگاه
Section titled “4. اصول نوری و ویژگیهای دستگاه”اصل اساسی میکروسکوپ کانفوکال «همکانونی (confocality)» است7). هم سیستم روشنایی و هم سیستم تشخیص دارای دهانه سوزنی هستند و تنها نور بازتابیده از صفحه کانونی عدسی شیئی به طور انتخابی تشخیص داده میشود. نور پراکنده از خارج از صفحه کانونی توسط دهانه سوزنی مسدود میشود، بنابراین کنتراست و وضوح عمق بالایی به دست میآید.
در نوع اسکن لیزری (HRT III-RCM)، لیزر دیودی 670 نانومتر به عنوان منبع نور نقطهای عمل میکند و با اسکن نقطهبهنقطه روی قرنیه تصویر را میسازد. ضخامت صفحه کانونی (ضخامت برش نوری) حدود 4 میکرومتر است که بسیار نازک بوده و تصاویر مقطعی واضح در سطح سلولی ارائه میدهد.
در نوع اسکن شکافی (Confoscan 4)، اسکن با پرتو شکافمانند انجام میشود، بنابراین همکانونی واقعی فقط در جهت عمود بر شکاف به دست میآید. در نتیجه وضوح عمق 25 تا 27 میکرومتر است و وضوح تصویر نسبت به نوع اسکن لیزری پایینتر است.
محدودیتهای IVCM شامل: تصاویر فقط به صورت مقیاس خاکستری (عدم مشاهده رنگی)، عدم توانایی در تفکیک ساختارهای درونسلولی، دشواری مشاهده در موارد کدورت شدید قرنیه، دشواری در تعیین دقیق محل مشاهده، و وابستگی به مهارت اپراتور است.
5. کاربردهای بالینی اصلی
Section titled “5. کاربردهای بالینی اصلی”کاربردهای بالینی IVCM متنوع است.
کمک به تشخیص عفونتهای قرنیه: به عنوان مکمل کشت میکروبی مفید است. میتوان هیفهای قارچی و کیستهای آکانتامبا را تشخیص داد، اما تفسیر یافتهها نیاز به دانش تخصصی دارد8). در کراتیت هرپسی، تغییرات اعصاب قرنیه قابل تشخیص است8). در اندوتلیت قرنیه ناشی از سیتومگالوویروس، ممکن است اجسام انکلوژن «چشم جغد» دیده شود.
تشخیص افتراقی دیستروفیهای قرنیه: هر دیستروفی یافتههای IVCM مشخصی دارد و تشخیص افتراقی غیرتهاجمی از طریق تشخیص الگو امکانپذیر است1). این روش به عنوان غربالگری قبل از آزمایش ژنتیک یا بیوپسی بسیار مفید است. همچنین برای ارزیابی اثر درمان (مانند PTK، DALK) قابل استفاده است1).
ارزیابی نارسایی سلولهای بنیادی لیمبوس (LSCD): ناپدید شدن ساختارهای حصار مانند فوگت، جایگزینی اپیتلیوم قرنیه توسط اپیتلیوم ملتحمه، و ظهور سلولهای جامی مبنای تشخیص هستند6). اندازهگیری تراکم سلولهای اپیتلیال پایه میتواند شدت LSCD را به صورت کمی ارزیابی کند6).
ارزیابی ادم قرنیه و بیماریهای اندوتلیال: IVCM میتواند سلولهای اندوتلیال را حتی از طریق ادم متوسط قرنیه مشاهده کند، بنابراین در مواردی که اسپکولار میکروسکوپی دشوار است، بسیار مفید است7). در دیستروفی اندوتلیال فوکس (FECD)، علاوه بر ارزیابی سلولهای اندوتلیال، کاهش تراکم عصبی و تغییرات تراکم سلولهای دندریتیک نیز قابل تشخیص است7).
ارزیابی عصب قرنیه: ارزیابی کمی شبکه عصبی زیرپایهای برای تشخیص کراتوپاتی نوروتروفیک و ارزیابی اثربخشی درمان استفاده میشود3). در ارزیابی بازسازی عصبی پس از پیوند عصب قرنیه (surgical corneal neurotization)، IVCM یافتههای بازسازی را در ۶ ماه تا ۱ سال پس از جراحی نشان میدهد3).
تشخیص زودهنگام بیماریهای خودایمنی سیستمیک: در سندرم شوگرن، کاهش تراکم رشتههای عصبی در مرکز قرنیه و افزایش سلولهای دندریتیک فعال ممکن است قبل از بروز علائم بالینی قابل تشخیص باشد4). وجود دو یا بیش از دو سلول دندریتیک فعال با سه یا بیش از سه زائده در قرنیه مرکزی، حساسیت ۶۰٪ و ویژگی ۷۷٪ برای بیماریهای ایمنی سیستمیک گزارش شده است4).
ارزیابی پس از جراحی: برای بررسی تغییرات لبه فلپ و غشای بومن پس از LASIK و PRK و همچنین پیگیری بازسازی عصبی استفاده میشود2). همچنین در تشخیص زودهنگام رد پیوند پس از پیوند قرنیه کاربرد دارد.
۶. تحقیقات جدید و چشمانداز آینده
Section titled “۶. تحقیقات جدید و چشمانداز آینده”تجزیه و تحلیل خودکار تصاویر: سیستمهای کمی خودکار برای رشتههای عصبی زیرپایهای مانند نرمافزار ACCMetrics توسعه یافتهاند2). پارامترهایی مانند تراکم رشتههای عصبی، تراکم انشعابات و پیچخوردگی به صورت عینی محاسبه شده و تغییرپذیری بین ارزیابان را کاهش میدهند.
تشخیص مرحله پیشبالینی بیماری: در موارد سندرم شوگرن، گزارش شده است که ناهنجاریهای IVCM چندین سال قبل از مثبت شدن آنتیبادیها یا ظهور علائم بالینی قابل تشخیص بوده است4). این نشان میدهد که IVCM میتواند به عنوان ابزاری برای غربالگری بیماریهای خودایمنی استفاده شود.
طبقهبندی زیرگروههای خشکی چشم: با تجزیه و تحلیل مورفولوژی و الگوی توزیع سلولهای دندریتیک، میتوان خشکی چشم با واسطه ایمنی را از خشکی چشم ناشی از تبخیر بیش از حد افتراق داد4).
پایش بازسازی عصبی پس از جراحی: تحقیقات برای پیگیری روند بازسازی عصبی پس از پیوند عصب قرنیه و کراسلینکینگ قرنیه با استفاده از IVCM در حال انجام است3). انتظار میرود که در آینده به عنوان یک نقطه پایانی عینی برای ارزیابی اثربخشی درمان استفاده شود.
ادغام هوش مصنوعی: سیستمهای طبقهبندی و تشخیص خودکار تصاویر IVCM با استفاده از یادگیری عمیق در حال توسعه هستند و انتظار میرود که برای تشخیص سریع عفونتها و افتراق خودکار دیستروفیهای قرنیه به کار روند.
۷. منابع
Section titled “۷. منابع”-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
