
Microscopía confocal (microscopía confocal corneal in vivo)
Puntos clave de un vistazo
Sección titulada «Puntos clave de un vistazo»1. ¿Qué es la microscopía confocal?
Sección titulada «1. ¿Qué es la microscopía confocal?»La microscopía confocal es un microscopio de alta resolución basado en el principio óptico de que la luz de iluminación y la luz de observación comparten el mismo plano focal. En oftalmología, se aplica a la observación in vivo de la córnea y también se utiliza para la evaluación de la distrofia endotelial de Fuchs 7).
Los principales dispositivos utilizados actualmente en la práctica clínica son los siguientes dos tipos.
Tipo de escaneo láser (HRT III-RCM): Fabricado por Heidelberg Engineering. Utiliza un láser de diodo de 670 nm como fuente de luz, con un objetivo de 63× y un campo de visión de 400×400 μm. Tiene alta resolución con resolución lateral de 1–2 μm y resolución de profundidad de aproximadamente 4 μm 1)2). Se utiliza en contacto con la córnea a través de un capuchón desechable de PMMA (TomoCap) y gel oftálmico.
Tipo de escaneo de hendidura (Confoscan 4): Fabricado por Nidek. Utiliza una fuente de luz halógena y también se puede usar sin contacto. Tiene una función de escaneo automático y es relativamente fácil de operar, pero la resolución de profundidad se limita a 25–27 μm. Actualmente está descontinuado.
El IVCM tiene tres modos de imagen. Escaneo de sección adquiere una imagen fija a una sola profundidad. Escaneo de volumen adquiere 30–40 secciones consecutivas a intervalos de 2 μm. Escaneo de secuencia adquiere hasta 100 fotogramas de video a la misma profundidad, adecuado para observar cambios dinámicos.
El IVCM requiere equipo especializado y un operador capacitado, por lo que se introduce principalmente en hospitales universitarios y centros oftalmológicos especializados. No está disponible en todas las clínicas oftalmológicas, pero es particularmente útil para diagnosticar infecciones corneales y distrofias corneales, y los pacientes son derivados según sea necesario.
2. Principales hallazgos y significado clínico
Sección titulada «2. Principales hallazgos y significado clínico»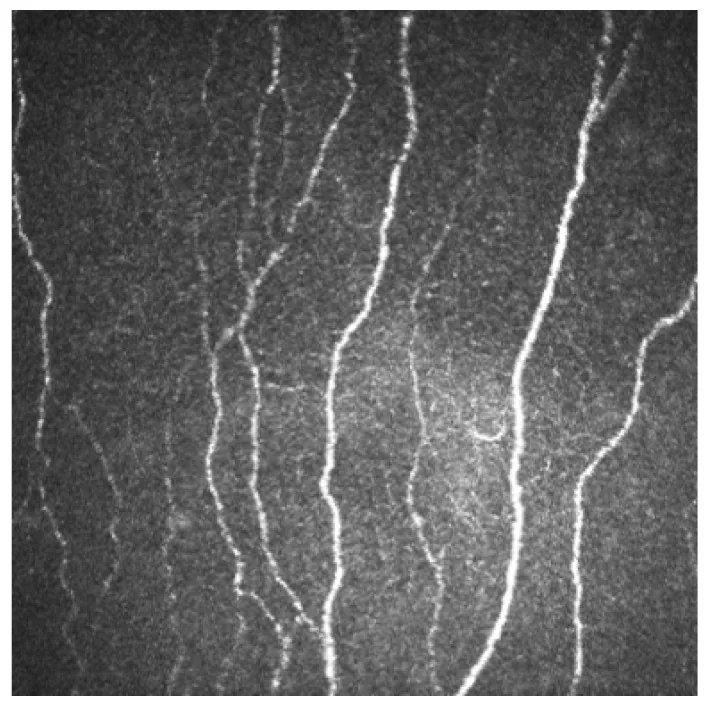
Hallazgos corneales normales
Sección titulada «Hallazgos corneales normales»La IVCM permite observar individualmente cada capa de la córnea.
Epitelio corneal: Las células superficiales son poligonales, de 40 a 50 μm. Las células aladas miden de 20 a 30 μm con bordes celulares brillantes, aproximadamente 5,000 células/mm². Las células basales miden de 8 a 10 μm con citoplasma oscuro y bordes brillantes (desmosomas), mostrando un patrón en panal. La densidad de células basales es de 3,600 a 8,996 células/mm².
Capa de Bowman: Se observa como una capa grisácea sin estructura de aproximadamente 10 μm de espesor. Los haces nerviosos la atraviesan.
Estroma corneal: Los queratocitos aparecen oscuros cuando están inactivos y brillantes con forma ameboide cuando están activados. La densidad celular es mayor en el estroma anterior.
Membrana de Descemet: Se reconoce como una capa nebulosa de 6 a 10 μm de espesor. Las estructuras celulares generalmente no son identificables.
Endotelio corneal: Células hexagonales dispuestas en mosaico. Diámetro celular de aproximadamente 20 μm, densidad de 2,550 a 2,720 células/mm², que disminuye aproximadamente un 0.6% anual con la edad.
Plexo nervioso subbasal: Se observa como estructuras curvas con forma de cuentas justo debajo de la capa de Bowman3). Forman un patrón en remolino aproximadamente a 1–2 mm inferonasal al centro corneal. El diámetro de las fibras es de 0.52 a 4.6 μm.
Células dendríticas (células de Langerhans): Se distribuyen a 34 ± 3 células/mm² en el centro corneal y 98 ± 8 células/mm² en la periferia. Son indicadores de la respuesta inmunitaria.
Hallazgos anormales
Sección titulada «Hallazgos anormales»Infecciones corneales: En la queratitis fúngica, se observan claramente hifas filamentosas dentro del estroma8). Acanthamoeba se detecta como quistes (esféricos con pared doble), pero la diferenciación de las células inflamatorias requiere experiencia8). Las bacterias son difíciles de visualizar directamente porque los organismos individuales son demasiado pequeños5).
Distrofias corneales: En la distrofia corneal de Avellino (GCD2), se observan depósitos granulares hiperreflectivos en la capa epitelial basal y grupos hiperreflectivos irregulares en el estroma superficial a medio1). La distrofia corneal reticular tipo I se caracteriza por depósitos reticulares y fibras ramificadas1). En la distrofia corneal macular se observan depósitos con bordes indistintos, y en la distrofia corneal cristalina de Schnyder se observan cristales en forma de aguja1).
Ectasia corneal: En el queratocono, se observa una disminución de la densidad de queratocitos, que se correlaciona con la gravedad. También se observan roturas en la capa de Bowman. En la ectasia corneal post-PRK, la pérdida de la capa de Bowman y la reducción de queratocitos anteriores son características, mostrando un patrón IVCM diferente al del queratocono2).
3. Técnica y método de exploración
Sección titulada «3. Técnica y método de exploración»El procedimiento de examen con IVCM es el siguiente.
Preparación: Administrar anestesia tópica (p. ej., oxibuprocaína). Aplicar gel oftálmico en un TomoCap desechable (de PMMA) y colocarlo en la punta del objetivo.
Realización del examen: Aplanar la córnea mientras se monitorea el contacto entre el lente y la córnea con una cámara CCD. Ajustar el enfoque manualmente y observar secuencialmente desde la capa superficial (0 μm) hasta las capas profundas. La fijación es muy importante y la cooperación del paciente es esencial. El examen dura aproximadamente de 5 a 15 minutos.
Complicaciones: Pueden ocurrir raramente abrasión del epitelio corneal e infección (mayor riesgo si hay un defecto epitelial preexistente).
| Parámetro | HRT III-RCM | Confoscan 4 |
|---|---|---|
| Fuente de luz | Láser de diodo | Luz halógena |
| Resolución de profundidad | 4 μm | 25–27 μm |
| Contacto | Requerido (TomoCap) | Opcional |
Debido a que se aplica anestesia tópica, casi no hay dolor durante el examen. Solo se siente un ligero contacto de la tapa sobre la córnea. Puede ocurrir una sensación temporal de cuerpo extraño después del examen, pero generalmente desaparece rápidamente.
4. Principios ópticos y características del dispositivo
Sección titulada «4. Principios ópticos y características del dispositivo»El principio básico de la microscopía confocal es la “confocalidad” 7). Tanto el sistema de iluminación como el de detección tienen aberturas de orificio, detectando selectivamente solo la luz reflejada desde el plano focal del objetivo. La luz dispersa desde fuera del plano focal es bloqueada por el orificio, proporcionando alto contraste y resolución de profundidad.
En el tipo de escaneo láser (HRT III-RCM), un láser de diodo de 670 nm funciona como fuente de luz puntual, escaneando punto por punto sobre la córnea para construir una imagen. El grosor del plano focal (grosor de la sección óptica) es extremadamente delgado, de aproximadamente 4 μm, proporcionando imágenes transversales nítidas a nivel celular.
En el tipo de escaneo de hendidura (Confoscan 4), el escaneo se realiza con un haz de luz en forma de hendidura, por lo que la verdadera confocalidad se obtiene solo en la dirección perpendicular a la hendidura. Por lo tanto, la resolución de profundidad es de 25–27 μm, y la nitidez de la imagen es inferior a la del tipo de escaneo láser.
Las limitaciones de la IVCM incluyen: solo imágenes en escala de grises (sin observación en color), incapacidad para resolver estructuras intracelulares, dificultad para observar casos con opacidad corneal severa, dificultad para localizar con precisión el sitio de observación y dependencia de la habilidad del examinador.
5. Principales aplicaciones clínicas
Sección titulada «5. Principales aplicaciones clínicas»Las aplicaciones clínicas de la IVCM son diversas.
Ayuda diagnóstica en infecciones corneales: Útil como complemento de los cultivos. Se pueden detectar hifas fúngicas y quistes de Acanthamoeba, pero la interpretación de los hallazgos requiere conocimiento especializado 8). En la queratitis herpética, se pueden capturar cambios en los nervios corneales 8). En la endotelitis corneal por citomegalovirus, a veces se observan cuerpos de inclusión en ojo de búho.
Diferenciación de distrofias corneales: Cada distrofia tiene hallazgos característicos en la IVCM, lo que permite una diferenciación no invasiva mediante reconocimiento de patrones 1). Es muy útil como herramienta de detección antes de pruebas genéticas o biopsia. También se puede aplicar para evaluar los resultados del tratamiento (PTK, DALK, etc.) 1).
Evaluación de la deficiencia de células madre limbares (LSCD): La pérdida de las empalizadas de Vogt, el reemplazo del epitelio corneal por epitelio conjuntival y la presencia de células caliciformes son criterios diagnósticos 6). La medición de la densidad de células epiteliales basales permite una evaluación cuantitativa de la gravedad de la LSCD 6).
Evaluación del edema corneal y enfermedades endoteliales: La IVCM puede observar las células endoteliales incluso a través de edema corneal moderado, por lo que es particularmente útil en casos donde la microscopía especular es difícil de realizar 7). En la distrofia endotelial corneal de Fuchs (FECD), además de evaluar las células endoteliales, también se pueden capturar la disminución de la densidad nerviosa y los cambios en la densidad de células dendríticas 7).
Evaluación de los nervios corneales: La evaluación cuantitativa del plexo nervioso subbasal se utiliza para el diagnóstico y la monitorización del tratamiento de la queratopatía neurotrófica 3). En la evaluación de la regeneración nerviosa tras la neurotización corneal quirúrgica, la IVCM puede confirmar hallazgos regenerativos entre 6 meses y 1 año después de la cirugía 3).
Detección temprana de enfermedades autoinmunes sistémicas: En el síndrome de Sjögren, la disminución de la densidad de fibras nerviosas en la córnea central y el aumento de células dendríticas activadas pueden detectarse antes de la aparición clínica 4). La presencia de dos o más células dendríticas activadas con tres o más prolongaciones en la córnea central se ha reportado con una sensibilidad del 60% y una especificidad del 77% para enfermedad inmunitaria sistémica 4).
Evaluación postoperatoria: Se utiliza para monitorizar los bordes del flap, los cambios en la membrana de Bowman y la regeneración nerviosa después de LASIK y PRK 2). También se aplica en la detección temprana del rechazo tras el trasplante de córnea.
6. Investigación más reciente y perspectivas futuras
Sección titulada «6. Investigación más reciente y perspectivas futuras»Análisis automatizado de imágenes: Se han desarrollado sistemas de cuantificación automatizada de fibras nerviosas subbasales, como el software ACCMetrics 2). Calculan objetivamente parámetros como la densidad de fibras nerviosas, la densidad de ramificaciones y la tortuosidad, reduciendo la variabilidad entre observadores.
Detección de etapas preclínicas de la enfermedad: En casos de síndrome de Sjögren, se ha reportado la detección de anomalías en la IVCM varios años antes de la positividad de anticuerpos o la aparición de síntomas clínicos 4). Esto sugiere que la IVCM podría ser una herramienta de cribado para enfermedades autoinmunes.
Clasificación de subtipos de ojo seco: El análisis de la morfología y los patrones de distribución de las células dendríticas puede ayudar a diferenciar el ojo seco inmunomediado del ojo seco evaporativo 4).
Monitorización de la regeneración nerviosa postoperatoria: Se están llevando a cabo estudios de seguimiento longitudinal del proceso de regeneración nerviosa después de la neurotización corneal y el cross-linking corneal mediante IVCM 3). Se espera su uso futuro como punto final objetivo de la eficacia del tratamiento.
Integración de inteligencia artificial: Se está desarrollando sistemas de clasificación y diagnóstico automatizados de imágenes de IVCM mediante aprendizaje profundo, con aplicaciones esperadas en el diagnóstico rápido de infecciones y la diferenciación automatizada de distrofias corneales.
7. Referencias
Sección titulada «7. Referencias»-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
