
Microscopio confocale (microscopio confocale corneale in vivo)
Punti chiave a colpo d’occhio
Sezione intitolata “Punti chiave a colpo d’occhio”1. Cos’è la microscopia confocale?
Sezione intitolata “1. Cos’è la microscopia confocale?”La microscopia confocale è un microscopio ad alta risoluzione basato sul principio ottico per cui la luce di illuminazione e la luce di osservazione condividono lo stesso piano focale. In campo oftalmico, viene applicata all’osservazione in vivo della cornea ed è utilizzata anche per la valutazione della distrofia endoteliale di Fuchs7).
I principali dispositivi attualmente utilizzati in clinica sono i seguenti due sistemi.
Tipo a scansione laser (HRT III-RCM) : Prodotto da Heidelberg Engineering. Utilizza un laser a diodi da 670 nm come sorgente luminosa, obiettivo 63x, campo visivo 400×400 μm. Ha una risoluzione laterale di 1-2 μm e una risoluzione in profondità di circa 4 μm1)2). Viene utilizzato a contatto con la cornea tramite un cappuccio monouso in PMMA (TomoCap) e gel oftalmico.
Tipo a scansione di fessura (Confoscan 4) : Prodotto da Nidek. Utilizza una sorgente luminosa alogena e può essere utilizzato anche senza contatto. Dispone di una funzione di scansione automatica ed è relativamente facile da usare, ma la risoluzione in profondità è limitata a 25-27 μm. Attualmente la produzione è stata interrotta.
L’IVCM dispone di tre modalità di imaging. La scansione di sezione acquisisce un’immagine fissa a una singola profondità. La scansione volumetrica acquisisce 30-40 sezioni consecutive a intervalli di 2 μm. La scansione sequenziale acquisisce fino a 100 fotogrammi video alla stessa profondità, adatta per l’osservazione di cambiamenti dinamici.
L’IVCM richiede apparecchiature specializzate e un operatore esperto, quindi è introdotta principalmente negli ospedali universitari e nelle cliniche oftalmiche specializzate. Non è un esame disponibile in tutti gli studi oftalmici, ma è particolarmente utile per la diagnosi di infezioni corneali e distrofie corneali, e i pazienti vengono indirizzati se necessario.
2. Principali reperti e significato clinico
Sezione intitolata “2. Principali reperti e significato clinico”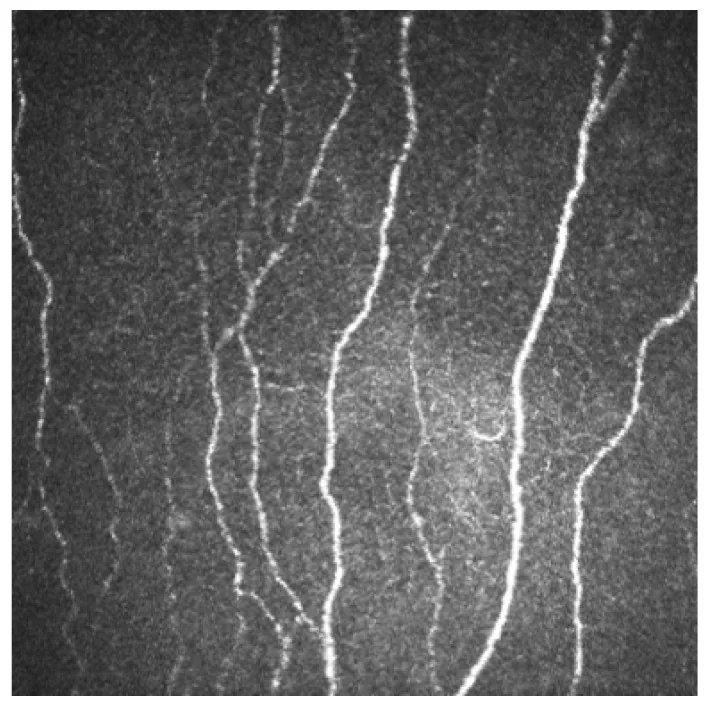
Reperti della cornea normale
Sezione intitolata “Reperti della cornea normale”Con l’IVCM è possibile osservare singolarmente ogni strato della cornea.
Epitelio corneale: Le cellule superficiali sono poligonali e misurano 40–50 μm. Le cellule alari sono di 20–30 μm con confini cellulari luminosi, circa 5.000 cellule/mm². Le cellule basali sono di 8–10 μm con citoplasma scuro e confini luminosi (desmosomi), mostrando un pattern a nido d’ape. La densità delle cellule basali è di 3.600–8.996 cellule/mm².
Membrana di Bowman: Osservata come uno strato amorfo grigio-bianco di circa 10 μm di spessore. I fasci nervosi la attraversano.
Stroma corneale: I cheratociti appaiono scuri nello stato inattivo e luminosi ameboidi nello stato attivato. La densità cellulare è maggiore nello stroma anteriore.
Membrana di Descemet: Riconosciuta come uno strato nebuloso di 6–10 μm di spessore. Le strutture cellulari di solito non sono identificabili.
Endotelio corneale: Cellule esagonali disposte a mosaico. Diametro cellulare circa 20 μm, densità 2.550–2.720 cellule/mm², che diminuisce con l’età di circa lo 0,6% all’anno.
Plesso nervoso subbasale: Osservato come strutture curve a forma di perle appena sotto la membrana di Bowman3). Forma un pattern a vortice (whorl pattern) a circa 1–2 mm in basso e all’interno dal centro della cornea. Il diametro delle fibre è di 0,52–4,6 μm.
Cellule dendritiche (cellule di Langerhans): Distribuite al centro della cornea con 34 ± 3 cellule/mm² e in periferia con 98 ± 8 cellule/mm². Sono un indicatore della risposta immunitaria.
Reperti anomali
Sezione intitolata “Reperti anomali”Infezioni corneali: Nella cheratite fungina, ife filamentose sono chiaramente osservate nello stroma8). Le acanthamoebe vengono rilevate come cisti (sferiche a doppia parete), ma la loro differenziazione dalle cellule infiammatorie richiede esperienza8). I batteri sono difficili da visualizzare direttamente perché i singoli corpi batterici sono troppo piccoli5).
Distrofie corneali: Nella distrofia corneale di Avellino (GCD2) si osservano depositi granulari iperriflettenti nello strato epiteliale basale e aggregati iperriflettenti irregolari nello stroma superficiale e medio1). La distrofia corneale reticolare di tipo I è caratterizzata da depositi reticolari e fibre ramificate1). Nella distrofia corneale maculare si osservano depositi con margini sfumati, e nella distrofia cristallina di Schnyder si osservano cristalli aghiformi1).
Ectasie corneali: Nel cheratocono si osserva una diminuzione della densità dei cheratociti, correlata alla gravità. Si notano anche rotture della membrana di Bowman. L’ectasia corneale dopo PRK è caratterizzata da assenza della membrana di Bowman e riduzione dei cheratociti anteriori, mostrando un pattern IVCM diverso dal cheratocono2).
3. Tecnica e metodo di esame
Sezione intitolata “3. Tecnica e metodo di esame”La procedura di esame IVCM è la seguente.
Preparazione : Somministrare un anestetico topico in gocce (es. ossibuprocaina). Applicare il gel oftalmico sul TomoCap monouso (in PMMA) e montarlo sulla punta dell’obiettivo.
Esecuzione dell’esame : Applanare la cornea monitorando il contatto lente-cornea tramite una telecamera CCD. Regolare manualmente la messa a fuoco e osservare sequenzialmente dallo strato superficiale (0 μm) agli strati profondi. La fissazione è molto importante, la collaborazione del paziente è essenziale. La durata dell’esame è di circa 5–15 minuti.
Complicanze : Raramente possono verificarsi abrasione dell’epitelio corneale o infezione (rischio elevato in caso di difetto epiteliale preesistente).
| Parametro | HRT III-RCM | Confoscan 4 |
|---|---|---|
| Sorgente luminosa | Laser a diodi | Luce alogena |
| Risoluzione in profondità | 4 μm | 25–27 μm |
| Contatto | Necessario (TomoCap) | Opzionale |
Grazie all’anestesia con collirio, il dolore durante l’esame è quasi assente. Si avverte solo un leggero contatto della capsula con la cornea. Dopo l’esame può verificarsi una temporanea sensazione di corpo estraneo, che di solito scompare rapidamente.
4. Principi ottici e caratteristiche dello strumento
Sezione intitolata “4. Principi ottici e caratteristiche dello strumento”Il principio di base del microscopio confocale è la « confocalità » 7). Sia il sistema di illuminazione che quello di rilevamento hanno un’apertura a foro stenopeico, rilevando selettivamente solo la luce riflessa dal piano focale dell’obiettivo. La luce diffusa al di fuori del piano focale viene bloccata dal foro stenopeico, ottenendo così un elevato contrasto e una buona risoluzione di profondità.
Nel tipo a scansione laser (HRT III-RCM), un laser a diodi da 670 nm funge da sorgente puntiforme, scandendo la cornea punto per punto per costruire l’immagine. Lo spessore del piano focale (spessore della sezione ottica) è di circa 4 µm, molto sottile, e fornisce immagini di sezione nitide a livello cellulare.
Nel tipo a scansione a fessura (Confoscan 4), la scansione viene eseguita con un fascio luminoso a forma di fessura, quindi la vera confocalità si ottiene solo nella direzione perpendicolare alla fessura. Di conseguenza, la risoluzione di profondità è di 25-27 µm e la nitidezza dell’immagine è inferiore rispetto al tipo a scansione laser.
I limiti dell’IVCM includono: solo immagini in scala di grigi (nessuna osservazione a colori), impossibilità di risolvere le strutture intracellulari, difficoltà di osservazione in caso di grave opacità corneale, difficoltà nel localizzare con precisione il sito di osservazione e dipendenza dall’abilità dell’operatore.
5. Principali applicazioni cliniche
Sezione intitolata “5. Principali applicazioni cliniche”Le applicazioni cliniche dell’IVCM sono molteplici.
Supporto diagnostico per le infezioni corneali: Utile come complemento all’esame colturale. Può rilevare ife fungine e cisti di Acanthamoeba, ma l’interpretazione dei reperti richiede conoscenze specialistiche 8). Nella cheratite erpetica è possibile cogliere i cambiamenti dei nervi corneali 8). Nell’endotelite corneale da citomegalovirus si possono osservare inclusioni a occhio di gufo.
Diagnosi differenziale delle distrofie corneali: Ogni distrofia presenta reperti IVCM caratteristici, consentendo una differenziazione non invasiva tramite riconoscimento di pattern 1). Molto utile come screening prima dei test genetici o della biopsia. Può essere applicato anche per la valutazione dell’effetto dopo il trattamento (PTK, DALK, ecc.) 1).
Valutazione della deficienza di cellule staminali limbari (LSCD): La scomparsa delle palizzate di Vogt, la sostituzione dell’epitelio corneale con epitelio congiuntivale e la comparsa di cellule caliciformi sono criteri diagnostici 6). La misurazione della densità delle cellule epiteliali basali può quantificare la gravità della LSCD 6).
Valutazione dell’edema corneale e delle malattie endoteliali: L’IVCM consente di osservare le cellule endoteliali anche attraverso un edema corneale moderato, risultando particolarmente utile nei casi in cui la microscopia speculare è difficile 7). Nella distrofia endoteliale di Fuchs (FECD), oltre alla valutazione delle cellule endoteliali, si possono rilevare una diminuzione della densità nervosa e cambiamenti nella densità delle cellule dendritiche 7).
Valutazione dei nervi corneali: La valutazione quantitativa del plesso nervoso subbasale è utilizzata per la diagnosi della cheratopatia neurotrofica e la valutazione dell’efficacia terapeutica3). Dopo la neurotizzazione corneale chirurgica, l’IVCM mostra segni di rigenerazione nervosa tra 6 mesi e 1 anno dopo l’intervento3).
Rilevazione precoce delle malattie autoimmuni sistemiche: Nella sindrome di Sjögren, una ridotta densità delle fibre nervose nella cornea centrale e un aumento delle cellule dendritiche attivate possono essere rilevati prima dell’esordio clinico4). La presenza di almeno 2 cellule dendritiche attivate con 3 o più prolungamenti nella cornea centrale ha una sensibilità del 60% e una specificità del 77% per le malattie autoimmuni sistemiche4).
Valutazione post-operatoria: Utilizzata per monitorare i cambiamenti del bordo del flap, della membrana di Bowman e la rigenerazione nervosa dopo LASIK e PRK2). Ha anche applicazione nella rilevazione precoce del rigetto dopo trapianto di cornea.
6. Ricerche recenti e prospettive future
Sezione intitolata “6. Ricerche recenti e prospettive future”Analisi automatica delle immagini: Sono stati sviluppati sistemi di quantificazione automatica delle fibre nervose subbasali, come il software ACCMetrics2). Calcolano oggettivamente parametri come densità delle fibre nervose, densità di ramificazione e tortuosità, riducendo la variabilità tra gli esaminatori.
Rilevazione dello stadio preclinico delle malattie: Nei casi di sindrome di Sjögren, sono state riportate anomalie all’IVCM diversi anni prima della sieroconversione o della comparsa dei sintomi clinici4). Ciò suggerisce che l’IVCM potrebbe diventare uno strumento di screening per le malattie autoimmuni.
Classificazione dei sottotipi di occhio secco: L’analisi della morfologia e della distribuzione delle cellule dendritiche potrebbe consentire di differenziare l’occhio secco immuno-mediato dall’occhio secco evaporativo4).
Monitoraggio della rigenerazione nervosa post-operatoria: Sono in corso ricerche per seguire nel tempo il processo di rigenerazione nervosa dopo neurotizzazione corneale o cross-linking corneale mediante IVCM3). In futuro, si prevede il suo utilizzo come endpoint oggettivo dell’efficacia terapeutica.
Integrazione dell’intelligenza artificiale: È in corso lo sviluppo di sistemi di classificazione e diagnosi automatica delle immagini IVCM utilizzando l’apprendimento profondo, con applicazioni previste per la diagnosi rapida delle infezioni e la differenziazione automatica delle distrofie corneali.
7. Riferimenti
Sezione intitolata “7. Riferimenti”-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
