
Konfokal Mikroskopi (Canlı Kornea Konfokal Mikroskopisi)
Bir bakışta önemli noktalar
Section titled “Bir bakışta önemli noktalar”1. Konfokal Mikroskopi Nedir?
Section titled “1. Konfokal Mikroskopi Nedir?”Konfokal mikroskopi, aydınlatma ve gözlem ışığının aynı odak düzlemini paylaştığı optik prensibe dayanan yüksek çözünürlüklü bir mikroskopidir. Oftalmolojide korneanın in vivo incelenmesinde kullanılır ve Fuchs endotel distrofisi gibi durumların değerlendirilmesinde de yer alır 7).
Klinikte kullanılan başlıca cihazlar iki tiptir:
Lazer taramalı tip (HRT III-RCM): Heidelberg Engineering tarafından üretilmiştir. Işık kaynağı olarak 670 nm diyot lazer kullanır, objektif lens 63x, görüş alanı 400×400 μm’dir. Yanal çözünürlük 1-2 μm, derinlik çözünürlüğü yaklaşık 4 μm’dir 1)2). PMMA tek kullanımlık kapak (TomoCap) ve oftalmik jel aracılığıyla korneaya temas ettirilerek kullanılır.
Yarık taramalı tip (Confoscan 4): Nidek tarafından üretilmiştir. Halojen ışık kaynağı kullanır ve temassız olarak da kullanılabilir. Otomatik tarama özelliği ile kullanımı nispeten kolaydır, ancak derinlik çözünürlüğü 25-27 μm ile sınırlıdır. Günümüzde üretimi durdurulmuştur.
IVCM üç görüntüleme moduna sahiptir. Kesit tarama tek bir derinlikte sabit görüntü alır. Hacim tarama 2 μm aralıklarla 30-40 ardışık kesit alır. Dizi tarama aynı derinlikte 100 kareye kadar video alır ve dinamik değişikliklerin gözlemlenmesi için uygundur.
IVCM, özel cihaz ve deneyimli bir operatör gerektirdiğinden, çoğunlukla üniversite hastaneleri ve uzman göz merkezlerinde bulunur. Her göz kliniğinde yapılamaz, ancak kornea enfeksiyonları ve kornea distrofilerinin tanısında özellikle yararlıdır ve gerektiğinde sevk edilir.
2. Başlıca Bulgular ve Klinik Önemi
Section titled “2. Başlıca Bulgular ve Klinik Önemi”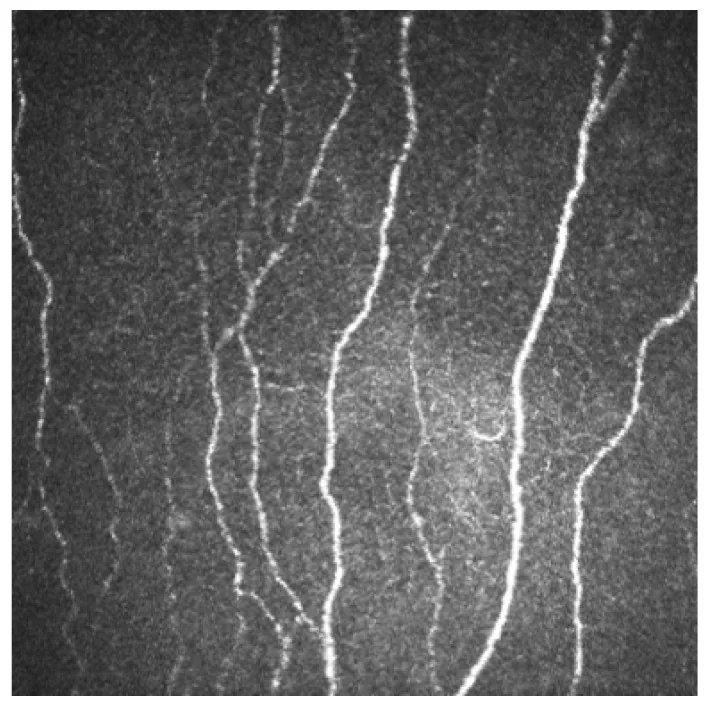
Normal Kornea Bulguları
Section titled “Normal Kornea Bulguları”IVCM ile korneanın her katmanı ayrı ayrı gözlemlenebilir.
Kornea Epiteli: Yüzey hücreleri poligonal, 40-50 μm. Kanat hücreleri 20-30 μm, parlak hücre sınırlarına sahip ve yaklaşık 5.000 hücre/mm². Bazal hücreler 8-10 μm, koyu sitoplazma ve parlak sınırlar (desmozom) gösterir, petek deseni oluşturur. Bazal hücre yoğunluğu 3.600-8.996 hücre/mm²’dir.
Bowman Membranı: Yaklaşık 10 μm kalınlığında, yapısız grimsi-beyaz bir tabaka olarak gözlenir. Sinir demetleri geçer.
Kornea Stroması: Keratositler inaktif durumda koyu, aktif durumda parlak ameboid olarak gözlenir. Ön stromada hücre yoğunluğu daha yüksektir.
Descemet Membranı: 6-10 μm kalınlığında puslu bir tabaka olarak görülür. Hücresel yapı genellikle ayırt edilemez.
Kornea Endoteli: Altıgen hücreler mozaik şeklinde dizilir. Hücre çapı yaklaşık 20 μm, yoğunluk 2.550-2.720 hücre/mm² ve yaşla birlikte yılda yaklaşık %0,6 azalır.
Subbazal Sinir Pleksusu: Bowman membranının hemen altında boncuklu kıvrımlı yapılar olarak gözlenir3). Kornea merkezinin yaklaşık 1-2 mm alt-nazalinde bir girdap deseni (whorl pattern) oluşturur. Lif çapı 0,52-4,6 μm’dir.
Dendritik Hücreler (Langerhans Hücreleri): Kornea merkezinde 34 ± 3 hücre/mm², periferde 98 ± 8 hücre/mm² dağılım gösterir. İmmün yanıtın göstergesidir.
Anormal Bulgular
Section titled “Anormal Bulgular”Kornea Enfeksiyonları: Fungal keratitte stromada filamentöz hifler net olarak gözlenir8). Acanthamoeba, kist (çift duvarlı küresel yapı) olarak saptanır, ancak inflamatuar hücrelerden ayırt edilmesi deneyim gerektirir8). Bakteriler, tek tek bakteri gövdeleri çok küçük olduğu için doğrudan görüntülenemez5).
Kornea Distrofileri: Avellino kornea distrofisinde (GCD2) bazal epitel tabakasında yüksek parlaklıkta granüler birikintiler, yüzeyel-orta stromada düzensiz yüksek parlaklıkta kümeler görülür1). Lattice kornea distrofisi tip I’de ağsı birikintiler ve dallanan lifler karakteristiktir1). Maküler kornea distrofisinde sınırları belirsiz birikintiler görülür, Schnyder kristalin kornea distrofisinde iğne şeklinde kristaller gözlenir1).
Kornea Ektazisi: Keratokonusta keratosit yoğunluğunda azalma görülür ve şiddetle ilişkilidir. Bowman membranında yırtılmalar da izlenir. PRK sonrası kornea ektazisinde Bowman membran defekti ve ön keratositlerde azalma karakteristiktir ve keratokonustan farklı bir IVCM paterni gösterir2).
3. Muayene Tekniği ve Yöntemi
Section titled “3. Muayene Tekniği ve Yöntemi”IVCM muayene prosedürü aşağıdaki gibidir.
Hazırlık: Topikal anestezi (oksibuprokain gibi) uygulanır. Tek kullanımlık TomoCap’e (PMMA) oftalmik jel sürülür ve objektif lensin ucuna takılır.
Muayene: CCD kamera ile lens-kornea teması izlenirken kornea aplane edilir. Odak manuel olarak ayarlanır ve korneanın yüzeyel tabakasından (0 μm) derin tabakalara doğru sırayla incelenir. Fiksasyon çok önemlidir ve hastanın işbirliği gereklidir. Muayene süresi yaklaşık 5-15 dakikadır.
Komplikasyonlar: Nadiren kornea epitel sıyrığı veya enfeksiyon (önceden epitel defekti varsa risk yüksektir) görülebilir.
| Özellik | HRT III-RCM | Confoscan 4 |
|---|---|---|
| Işık kaynağı | Diyot lazer | Halojen ışık |
| Derinlik çözünürlüğü | 4 μm | 25-27 μm |
| Temas | Gerekli (TomoCap) | İsteğe bağlı |
Damla anestezisi uygulandığı için muayene sırasında neredeyse hiç ağrı olmaz. Sadece kapağın korneaya hafifçe temas ettiği hissi vardır. Muayene sonrası geçici bir yabancı cisim hissi oluşabilir ancak genellikle hızla kaybolur.
4. Optik prensipler ve cihaz özellikleri
Section titled “4. Optik prensipler ve cihaz özellikleri”Konfokal mikroskobun temel prensibi «konfokalite (confocality)» dir7). Hem aydınlatma sistemi hem de algılama sistemi birer iğne deliği açıklığına sahiptir ve objektif merceğin odak düzleminden gelen yansıyan ışığı seçici olarak algılar. Odak düzlemi dışındaki saçılan ışık iğne deliği tarafından engellendiği için yüksek kontrast ve derinlik çözünürlüğü elde edilir.
Lazer taramalı tipte (HRT III-RCM), 670 nm diyot lazer noktasal ışık kaynağı olarak işlev görür ve korneayı nokta nokta tarayarak görüntü oluşturur. Odak düzlemi kalınlığı (optik kesit kalınlığı) yaklaşık 4 μm gibi çok incedir ve hücresel düzeyde net kesit görüntüleri sağlar.
Yarık taramalı tipte (Confoscan 4) tarama yarık şeklindeki bir ışınla yapıldığından, gerçek konfokalite yalnızca yarığa dik yönde elde edilir. Bu nedenle derinlik çözünürlüğü 25-27 μm olup, lazer taramalı tipe göre görüntü keskinliği daha düşüktür.
IVCM’nin sınırlamaları arasında: yalnızca gri tonlamalı görüntüler (renkli gözlem mümkün değil), hücre içi yapıların ayırt edilememesi, ileri kornea bulanıklığı olgularında gözlem zorluğu, gözlem bölgesinin tam olarak belirlenmesindeki güçlük ve operatör becerisine bağımlılık sayılabilir.
5. Başlıca klinik uygulamalar
Section titled “5. Başlıca klinik uygulamalar”IVCM’nin klinik uygulamaları çeşitlidir.
Kornea enfeksiyonlarının tanısına yardım: Kültür testlerine yardımcı olarak faydalıdır. Mantar hifleri ve Acanthamoeba kistleri tespit edilebilir, ancak bulguların yorumlanması uzmanlık bilgisi gerektirir8). Herpetik keratitte kornea sinirlerindeki değişiklikler yakalanabilir8). Sitomegalovirüs kornea endotelitinde baykuş gözü inklüzyon cisimcikleri görülebilir.
Kornea distrofilerinin ayırıcı tanısı: Her distrofinin karakteristik IVCM bulguları vardır ve patern tanıma yoluyla non-invaziv ayırıcı tanı mümkündür1). Genetik test veya biyopsi öncesi tarama olarak oldukça faydalıdır. Tedavi (PTK, DALK vb.) sonrası etkinlik değerlendirmesinde de kullanılabilir1).
Limbus kök hücre yetmezliği (LSCD) değerlendirmesi: Vogt palizad yapılarının kaybı, kornea epitelinin konjonktiva epiteli ile yer değiştirmesi ve goblet hücrelerinin ortaya çıkması tanı kriterleridir6). Bazal epitel hücre yoğunluğunun ölçümü ile LSCD şiddeti kantitatif olarak değerlendirilebilir6).
Kornea ödemi ve endotel hastalıklarının değerlendirmesi: IVCM, orta dereceli kornea ödemi aracılığıyla bile endotel hücrelerini gözlemleyebildiğinden, speküler mikroskobinin zor olduğu olgularda özellikle faydalıdır7). Fuchs endotel distrofisinde (FECD), endotel hücre değerlendirmesine ek olarak sinir yoğunluğunda azalma ve dendritik hücre yoğunluğunda değişiklikler de tespit edilebilir7).
Kornea sinirinin değerlendirilmesi: Subbazal sinir pleksusunun kantitatif değerlendirmesi, nörotrofik keratopatinin tanısı ve tedavi etkinliğinin belirlenmesinde kullanılır3). Cerrahi kornea nörotizasyonu sonrası sinir rejenerasyonunun değerlendirilmesinde, IVCM ile postoperatif 6 ay-1 yıl içinde rejenerasyon bulguları tespit edilir3).
Sistemik otoimmün hastalıkların erken tespiti: Sjögren sendromunda, santral korneada sinir lifi yoğunluğunda azalma ve aktif dendritik hücrelerde artış, klinik başlangıçtan önce tespit edilebilir4). Santral korneada üç veya daha fazla uzantıya sahip iki veya daha fazla aktif dendritik hücre varlığı, sistemik immün hastalıklar için %60 duyarlılık ve %77 özgüllük ile rapor edilmiştir4).
Postoperatif değerlendirme: LASIK, PRK sonrası flep kenarı ve Bowman membranındaki değişikliklerin yanı sıra sinir rejenerasyonunun takibinde kullanılır2). Kornea nakli sonrası rejeksiyonun erken tespitinde de uygulama alanı vardır.
6. Güncel Araştırmalar ve Gelecek Perspektifler
Section titled “6. Güncel Araştırmalar ve Gelecek Perspektifler”Otomatik görüntü analizi: ACCMetrics yazılımı gibi subbazal sinir liflerinin otomatik kantitatif sistemleri geliştirilmiştir2). Sinir lifi yoğunluğu, dallanma yoğunluğu ve kıvrımlılık gibi parametreler objektif olarak hesaplanarak değerlendiriciler arası değişkenlik azaltılır.
Hastalığın preklinik evresinin tespiti: Sjögren sendromu vakalarında, antikor pozitifliği veya klinik semptomların ortaya çıkmasından birkaç yıl önce IVCM anormalliklerinin tespit edildiği bildirilmiştir4). IVCM’nin otoimmün hastalıklar için bir tarama aracı olabileceği öne sürülmektedir.
Kuru göz alt tiplerinin sınıflandırılması: Dendritik hücre morfolojisi ve dağılım paternlerinin analizi ile immün aracılı kuru göz ile evaporatif kuru gözün ayırt edilebilmesi mümkün olabilir4).
Postoperatif sinir rejenerasyonunun izlenmesi: Kornea sinir transplantasyonu ve kornea çapraz bağlama sonrası sinir rejenerasyon sürecinin IVCM ile zaman içinde takip edildiği çalışmalar devam etmektedir3). Gelecekte tedavi etkinliği için objektif bir son nokta olarak kullanılması beklenmektedir.
Yapay zeka entegrasyonu: Derin öğrenme kullanılarak IVCM görüntülerinin otomatik sınıflandırma ve otomatik tanı sistemlerinin geliştirilmesi devam etmekte olup, enfeksiyonların hızlı tanısı ve kornea distrofilerinin otomatik ayırıcı tanısında uygulanması beklenmektedir.
7. Kaynaklar
Section titled “7. Kaynaklar”-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
