
Konfokalmikroskop (In-vivo-Konfokalmikroskop der Hornhaut)
Auf einen Blick: Wichtige Punkte
Abschnitt betitelt „Auf einen Blick: Wichtige Punkte“1. Was ist Konfokalmikroskopie?
Abschnitt betitelt „1. Was ist Konfokalmikroskopie?“Die Konfokalmikroskopie ist ein hochauflösendes Mikroskop, das auf dem optischen Prinzip basiert, dass Beleuchtungslicht und Beobachtungslicht dieselbe Fokusebene teilen. Im ophthalmologischen Bereich wird sie zur In-vivo-Beobachtung der Hornhaut eingesetzt und auch zur Beurteilung der Fuchs-Endotheldystrophie verwendet7).
Die derzeit klinisch verwendeten Hauptgeräte sind die folgenden zwei Systeme.
Laserscanning-Typ (HRT III-RCM) : Hergestellt von Heidelberg Engineering. Verwendet einen 670-nm-Diodenlaser als Lichtquelle, Objektiv 63x, Sichtfeld 400×400 μm. Es bietet eine laterale Auflösung von 1–2 μm und eine Tiefenauflösung von etwa 4 μm1)2). Es wird über eine PMMA-Einwegkappe (TomoCap) und Augengel in Kontakt mit der Hornhaut verwendet.
Spaltscan-Typ (Confoscan 4) : Hergestellt von Nidek. Verwendet eine Halogenlichtquelle und kann auch kontaktlos verwendet werden. Es verfügt über eine automatische Scanfunktion und ist relativ einfach zu bedienen, aber die Tiefenauflösung beträgt nur 25–27 μm. Die Produktion wurde inzwischen eingestellt.
Das IVCM verfügt über drei Aufnahmemodi. Der Sektionsscan erfasst ein Standbild in einer einzigen Tiefe. Der Volumenscan erfasst 30–40 aufeinanderfolgende Schnitte im Abstand von 2 μm. Der Sequenzscan erfasst bis zu 100 Videobilder in derselben Tiefe und eignet sich zur Beobachtung dynamischer Veränderungen.
Die IVCM erfordert spezielle Geräte und einen erfahrenen Untersucher, daher wird sie hauptsächlich in Universitätskliniken und spezialisierten Augenkliniken eingesetzt. Sie ist nicht in jeder augenärztlichen Praxis verfügbar, aber besonders nützlich für die Diagnose von Hornhautinfektionen und Hornhautdystrophien, und Patienten werden bei Bedarf überwiesen.
2. Wichtige Befunde und klinische Bedeutung
Abschnitt betitelt „2. Wichtige Befunde und klinische Bedeutung“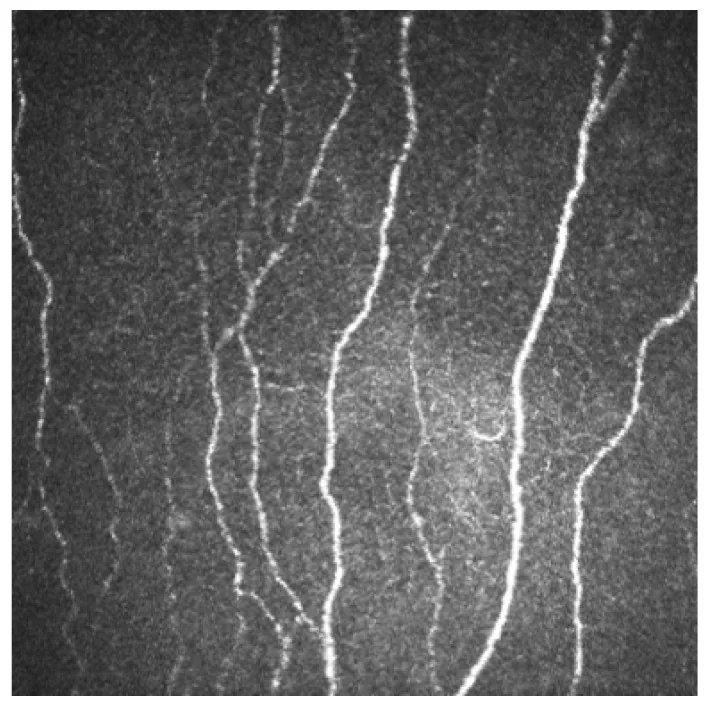
Befunde der normalen Hornhaut
Abschnitt betitelt „Befunde der normalen Hornhaut“Mit der IVCM können die einzelnen Schichten der Hornhaut getrennt beobachtet werden.
Hornhautepithel: Oberflächliche Zellen sind polygonal und 40–50 μm groß. Flügelzellen sind 20–30 μm groß mit hellen Zellgrenzen, etwa 5.000 Zellen/mm². Basalzellen sind 8–10 μm groß, haben ein dunkles Zytoplasma und helle Grenzen (Desmosomen) und zeigen ein wabenartiges Muster. Die Basalzelldichte beträgt 3.600–8.996 Zellen/mm².
Bowman-Membran: Wird als etwa 10 μm dicke, strukturlose grau-weiße Schicht beobachtet. Nervenbündel verlaufen durch sie.
Hornhautstroma: Hornhautstromazellen (Keratinozyten) erscheinen im inaktiven Zustand dunkel und im aktivierten Zustand hell amöboid. Im vorderen Stroma ist die Zelldichte höher.
Descemet-Membran: Wird als 6–10 μm dicke, neblige Schicht erkannt. Zellstrukturen sind normalerweise nicht erkennbar.
Hornhautendothel: Sechseckige Zellen in mosaikartiger Anordnung. Zelldurchmesser etwa 20 μm, Dichte 2.550–2.720 Zellen/mm², die mit dem Alter um etwa 0,6 % pro Jahr abnimmt.
Subbasaler Nervenplexus: Wird als perlenartige, geschwungene Struktur direkt unter der Bowman-Membran beobachtet3). Er bildet etwa 1–2 mm nasal inferior des Hornhautzentrums ein wirbelartiges Muster (Whorl-Muster). Der Faserdurchmesser beträgt 0,52–4,6 μm.
Dendritische Zellen (Langerhans-Zellen): Im Hornhautzentrum 34 ± 3 Zellen/mm², in der Peripherie 98 ± 8 Zellen/mm². Sie sind ein Indikator für die Immunantwort.
Abnorme Befunde
Abschnitt betitelt „Abnorme Befunde“Hornhautinfektionen: Bei Pilzkeratitis werden filamentöse Hyphen im Stroma deutlich beobachtet8). Acanthamöben werden als Zysten (kugelförmig mit Doppelwand) nachgewiesen, ihre Unterscheidung von Entzündungszellen erfordert jedoch Erfahrung8). Bakterien sind aufgrund ihrer geringen Größe direkt schwer sichtbar5).
Hornhautdystrophien: Bei der Avellino-Hornhautdystrophie (GCD2) zeigen sich hochreflektive granuläre Ablagerungen in der basalen Epithelschicht und unregelmäßige hochreflektive Cluster im oberflächlichen bis mittleren Stroma1). Die gittrige Hornhautdystrophie Typ I ist durch netzartige Ablagerungen und verzweigte Fasern gekennzeichnet1). Bei der makulären Hornhautdystrophie finden sich unscharf begrenzte Ablagerungen, bei der Schnyder-kristallinen Hornhautdystrophie nadelartige Kristalle1).
Hornhautektasien: Beim Keratokonus zeigt sich eine verminderte Keratinozytendichte, die mit dem Schweregrad korreliert. Auch Bowman-Membran-Risse sind zu sehen. Die Hornhautektasie nach PRK ist durch das Fehlen der Bowman-Membran und eine verminderte Anzahl vorderer Keratinozyten gekennzeichnet und zeigt ein vom Keratokonus unterschiedliches IVCM-Muster2).
3. Untersuchungstechnik und Methode
Abschnitt betitelt „3. Untersuchungstechnik und Methode“Das IVCM-Untersuchungsverfahren ist wie folgt.
Vorbereitung : Tropfanästhesie (z. B. Oxybuprocain) durchführen. Ophthalmologisches Gel auf die Einweg-TomoCap (aus PMMA) auftragen und auf die Spitze des Objektivs aufsetzen.
Durchführung der Untersuchung : Die Hornhaut applanationieren, während der Kontakt zwischen Linse und Hornhaut über eine CCD-Kamera überwacht wird. Manuell fokussieren und nacheinander von der oberflächlichen Schicht (0 μm) bis in die tiefen Schichten beobachten. Die Fixation ist sehr wichtig, die Mitarbeit des Patienten ist unerlässlich. Die Untersuchungsdauer beträgt etwa 5–15 Minuten.
Komplikationen : Selten können Hornhautepithelabschürfungen oder Infektionen (bei bestehenden Epitheldefekten hohes Risiko) auftreten.
| Parameter | HRT III-RCM | Confoscan 4 |
|---|---|---|
| Lichtquelle | Diodenlaser | Halogenlicht |
| Tiefenauflösung | 4 μm | 25–27 μm |
| Kontakt | Erforderlich (TomoCap) | Optional |
Durch die Anästhesie-Augentropfen ist der Schmerz während der Untersuchung nahezu nicht vorhanden. Man spürt lediglich ein leichtes Berühren der Kappe auf der Hornhaut. Nach der Untersuchung kann ein vorübergehendes Fremdkörpergefühl auftreten, das jedoch in der Regel schnell abklingt.
4. Optische Prinzipien und Gerätemerkmale
Abschnitt betitelt „4. Optische Prinzipien und Gerätemerkmale“Das Grundprinzip des Konfokalmikroskops ist die „Konfokalität“ 7). Sowohl das Beleuchtungs- als auch das Detektionssystem verfügen über eine Lochblende, die nur das vom Fokusebene des Objektivs reflektierte Licht selektiv detektiert. Streulicht von außerhalb der Fokusebene wird durch die Lochblende blockiert, wodurch ein hoher Kontrast und eine hohe Tiefenauflösung erreicht werden.
Beim Laserscanning-Typ (HRT III-RCM) fungiert ein 670-nm-Diodenlaser als Punktlichtquelle, der die Hornhaut Punkt für Punkt abtastet und ein Bild aufbaut. Die Dicke der Fokusebene (optische Schnittdicke) beträgt etwa 4 µm, was sehr dünn ist und klare Querschnittsbilder auf zellulärer Ebene liefert.
Beim Schlitzscan-Typ (Confoscan 4) wird mit einem schlitzförmigen Lichtstrahl gescannt, sodass echte Konfokalität nur in der Richtung senkrecht zum Schlitz erreicht wird. Daher beträgt die Tiefenauflösung 25–27 µm, und die Bildschärfe ist geringer als beim Laserscanning-Typ.
Zu den Grenzen der IVCM gehören: nur Graustufenbilder (keine Farbbeobachtung), Unfähigkeit, intrazelluläre Strukturen aufzulösen, Schwierigkeiten bei starker Hornhauttrübung, Schwierigkeiten bei der genauen Lokalisierung der Beobachtungsstelle und Abhängigkeit von der Geschicklichkeit des Untersuchers.
5. Hauptanwendungen in der Klinik
Abschnitt betitelt „5. Hauptanwendungen in der Klinik“Die klinischen Anwendungen der IVCM sind vielfältig.
Diagnosehilfe bei Hornhautinfektionen: Nützlich als Ergänzung zur Kulturuntersuchung. Pilzhyphen und Acanthamoeba-Zysten können nachgewiesen werden, aber die Interpretation der Befunde erfordert Fachwissen 8). Bei Herpeskeratitis können Veränderungen der Hornhautnerven erfasst werden 8). Bei Zytomegalievirus-Hornhautendothelitis können Eulenaugeneinschlusskörperchen beobachtet werden.
Differenzialdiagnose von Hornhautdystrophien: Jede Dystrophie weist charakteristische IVCM-Befunde auf, die eine nicht-invasive Unterscheidung durch Mustererkennung ermöglichen 1). Als Screening vor Gentests oder Biopsie sehr nützlich. Auch zur Beurteilung des Behandlungserfolgs (PTK, DALK usw.) anwendbar 1).
Beurteilung des Limbusstammzellmangels (LSCD): Das Verschwinden der Vogt-Palisaden, die Ersetzung des Hornhautepithels durch Bindehautepithel und das Auftreten von Becherzellen sind diagnostische Kriterien 6). Die Messung der Dichte der basalen Epithelzellen ermöglicht eine quantitative Beurteilung des Schweregrads der LSCD 6).
Beurteilung von Hornhautödem und Endothelerkrankungen: Die IVCM kann Endothelzellen auch durch ein mäßiges Hornhautödem hindurch beobachten, was besonders bei Fällen nützlich ist, in denen die Spiegelmikroskopie schwierig ist 7). Bei der Fuchs-Endotheldystrophie (FECD) können neben der Beurteilung der Endothelzellen auch eine verminderte Nervendichte und Veränderungen der dendritischen Zelldichte erfasst werden 7).
Beurteilung der Hornhautnerven: Die quantitative Beurteilung des subbasalen Nervenplexus wird zur Diagnose der neurotrophen Keratopathie und zur Beurteilung des Therapieerfolgs eingesetzt3). Nach einer chirurgischen Hornhautneurotisation zeigt die IVCM 6 Monate bis 1 Jahr postoperativ Regenerationsbefunde3).
Früherkennung systemischer Autoimmunerkrankungen: Beim Sjögren-Syndrom können eine verminderte Nervenfaserdichte im zentralen Hornhautbereich und eine Zunahme aktivierter dendritischer Zellen vor dem klinischen Ausbruch nachgewiesen werden4). Das Vorhandensein von mindestens 2 aktivierten dendritischen Zellen mit 3 oder mehr Fortsätzen in der zentralen Hornhaut wird mit einer Sensitivität von 60% und einer Spezifität von 77% für systemische Autoimmunerkrankungen angegeben4).
Postoperative Beurteilung: Wird zur Überwachung von Veränderungen des Flap-Randes, der Bowman-Membran und der Nervenregeneration nach LASIK und PRK verwendet2). Auch zur Früherkennung von Abstoßungsreaktionen nach Hornhauttransplantation geeignet.
6. Aktuelle Forschung und Zukunftsperspektiven
Abschnitt betitelt „6. Aktuelle Forschung und Zukunftsperspektiven“Automatische Bildanalyse: Es wurden automatische Quantifizierungssysteme für subbasale Nervenfasern entwickelt, wie die ACCMetrics-Software2). Sie berechnen objektiv Parameter wie Nervenfaserdichte, Verzweigungsdichte und Tortuosität und reduzieren so die Inter-Untersucher-Variabilität.
Erkennung präklinischer Krankheitsstadien: Bei Sjögren-Syndrom-Fällen wurden IVCM-Anomalien mehrere Jahre vor der Antikörper-Positivität oder dem Auftreten klinischer Symptome berichtet4). Dies deutet darauf hin, dass die IVCM ein Screening-Instrument für Autoimmunerkrankungen werden könnte.
Subtyp-Klassifikation des trockenen Auges: Durch die Analyse der Morphologie und Verteilungsmuster dendritischer Zellen könnte eine Unterscheidung zwischen immunvermitteltem trockenem Auge und verdunstungsbedingtem trockenem Auge möglich sein4).
Überwachung der postoperativen Nervenregeneration: Es laufen Studien, die den Nervenregenerationsprozess nach Hornhautneurotisation oder Hornhautcrosslinking mittels IVCM im Zeitverlauf verfolgen3). Zukünftig wird ein Einsatz als objektiver Endpunkt für die Therapiewirksamkeit erwartet.
Integration künstlicher Intelligenz: Die Entwicklung automatischer Klassifikations- und Diagnosesysteme für IVCM-Bilder mittels Deep Learning schreitet voran, mit erwarteten Anwendungen in der schnellen Diagnose von Infektionen und der automatischen Differenzierung von Hornhautdystrophien.
7. Referenzen
Abschnitt betitelt „7. Referenzen“-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
