
Microscope confocal (microscope confocal cornéen in vivo)
Points clés en un coup d’œil
Section intitulée « Points clés en un coup d’œil »1. Qu’est-ce que la microscopie confocale ?
Section intitulée « 1. Qu’est-ce que la microscopie confocale ? »La microscopie confocale est un microscope à haute résolution basé sur le principe optique selon lequel la lumière d’éclairage et la lumière d’observation partagent le même plan focal. Dans le domaine ophtalmique, elle est appliquée à l’observation in vivo de la cornée et est également utilisée pour l’évaluation de la dystrophie endothéliale de Fuchs7).
Les principaux appareils actuellement utilisés en clinique sont les deux suivants.
Type à balayage laser (HRT III-RCM) : Fabriqué par Heidelberg Engineering. Utilise un laser diode de 670 nm comme source lumineuse, avec un objectif 63x et un champ d’observation de 400×400 μm. Il offre une résolution latérale de 1 à 2 μm et une résolution en profondeur d’environ 4 μm1)2). Il est utilisé en contact avec la cornée via un capuchon jetable en PMMA (TomoCap) et un gel ophtalmique.
Type à balayage de fente (Confoscan 4) : Fabriqué par Nidek. Utilise une source lumineuse halogène et peut être utilisé sans contact. Il dispose d’une fonction de balayage automatique et est relativement facile à manipuler, mais sa résolution en profondeur est limitée à 25-27 μm. Sa production est actuellement arrêtée.
L’IVCM dispose de trois modes d’imagerie. Le balayage de section acquiert une image fixe à une seule profondeur. Le balayage volumique acquiert 30 à 40 coupes consécutives à intervalles de 2 μm. Le balayage séquentiel acquiert jusqu’à 100 images animées à la même profondeur, adapté à l’observation des changements dynamiques.
L’IVCM nécessite un équipement spécialisé et un opérateur expérimenté, elle est donc principalement introduite dans les hôpitaux universitaires et les cliniques ophtalmologiques spécialisées. Ce n’est pas un examen disponible dans tous les cabinets d’ophtalmologie, mais il est particulièrement utile pour le diagnostic des infections cornéennes et des dystrophies cornéennes, et les patients sont référés si nécessaire.
2. Principales observations et signification clinique
Section intitulée « 2. Principales observations et signification clinique »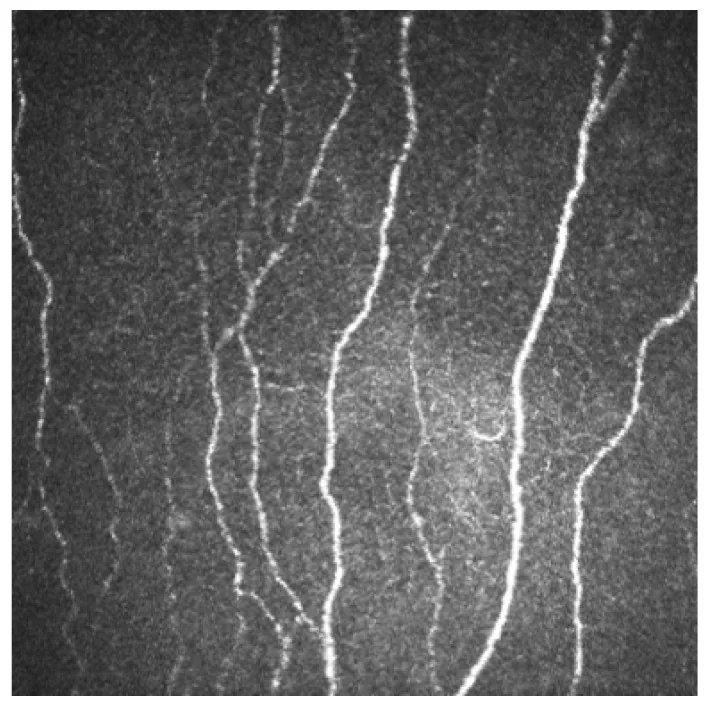
Aspects de la cornée normale
Section intitulée « Aspects de la cornée normale »L’IVCM permet d’observer chaque couche de la cornée individuellement.
Épithélium cornéen : Les cellules superficielles sont polygonales, de 40 à 50 μm. Les cellules alaires mesurent 20 à 30 μm avec des limites cellulaires brillantes, environ 5 000 cellules/mm². Les cellules basales mesurent 8 à 10 μm, présentent un cytoplasme sombre et des limites brillantes (desmosomes), et forment un motif en nid d’abeille. La densité des cellules basales est de 3 600 à 8 996 cellules/mm².
Membrane de Bowman : Observée comme une couche amorphe gris-blanc d’environ 10 μm d’épaisseur. Des faisceaux nerveux la traversent.
Stroma cornéen : Les kératocytes sont sombres à l’état inactif et apparaissent comme des amibes brillantes à l’état activé. La densité cellulaire est plus élevée dans le stroma antérieur.
Membrane de Descemet : Observée comme une couche brumeuse de 6 à 10 μm d’épaisseur. Les structures cellulaires ne sont généralement pas identifiables.
Endothélium cornéen : Cellules hexagonales disposées en mosaïque. Diamètre cellulaire d’environ 20 μm, densité de 2 550 à 2 720 cellules/mm², diminuant d’environ 0,6 % par an avec l’âge.
Plexus nerveux sous-basal : Observé comme des structures courbes en forme de perles juste sous la membrane de Bowman3). Il forme un motif en spirale (whorl pattern) à environ 1 à 2 mm en bas et en dedans du centre de la cornée. Le diamètre des fibres est de 0,52 à 4,6 μm.
Cellules dendritiques (cellules de Langerhans) : Distribuées à 34 ± 3 cellules/mm² au centre de la cornée et 98 ± 8 cellules/mm² en périphérie. Elles sont un indicateur de la réponse immunitaire.
Aspects anormaux
Section intitulée « Aspects anormaux »Infections cornéennes : Dans la kératite fongique, des filaments d’hyphes sont clairement observés dans le stroma8). Les acanthamibes sont détectées sous forme de kystes (sphériques à double paroi), mais leur différenciation des cellules inflammatoires nécessite de l’expérience8). Les bactéries sont difficiles à visualiser directement car les corps bactériens individuels sont trop petits5).
Dystrophies cornéennes : Dans la dystrophie cornéenne d’Avellino (GCD2), on observe des dépôts granulaires hyperréflectifs dans la couche épithéliale basale et des amas hyperréflectifs irréguliers dans le stroma superficiel à moyen1). La dystrophie cornéenne grillagée de type I se caractérise par des dépôts réticulaires et des fibres ramifiées1). Dans la dystrophie cornéenne maculaire, on observe des dépôts aux limites floues, et dans la dystrophie cristalline de Schnyder, des cristaux en forme d’aiguilles1).
Ectasies cornéennes : Dans le kératocône, on observe une diminution de la densité des kératocytes, corrélée à la sévérité. On note également des ruptures de la membrane de Bowman. L’ectasie cornéenne après PRK se caractérise par une absence de membrane de Bowman et une diminution des kératocytes antérieurs, montrant un motif IVCM différent de celui du kératocône2).
3. Technique et méthode d’examen
Section intitulée « 3. Technique et méthode d’examen »La procédure d’examen IVCM est la suivante.
Prétraitement : Instillation d’un anesthésique topique (par exemple, oxybuprocaïne). Appliquer un gel ophtalmique sur le TomoCap jetable (en PMMA) et le fixer à l’extrémité de l’objectif.
Réalisation de l’examen : Aplanir la cornée tout en surveillant le contact entre la lentille et la cornée via une caméra CCD. Ajuster manuellement la mise au point et observer séquentiellement de la couche superficielle (0 μm) aux couches profondes. La fixation est très importante, la coopération du patient est essentielle. La durée de l’examen est d’environ 5 à 15 minutes.
Complications : Rarement, une abrasion de l’épithélium cornéen ou une infection (risque élevé en cas de perte épithéliale préexistante) peut survenir.
| Paramètre | HRT III-RCM | Confoscan 4 |
|---|---|---|
| Source lumineuse | Laser à diode | Lumière halogène |
| Résolution axiale | 4 μm | 25–27 μm |
| Contact | Nécessaire (TomoCap) | Optionnel |
Grâce à l’anesthésie par gouttes, la douleur pendant l’examen est presque inexistante. On ressent seulement un léger contact de la capsule sur la cornée. Une sensation de corps étranger temporaire peut survenir après l’examen, mais elle disparaît généralement rapidement.
4. Principes optiques et caractéristiques de l’appareil
Section intitulée « 4. Principes optiques et caractéristiques de l’appareil »Le principe de base du microscope confocal est la « confocalité » 7). Les systèmes d’éclairage et de détection possèdent tous deux une ouverture à trou d’épingle, ne détectant sélectivement que la lumière réfléchie par le plan focal de l’objectif. La lumière diffusée hors du plan focal est bloquée par le trou d’épingle, offrant ainsi un contraste et une résolution en profondeur élevés.
Dans le type à balayage laser (HRT III-RCM), un laser à diode de 670 nm sert de source ponctuelle, balayant la cornée point par point pour construire l’image. L’épaisseur du plan focal (épaisseur de coupe optique) est d’environ 4 µm, très fine, fournissant des images de coupe nettes au niveau cellulaire.
Dans le type à balayage par fente (Confoscan 4), le balayage est effectué par un faisceau lumineux en forme de fente, de sorte que la véritable confocalité n’est obtenue que dans la direction perpendiculaire à la fente. Par conséquent, la résolution en profondeur est de 25 à 27 µm, et la netteté de l’image est inférieure à celle du type à balayage laser.
Les limites de l’IVCM incluent : images en niveaux de gris uniquement (pas d’observation en couleur), incapacité à résoudre les structures intracellulaires, difficulté d’observation en cas d’opacité cornéenne sévère, difficulté à localiser précisément le site d’observation, et dépendance à l’habileté de l’opérateur.
5. Principales applications cliniques
Section intitulée « 5. Principales applications cliniques »Les applications cliniques de l’IVCM sont variées.
Aide au diagnostic des infections cornéennes : Utile en complément des cultures. Permet de détecter les filaments fongiques et les kystes d’Acanthamoeba, mais l’interprétation nécessite une expertise spécialisée 8). Dans la kératite herpétique, les modifications des nerfs cornéens peuvent être observées 8). Dans l’endothélite cornéenne à cytomégalovirus, des inclusions en œil de hibou peuvent être présentes.
Diagnostic différentiel des dystrophies cornéennes : Chaque dystrophie présente des signes IVCM caractéristiques, permettant une différenciation non invasive par reconnaissance de motifs 1). Utile comme dépistage avant les tests génétiques ou la biopsie. Peut également être appliqué pour l’évaluation post-traitement (PTK, DALK, etc.) 1).
Évaluation de la déficience en cellules souches limbiques (LSCD) : La disparition des palissades de Vogt, le remplacement de l’épithélium cornéen par l’épithélium conjonctival et l’apparition de cellules caliciformes sont des critères diagnostiques 6). La mesure de la densité des cellules épithéliales basales permet une évaluation quantitative de la sévérité de la LSCD 6).
Évaluation de l’œdème cornéen et des maladies endothéliales : L’IVCM permet d’observer les cellules endothéliales même à travers un œdème cornéen modéré, ce qui est particulièrement utile dans les cas où la microscopie spéculaire est difficile 7). Dans la dystrophie endothéliale de Fuchs (FECD), en plus de l’évaluation des cellules endothéliales, une diminution de la densité nerveuse et des changements de densité des cellules dendritiques peuvent être observés 7).
Évaluation des nerfs cornéens : L’évaluation quantitative du plexus sous-basal est utilisée pour le diagnostic de la kératopathie neurotrophique et l’évaluation de l’efficacité thérapeutique3). Après une neurotisation cornéenne chirurgicale, l’IVCM montre des signes de régénération nerveuse entre 6 mois et 1 an postopératoire3).
Détection précoce des maladies auto-immunes systémiques : Dans le syndrome de Sjögren, une diminution de la densité des fibres nerveuses au centre de la cornée et une augmentation des cellules dendritiques activées peuvent être détectées avant l’apparition clinique4). La présence d’au moins 2 cellules dendritiques activées avec 3 prolongements ou plus dans la cornée centrale a une sensibilité de 60% et une spécificité de 77% pour les maladies auto-immunes systémiques4).
Évaluation postopératoire : Utilisée pour surveiller les changements du bord du capot, de la membrane de Bowman et la régénération nerveuse après LASIK et PRK2). Elle est également utile pour la détection précoce du rejet après une greffe de cornée.
6. Recherches récentes et perspectives futures
Section intitulée « 6. Recherches récentes et perspectives futures »Analyse d’image automatisée : Des systèmes de quantification automatique des fibres nerveuses sous-basales, comme le logiciel ACCMetrics, ont été développés2). Ils calculent objectivement des paramètres tels que la densité des fibres nerveuses, la densité de ramification et la tortuosité, réduisant ainsi la variabilité inter-examinateur.
Détection du stade préclinique des maladies : Dans les cas de syndrome de Sjögren, des anomalies à l’IVCM ont été rapportées plusieurs années avant la séroconversion ou l’apparition des symptômes cliniques4). Cela suggère que l’IVCM pourrait devenir un outil de dépistage des maladies auto-immunes.
Classification des sous-types de sécheresse oculaire : L’analyse de la morphologie et de la distribution des cellules dendritiques pourrait permettre de différencier la sécheresse oculaire immunitaire de la sécheresse par évaporation4).
Suivi de la régénération nerveuse postopératoire : Des recherches sont en cours pour suivre dans le temps le processus de régénération nerveuse après une neurotisation cornéenne ou un cross-linking cornéen par IVCM3). À l’avenir, cela pourrait servir de critère d’évaluation objectif de l’efficacité thérapeutique.
Intégration de l’intelligence artificielle : Le développement de systèmes de classification et de diagnostic automatiques des images IVCM utilisant l’apprentissage profond est en cours, avec des applications potentielles pour le diagnostic rapide des infections et la différenciation automatique des dystrophies cornéennes.
7. Références
Section intitulée « 7. Références »-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
