
共軛焦顯微鏡(活體角膜共軛焦顯微鏡)
一目瞭然的要點
Section titled “一目瞭然的要點”1. 什麼是共軛焦顯微鏡?
Section titled “1. 什麼是共軛焦顯微鏡?”共軛焦顯微鏡是一種基於照明光和觀察光共享同一焦面光學原理的高解析度顯微鏡。在眼科領域,它應用於角膜的活體觀察,也用於Fuchs角膜內皮營養不良等的評估 7)。
目前臨床使用的主要設備有以下兩種。
雷射掃描型(HRT III-RCM):由Heidelberg Engineering公司製造。使用670 nm二極體雷射作為光源,物鏡63倍,觀察視野400×400 μm。具有高解析度,側向解析度1~2 μm,深度解析度約4 μm 1)2)。透過PMA一次性帽(TomoCap)和眼科凝膠接觸角膜使用。
裂隙掃描型(Confoscan 4):由Nidek公司製造。使用鹵素光源,也可非接觸使用。具備自動掃描功能,操作相對簡單,但深度解析度僅為25~27 μm。目前已停產。
IVCM具有三種成像模式。截面掃描獲取單一深度的靜態影像。體積掃描以2 μm間隔獲取30~40張連續截面。序列掃描在同一深度獲取最多100幀影片,適合觀察動態變化。
IVCM需要專用設備和熟練的操作者,因此主要在大學醫院和專科眼科機構引入。並非所有眼科都能進行,但在診斷角膜感染和角膜營養不良方面特別有用,必要時會轉診。
2. 主要所見和臨床意義
Section titled “2. 主要所見和臨床意義”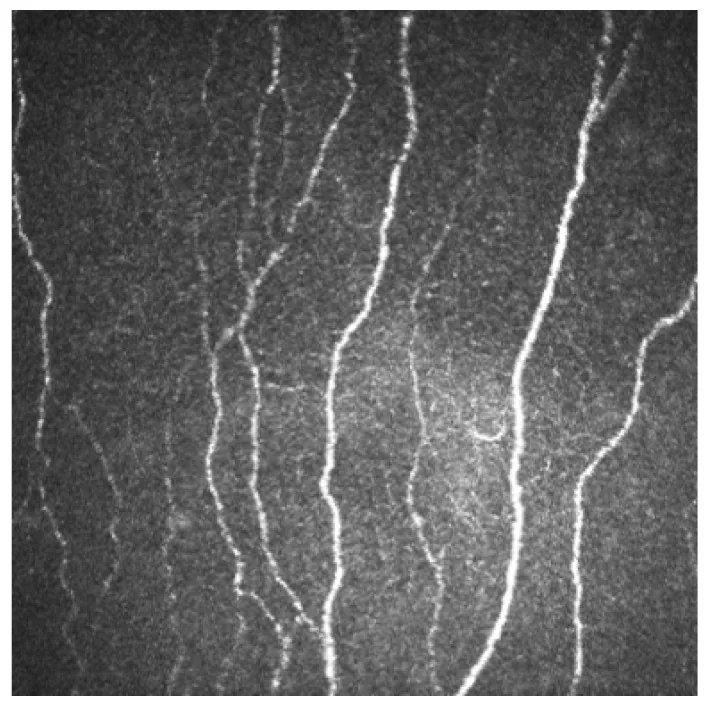
正常角膜所見
Section titled “正常角膜所見”IVCM可以分別觀察角膜的各層。
角膜上皮:表層細胞呈多邊形,40~50 μm。翼狀細胞20~30 μm,細胞邊界明亮,約5,000 cells/mm²。基底細胞8~10 μm,胞質暗,邊界明亮(橋粒),呈蜂窩狀。基底細胞密度為3,600~8,996 cells/mm²。
鮑曼層:觀察為無結構的灰白色層,厚約10 μm。神經束穿行其中。
角膜基質:角膜基質細胞(角膜細胞)在非活躍狀態時呈暗色,活躍狀態時呈明亮的阿米巴樣。前部基質細胞密度較高。
後彈力層:呈霧狀層,厚6~10 μm。通常無法識別細胞結構。
角膜內皮:六角形細胞呈鑲嵌排列。細胞直徑約20 μm,密度2,550~2,720 cells/mm²,隨年齡每年減少約0.6%。
角膜基底神經叢:在鮑曼層正下方觀察為串珠狀彎曲結構3)。在角膜中心鼻下方約1~2 mm處形成漩渦狀圖案。纖維直徑0.52~4.6 μm。
樹突狀細胞(蘭格漢氏細胞):角膜中央分布為34 ± 3 cells/mm²,周邊為98 ± 8 cells/mm²。是免疫反應的指標。
角膜感染:真菌性角膜炎時,基質內可清晰觀察到絲狀菌絲8)。棘阿米巴以囊體(雙層壁結構的球形)形式檢出,但與發炎細胞的鑑別需要經驗8)。細菌因菌體過小,直接可視化困難5)。
角膜營養不良:Avellino角膜營養不良(GCD2)中,基底上皮層可見高反射顆粒狀沉積物,淺層至中層基質可見不規則高反射簇1)。格子狀角膜營養不良I型以網狀沉積物和分支纖維為特徵1)。斑塊狀角膜營養不良可見邊界不清的沉積物,Schnyder結晶狀角膜營養不良可見針狀結晶1)。
角膜擴張:圓錐角膜中可見角膜細胞密度降低,與嚴重程度相關。鮑曼層斷裂也可見。PRK術後角膜擴張的特徵是鮑曼層缺損和前部角膜細胞減少,與圓錐角膜的IVCM模式不同2)。
3. 檢查技術與方法
Section titled “3. 檢查技術與方法”IVCM檢查步驟如下。
前處理:進行點眼麻醉(如奧布卡因)。將眼科凝膠塗抹於一次性TomoCap(PMMA材質)上,並安裝到物鏡前端。
檢查實施:透過CCD攝影機監測鏡頭與角膜的接觸情況,同時壓平角膜。手動調整焦距,從角膜表層(0 μm)向深層依序觀察。固視非常重要,需要患者的配合。檢查時間約為5至15分鐘。
併發症:偶有角膜上皮擦傷、感染(若存在既有上皮缺損則風險較高)發生。
| 項目 | HRT III-RCM | Confoscan 4 |
|---|---|---|
| 光源 | 二極體雷射 | 鹵素光 |
| 深度解析度 | 4 μm | 25~27 μm |
| 接觸 | 需要(TomoCap) | 可不需要 |
由於使用表面麻醉,檢查過程中幾乎沒有疼痛。僅能感覺到角膜帽輕微接觸。檢查後可能出現短暫的異物感,但通常很快消退。
4. 光學原理與設備特點
Section titled “4. 光學原理與設備特點”共焦顯微鏡的基本原理是「共焦性」7)。照明系統和檢測系統均具有針孔孔徑,僅選擇性檢測來自物鏡焦平面的反射光。焦平面外的散射光被針孔阻擋,從而獲得高對比度和深度解析度。
在雷射掃描型(HRT III-RCM)中,670 nm二極體雷射作為點光源,逐點掃描角膜以構建圖像。焦平面厚度(光學切片厚度)極薄,約4 μm,提供細胞層級的清晰橫截面圖像。
在裂隙掃描型(Confoscan 4)中,使用裂隙狀光束進行掃描,因此僅在垂直於裂隙的方向上獲得真正的共焦性。因此深度解析度為25–27 μm,圖像清晰度不如雷射掃描型。
IVCM的限制包括:僅灰階圖像(無法彩色觀察)、無法解析細胞內結構、嚴重角膜混濁病例觀察困難、難以精確定位觀察部位、依賴檢查者技能。
5. 主要臨床應用
Section titled “5. 主要臨床應用”IVCM的臨床應用多種多樣。
角膜感染的診斷輔助:作為培養檢查的輔助工具很有用。可檢測真菌菌絲和棘阿米巴囊體,但判讀結果需要專業知識8)。在疱疹性角膜炎中,可捕捉角膜神經的變化8)。在巨細胞病毒性角膜內皮炎中,有時可見貓頭鷹眼樣包涵體。
角膜營養不良的鑑別:每種營養不良具有特徵性IVCM表現,可透過模式識別進行非侵入性鑑別1)。作為基因檢測或切片檢查前的篩檢工具非常有用。也可用於評估治療效果(PTK、DALK等)1)。
角膜緣幹細胞缺乏症(LSCD)的評估:Vogt柵欄結構消失、結膜上皮替代角膜上皮、杯細胞出現是診斷依據6)。基底上皮細胞密度測量可定量評估LSCD嚴重程度6)。
角膜水腫和內皮疾病的評估:IVCM可透過中度角膜水腫觀察內皮細胞,因此在鏡面顯微鏡難以拍攝的病例中特別有用7)。在Fuchs角膜內皮營養不良(FECD)中,除評估內皮細胞外,還可捕捉神經密度降低和樹突狀細胞密度變化7)。
角膜神經評估:對基底下神經叢的定量評估用於神經營養性角膜病變的診斷和治療效果判定3)。在角膜神經移植術後的神經再生評估中,IVCM可在術後6個月至1年確認再生表現3)。
全身性自體免疫疾病的早期發現:在乾燥症候群中,角膜中央神經纖維密度降低和活化樹突狀細胞增加可能在臨床症狀出現前被檢測到4)。當中央角膜存在2個以上具有3個以上突起的活化樹突狀細胞時,對全身性免疫疾病的敏感性為60%,特異性為77%4)。
術後評估:用於LASIK、PRK術後角膜瓣邊緣、鮑曼層變化及神經再生的追蹤觀察2)。也應用於角膜移植術後排斥反應的早期檢測。
6. 最新研究與未來展望
Section titled “6. 最新研究與未來展望”自動影像分析:已開發出如ACCMetrics軟體等基底下神經纖維自動定量系統2)。可客觀計算神經纖維密度、分支密度、彎曲度等參數,減少觀察者間差異。
疾病臨床前階段的檢測:有報導稱,在乾燥症候群病例中,IVCM異常可在抗體陽性或臨床症狀出現前數年檢測到4)。這表明IVCM可能成為自體免疫疾病的篩檢工具。
乾眼的亞型分類:透過分析樹突狀細胞的形態和分佈模式,可能有助於區分免疫介導性乾眼和蒸發過強型乾眼4)。
術後神經再生的監測:利用IVCM對角膜神經移植術和角膜交聯術後的神經再生過程進行縱向追蹤的研究正在進展中3)。未來有望作為治療效果的客觀終點指標。
人工智慧的整合:利用深度學習開發IVCM影像的自動分類和自動診斷系統的工作正在進行中,預計將應用於感染的快速診斷和角膜營養不良的自動鑑別。
7. 參考文獻
Section titled “7. 參考文獻”-
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
-
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
-
Rathi A, Bothra N, Priyadarshini SR, et al. Neurotization of the human cornea - A comprehensive review and an interim report. Indian J Ophthalmol. 2022;70(6):1905-1917. doi:10.4103/ijo.IJO_2030_21. PMID:35647955; PMCID:PMC9359267.
-
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
-
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2017;124(11):1678-1689. doi:10.1016/j.ophtha.2017.05.012. PMID:28942073; PMCID:PMC5710829.
-
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
-
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
-
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
