مرحله 1 (خفیف)
کراتوپاتی نقطهای سطحی: نامنظمی و هیپرپلازی اپیتلیوم قرنیه
کاهش زمان شکست اشک: کاهش پایداری اشک
عروق جدید سطحی: تهاجم عروق از لیمبوس

بازسازی عصب قرنیه (corneal neurotization; CN) یک عمل جراحی است که در آن یک عصب حسی سالم به قرنیه منتقل میشود تا عصبدهی مجدد برای درمان کراتوپاتی نوروتروفیک (neurotrophic keratopathy; NK) انجام شود 1). NK یک بیماری مقاوم به درمان است که در اثر آسیب عصب سهقلو ایجاد میشود و منجر به کاهش یا از دست رفتن حس قرنیه و اختلال در هموستاز اپیتلیال میگردد. شیوع آن حدود ۵ نفر در هر ۱۰۰۰۰ نفر تخمین زده میشود.
درمانهای سنتی NK مانند اشک مصنوعی و تارسورافی علامتی هستند و به علت اصلی عصبی نمیپردازند. CN تنها روش جراحی است که میتواند با بازگرداندن حس قرنیه، سطح چشم را تثبیت کرده و پیشآگهی بلندمدت را بهبود بخشد 1).
از آن زمان، روشهای جراحی به سرعت متنوع شدهاند، از جمله رویکرد آندوسکوپیک و استفاده از آلوگرافت بدون سلول 1).
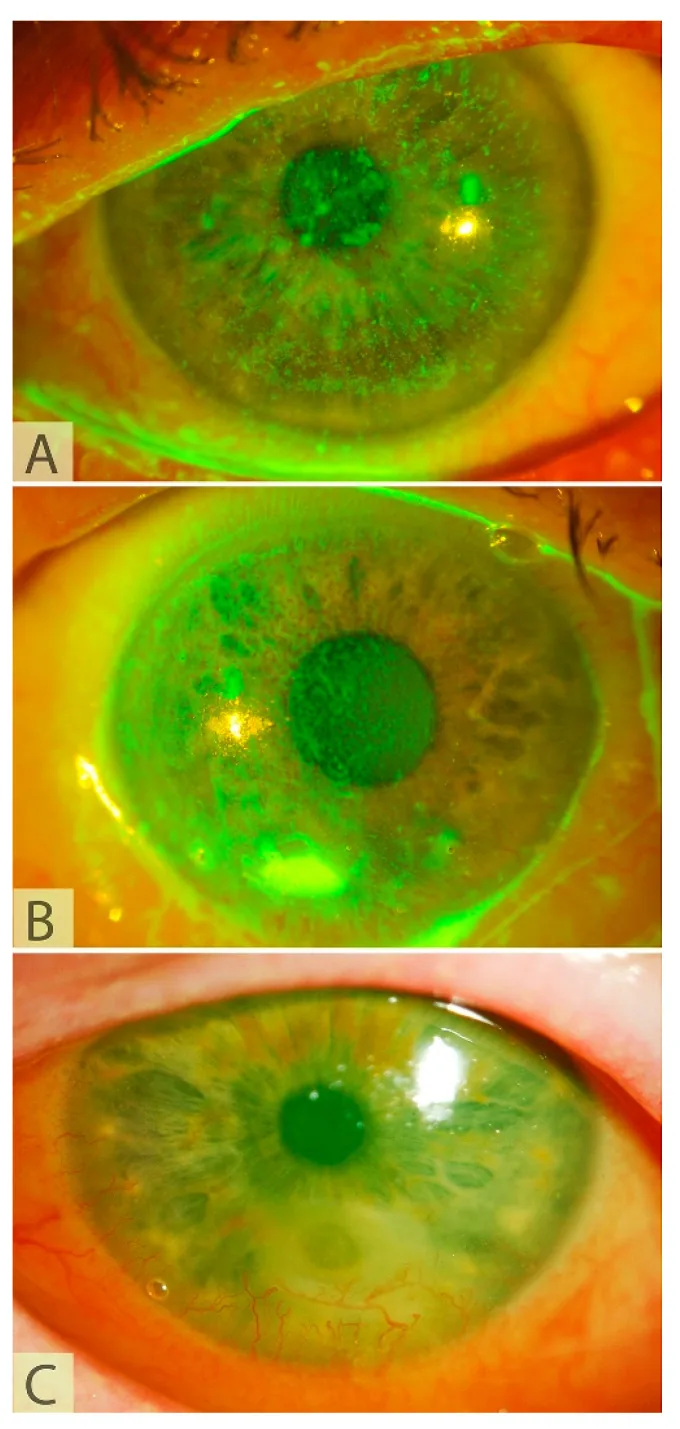
علائم و یافتههای کراتوپاتی نوروتروفیک که هدف CN هستند در زیر آورده شده است.
بیماران NK به دلیل کاهش حس قرنیه، علائم را به سختی احساس میکنند.
شدت NK با طبقهبندی Mackie ارزیابی میشود.
مرحله 1 (خفیف)
کراتوپاتی نقطهای سطحی: نامنظمی و هیپرپلازی اپیتلیوم قرنیه
کاهش زمان شکست اشک: کاهش پایداری اشک
عروق جدید سطحی: تهاجم عروق از لیمبوس
مرحله 2 (متوسط)
نقص اپیتلیال پایدار: نقص اپیتلیال با لبههای گرد و برآمده (rolled edge)
ادم پارانشیم: همراه با چینهای غشای دسمه
التهاب اتاق قدامی: فلر خفیف مشاهده میشود
مرحله ۳ (شدید)
ذوب قرنیه: نازک شدن پارانشیم و تشکیل زخم
سوراخ شدن قرنیه: شدیدترین حالت با پیشرفت ذوب
عفونت ثانویه: خطر عفونت ثانویه افزایش مییابد
حساسیت قرنیه با استفاده از Cochet-Bonnet esthesiometer (CB) به صورت کمی ارزیابی میشود. در مقیاس ۰ میلیمتر (بیحسی) تا ۶۰ میلیمتر (طبیعی)، کمتر از ۲۰ میلیمتر به عنوان حساسیت کم در نظر گرفته میشود1).
NK در اثر آسیب در هر نقطه از مسیر عصب سهقلو ایجاد میشود1)3).
تراکم و مورفولوژی شبکه عصبی زیر اپیتلیال قرنیه را به صورت غیرتهاجمی مشاهده میکند2). برای ارزیابی پایه قبل از عمل و پایش بازسازی عصبی پس از عمل مفید است. بهبود پارامترهای عصبی از 3 ماه پس از عمل قابل مشاهده است2)4).
حسسنج قرنیه Cochet-Bonnet (CBA) تست استاندارد کمی است. یک فیلامنت نایلونی به قطر 0.12 میلیمتر از طول 60 میلیمتر (حداکثر طول، حداقل فشار) به صورت عمودی روی قرنیه قرار میگیرد و تا زمانی که حس شود، به تدریج 10 میلیمتر کوتاه میشود. هرچه فیلامنت کوتاهتر باشد، فشار بیشتر و کاهش حساسیت شدیدتر است. کمتر از 20 میلیمتر نشاندهنده حساسیت کم و بیش از 50 میلیمتر نشاندهنده حساسیت بالا است.
درمان نوروپاتی قرنیه بر اساس رویکرد مرحلهای مطابق با مرحله Mackie است.
مواردی که به درمان محافظهکارانه پاسخ نمیدهند و مواردی که بیش از یک سال بیحسی مداوم قرنیه دارند، کاندیدای CN هستند1).
روشی که در آن عصب دهنده مستقیماً به لیمبوس قرنیه منتقل میشود.
روشی که در آن از یک پیوند عصبی واسطه برای پل زدن بین عصب دهنده و قرنیه استفاده میشود. در 63٪ موارد استفاده میشود2).
| ویژگی | روش مستقیم | روش غیرمستقیم |
|---|---|---|
| سرعت بازگشت حس | سریع | نسبتاً کند |
| نتایج در ۱۲ ماه | مشابه | مشابه |
| محل جراحی ثانویه | ندارد | دارد |
در ۱۲ ماه، تفاوت معنیداری در بازگشت حس بین روش مستقیم و غیرمستقیم وجود ندارد1)2).
انتخاب عصب دهنده بر اساس زندهمانی عصب، تعداد آکسون و نزدیکی به قرنیه است5).
| عصب | تعداد آکسونهای میلیندار | ویژگیها |
|---|---|---|
| عصب فوقچشمخانای | حدود ۶۰۰۰ | نزدیک به قرنیه، انتخاب اول |
| عصب تروکلئار فوقانی | حدود ۲۵۰۰ | دارای تغییرات آناتومیک |
| عصب گوشی بزرگ | حدود ۶۵۳۰ | مفید در نوروکراتوپاتی دوطرفه |
Terzis و همکارانش حداقل تعداد آکسونهای میلیندار لازم برای بازسازی عصبی مؤثر را ۹۰۰ عدد پیشنهاد کردهاند4). بخشهای انتهایی اعصاب فوقچشمخانای و تروکلئار فوقانی هر کدام بیش از ۲۰۰۰ آکسون میلیندار دارند که این معیار را به خوبی برآورده میکنند4)5).
در مطالعات مقایسهای، تفاوت معنیداری در بازیابی حس قرنیه در ۱۲ ماه وجود ندارد. روش مستقیم نیازی به پیوند ندارد و بازیابی حس کمی سریعتر است (مقدار CB در ۳ تا ۶ ماه به طور آماری معنیدار بهبود مییابد)، اما روش غیرمستقیم با برش کوچک قابل انجام است و برای NK دوطرفه نیز قابل استفاده است. انتخاب روش جراحی بر اساس در دسترس بودن عصب اهداکننده، فاصله تا قرنیه و تجربه جراح تعیین میشود.
قرنیه یکی از بافتهایی با بالاترین تراکم عصبی در بدن است و در هر میلیمتر مربع حدود ۷۰۰۰ گیرنده درد وجود دارد. حساسیت آن ۴۰ برابر پالپ دندان و ۴۰۰ تا ۶۰۰ برابر پوست است.
عصبدهی از شاخه اول عصب سهقلو (عصب چشمی) → عصب نازوسیلیاری → عصب سیلیاری بلند به قرنیه میرسد. اعصاب از غشای بومن عبور کرده و شبکه عصبی زیراپیتلیال را تشکیل میدهند. ۷۰٪ گیرندهها چندوجهی (پاسخ به محرکهای شیمیایی، حرارتی و مکانیکی)، ۲۰٪ گیرندههای مکانیکی و ۱۰٪ گیرندههای سرما هستند.
اعصاب قرنیه حاوی و ترشحکننده انتقالدهندههای عصبی مانند ماده P، CGRP، نوروپپتید Y و VIP هستند. این مواد تکثیر، مهاجرت و بازسازی سلولهای اپیتلیال را تنظیم کرده و برای حفظ هموستاز قرنیه ضروری هستند.
عوامل تغذیهای مانند NGF، BDNF، GDNF، NT-3 و NT-4/5 نیز از اعصاب قرنیه تأمین میشوند. از دست دادن این عوامل علت اصلی تأخیر در بهبود اپیتلیوم و اختلال در هموستاز در کراتوپاتی نوروتروفیک (NK) است.
در جراحی بازسازی عصب قرنیه (CN)، یک عصب سالم اهداکننده در محل اتصال قرنیه-صلبیه قرار داده میشود 1).
در روش مستقیم، انتهای دیستال عصب اهداکننده مستقیماً در قرنیه کاشته میشود. در روش غیرمستقیم، یک پیوند واسطهای عصب اهداکننده را به قرنیه متصل میکند. در هر دو مورد، رشتههای عصبی از عصب اهداکننده به سمت استروما و زیر اپیتلیوم قرنیه رشد کرده و عصبدهی مجدد قرنیه رخ میدهد 1).
بازسازی آکسون از الگوی کلاسیک دژنراسیون والرین پیروی میکند 1). پس از تخریب اولیه آکسون، ماکروفاژها میلین تخریب شده را پاکسازی میکنند و سلولهای شوان از بخش سالم پروگزیمال عصب اهداکننده تمایز یافته و مهاجرت میکنند تا بازسازی آکسون را تسهیل کنند. افزایش تنظیم NGF و IL-1 نقش مهمی در تحریک جوانهزنی آکسون ایفا میکند 1).
در مدل موش صحرایی، CN تراکم عصب قرنیه را افزایش داد، اما تنها بخش کوچکی از آکسونهای بازسازی شده از طریق پیوند به قرنیه رسیدند. این احتمال وجود دارد که قرنیه به طور انتخابی تنها رشد رشتههای عصبی بدون میلین با فنوتیپ خاص را مجاز میداند 1).
عملکرد تغذیهای عصب قرنیه تمایل دارد زودتر از عملکرد حسی بهبود یابد. بنابراین، حتی اگر بهبود CB در ۱۲ ماهگی اندک باشد، مواردی وجود دارد که IVCM اعصاب قرنیه را نشان میدهد و نقص اپیتلیال بهبود یافته است 1).
در یک مرور دامنه در سال ۲۰۲۵ (۱۲ مطالعه، ۱۶۴ چشم)، میزان موفقیت CN بین ۶۰.۷ تا ۱۰۰٪ (میانگین ۹۰٪) بود. میانگین CCS قبل از عمل ۲.۷ میلیمتر (CBA) به طور معنیداری به ۳۶.۰ میلیمتر پس از عمل بهبود یافت (دامنه: ۲۱.۱ تا ۴۹.۷ میلیمتر). حس قرنیه به طور متوسط پس از ۴.۱ ماه ظاهر شد و در ۱۲ ماه به اوج رسید 2).
روش غیرمستقیم (پیوند عصب سورال) 63% از کل موارد را تشکیل میداد که بیشترین میزان بود. پیوند آلوگرافت بدون سلول نتایج مشابهی با پیوند اتولوگ داشت و مزایای آن کاهش زمان جراحی و اجتناب از عوارض محل دهنده است 2).
در گزارش Catapano و همکاران از 19 چشم (میانگین سنی 12.5 سال)، 87% از بیماران به CB 40mm رسیدند و 64% حس کامل را بازیافتند. گروهی که فاسیکول در تونل قرنیه-صلبیه قرار داده شد، بهبود حس زودتری نشان دادند 2).
در یک پسر 11 ساله با مرحله 1 Mackie، بهبود عینی حس 6 ماه پس از MICN ظاهر شد و حس مرکزی قرنیه در 21 ماه به 20mm رسید. تست شیرمر از 15mm به 30mm بهبود یافت و بینایی از 6/18 به 6/5 بازگشت 6).
در دو مورد با سن بالا (62 و 70 سال) و عصبزدایی طولانیمدت (23 سال)، بهبود پایدار حس پس از MICN حاصل نشد. در آسیب پروگزیمال عصب سهقلو (مانند پس از جراحی نوروم آکوستیک)، «ذخیره عملکردی» کم است و ممکن است در مقایسه با علل محیطی (مانند کراتیت هرپسی) پیشآگهی بدتری داشته باشد 7).
این یافتهها نشان میدهد که سن بالا، عصبزدایی طولانیمدت و آسیب پروگزیمال عصب سهقلو عوامل پیشآگهی بد برای CN هستند و باید در انتخاب بیمار و مشاوره در نظر گرفته شوند 7).
در یک مرور دامنهای در سال ۲۰۲۵ (۱۶۴ چشم)، میزان موفقیت بین ۶۰.۷ تا ۱۰۰٪ (میانگین ۹۰٪) گزارش شده است. حس قرنیه قبل از عمل (CBA) از میانگین ۲.۷ میلیمتر به ۳۶.۰ میلیمتر پس از عمل بهبود یافت و در ۱۲ ماهگی، بیش از ۶۰٪ از کودکان به حس طبیعی دست یافتند. با این حال، در موارد کهنسالی و عصبزدایی طولانیمدت، نتایج ممکن است ضعیفتر باشد.
- Hubschman S, Rosenblatt MI, Cortina MS. Corneal neurotization for the treatment of neurotrophic keratopathy. Curr Opin Ophthalmol 2025;36:294-301.
- Samoilă O, Samoilă L, Petrescu L. Corneal Neurotization, Recent Progress, and Future Perspectives. Biomedicines 2025;13:961.
- Dragnea DC, Krolo I, Koppen C, et al. Corneal Neurotization-Indications, Surgical Techniques and Outcomes. J Clin Med 2023;12:2214.
- Saini M, Jain A, Vanathi M, et al. Current perspectives and concerns in corneal neurotization. Indian J Ophthalmol 2024;72:1404-11.
- Serra PL, Giannaccare G, Cuccu A, et al. Insights on the Choice and Preparation of the Donor Nerve in Corneal Neurotization for Neurotrophic Keratopathy: A Narrative Review. J Clin Med 2024;13:2268.
- Lee BWH, Khan MA, Ngo QD, et al. Minimally invasive, indirect corneal neurotization using an ipsilateral sural nerve graft for early neurotrophic keratopathy. Am J Ophthalmol Case Rep 2022;27:101585.
- Ting DSJ, Pradhan SP, Barnes E, et al. Minimally invasive corneal neurotization for neurotrophic keratopathy: The potential effect of age, denervation chronicity and lesion location. Am J Ophthalmol Case Rep 2023;29:101804.