الدرجة I (خفيفة)
التهاب القرنية النقطي السطحي: عدم انتظام نقطي في ظهارة القرنية دون عجز ظهاري.
خلل نوعي في الظهارة: عتامة ظهارة القرنية وانخفاض شفافيتها.
عدم استقرار الطبقة الدمعية: قد يترافق مع انخفاض إفراز الدموع أو انخفاض كثافة الخلايا الكأسية.

التهاب القرنية العصبي التغذوي (neurotrophic keratitis: NK) هو مرض تنكسي في القرنية يتميز بانخفاض أو فقدان الإحساس بالقرنية. يُسمى أيضًا اعتلال القرنية العصبي التغذوي (neurotrophic keratopathy) أو اعتلال القرنية العصبي الشللي (neuroparalytic keratopathy). يحدث بسبب تلف التعصيب الحسي المنبثق من الفرع الأول للعصب ثلاثي التوائم (العصب القحفي الخامس)، وهو العصب البصري.
توجد في نهايات الأعصاب القرنية العديد من الناقلات العصبية مثل المادة P، والببتيد المرتبط بجين الكالسيتونين (CGRP)، والببتيد العصبي Y (NPY)، والببتيد المعوي الفعال وعائيًا (VIP)، والغالانين، والميثيونين إنكيفالين، والكاتيكولامينات، والأسيتيل كولين. تنظم هذه العوامل العصبية المشتقة من الأعصاب عملية الأيض، والتجدد، والتئام الجروح في ظهارة القرنية، ويعد انخفاض إمداد هذه العوامل بسبب تلف العصب ثلاثي التوائم الآلية الأساسية لخلل توازن القرنية.
يتطور المسار السريري تدريجيًا. يؤدي الفقدان الجزئي أو الكامل للإحساس بالقرنية إلى اعتلال ظهاري (تنقيط ظهاري سطحي: SPK)، ثم عيب ظهاري مستمر (PED)، ثم قرحة سدى القرنية، وقد يتطور إلى انثقاب القرنية 5). ومع ذلك، يمكن إبطاء التقدم إذا تمت الإدارة المناسبة في المراحل المبكرة.
يقدر معدل الانتشار بأقل من 50 لكل 100,000 شخص، مما يجعله مرضًا نادرًا 11). رمز ICD-10 هو H16.239. هذا المرض ليس له سبب واحد، بل يمكن أن يحدث بسبب أي حالة تؤدي إلى تلف في أي مكان على طول مسار العصب ثلاثي التوائم، مما يمنحه طابعًا متلازميًا.
التهاب القرنية العصبي التغذوي (neurotrophic keratitis)، واعتلال القرنية العصبي التغذوي (neurotrophic keratopathy)، واعتلال القرنية العصبي الشللي (neuroparalytic keratopathy) كلها تشير إلى نفس الحالة الناتجة عن تلف العصب ثلاثي التوائم. تختلف التسميات بناءً على التركيز على ما إذا كان الضرر الذي يصيب ظهارة القرنية التهابيًا أم تنكسيًا، ولكنها متكافئة سريريًا.
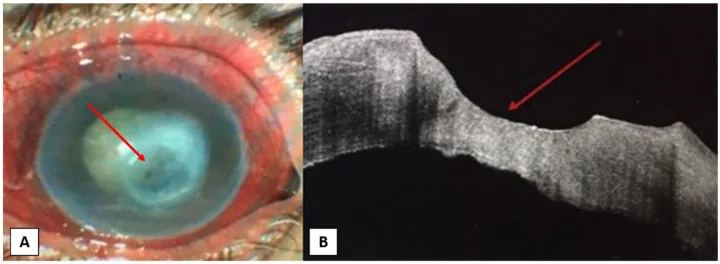
في التهاب القرنية العصبي التغذوي (NK)، نظرًا لضعف التعصيب الحسي للقرنية، نادرًا ما يشكو المرضى من أعراض سطح العين. ولهذا، قد تمر عدة أشهر إلى سنوات قبل أن يطلب المريض الاستشارة الطبية.
تتنوع الصورة السريرية لالتهاب القرنية العصبي التغذوي من عدم انتظام دقيق في سطح القرنية إلى تآكل وانثقاب القرنية. تقليديًا، يُستخدم تصنيف Mackie ثلاثي المراحل على نطاق واسع 12,13).
الدرجة I (خفيفة)
التهاب القرنية النقطي السطحي: عدم انتظام نقطي في ظهارة القرنية دون عجز ظهاري.
خلل نوعي في الظهارة: عتامة ظهارة القرنية وانخفاض شفافيتها.
عدم استقرار الطبقة الدمعية: قد يترافق مع انخفاض إفراز الدموع أو انخفاض كثافة الخلايا الكأسية.
الدرجة الثانية (متوسطة)
عيب ظهاري مستمر (PED): يتميز بشكل بيضاوي وحواف مرتفعة (rolled margins). قد يترافق مع عتامة أو تكون أوعية دموية جديدة.
طيات غشاء ديسيميه: علامة مرتبطة بوذمة القرنية.
التهاب خفيف في الغرفة الأمامية: قد يُلاحظ التهاب خفيف في الغرفة الأمامية (خلايا/وهج).
الدرجة الثالثة (شديدة)
قرحة سدى القرنية: نقص في السدى مع ذوبان القرنية (melting).
انثقاب القرنية: أخطر المضاعفات. يتطلب تدخلاً جراحياً عاجلاً.
ندبة القرنية: قد تسبب ضعفاً دائماً في الرؤية حتى بعد الشفاء.
انخفاض إفراز الدموع هو علامة مرافقة شائعة جداً في التهاب القرنية العصبي، ويجب عند التقييم استخدام اختبار شيرمر وزمن تكسر الدمع (BUT) بالإضافة إلى فحص القرنية 11).
في التهاب القرنية العصبي، يؤدي تلف العصب ثلاثي التوائم إلى انخفاض أو فقدان الإحساس في القرنية. عادةً، يُلاحظ تلف ظهارة القرنية كألم أو إحساس بجسم غريب، لكن في التهاب القرنية العصبي لا تعمل إشارة التحذير هذه. بالإضافة إلى ذلك، يقل إفراز الدموع الانعكاسي والرمش، مما يؤدي إلى تقدم العيوب الظهارية أو القرحات دون أعراض ذاتية، مما يسبب تأخراً في مراجعة الطبيب وشدة المرض.
أي مرض عيني موضعي أو جهازي يضر بالمسار العصبي الحسي من القرنية إلى نواة العصب ثلاثي التوائم في الجسر يمكن أن يسبب التهاب القرنية العصبي. من منظور الفيزيولوجيا المرضية، يُصنف إلى أسباب محيطية (موضعية في القرنية إلى الحجاج)، وأسباب مركزية (داخل الجمجمة)، وأسباب استقلابية (داء السكري) 13).
في مرضى السكري، تتقدم التغيرات الشكلية والوظيفية في العصب الحسي للقرنية، وينخفض الإحساس القرني بما يتناسب مع شدة اعتلال الشبكية السكري. يُعتبر هذا جانبًا من الاعتلال العصبي المحيطي السكري، ويُعتقد أنه مشابه لقرحة الجلد المستعصية والغرغرينا السكرية في القدم. تم الإبلاغ عن حالات تم فيها اكتشاف التهاب القرنية العصبي كأول علامة على مرض السكري 11).
في الليزك، يتم قطع الأعصاب القرنية أثناء إنشاء السديلة، مما يؤدي إلى انخفاض مؤقت في الإحساس القرني بعد الجراحة. في معظم الحالات، يتعافى في غضون بضعة أشهر إلى سنة، ولكن في حالات نادرة، قد يستمر ويؤدي إلى التهاب القرنية العصبي. لا يتضمن PRK إنشاء سديلة، لذا فإن معدل حدوث الاعتلال العصبي أقل. في الحالات التي تعاني من جفاف العين أو انخفاض الإحساس القرني قبل الجراحة، يلزم إجراء تقييم دقيق في مرحلة اختيار التقنية الجراحية.
هو الاختبار الأكثر أهمية لتشخيص التهاب القرنية العصبي.
نظرًا لأن قطرات العين (خاصة المخدرة أو المحتوية على مواد حافظة) تغير قيم القياس، يجب إجراء اختبار الحساسية قبل وضع القطرات.
عند وجود اعتلال ظهاري قرني شديد دون أعراض انزعاج في العين بسبب تخدير القرنية، يُشتبه بقوة في التهاب القرنية العصبي. يجب التفريق بين الأمراض التالية.
بعد تأكيد التشخيص، من الضروري التحقق من السبب. يتم أخذ التاريخ المرضي (الهربس، السكري، جراحة العين، الصدمة، آفات داخل الجمجمة، قطرات العين) وإجراء التصوير بالرنين المغناطيسي للدماغ أو استشارة طبيب أعصاب/جراحة أعصاب حسب الحاجة.
يعتمد علاج التهاب القرنية العصبي على إدارة مرحلية حسب مرحلة المرض. في جميع المراحل، استخدم قطرات عين خالية من المواد الحافظة. إذا كانت هناك أمراض سطح العين الأخرى (جفاف العين، التهاب الجفن، اعتلال القرنية التعرضي، إلخ) يتم علاجها بالتوازي. يتم أيضًا علاج المرض المسبب.
| المرحلة | هدف العلاج | العلاج الرئيسي |
|---|---|---|
| الدرجة الأولى | تحسين جودة وشفافية الظهارة، منع فقدان الظهارة | دموع اصطناعية خالية من المواد الحافظة، مرهم مرطب، سد النقاط الدمعية، قطرات مصل ذاتي |
| الدرجة الثانية | تعزيز التئام العيب الظهاري المستمر | العدسات اللاصقة العلاجية، زرع الغشاء الأمنيوسي، خياطة الجفن، سينيجيرمين |
| الدرجة الثالثة | التئام القرحة والوقاية من الانثقاب | أسيتيل سيستئين، تتراسيكلين فموي، مادة لاصقة للأنسجة، زرع القرنية |
الهدف هو حماية الظهارة وتثبيت الطبقة الدمعية.
بالإضافة إلى علاج الدرجة الأولى، يُستخدم ما يلي:
في التجارب السريرية للسينيجرمين، أجريت دراسة عشوائية مزدوجة التعمية مضبوطة بالغفل (المرحلة الثانية REPARO، تجربة Pflugfelder 2020 المحورية) على مرضى NK من الدرجة الثانية أو الثالثة8,9).
عند دمج تجربتين عشوائيتين مضبوطتين، حقق 65-72% من المرضى في مجموعة rhNGF التئاماً كاملاً للقرنية بعد 8 أسابيع، مقارنة بـ 17-33% في مجموعة الغفل. كان الحدث الضار الأكثر شيوعاً هو الألم في موقع التقطير، وحدث في حوالي 16% من الحالات3).
أظهرت تجربة REPARO المرحلة الأولى/الثانية (NGF0212) تقصير وقت التئام عيب الظهارة وانخفاض معدل التكرار، لكنها لم تظهر تحسناً كبيراً في الإحساس القرني نفسه2). بعض المرضى يعانون من تكرار NK بعد التوقف عن العلاج، مما يستلزم متابعة منتظمة.
يجب تجنب الستيرويدات الموضعية لأنها قد تحفز انحلال السدى، وإذا استخدمت للسيطرة على الالتهاب، يجب إعطاؤها بحذر. يجب تجنب مضادات الالتهاب غير الستيرويدية الموضعية لأنها تقلل الإحساس القرني أكثر. الاستخدام المستمر لقطرات التخدير الموضعي ممنوع منعاً باتاً.
بالإضافة إلى علاج الدرجة الأولى والثانية، إذا كان هناك تقدم في انحلال السدى، يتم إضافة ما يلي:
عند حدوث ثقب في القرنية، يتم تقسيم العلاج حسب قطر الثقب.
في اليابان، تم الإبلاغ عن العلاجات التالية على مستوى البحث السريري لتعزيز التئام الجروح الظهارية للقرنية. في الحالات التي لا تستجيب للعلاج القياسي، يُنظر في استشارة المرافق التي يمكنها إجراء هذه العلاجات.
تقليديًا، كان تجديد العصب القرني مخصصًا للحالات الشديدة التي لا تستجيب للعلاج المحافظ، لكن مع التطورات الحديثة في التقنيات الأقل تدخلاً، تتوسع مؤشرات استخدامه 1). تشمل المؤشرات المرضى الذين يعانون من نقص أو فقدان الإحساس القرني المتوسط إلى الشديد المقاوم للعلاج المحافظ، والذين تتوفر لديهم أعصاب مانحة سليمة 4). تُستخدم فروع العصب ثلاثي التوائم (فوق الحجاجي، فوق البكرية، تحت الحجاجي) والعصب الأذني الكبير في الرقبة 1).
يبلغ متوسط عدد المحاور العصبية للعصب الأذني الكبير 6,530، وللعصب فوق الحجاجي حوالي 3,146 (في المحيط، حوالي 6,000 عند حافة الحجاج)، وللعصب فوق البكري 1,882 (في المحيط، 2,534 عند حافة الحجاج)، وللعصب الربلي 3,179-3,972 1). يُعتقد أن زيادة عدد المحاور العصبية تؤدي إلى تأثير أفضل في تجديد الأعصاب.
تنقسم التقنيات الجراحية إلى طريقة مباشرة وطريقة غير مباشرة 1,7).
تشمل طرق المفاغرة: نهاية إلى نهاية (قطع كامل للعصب المانح لتعظيم تحميل المحاور) ونهاية إلى جانب (إنشاء نافذة في غمد العصب المانح للحفاظ على الوظيفة المتبقية)، حيث يمكن للطريقة الأخيرة تقليل فقدان الإحساس في المنطقة المانحة 1). في تجربة مقارنة متعددة المراكز، لم يُلاحظ فرق كبير في تحسن Cochet-Bonnet بين الطريقة المباشرة وغير المباشرة عند 12 شهرًا 7).
يتم تقسيم العصب المانح الذي يصل إلى القرنية إلى 3-4 حزم، ثم يتم إدخالها في نفق صلبي-قرني حول حوف القرنية، أو تثبيتها على الحوف باستخدام غراء الفيبرين أو الغرز 1). بعد الجراحة، يتم استخدام عدسة لاصقة ضمادية وخياطة جفنية مؤقتة للحماية، بالإضافة إلى قطرات دموع صناعية خالية من المواد الحافظة وقطرات مضادة للبكتيريا. بعد شهر واحد، يمكن استخدام قطرات سينيجيرمين للمساعدة في نمو العصب القرني 1).
السينيجيرمين هو قطرة عين تحتوي على 20 ميكروغرام/مل من عامل النمو العصبي البشري المؤتلف (rhNGF)، وهو أول علاج معتمد لالتهاب القرنية العصبي. في التجارب السريرية (REPARO المرحلة الثانية، والتجربة المحورية المرحلة الثانية) التي شملت التهاب القرنية العصبي من الدرجة الثانية والثالثة، تم الإبلاغ عن تحقيق شفاء قرني كامل لدى 65-72% من المرضى بعد التقطير 6 مرات يوميًا لمدة 8 أسابيع. من ناحية أخرى، لم يظهر تحسن ملحوظ في الإحساس القرني نفسه، وهناك حالات انتكاسة بعد التوقف عن العلاج. الألم في موقع التقطير (حوالي 16%) هو التأثير الجانبي الرئيسي.
جراحة تجديد العصب القرني هي عملية يتم فيها نقل عصب حسي سليم (مثل العصب فوق الحجاج، والعصب فوق البكرة، والعصب تحت الحجاج، والعصب الأذني الكبير) إلى محيط القرنية لاستعادة الإحساس في القرنية العصبية التغذوية. هناك طريقتان: النقل العصبي المباشر، والطعم العصبي غير المباشر عبر العصب الربلي وغيره. يبدأ استعادة الإحساس القرني بعد 3-6 أشهر من الجراحة، ويستمر التحسن لمدة 12-18 شهرًا أو أكثر. في مراجعة لـ 54 عينًا بواسطة Park وآخرين، تم الإبلاغ عن تحسن متوسط قيمة Cochet-Bonnet من 2.18 مم إلى 40.1 مم. يميل المرضى الأصغر سنًا (أقل من 18 عامًا) إلى تحقيق استعادة أفضل.
القرنية هي واحدة من أكثر الأنسجة كثافة في التعصيب في جسم الإنسان. تصل الأعصاب الهدبية الطويلة المتفرعة من الفرع الأول للعصب ثلاثي التوائم (العصب البصري) إلى القرنية. تدخل الألياف العصبية بشكل شعاعي من الحوف إلى سدى القرنية، وتشكل الضفيرة تحت الظهارية تحت غشاء بومان مباشرة. ثم تخترق غشاء بومان لتشكل الضفيرة العصبية القاعدية، وتمتد النهايات العصبية الحرة بين الخلايا الظهارية. تتكون الألياف العصبية من ألياف Aδ رفيعة وألياف C غير ميلينية، مما يساهم في شفافية القرنية.
توفر هذه الضفيرة العصبية القاعدية عوامل التغذية العصبية الضرورية للحفاظ على توازن الظهارة القرنية 1,8). تحتوي الألياف العصبية على مادة P، التي تعزز تأثير عامل النمو البطاني وعامل النمو الشبيه بالأنسولين-1 على تقدم الخلايا الظهارية القرنية، وبالتالي تنظم التئام الجروح الظهارية. عندما يتضرر العصب ثلاثي التوائم، تفقد هذه الآلية التنظيمية، ويقل إفراز الدموع الانعكاسي والرمش، مما يؤدي إلى تطور إصابة الظهارة القرنية بسهولة ويؤدي إلى حالة من تأخر الشفاء.
عند انقطاع إمداد عوامل التغذية العصبية، تحدث التغيرات النسيجية التالية بشكل تدريجي.
في النماذج الحيوانية، أظهرت الفئران التي تم تدمير العصب ثلاثي التوائم لديها تأخرًا ملحوظًا في التئام عيوب الظهارة القرنية الاصطناعية مقارنة بالمجموعة الضابطة، مما يؤكد تجريبيًا أن فقدان العوامل العصبية هو الآلية المركزية لتأخر التئام الجروح.
NGF هو جزيء ممثل لعائلة العوامل التغذوية العصبية (neurotrophin)، ويصبح نشطًا بعد قطعه من السلائف pro-NGF. الشكل النشط هو ثنائي β-NGF (وزن جزيئي 26 كيلو دالتون)، ويتكون من وحدتين فرعيتين β غير مرتبطتين تساهميًا2).
يرتبط NGF بمستقبلين اثنين2):
يتم التعبير عن هذه المستقبلات باستمرار في الخلايا الظهارية للقرنية والخلايا الظهارية القاعدية للملتحمة، ويعزز NGF تكاثر وتمايز الخلايا الظهارية للقرنية، مما يساهم في التئام الجروح2). في مرضى التهاب القرنية العصبي (NK)، ينخفض إمداد NGF، مما يساهم في انهيار الاستتباب الظهاري. يُعتبر التأثير السريري لقطرات rhNGF في تجربة REPARO علاجًا خاصًا بالسبب المرضي بناءً على هذه الآلية الجزيئية8,9).
يُعتبر انخفاض حساسية القرنية لدى مرضى السكري نمطًا ظاهريًا للاعتلال العصبي المحيطي السكري. من المعروف أن حساسية القرنية تنخفض بالتوافق مع شدة اعتلال الشبكية السكري، وتتقدم التغيرات الشكلية في أعصاب القرنية بالارتباط مع انخفاض وظائف الكلى. هذا هو تعبير على سطح العين لاعتلال الأعصاب الحسية المحيطية المشابه للغرغرينا السكرية في القدم وتقرحات الجلد المستعصية، وهو أحد الأسس المرضية الهامة لاعتلال القرنية العصبي13).
في جراحة تجديد العصب القرني، بعد نقل العصب الحسي السليم إلى محيط القرنية، يحدث تجديد المحور العصبي وفقًا لعملية التنكس الواليري 1).
من المثير للاهتمام أن التجارب على الحيوانات أظهرت أن الأعصاب القرنية المتجددة ليست بالضرورة مستمرة مع العصب المانح، مما يشير إلى أن العصب المانح قد لا يعمل فقط كمصدر للمحاور ولكن أيضًا كمصدر لعوامل التغذية العصبية 1).
تطورت جراحة تجديد العصب القرني من إجراء جراحي كبير يتطلب شقًا تاجيًا إلى نهج طفيف التوغل وتقنيات التنظير الداخلي 1,14). مع إدخال الطعوم العصبية الخيفية اللاخلوية، يمكن تجنب المضاعفات المرتبطة بأخذ العصب الذاتي، ويتوسع المؤشر باستخدام أعصاب مانحة بديلة (مثل العصب الأذني الكبير) 1).
فيما يتعلق بالنتائج، أبلغت مراجعة بارك (Park) لـ 54 عينًا عن تعافي قيمة Cochet-Bonnet من متوسط 2.18 مم قبل الجراحة إلى 40.1 مم بعد الجراحة 1,6). يميل المرضى الصغار الذين تقل أعمارهم عن 18 عامًا إلى تحقيق استرداد حسي مبكر وأكثر اكتمالًا وتحسن في الرؤية، ويُعتقد أن هذا يرجع إلى ارتفاع كثافة الألياف العصبية تحت القاعدية في القرنية في سن مبكرة 1,6). يبدأ التصور المجهري متحد البؤر للأعصاب القرنية بعد 3 أشهر من الجراحة، ويستمر التحسن لمدة 12-18 شهرًا 1,14). بعد استقرار سطح العين بجراحة تجديد العصب القرني، يتم إجراء إعادة التأهيل البصري التدريجي عن طريق زرع القرنية كامل السمك (PK) أو زرع القرنية الأمامي العميق الطبقي (DALK) بنتائج جيدة 1).
بعد موافقة FDA/EMA على السينيجيرمين، يستمر تراكم البيانات السريرية الحقيقية. في الآونة الأخيرة، تم الإبلاغ عن تحسن في الأعراض وتلطيخ سطح العين وإفراز الدموع في تجربة المرحلة الثانية لمتلازمة جفاف العين 2). كما يتم دراسة تطبيقاته على أمراض سطح العين الأخرى.
أظهر محلول عيني يحتوي على 0.1% من ثيموسين بيتا 4 (RGN-259) في تجربة سريرية عشوائية مزدوجة التعمية محكومة بالغفل من المرحلة الثالثة على مرضى التهاب القرنية العصبي أنه يعزز التئام القرنية ويحسن الأعراض الذاتية 3).
ثيموسين بيتا 4 هو بروتين رابط للأكتين، ويُعتقد أنه يعزز إصلاح الظهارة من خلال تحفيز هجرة الخلايا، وتأثيرات مضادة للالتهابات ومضادة للاستماتة 15).
تم الإبلاغ عن استخدام الأنسولين الموضعي لأمراض القرنية منذ عام 1945، حيث يعزز إعادة تكون الظهارة القرنية. تم تأكيد وجود مستقبلات الأنسولين ومستقبلات IGF-1 على سطح العين البشري. لم يتم التوصل إلى إجماع حول الجرعة، ولكن عادة ما يتم تطبيقه 4 مرات يوميًا. نظرًا لانخفاض تكلفته وتوافره، يُتوقع أن يكون مفيدًا في مناطق واسعة بما في ذلك البلدان النامية.
RGTA (عامل تجديد) الذي يُعطى موضعيًا هو مادة محاكية لبروتيوغليكان كبريتات الهيباران، وقد تم الإبلاغ عن تعزيز التئام القرنية في دراسات رصدية. وهو متوفر حاليًا في أوروبا فقط.
محليًا، يستمر البحث في قطرات العين التي تحتوي على مزيج من الببتيدات العصبية التي تعمل مباشرة على خلايا ظهارة القرنية. أظهر المزيج من التسلسل الأدنى الضروري FGLM-NH₂ (المشتق من المادة P) وSSSR (المشتق من IGF-1) أنه يعزز التئام الجروح الظهارية، ومن المتوقع تطبيقه في الحالات المقاومة للعلاج.