进行性虹膜萎缩
瞳孔偏位:瞳孔被牵拉向PAS较多的方向。
虹膜孔形成:在瞳孔被牵拉的相反方向多发。
葡萄膜外翻:虹膜色素上皮暴露于表面。
PAS:特征为越过Schwalbe线向高处延伸的高脚PAS。
合并青光眼:在3型中最为常见。

ICE综合征(虹膜角膜内皮综合征;iridocorneal endothelial syndrome)是一种由于异常角膜内皮细胞伴随膜样组织向房角和虹膜延伸,导致小梁网阻塞而引起眼压升高的疾病。角膜内皮异常引起角膜水肿,膜样组织收缩导致虹膜异常及周边虹膜前粘连(PAS)。
好发于30~40岁女性,单眼发病2)。无遗传性,为散发性。罕见家族史,与其他眼病或全身疾病无一致关联。
ICE综合征根据虹膜异常状态分为以下三种临床类型:
ICE综合征为单眼、散发性,这是与双眼、常染色体显性遗传的后部多形性角膜营养不良(PPMD)和Axenfeld-Rieger综合征最简单的鉴别点。
三种类型的区分主要基于虹膜和角膜的临床所见。进行性虹膜萎缩表现为多瞳症、瞳孔偏位、虹膜孔形成、葡萄膜外翻显著,青光眼合并最多。Chandler综合征以角膜水肿为主,虹膜变化轻微,无虹膜孔形成,PAS高度也低。Cogan-Reese综合征的特征是虹膜前表面的有蒂结节或平坦色素病灶,通常无虹膜萎缩。所有类型的基本病理生理相同,治疗方针也相同。
单眼视力下降(因角膜水肿引起的雾视)是最常见的初发症状。有时会感到畏光和疼痛。也可能因注意到瞳孔偏位、虹膜异色等外观异常而就诊。角膜水肿引起的疼痛与房角关闭导致的眼压升高引起的疼痛并存。
角膜所见:Chandler综合征可见角膜内皮呈金属样光泽,即“锤击银样外观”。与Fuchs角膜内皮营养不良的角膜滴状赘相似,但可通过单眼性进行鉴别。即使眼压在正常范围内,也可能出现角膜水肿。有时可见Descemet膜皱褶形成。
虹膜所见:根据类型不同,可出现以下所见2)。
进行性虹膜萎缩
瞳孔偏位:瞳孔被牵拉向PAS较多的方向。
虹膜孔形成:在瞳孔被牵拉的相反方向多发。
葡萄膜外翻:虹膜色素上皮暴露于表面。
PAS:特征为越过Schwalbe线向高处延伸的高脚PAS。
合并青光眼:在3型中最为常见。
Chandler综合征
角膜水肿:即使眼压轻度升高也容易发生,在3型中最为显著。
虹膜表现:瞳孔偏位和虹膜萎缩较轻。未见虹膜孔。
PAS:高度较低。
内皮表现:锤银样外观。镜面显微镜下可见大小不等、异型性广泛。
Cogan-Reese综合征
房角所见:房角镜检查可见越过Schwalbe线向前延伸的PAS,这是ICE综合征的特征性表现5)。PAS呈斑片状且位置非常靠前,PAS之间的小梁网外观正常5)。PAS的形态多样,可呈帐篷状、梯形或广泛粘连。
| 临床类型 | 角膜水肿 | 虹膜所见 | PAS高度 | 青光眼频率 |
|---|---|---|---|---|
| 进行性虹膜萎缩 | 中度 | 孔形成/偏位 | 高 | 最多 |
| Chandler | 显著 | 轻度 | 低 | 中度 |
| Cogan-Reese | 中度 | 色素性结节 | 中度 | 中度 |
ICE综合征的真正病因尚未明确,但有假说认为单纯疱疹病毒(HSV)的潜伏感染在角膜内皮水平引起低度炎症,导致上皮样激活。据报道,PCR检测在ICE患者的角膜和房水样本中超过60%检测到HSV DNA2)。EB病毒(EBV)的参与也被指出。
病理学上,正常内皮细胞被具有迁移特性的上皮样细胞取代。电子显微镜下可见桥粒、张力丝和微绒毛等上皮特征。邻近正常内皮细胞的毒性损伤(坏死性改变)也有报道。
对ICE综合征眼切除的Descemet膜进行病理组织检查,可见低立方细胞单层结构出现部分双层/多层化,免疫组织化学显示上皮标志物(AE1/AE3、CK8/18)和内皮标志物(CD56、vimentin)的混合表达模式7)。这一发现从病理学上证实了ICE综合征的本质——上皮样化生。
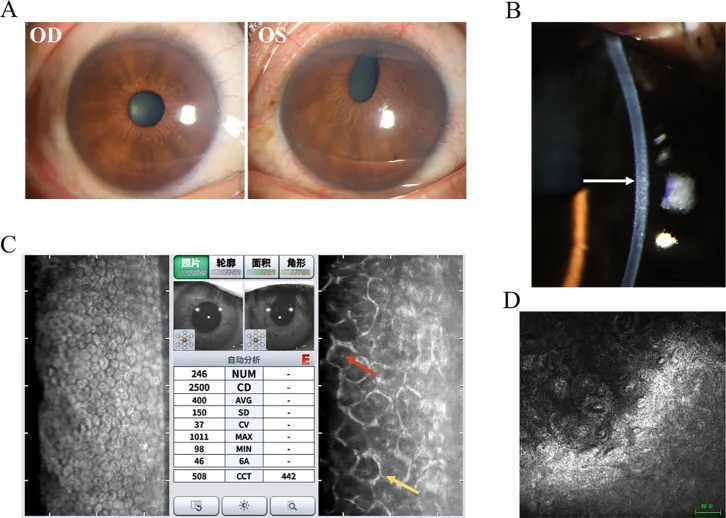
这是确诊ICE综合征最重要的检查2)。通过镜面显微镜观察细胞内具有暗区的异常细胞(ICE细胞)进行诊断。正常的六边形内皮镶嵌结构消失,出现多形性及“明暗反转”现象。特征性表现为比正常更大、更暗的内皮细胞,中央有亮点。
角膜内皮细胞密度显著减少。正常值在年轻人为约3,500 cells/mm²,老年人也有2,500~3,000 cells/mm²,但当降至500 cells/mm²以下时,泵功能会崩溃,导致大疱性角膜病变。有报道称Cogan-Reese综合征的1例病例降至763 cells/mm²3)。
在Chandler综合征中,镜面显微镜检查可广泛观察到细胞大小不一、异型性,内皮细胞边界不清,有助于诊断。变异系数(CV值)≥0.35视为异常,六角形细胞出现率≤50%视为异常。
可显示角膜内皮的鹅卵石样肿胀细胞、六角形结构消失、多形性高亮度细胞、单核/双核巨大内皮细胞2)。在因角膜水肿而难以通过镜面显微镜评估时也很有用。
可显示虹膜角膜角的粘连、角膜内皮层的高亮度增厚、虹膜上的膜样组织2)。在定量评估PAS的范围和高度方面表现出色。
对PAS的评估不可或缺,用于继发性闭角型青光眼的诊断和随访。ICE综合征的特征性表现是PAS超过Schwalbe线,且PAS之间的小梁网外观正常,这有助于与POAG鉴别5)。
眼压测量、视神经乳头照片、视野检查(Humphrey或Goldmann)、OCT视网膜神经纤维层(RNFL)厚度评估应纳入初始精密检查和随访观察2)。
在鉴别ICE综合征时,需排除以下疾病。
| 鉴别疾病 | 鉴别要点 |
|---|---|
| Axenfeld-Rieger综合征 | 双眼性、先天性 |
| 后部多形性角膜营养不良(PPMD) | 双眼性、家族性、无性别差异 |
| 虹膜分离症 | 多见于老年人、无性别差异 |
| Fuchs角膜内皮营养不良 | 双眼性、角膜滴状赘疣 |
| 虹膜恶性黑色素瘤 | 需与Cogan-Reese综合征鉴别 |
向前生长的角膜内皮细胞膜有时会在没有收缩的情况下功能性关闭小梁网。在这种情况下,由于房角镜检查未发现明显的周边虹膜前粘连(PAS),尽管存在“功能性”房角关闭,但仍被误认为是开角型青光眼。当遇到单眼青光眼时,应将ICE综合征纳入鉴别诊断,并应使用镜面显微镜仔细评估角膜内皮。
ICE综合征的治疗包括两个方面:控制青光眼的眼压和处理角膜代偿失调。药物治疗通常难以长期控制眼压,许多病例最终需要手术干预。
内科治疗
外科治疗
当角膜内皮障碍进展导致角膜混浊严重时,适合进行角膜内皮移植。
Saleki等人(2025)发表了首例对ICE综合征施行DMEK的报道7)。对一名60岁男性左眼施行DMEK,裸眼视力从术前的1.1 LogMAR改善至术后2个月的0.54 LogMAR,10个月时达到0.4 LogMAR。眼压稳定在16mmHg,角膜透明度维持了18个月。
作为两步手术方案,有报道先行白内障超声乳化术+人工虹膜植入,6个月后再行DSAEK1)。在一例54岁女性患者中,术后矫正视力从20/100改善至20/32,角膜内皮细胞密度维持在1,640 cells/mm²1)。
Cogan-Reese综合征罕见合并囊样黄斑水肿(CME)3)。有报道局部使用NSAIDs(氟比洛芬每日3次)治疗后消退,但停药后复发3)。
可以同时进行,但对于ICE综合征,有报道采用分阶段进行眼压控制和角膜移植的方法。首先稳定眼压,然后进行角膜内皮移植,有望提高移植片的存活率。青光眼手术和角膜移植的最佳时机应根据具体病例判断1)。
ICE综合征的根本异常在于角膜内皮的上皮样化生。正常的角膜内皮细胞是非增殖性的单层细胞,但在ICE综合征中,这些细胞被具有增殖和迁移能力的上皮样细胞所取代。这一过程与PPMD相同,但ICE是单眼性、散发性,而PPMD是双眼性、常染色体显性遗传。
当角膜内皮出现异常时,膜样组织从角膜背面向房角和虹膜前面增殖,越过Schwalbe线延伸到小梁网上,并进一步扩展到虹膜前面5)。这种膜样组织的收缩会导致以下病理状态。
高耸的周边前粘连(PAS)形成导致房水流出通道阻塞是主要机制5)。此外,膜样组织本身也可能功能性关闭小梁网,即使没有明显的PAS也可能发生青光眼。对药物治疗耐药是因为膜样组织的进展持续存在。
变性的内皮细胞泵功能不全和青光眼引起的眼压升高双重机制参与。在Chandler综合征中,内皮细胞损伤显著,即使眼压在正常范围内也可能发生角膜水肿。当角膜内皮细胞密度降至500 cells/mm²以下时,会导致大疱性角膜病变。
膜样组织收缩牵拉虹膜,导致瞳孔移位、虹膜孔形成和葡萄膜外翻。在进展性虹膜萎缩中最为显著。瞳孔移位偏向PAS较多的方向,虹膜孔则多发生在相反方向。
虹膜结节组织学上由含黑色素的梭形痣细胞组成,Ki-67阳性率低于1%,melan-A阳性,为良性病变4)。罕见情况下伴有晶状体悬韧带脆弱性,白内障手术时可能出现弥漫性悬韧带离断4)。
对ICE综合征眼切除的Descemet膜进行免疫组织化学检查,证实了上皮标志物(AE1/AE3、CK8/18)和内皮标志物(CD56、vimentin)的混合表达模式,这支持上皮样化生是ICE综合征的本质病理7)。与上皮性向下生长(上皮内殖)的鉴别很重要,但需结合临床病程和组织学结果进行判断。