進行性虹膜萎縮
瞳孔偏位:瞳孔被牽引至PAS較多的方向。
虹膜孔形成:在瞳孔被牽引的相反方向多發。
葡萄膜外翻:虹膜色素上皮暴露於表面。
PAS:特徵為越過Schwalbe線高高延伸的高腳PAS。
青光眼合併:在三型中最常見。

ICE症候群(虹膜角膜內皮症候群;iridocorneal endothelial syndrome)是一種因異常角膜內皮細胞伴隨膜狀組織延伸至隅角及虹膜,導致小樑網阻塞而引起眼壓升高的疾病。角膜內皮異常會引起角膜水腫,膜狀組織收縮則導致虹膜異常及周邊虹膜前粘連(PAS)。
好發於30至40歲女性,多為單眼發病2)。無遺傳性,為散發病例。家族史罕見,與其他眼部疾病或全身性疾病無一致關聯。
ICE症候群根據虹膜異常的狀態可分為以下三種臨床類型:
ICE症候群為單眼性、散發性,這與雙眼性、體染色體顯性遺傳的後部多形性角膜失養症(PPMD)和Axenfeld-Rieger症候群是最簡單的鑑別點。
三型的區別主要基於虹膜和角膜的臨床所見。進行性虹膜萎縮以多瞳孔、瞳孔偏位、虹膜孔形成、葡萄膜外翻為顯著,最常合併青光眼。Chandler症候群以角膜水腫為主,虹膜變化輕微,無虹膜孔,PAS高度也較低。Cogan-Reese症候群的特徵為虹膜前面的有莖結節或扁平色素病灶,通常無虹膜萎縮。無論哪一型,基本病理生理學共通,治療方針也相同。
最常見的初發症狀為單眼視力下降(因角膜水腫導致的霧視)。可能自覺畏光或疼痛。也可能因注意到瞳孔偏位、虹膜異色等外觀異常而就診。角膜水腫引起的疼痛與隅角閉鎖導致眼壓升高引起的疼痛可能同時存在。
角膜所見:在Chandler症候群中,角膜內皮會呈現金屬光澤,稱為「hammered silver appearance(錘打銀樣外觀)」。雖然類似於Fuchs角膜內皮營養不良的角膜滴狀粉,但可藉由單眼性來鑑別。即使眼壓在正常範圍內,也可能出現角膜水腫。有時也可見Descemet膜皺褶形成。
虹膜所見:根據類型會出現以下所見2)。
進行性虹膜萎縮
瞳孔偏位:瞳孔被牽引至PAS較多的方向。
虹膜孔形成:在瞳孔被牽引的相反方向多發。
葡萄膜外翻:虹膜色素上皮暴露於表面。
PAS:特徵為越過Schwalbe線高高延伸的高腳PAS。
青光眼合併:在三型中最常見。
Chandler症候群
角膜水腫:即使眼壓輕度上升也容易發生,在三型中最為顯著。
虹膜所見:瞳孔偏位、虹膜萎縮輕微。未見虹膜穿孔。
PAS:高度較低。
內皮所見:錘打銀外觀(hammered silver appearance)。在鏡面顯微鏡下可見大小不一、異型性廣泛。
Cogan-Reese症候群
隅角所見:隅角鏡檢查可見到越過Schwalbe線並向上延伸的PAS,這是ICE症候群的特徵性所見5)。PAS呈斑塊狀且位置非常靠前,PAS之間的線維柱帶看起來正常5)。PAS的形狀多樣,包括帳篷狀、梯形和廣泛粘連等。
| 臨床類型 | 角膜水腫 | 虹膜所見 | PAS高度 | 青光眼發生率 |
|---|---|---|---|---|
| 進行性虹彩萎縮 | 中度 | 孔洞形成、偏移 | 高 | 最多 |
| Chandler | 顯著 | 輕度 | 低 | 中度 |
| Cogan-Reese | 中度 | 有色素結節 | 中度 | 中度 |
ICE症候群的真正病因尚未明確,但有假說認為單純皰疹病毒(HSV)的潛伏感染在角膜內皮層引起低度發炎,導致上皮樣活化。據報導,PCR檢測在ICE患者的角膜和房水樣本中,超過60%檢出HSV DNA2)。EB病毒(EBV)的參與也被指出。
病理學上,正常的內皮細胞被具有遷移特性的上皮樣細胞取代。電子顯微鏡下可觀察到橋粒、張力絲、微絨毛等上皮特徵。相鄰正常內皮細胞的毒性損傷(壞死性變化)也有報導。
在ICE症候群患者切除的Descemet膜病理組織檢查中,可觀察到低立方細胞的單層結構出現部分雙層或多層化,免疫組織化學顯示上皮標記(AE1/AE3、CK8/18)與內皮標記(CD56、vimentin)的混合表現模式7)。此發現從病理學上證實了ICE症候群的本質——上皮樣化生。
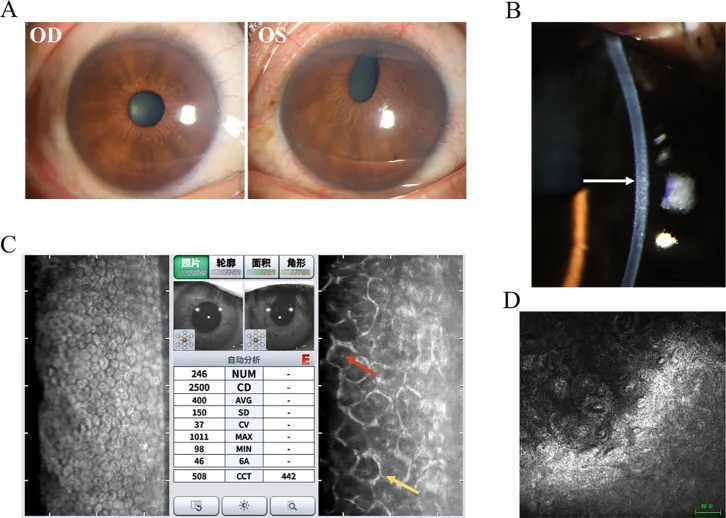
這是確診ICE症候群最重要的檢查2)。透過鏡面顯微鏡觀察細胞內具有暗區的異常細胞(ICE細胞)來進行診斷。正常的六角形內皮鑲嵌結構消失,出現多形性及「明暗反轉」現象。特徵是出現比正常更大、更暗的內皮細胞,中央帶有亮點。
角膜內皮細胞密度顯著減少。正常值在年輕人大約為3,500 cells/mm²,老年人也有2,500~3,000 cells/mm²,但若降至500 cells/mm²以下,幫浦功能會失調,導致水泡性角膜病變。Cogan-Reese症候群的一個病例報告指出,密度曾降至763 cells/mm²3)。
在Chandler症候群中,鏡面顯微鏡檢查可廣泛觀察到細胞大小不一及異型性,且內皮細胞邊界不明顯,有助於診斷。變異係數(CV值)大於0.35視為異常,六角形細胞比率低於50%亦判定為異常。
可描繪角膜內皮的鵝卵石樣腫脹細胞、六角形結構消失、多形性高亮度細胞,以及單核或雙核的巨大內皮細胞2)。在因角膜水腫而難以透過鏡面顯微鏡評估時,此檢查亦有用。
可將虹膜角膜角的沾黏、角膜內皮層的高亮度增厚,以及虹膜上的膜狀組織可視化2)。對於周邊前沾黏(PAS)的範圍與高度之定量評估表現優異。
對於評估周邊前沾黏(PAS)不可或缺,用於續發性閉鎖隅角青光眼的診斷與追蹤。在ICE症候群中,PAS超越Schwalbe線是特徵,且PAS之間的線維柱帶看似正常,此點有助於與原發性開放隅角青光眼(POAG)鑑別5)。
將眼壓測量、視神經盤攝影、視野檢查(Humphrey或Goldmann)、OCT視網膜神經纖維層(RNFL)厚度評估納入初期精密檢查及追蹤觀察2)。
在鑑別ICE症候群時,需排除以下疾病。
| 鑑別疾病 | 鑑別要點 |
|---|---|
| Axenfeld-Rieger症候群 | 雙側性、先天性 |
| 後部多形性角膜失養症(PPMD) | 雙眼性、家族性、無性別差異 |
| 虹膜分離症 | 多見於老年人、無性別差異 |
| 福克斯角膜內皮失養症 | 雙眼性、角膜滴狀粉 |
| 虹膜惡性黑色素瘤 | 需與Cogan-Reese症候群鑑別 |
前移的角膜內皮細胞膜有時會在沒有收縮的情況下功能性關閉小梁網。此時,由於隅角鏡檢查未見明顯的周邊前粘連(PAS),儘管存在「功能性」隅角關閉,仍可能被誤認為開放隅角青光眼。若遇到單眼性青光眼,應將ICE症候群納入鑑別診斷,並使用鏡面顯微鏡仔細評估角膜內皮。
ICE症候群的治療包括兩個主要方面:青光眼的眼壓控制和角膜代償不全的處理。藥物治療通常難以長期控制眼壓,許多病例最終需要手術介入。
內科治療
外科治療
當角膜內皮障礙進展導致角膜混濁嚴重時,適用角膜內皮移植。
Saleki等人(2025)發表了首篇對ICE症候群施行DMEK的報告7)。一名60歲男性左眼接受DMEK,裸眼視力從術前1.1 LogMAR改善至術後2個月0.54 LogMAR,10個月時為0.4 LogMAR。眼壓穩定在16mmHg,角膜透明度維持至18個月。
兩階段手術方法:先進行白內障超聲乳化術+人工虹膜植入,6個月後再進行DSAEK,已有報告1)。一名54歲女性病例,術後矯正視力從20/100改善至20/32,角膜內皮細胞密度維持在1,640 cells/mm²1)。
Cogan-Reese症候群罕見合併囊樣黃斑水腫(CME)3)。有報告指出,局部使用NSAIDs(氟比洛芬每日3次)治療後消退,但停藥後復發3)。
可以同時進行,但對於ICE症候群,有報告建議採取階段性處理眼壓控制和角膜移植的方法。先穩定眼壓再進行角膜內皮移植,可望提高移植片的存活率。青光眼手術和角膜移植的最佳時機應根據個別病例判斷1)。
ICE症候群的根本異常在於角膜內皮的上皮樣化生(epithelialization)。正常的角膜內皮細胞是非增殖性的單層細胞,但在ICE症候群中,這些細胞被具有增殖和遷移能力的上皮樣細胞取代。這個過程也見於PPMD,但ICE是單眼性且散發性,而PPMD是雙眼性且為體染色體顯性遺傳。
當角膜內皮發生異常時,膜樣組織會從角膜內表面向隅角和虹膜前面增生,越過Schwalbe線延伸到小樑網上,再進一步擴展到虹膜前面5)。這種膜樣組織的收縮會導致以下病態。
高聳的周邊前粘連(PAS)形成導致房水流出通道阻塞是主要機轉5)。此外,膜樣組織本身也可能功能性關閉小梁網,即使沒有明顯的PAS,仍可能發生青光眼。對藥物治療產生抗藥性的原因是膜樣組織持續進展。
變性內皮細胞的幫浦功能不全與青光眼引起的眼壓升高,兩重機轉共同參與。在Chandler症候群中,內皮細胞損傷顯著,即使眼壓在正常範圍內也可能發生角膜水腫。當角膜內皮細胞密度降至500 cells/mm²以下時,會導致水泡性角膜病變。
膜樣組織收縮牽拉虹膜,導致瞳孔偏位、虹膜孔形成及葡萄膜外翻。在進行性虹膜萎縮中最為顯著。瞳孔偏位朝向PAS較多的方向,而虹膜孔則多發於相反方向。
虹膜結節組織學上由含黑色素的梭形痣細胞組成,Ki-67陽性率低於1%,melan-A陽性,為良性病變4)。罕見情況下伴隨水晶體小帶脆弱性,白內障手術時可能出現瀰漫性小帶斷裂4)。
對ICE症候群患者切除的Descemet膜進行免疫組織化學檢查,確認了上皮標記(AE1/AE3、CK8/18)和內皮標記(CD56、vimentin)的混合表現模式,這支持了上皮樣化生是ICE症候群本質病變的觀點7)。與上皮性向下生長(上皮性內殖)的鑑別很重要,需結合臨床病程和組織學發現來判斷。