CLAu(结膜角膜缘自体移植)
眼表面再建術
1. 什么是眼表重建术?
Section titled “1. 什么是眼表重建术?”角膜上皮的干细胞位于角膜和结膜交界处的角膜缘(limbus)。角膜缘的栅栏结构(Vogt栅栏,POV)作为干细胞微环境,维持角膜上皮的稳态。
当这些角膜缘干细胞广泛受损时,会发生角膜缘干细胞缺乏症(LSCD)。LSCD时角膜上皮无法再生,结膜上皮侵入角膜表面(结膜化)4),导致角膜混浊、浅层新生血管形成和视力障碍。
常规角膜移植对LSCD无效,因为移植片表面会再次结膜化而失败3)。因此,需要眼表重建术来补充正常的角膜上皮干细胞并稳定眼表。
重建手术的目标不是恢复视力,而是稳定眼表。如果角膜基质混浊仍然存在,在眼表稳定后分两阶段进行全层角膜移植术(PKP)或深板层角膜移植术(DALK)。
适用于角膜缘干细胞广泛受损、结膜上皮侵入角膜的患者。常见原因包括化学烧伤、Stevens-Johnson综合征、眼瘢痕性类天疱疮、无虹膜症等。在结膜侵入仅限于周边部的轻症病例中,首先进行观察。
2. 主要症状与临床所见
Section titled “2. 主要症状与临床所见”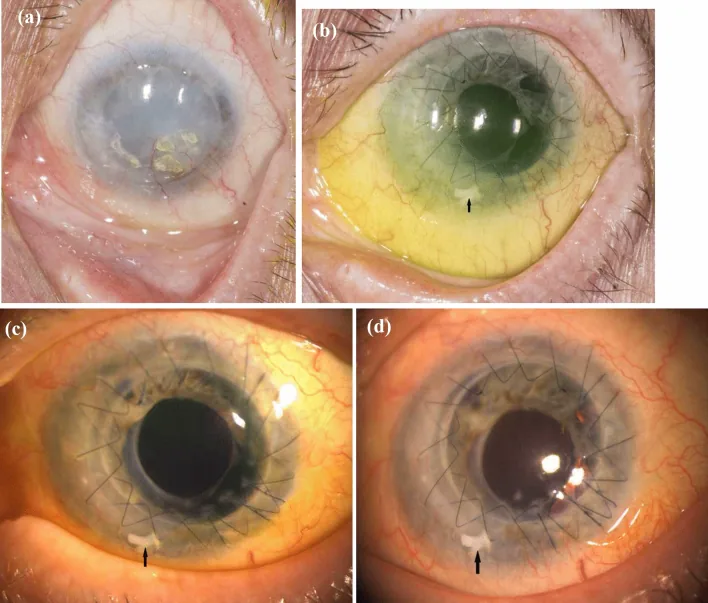
- 视力下降:因结膜化导致的角膜混浊而进行性恶化
- 异物感、眼痛:伴随角膜上皮不稳定
- 畏光:角膜表面不规则引起的光散射
- 流泪:由慢性眼表炎症引起
临床所见(医生检查确认的所见)
Section titled “临床所见(医生检查确认的所见)”LSCD的严重程度根据Deng等人的国际分类1)分为以下三个阶段。
| 分类 | 结膜化范围 | 中央角膜 |
|---|---|---|
| I期 | 角膜缘受累<50% | 非侵袭性 |
| II期 | 角膜缘受累≥50% | 非侵袭性 |
| III期 | 全周性角膜缘受累 | 中央区侵袭 |
主要临床所见如下。
- Vogt栅栏(POV)消失:裂隙灯显微镜下无法观察到角膜缘的栅栏状结构。
- 结膜化:结膜上皮侵入角膜及角膜浅层新生血管。
- 持续性上皮缺损:角膜上皮愈合延迟。
- 角膜基质瘢痕:慢性炎症导致的混浊。
- 睑球粘连:见于重症病例(SJS、眼类天疱疮)。
3. 原因和风险因素
Section titled “3. 原因和风险因素”LSCD的原因多种多样,但化学烧伤最为常见。在自体角膜缘移植的系统综述中,88%的患眼为化学烧伤3)。
主要原因如下所示。
- 化学烧伤(碱/酸):最常见原因。碱因pH升高而渗透至深层,广泛破坏角膜缘干细胞4)。多发生于工作场所,低收入人群多见4)。
- 热烧伤:高温金属、火焰等导致的角膜热凝固。
- Stevens-Johnson综合征(SJS)/ 中毒性表皮坏死松解症(TEN):急性期炎症导致角膜缘损伤。
- 眼瘢痕性类天疱疮:慢性结膜炎和瘢痕化导致角膜缘干细胞消失。
- 无虹膜症:与PAX6基因突变相关的先天性LSCD。
- 多次手术后:反复的翼状胬肉手术等导致角膜缘损伤。
- 隐形眼镜佩戴:长期佩戴罕见但有报道。
4. 诊断和检查方法
Section titled “4. 诊断和检查方法”裂隙灯显微镜检查
Section titled “裂隙灯显微镜检查”这是最基本的诊断方法。评估Vogt栅栏(POV)的消失、结膜化的范围以及浅层新生血管的程度。正常情况下,上方和下方的角膜缘POV易于观察,但10岁以下和70岁以上者可能难以观察。
可视化角膜上皮缺损的范围。结膜化的区域呈现点状染色模式。
采集角膜表面细胞进行免疫染色。角膜上皮标志物细胞角蛋白3(CK3)/CK12的消失和结膜上皮标志物CK13/MUC5AC的表达对LSCD的确诊有用1)。
眼前节光学相干断层扫描(AS-OCT)
Section titled “眼前节光学相干断层扫描(AS-OCT)”可无创评估角膜上皮厚度和结构的变化。结膜化区域显示与正常角膜上皮不同的反射模式。
活体共聚焦显微镜
Section titled “活体共聚焦显微镜”可在细胞水平观察POV结构和基底细胞形态。对角膜上皮和结膜上皮的鉴别也有用,但检查设备仅限部分设施。
5. 标准治疗方法
Section titled “5. 标准治疗方法”治疗策略的确定
Section titled “治疗策略的确定”治疗方法的选择因单眼还是双眼而异。单眼LSCD可从健康眼的角膜缘采集自体组织,但双眼病例无法使用自体角膜缘组织,因此使用口腔黏膜上皮等替代细胞来源。
SLET(简易角膜缘上皮移植术)
CLET(培养角膜缘上皮移植术)
适应症:单眼(少量取材)或活体供体异体移植。
方法:角膜缘上皮细胞在体外培养后以片状移植。
优点:可从微小组织制备大面积片状移植物。
COMET(培养口腔黏膜上皮移植术)
不同术式的疗效
Section titled “不同术式的疗效”Shanbhag等人的系统综述3)对三种自体角膜缘干细胞移植术进行了如下比较。
| 术式 | 解剖学成功率 | 功能性成功率 |
|---|---|---|
| CLAu | 69% | 60% |
| SLET | 78% | 69% |
| CLET | 61% | 52% |
分析:CLAu 22个病例系列(1023眼)、SLET 4项研究(253眼)、CLET 8项研究(581眼)。CLAu组88%、CLET/SLET组90%以上为化学烧伤。SLET和CLAu的解剖学成功率显著高于CLET。3)
SLET + 结膜自体移植(CAG)
Section titled “SLET + 结膜自体移植(CAG)”Mazumdar等人报告了一例因碱烧伤导致单眼LSCD的患者,采用SLET联合结膜自体移植的一期手术进行治疗2)。
24岁男性,碱烧伤后III期LSCD。术后24天角膜上皮化完成,随访24个月最佳矫正视力(BCVA)达到6/12p。该病例显示了一期手术同时修复结膜缺损和重建角膜缘的优势。2)
如果眼表重建后角膜基质混浊仍然存在,则需进行全层角膜移植或DALK。为避免内皮型排斥反应,DALK更为可取。可能需要长期使用免疫抑制剂(环孢素、他克莫司)。
单眼病例可以从健康对侧眼的角膜缘采集角膜上皮干细胞。双眼病例双眼角膜缘均受损,无法采集角膜上皮干细胞。因此,选择使用口腔黏膜上皮等替代细胞源的培养移植(COMET)。
眼表重建的主要目的是稳定眼表,并不保证直接恢复视力。如果角膜实质混浊,需要在重建后进行角膜移植的两阶段治疗。视力改善可能需要数月到一年以上。
6. 病理生理学与详细发病机制
Section titled “6. 病理生理学与详细发病机制”角膜缘干细胞微环境的结构
Section titled “角膜缘干细胞微环境的结构”角膜上皮干细胞存在于角膜缘基底层Vogt栅栏内。Vogt栅栏由间质乳头状突起构成,富含血管和神经。这种微环境(微环境)调控干细胞的自我更新和分化。
干细胞通过不对称分裂进行自我更新,同时产生瞬时扩增细胞(TAC)。TAC向角膜中心方向迁移、分裂和分化,最终成为角膜上皮细胞并从表面脱落。
LSCD的发病机制
Section titled “LSCD的发病机制”当角膜缘干细胞受损时,以下病理过程会连锁发生。
- 角膜上皮补充停止
- 结膜上皮侵入角膜表面(结膜化)
- 杯细胞出现在角膜上(MUC5AC阳性)
- 表层新生血管和慢性炎症
- 角膜基质瘢痕化
结膜化的角膜表面屏障功能下降,反复出现持续性上皮缺损。持续的炎症也可能导致基质溶解或穿孔。
培养上皮片的制备技术
Section titled “培养上皮片的制备技术”在COMET(培养口腔黏膜上皮移植)中,温度响应性培养皿是核心技术1)。培养皿表面的聚(N-异丙基丙烯酰胺)涂层在37°C时疏水,温度降低后变为亲水。这样无需酶处理即可将细胞片从培养皿上剥离,从而在保持细胞间连接和基质的情况下进行移植1)。
利用干细胞标志物进行移植后评估
Section titled “利用干细胞标志物进行移植后评估”在PMC10219018的COMET病例中,对移植后的片和组织进行了免疫组织化学评估1)。
- p63:上皮干细胞标志物。移植片的基底细胞阳性
- p75NTR:神经营养因子受体。在干/祖细胞中表达
- Ki-67:增殖标志物。确认基底层的细胞分裂
- CK3:角膜上皮标志物。评估移植后的上皮分化
- CK4/CK13:口腔黏膜上皮标志物。确认移植物的来源
7. 最新研究与未来展望
Section titled “7. 最新研究与未来展望”日本起源的再生医疗产品
Section titled “日本起源的再生医疗产品”在日本,2021年6月,全球首个COMET产品**Ocural®**被纳入医保1)。Ocural®适用于无睑球粘连的双侧LSCD。对于伴有睑球粘连的病例,则选择Sakracy®1)。
Toshida等人报告了两例Ocural®的初步结果。病例1为79岁男性(双侧III期LSCD),病例2也为双侧LSCD,两例均确认移植成功。移植后的细胞片检测到p63、p75NTR和Ki-67的表达,表明干细胞特性和增殖能力得以维持。1)
对于单侧LSCD,可使用Nepic®(培养的自体角膜缘上皮细胞片)1)。
Holoclar®(欧盟批准)
Section titled “Holoclar®(欧盟批准)”在欧洲,Holoclar®是首个作为欧盟药品获批的培养自体角膜缘上皮移植产品1)。它是LSCD治疗中再生医学的先驱,与日本的Ocural®采用不同的方法(角膜缘上皮来源 vs 口腔黏膜上皮来源)。
SLET + CAG 单阶段手术
Section titled “SLET + CAG 单阶段手术”Mazumdar等人报告,将SLET与结膜自体移植(CAG)单阶段联合实施,可同时实现结膜缺损修复和角膜缘重建。术后24天完全上皮化,24个月时最佳矫正视力改善至6/12p。2)
传统SLET中,结膜缺损处要么暴露巩膜,要么用羊膜覆盖,而同时进行CAG可能提供早期结膜覆盖和稳定的眼表2)。
术式间疗效比较
Section titled “术式间疗效比较”Shanbhag等人的系统综述(1857只眼)显示,自体角膜缘移植总体解剖成功率为69%,功能成功率为61%。按术式分,SLET和CLAu的效果显著优于CLET。但各组间研究质量和样本量存在显著差异,解释时需谨慎。3)
未来需要积累随机对照试验和长期结果。下一代细胞疗法,如iPS细胞来源的角膜上皮细胞片,也处于研究阶段。
培养口腔黏膜上皮的长期挑战
Section titled “培养口腔黏膜上皮的长期挑战”培养的自体口腔黏膜上皮细胞片(CAOMECS)于2004年报道,已被证实作为双侧LSCD的自体移植有效。然而,长期观察发现,部分病例因角膜周边血管侵入导致再次混浊。原因被认为是角膜上皮与口腔黏膜上皮的性质差异,因此根治性治疗更倾向于使用角膜上皮细胞本身。
替代干细胞来源的研究
Section titled “替代干细胞来源的研究”利用角膜缘干细胞以外的细胞源进行角膜再生的研究正在进展中。
- 间充质干细胞(MSC):有报道将骨髓来源的MSC移植到人羊膜上重建大鼠角膜表面。提示抑制炎症和血管新生而非上皮分化可能参与治疗效果。脂肪来源的MSC经角膜基质内注射后已确认分化为功能性角膜基质细胞。
- 牙髓干细胞:从乳牙中分离,表达角膜缘干细胞标志物。在兔模型中显示了眼表面重建,但在人类中的有效性尚未确认。
- 毛囊干细胞:使用角膜和角膜缘基质来源的条件培养基在体外实验中显示了向角膜上皮表型的重编程。
角膜基质中也存在前体细胞,针对角膜内皮,如大疱性角膜病变等新治疗方法的研究也在进行中。
是的,2021年COMET产品Ocural®已被纳入医保。但仅限于拥有日本角膜学会和日本角膜移植学会会员资格并完成指定培训的眼科医生所在的机构。适应症为中度至重度角膜缘干细胞缺乏症。
8. 参考文献
Section titled “8. 参考文献”- Toshida H, Seki T, Kuroda M, et al. Early Clinical Outcomes of the First Commercialized Human Autologous Ex Vivo Cultivated Oral Mucosal Epithelial Cell Sheet Transplantation for Limbal Stem Cell Deficiency. Int J Mol Sci. 2023;24(10):8926.
- Mazumdar S, Trehan HS, Agarwal T, et al. Autologous simple limbal stem cell transplantation with conjunctival autograft in a case of unilateral limbal stem cell deficiency secondary to alkali injury. BMJ Case Rep. 2024;17:e261555.
- Shanbhag SS, Nikpoor N, Patel CN, et al. Autologous limbal stem cell transplantation: a systematic review of clinical outcomes with different surgical techniques. Br J Ophthalmol. 2020;104:247-253.
- Trief D, Prescott C. Limbal stem cell deficiency. Ann Eye Sci. 2023;8:13.
