CLAu (زرع الحوف والملتحمة الذاتي)
المؤشرات: LSCD أحادي العين
الطريقة: أخذ نسيج من حوف وملتحمة العين السليمة لمدة 2-4 ساعات وزرعه في حوف العين المصابة
المزايا: إجراء بمرحلة واحدة ولا يحتاج إلى مختبر زراعة
توجد الخلايا الجذعية لظهارة القرنية في الحوف (limbus)، وهو الحد الفاصل بين القرنية والملتحمة. تعمل الهياكل السياجية للحوف (Palisades of Vogt: POV) كموقع للخلايا الجذعية (بيئة دقيقة) وتحافظ على استقرار ظهارة القرنية.
عندما تتضرر هذه الخلايا الجذعية الحوفية بشكل واسع، يحدث نقص الخلايا الجذعية الحوفية (LSCD). في LSCD، يصبح تجديد ظهارة القرنية مستحيلاً، وتغزو ظهارة الملتحمة سطح القرنية (التحول الملتحمي) 4). ونتيجة لذلك، يتطور عتامة القرنية وتكون الأوعية الدموية السطحية وضعف البصر.
زرع القرنية التقليدي غير فعال في LSCD، حيث يتحول سطح الطعم مرة أخرى إلى ملتحمة ويفشل 3). لذلك، هناك حاجة إلى إعادة بناء سطح العين لتجديد الخلايا الجذعية الطبيعية لظهارة القرنية وتثبيت سطح العين.
هدف إعادة البناء ليس استعادة الرؤية بل تثبيت سطح العين. إذا بقي عتامة في سدى القرنية، يتم إجراء زراعة القرنية كاملة السمك (PKP) أو زراعة القرنية العميقة (DALK) على مرحلتين بعد تثبيت سطح العين.
المرضى المستهدفون هم أولئك الذين يعانون من تلف واسع في الخلايا الجذعية لحوف القرنية مع غزو ظهارة الملتحمة للقرنية. تشمل الأسباب الشائعة الحروق الكيميائية، متلازمة ستيفنز جونسون، الفقاع العيني، وانعدام القزحية. في الحالات الخفيفة حيث يقتصر غزو الملتحمة على المنطقة المحيطية، يتم أولاً المراقبة.
يتم تصنيف شدة LSCD وفقًا للتصنيف الدولي لدينغ وآخرين 1) إلى ثلاث درجات.
| التصنيف | مدى التغطية بالملتحمة | مركز القرنية |
|---|---|---|
| المرحلة الأولى | أقل من 50% من الحوف | غير غازية |
| المرحلة الثانية | 50% أو أكثر من الحوف | غير غازية |
| المرحلة الثالثة | محيطية كاملة | غزو مركزي |
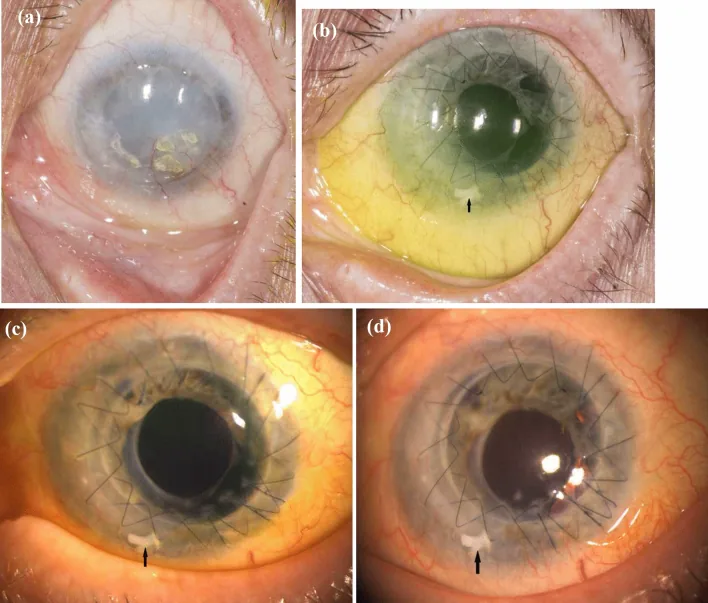
العلامات السريرية الرئيسية هي كما يلي:
تتنوع أسباب LSCD، لكن الحروق الكيميائية هي الأكثر شيوعًا. في مراجعة منهجية لزرع الحوف الذاتي، كانت 88% من العيون المصابة تعاني من حروق كيميائية 3).
فيما يلي الأسباب الرئيسية:
هذه هي الطريقة التشخيصية الأساسية. يتم تقييم اختفاء POV، ومدى التحول الملتحمي، ودرجة الأوعية الدموية السطحية. في الحالة الطبيعية، يمكن ملاحظة POV بسهولة في الحوف العلوي والسفلي، ولكن قد يكون من الصعب ملاحظته لدى الأطفال دون سن 10 سنوات وكبار السن فوق 70 عامًا.
لتحديد مدى عيوب ظهارة القرنية. تظهر المناطق المُلتحمة نمط تلطيخ نقطي.
يتم جمع خلايا سطح القرنية وإجراء التلوين المناعي. اختفاء الكيراتين 3 (CK3)/CK12 كعلامات ظهارة القرنية وظهور علامات ظهارة الملتحمة CK13/MUC5AC مفيد في التشخيص المؤكد لـ LSCD 1).
يمكن تقييم التغيرات في سمك وبنية ظهارة القرنية بطريقة غير جراحية. تظهر المناطق المُلتحمة نمط انعكاس مختلف عن ظهارة القرنية الطبيعية.
يمكن ملاحظة بنية POV وشكل الخلايا القاعدية على المستوى الخلوي. مفيد أيضًا في التمييز بين ظهارة القرنية وظهارة الملتحمة، لكن الأجهزة محدودة التوفر.
يختلف اختيار العلاج بشكل كبير حسب ما إذا كانت الحالة أحادية العين أم ثنائية العين. في LSCD أحادي العين، يمكن أخذ نسيج من الحوف السليم للعين السليمة، أما في الحالة ثنائية العين فلا يتوفر نسيج حوفي ذاتي، لذلك تُستخدم مصادر خلوية بديلة مثل ظهارة الغشاء المخاطي للفم.
CLAu (زرع الحوف والملتحمة الذاتي)
المؤشرات: LSCD أحادي العين
الطريقة: أخذ نسيج من حوف وملتحمة العين السليمة لمدة 2-4 ساعات وزرعه في حوف العين المصابة
المزايا: إجراء بمرحلة واحدة ولا يحتاج إلى مختبر زراعة
SLET (زرع الخلايا الجذعية الحوفية المبسط)
المؤشرات: نقص الخلايا الجذعية الحوفية أحادي العين
الطريقة: يتم أخذ قطعة صغيرة من النسيج الحوفي من العين السليمة وتوزيعها على الغشاء الأمنيوسي وزرعها
المزايا: كمية صغيرة مأخوذة وضغط ضئيل على العين السليمة
CLET (زرع الخلايا الجذعية الحوفية المزروعة)
المؤشرات: أحادي العين (أخذ كمية صغيرة) أو زرع خيفي من متبرع حي
الطريقة: يتم زراعة الخلايا الظهارية الحوفية خارج الجسم الحي وزرعها كصفائح
المزايا: يمكن إنتاج صفائح كبيرة المساحة من نسيج صغير جدًا
COMET (زرع الخلايا الظهارية الفموية المزروعة)
المؤشرات: نقص الخلايا الجذعية الحوفية ثنائي العين
الطريقة: يتم زراعة الخلايا الظهارية الفموية للمريض نفسه خارج الجسم الحي وزرعها كصفائح
المزايا: نظرًا لكونه زرعًا ذاتيًا، فإن رفض الطعم قليل ويمكن استخدامه للحالات ثنائية العين
في المراجعة المنهجية لشانباغ وآخرين 3)، تمت مقارنة التقنيات الجراحية الثلاث لزرع الخلايا الجذعية الحوفية الذاتية على النحو التالي.
| التقنية الجراحية | معدل النجاح التشريحي | معدل النجاح الوظيفي |
|---|---|---|
| CLAu | 69% | 60% |
| SLET | 78% | 69% |
| CLET | 61% | 52% |
تحليل 22 سلسلة حالات CLAu (1023 عينًا)، و4 دراسات SLET (253 عينًا)، و8 دراسات CLET (581 عينًا). 88% من حالات CLAu وأكثر من 90% من حالات CLET وSLET كانت بسبب حروق كيميائية. كان معدل النجاح التشريحي لـ SLET وCLAu أعلى بشكل ملحوظ من CLET. 3)
أبلغ Mazumdar وزملاؤه عن حالة من نقص الخلايا الجذعية الحوفي أحادي الجانب بسبب إصابة قلوية، تم علاجها بجراحة مشتركة في مرحلة واحدة من SLET وتطعيم الملتحمة الذاتي 2).
رجل يبلغ من العمر 24 عامًا، مصاب بنقص الخلايا الجذعية الحوفي من المرحلة الثالثة بعد إصابة قلوية. اكتمل تكون الظهارة القرنية بعد 24 يومًا من الجراحة، وتم تحقيق أفضل حدة بصرية مصححة (BCVA) 6/12p خلال متابعة لمدة 24 شهرًا. أظهرت الجراحة أحادية المرحلة فائدة إصلاح عيب الملتحمة وإعادة بناء الحوف في وقت واحد. 2)
إذا بقي عتامة في سدى القرنية بعد إعادة بناء سطح العين، يتم إضافة زرع القرنية كامل السمك أو DALK. يُفضل DALK لتجنب رفض البطانة. قد تكون هناك حاجة إلى استخدام طويل الأمد للأدوية المثبطة للمناعة (السيكلوسبورين، التاكروليموس).
في الحالات أحادية العين، يمكن أخذ الخلايا الجذعية الظهارية للقرنية من حوف العين السليمة المقابلة. أما في الحالات ثنائية العين، فكلتا العينين مصابتان بتلف الحوف، لذا لا يمكن أخذ الخلايا الجذعية الظهارية للقرنية. لذلك يتم اختيار الزرع المزروع باستخدام مصدر خلوي بديل مثل الظهارة المخاطية الفموية (COMET).
الهدف الرئيسي من إعادة بناء سطح العين هو استقرار سطح العين، وليس ضمان تحسن الرؤية بشكل مباشر. إذا كان هناك عتامة في سدى القرنية، فقد تكون هناك حاجة إلى علاج على مرحلتين يتضمن زرع القرنية بعد إعادة البناء. قد يستغرق تحسن الرؤية من عدة أشهر إلى أكثر من عام.
توجد الخلايا الجذعية الظهارية للقرنية داخل نتوءات الحوف (POV) في الطبقة القاعدية للحوف. تتكون نتوءات الحوف من نتوءات حليمية في السدى، وتحتوي على أوعية دموية وأعصاب غزيرة. تتحكم هذه البيئة الدقيقة (المكانة) في قدرة الخلايا الجذعية على التجديد الذاتي والتمايز.
تتجدد الخلايا الجذعية ذاتيًا من خلال الانقسام غير المتماثل، بينما تنتج أيضًا خلايا عابرة للتضخيم (TAC). تهاجر خلايا TAC نحو مركز القرنية أثناء انقسامها وتمايزها، وتصبح في النهاية خلايا ظهارية قرنية وتتساقط من السطح.
عند تلف الخلايا الجذعية الحوفية، تتطور الحالات المرضية التالية بشكل متسلسل.
سطح القرنية المتلحم يقلل من وظيفة الحاجز، مما يؤدي إلى عيوب ظهارية مستمرة. قد يؤدي الالتهاب المستمر إلى انحلال السدى أو ثقب القرنية.
في COMET (زرع الغشاء المخاطي الفموي المزروع)، تعتبر أطباق الزرع الحساسة لدرجة الحرارة تقنية أساسية 1). طلاء البولي (N-إيزوبروبيل أكريلاميد) على سطح طبق الزرع يكون كارهًا للماء عند 37 درجة مئوية ويتحول إلى محب للماء عند خفض درجة الحرارة. هذا يسمح بفصل الصفيحة الخلوية عن طبق الزرع دون معالجة إنزيمية، مما يتيح الزرع مع الحفاظ على الالتصاقات بين الخلايا والمصفوفة 1).
في حالات COMET من PMC10219018، تم تقييم الصفيحة والأنسجة بعد الزرع باستخدام الكيمياء المناعية النسيجية 1).
في اليابان، تم تغطية أول منتج COMET في العالم Ocural® بالتأمين الصحي في يونيو 2021 1). يُستخدم Ocural® لعلاج LSCD الثنائي بدون Symblepharon (التصاق الجفن بمقلة العين). للحالات المصحوبة بـ Symblepharon، يُختار Sakracy® 1).
أبلغ Toshida وزملاؤه عن النتائج الأولية لحالتين باستخدام Ocural®. الحالة الأولى: رجل يبلغ من العمر 79 عامًا (LSCD ثنائي من المرحلة الثالثة)، والحالة الثانية: LSCD ثنائي أيضًا، وتم تأكيد الاندماج في كلتا الحالتين. أظهرت الصفائح بعد الزرع تعبير p63 وp75NTR وKi-67، مما يشير إلى الحفاظ على خصائص الخلايا الجذعية والقدرة على التكاثر. 1)
بالنسبة لـ LSCD أحادي العين، يمكن استخدام Nepic® (صفائح الخلايا الظهارية للحوف القرنية الذاتية المزروعة) 1).
في أوروبا، تم اعتماد Holoclar® كأول دواء أوروبي لزرع الخلايا الظهارية للحوف القرنية الذاتية المزروعة 1). إنها رائدة في الطب التجديدي لعلاج LSCD، وتتبع نهجًا مختلفًا عن Ocural® الياباني (مشتق من ظهارة الحوف مقابل مشتق من ظهارة الغشاء المخاطي للفم).
في تقرير Mazumdar وزملائه، تم الجمع بين SLET وزرع الملتحمة الذاتي (CAG) في مرحلة واحدة، مما حقق إصلاح عيب الملتحمة وإعادة بناء الحوف في وقت واحد. تمت إعادة الظهارة بالكامل بعد 24 يومًا من الجراحة، وتحسنت حدة البصر المصححة (BCVA) إلى 6/12p بعد 24 شهرًا. 2)
في SLET التقليدية، يُترك عيب الملتحمة مكشوفًا على الصلبة أو يُغطى بالسلى، ولكن إجراء CAG في نفس الوقت قد يوفر تغطية مبكرة للملتحمة وسطح عين مستقر 2).
في المراجعة المنهجية لـ Shanbhag وزملائه (1857 عينًا)، كان معدل النجاح التشريحي الإجمالي لزرع الحوف الذاتي 69%، والنجاح الوظيفي 61%. حسب التقنية، أظهرت SLET وCLAu نتائج أفضل بشكل ملحوظ من CLET. ومع ذلك، كانت هناك اختلافات كبيرة في جودة الدراسة وحجم العينة بين المجموعات، مما يتطلب الحذر في التفسير. 3)
في المستقبل، هناك حاجة إلى تجارب عشوائية محكومة وتراكم نتائج طويلة الأجل. كما أن العلاجات الخلوية من الجيل التالي، مثل صفائح الخلايا الظهارية القرنية المشتقة من الخلايا الجذعية المحفزة (iPS)، لا تزال في مرحلة البحث.
تم الإبلاغ عن صفائح الخلايا الظهارية للغشاء المخاطي للفم المزروعة (CAOMECS) في عام 2004، وتم تأكيد فعاليتها كزرع ذاتي لـ LSCD الثنائي. ومع ذلك، في الملاحظة طويلة الأجل، لوحظ إعادة تعكر في بعض الحالات بسبب غزو الأوعية الدموية من محيط القرنية. يُقترح أن الاختلاف في خصائص ظهارة القرنية وظهارة الغشاء المخاطي للفم هو السبب، ويُعتقد أن استخدام خلايا ظهارة القرنية نفسها هو الأفضل للعلاج الجذري.
يجري البحث في تجديد القرنية باستخدام مصادر خلوية غير الخلايا الجذعية للحوف.
كما تم إظهار وجود خلايا سلفية في سدى القرنية، ويجري البحث في علاجات جديدة لبطانة القرنية، مثل اعتلال القرنية الفقاعي.
نعم، تم تغطية منتج COMET Ocural® بالتأمين في عام 2021. ومع ذلك، لا يمكن استخدامه إلا في المرافق التي يوجد بها أطباء عيون متخصصون ينتمون إلى الجمعية اليابانية للقرنية والجمعية اليابانية لزرع القرنية وقد أكملوا التدريب المحدد. المؤشر هو نقص الخلايا الجذعية للحوف من متوسط إلى شديد.