CLAu (Ghép rìa và kết mạc tự thân)
Chỉ định: LSCD một mắt
Phương pháp: Lấy mô rìa và kết mạc từ mắt lành trong 2-4 giờ và ghép vào rìa mắt bệnh
Ưu điểm: Quy trình một bước và không cần cơ sở nuôi cấy
Tế bào gốc biểu mô giác mạc nằm ở vùng rìa (limbus), ranh giới giữa giác mạc và kết mạc. Cấu trúc hình hàng rào của vùng rìa (Palisades of Vogt: POV) hoạt động như ngách (vi môi trường) của tế bào gốc và duy trì cân bằng nội môi của biểu mô giác mạc.
Khi các tế bào gốc vùng rìa này bị tổn thương rộng, sẽ xảy ra thiếu hụt tế bào gốc vùng rìa (LSCD). Trong LSCD, sự tái tạo biểu mô giác mạc trở nên không thể, và biểu mô kết mạc xâm lấn bề mặt giác mạc (kết mạc hóa) 4). Kết quả là, phát triển đục giác mạc, tân mạch nông và suy giảm thị lực.
Ghép giác mạc thông thường không hiệu quả trong LSCD vì bề mặt mảnh ghép lại bị kết mạc hóa và thất bại 3). Do đó, cần phải tái tạo bề mặt nhãn cầu để bổ sung các tế bào gốc biểu mô giác mạc bình thường và ổn định bề mặt nhãn cầu.
Mục tiêu của tái tạo không phải là phục hồi thị lực mà là ổn định bề mặt nhãn cầu. Nếu vẫn còn đục nhu mô giác mạc, sẽ tiến hành ghép giác mạc toàn phần (PKP) hoặc ghép giác mạc lớp sâu (DALK) theo hai giai đoạn sau khi ổn định bề mặt nhãn cầu.
Bệnh nhân mục tiêu là những người bị tổn thương rộng tế bào gốc vùng rìa giác mạc với sự xâm lấn của biểu mô kết mạc lên giác mạc. Các nguyên nhân phổ biến bao gồm bỏng hóa chất, hội chứng Stevens-Johnson, pemphigoid mắt và vô mống mắt. Trong các trường hợp nhẹ, nơi xâm lấn kết mạc chỉ giới hạn ở vùng ngoại vi, việc theo dõi được thực hiện trước.
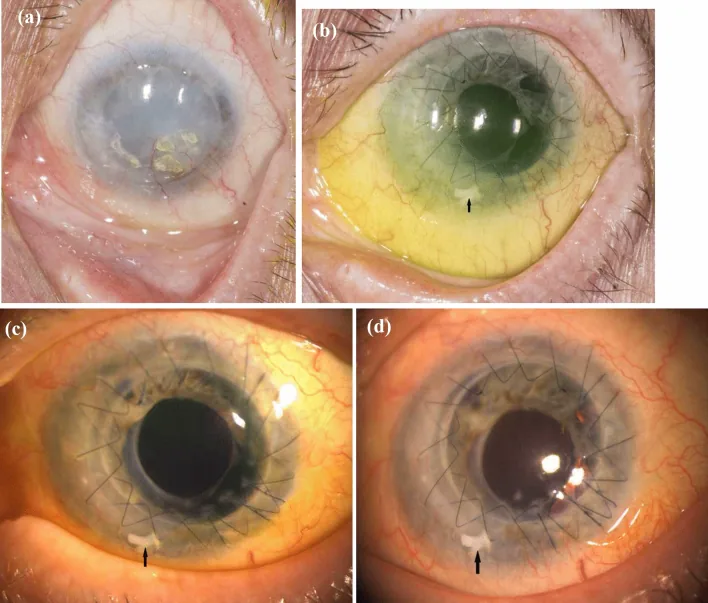
Mức độ nghiêm trọng của LSCD được phân loại thành ba giai đoạn theo phân loại quốc tế của Deng và cộng sự 1).
| Phân loại | Mức độ kết mạc hóa | Giác mạc trung tâm |
|---|---|---|
| Giai đoạn I | Dưới 50% vùng rìa | Không xâm lấn |
| Giai đoạn II | Từ 50% vùng rìa trở lên | Không xâm lấn |
| Giai đoạn III | Toàn bộ chu vi | Xâm lấn trung tâm |
Các dấu hiệu lâm sàng chính như sau:
Nguyên nhân của LSCD rất đa dạng, nhưng bỏng hóa chất là phổ biến nhất. Trong một tổng quan hệ thống về ghép vùng rìa tự thân, 88% số mắt bị ảnh hưởng là do bỏng hóa chất 3).
Dưới đây là các nguyên nhân chính:
Đây là phương pháp chẩn đoán cơ bản nhất. Đánh giá sự mất đi của POV, mức độ kết mạc hóa và mức độ tân mạch nông. Bình thường, POV dễ quan sát ở vùng rìa trên và dưới, nhưng có thể khó quan sát ở trẻ dưới 10 tuổi và người già trên 70 tuổi.
Để hình dung phạm vi khuyết tật biểu mô giác mạc. Các vùng kết mạc hóa cho thấy kiểu nhuộm chấm.
Thu thập tế bào bề mặt giác mạc và thực hiện nhuộm hóa mô miễn dịch. Sự biến mất của cytokeratin 3 (CK3)/CK12 là dấu ấn biểu mô giác mạc và sự xuất hiện của dấu ấn biểu mô kết mạc CK13/MUC5AC hữu ích cho chẩn đoán xác định LSCD 1).
Có thể đánh giá không xâm lấn những thay đổi về độ dày và cấu trúc biểu mô giác mạc. Các vùng kết mạc hóa cho thấy kiểu phản xạ khác với biểu mô giác mạc bình thường.
Có thể quan sát cấu trúc POV và hình thái tế bào đáy ở cấp độ tế bào. Cũng hữu ích để phân biệt biểu mô giác mạc và kết mạc, nhưng thiết bị chỉ có ở một số cơ sở nhất định.
Việc lựa chọn điều trị khác nhau đáng kể tùy thuộc vào một mắt hay hai mắt. Trong LSCD một mắt, có thể lấy mô rìa từ mắt lành, nhưng ở hai mắt không có mô rìa tự thân, do đó sử dụng nguồn tế bào thay thế như biểu mô niêm mạc miệng.
CLAu (Ghép rìa và kết mạc tự thân)
Chỉ định: LSCD một mắt
Phương pháp: Lấy mô rìa và kết mạc từ mắt lành trong 2-4 giờ và ghép vào rìa mắt bệnh
Ưu điểm: Quy trình một bước và không cần cơ sở nuôi cấy
SLET (Ghép biểu mô rìa đơn giản)
Chỉ định: LSCD một mắt
Phương pháp: Lấy một mảnh mô rìa nhỏ từ mắt lành và ghép rải rác trên màng ối
Ưu điểm: Lượng lấy ít, gánh nặng lên mắt lành nhỏ
CLET (Ghép biểu mô rìa nuôi cấy)
Chỉ định: Một mắt (lấy ít) hoặc ghép đồng loại từ người hiến sống
Phương pháp: Tế bào biểu mô rìa được nuôi cấy ex vivo và ghép dưới dạng tấm
Ưu điểm: Có thể tạo tấm diện tích lớn từ mô rất nhỏ
COMET (Ghép biểu mô niêm mạc miệng nuôi cấy)
Chỉ định: LSCD hai mắt
Phương pháp: Tế bào biểu mô niêm mạc miệng của chính bệnh nhân được nuôi cấy ex vivo và ghép dưới dạng tấm
Ưu điểm: Vì là ghép tự thân, ít phản ứng thải ghép và có thể áp dụng cho trường hợp hai mắt
Trong tổng quan hệ thống của Shanbhag và cộng sự 3), ba phương pháp ghép tế bào gốc rìa tự thân được so sánh như sau.
| Phương pháp phẫu thuật | Tỷ lệ thành công về giải phẫu | Tỷ lệ thành công về chức năng |
|---|---|---|
| CLAu | 69% | 60% |
| SLET | 78% | 69% |
| CLET | 61% | 52% |
Phân tích 22 chuỗi ca CLAu (1023 mắt), 4 nghiên cứu SLET (253 mắt), 8 nghiên cứu CLET (581 mắt). 88% đối tượng CLAu và hơn 90% CLET/SLET là bỏng hóa chất. SLET và CLAu có tỷ lệ thành công giải phẫu cao hơn đáng kể so với CLET. 3)
Mazumdar và cộng sự đã báo cáo một trường hợp LSCD một bên do chấn thương kiềm được điều trị bằng SLET và ghép kết mạc tự thân trong một giai đoạn 2).
Nam 24 tuổi, LSCD giai đoạn III sau chấn thương kiềm. Biểu mô hóa giác mạc hoàn tất vào ngày thứ 24 sau phẫu thuật, và đạt thị lực tốt nhất có điều chỉnh (BCVA) 6/12p sau 24 tháng theo dõi. Phẫu thuật một giai đoạn cho thấy lợi ích sửa chữa khuyết kết mạc và tái tạo vùng rìa đồng thời. 2)
Nếu độ mờ nhu mô giác mạc còn tồn tại sau tái tạo bề mặt nhãn cầu, sẽ thực hiện thêm ghép giác mạc xuyên hoặc DALK. DALK được ưa chuộng để tránh thải ghép nội mô. Có thể cần dùng thuốc ức chế miễn dịch dài hạn (cyclosporine, tacrolimus).
Trong trường hợp một mắt, có thể lấy tế bào gốc biểu mô giác mạc từ vùng rìa của mắt lành đối diện. Trong trường hợp hai mắt, cả hai mắt đều bị tổn thương vùng rìa, do đó không thể lấy tế bào gốc biểu mô giác mạc. Vì vậy, ghép nuôi cấy sử dụng nguồn tế bào thay thế như biểu mô niêm mạc miệng (COMET) được lựa chọn.
Mục tiêu chính của tái tạo bề mặt nhãn cầu là ổn định bề mặt nhãn cầu, không đảm bảo phục hồi thị lực trực tiếp. Nếu có đục ở nhu mô giác mạc, có thể cần điều trị hai giai đoạn bao gồm ghép giác mạc sau tái tạo. Cải thiện thị lực có thể mất vài tháng đến hơn một năm.
Tế bào gốc biểu mô giác mạc nằm trong các POV (hàng rào Vogt) ở lớp đáy của vùng rìa. POV được cấu tạo bởi các nhú mô đệm, giàu mạch máu và thần kinh. Vi môi trường (ngách) này điều chỉnh khả năng tự tái tạo và biệt hóa của tế bào gốc.
Tế bào gốc tự tái tạo thông qua phân chia không đối xứng, đồng thời tạo ra tế bào khuếch đại chuyển tiếp (TAC). TAC di chuyển về phía trung tâm giác mạc trong khi phân chia và biệt hóa, cuối cùng trở thành tế bào biểu mô giác mạc và bong ra khỏi bề mặt.
Khi tế bào gốc vùng rìa bị tổn thương, các tình trạng bệnh lý sau đây phát triển theo chuỗi.
Bề mặt giác mạc bị kết mạc hóa có chức năng hàng rào suy giảm, dẫn đến các khuyết hổng biểu mô kéo dài. Viêm dai dẳng có thể gây tiêu nhu mô hoặc thủng.
Trong COMET (Ghép biểu mô niêm mạc miệng nuôi cấy), đĩa nuôi cấy đáp ứng nhiệt là công nghệ cốt lõi 1). Lớp phủ poly(N-isopropylacrylamide) trên bề mặt đĩa nuôi cấy có tính kỵ nước ở 37°C và chuyển sang ưa nước khi nhiệt độ giảm. Điều này cho phép tách mảnh tế bào khỏi đĩa nuôi cấy mà không cần xử lý enzyme, cho phép ghép trong khi vẫn duy trì sự kết dính giữa các tế bào và chất nền 1).
Trong các ca COMET từ PMC10219018, mảnh ghép và mô sau ghép được đánh giá bằng hóa mô miễn dịch 1).
Tại Nhật Bản, vào tháng 6 năm 2021, sản phẩm COMET đầu tiên trên thế giới Ocural® đã được bảo hiểm y tế chi trả 1). Ocural® được chỉ định cho LSCD hai mắt không có Symblepharon (dính mi cầu). Đối với các trường hợp có Symblepharon, Sakracy® được lựa chọn 1).
Toshida và cộng sự đã báo cáo kết quả ban đầu của hai ca sử dụng Ocural®. Ca 1 là nam 79 tuổi (LSCD hai mắt giai đoạn III), ca 2 cũng là LSCD hai mắt, và cả hai đều có sự bám dính mảnh ghép. Các mảnh ghép sau cấy ghép cho thấy biểu hiện p63, p75NTR, Ki-67, cho thấy duy trì đặc tính tế bào gốc và khả năng tăng sinh. 1)
Đối với LSCD một mắt, có thể sử dụng Nepic® (mảnh tế bào biểu mô vùng rìa giác mạc tự thân nuôi cấy) 1).
Tại châu Âu, Holoclar® đã được phê duyệt là thuốc EU đầu tiên cho ghép biểu mô vùng rìa tự thân nuôi cấy 1). Đây là tiên phong trong y học tái tạo điều trị LSCD, với cách tiếp cận khác với Ocural® của Nhật (nguồn gốc biểu mô vùng rìa so với nguồn gốc biểu mô niêm mạc miệng).
Trong báo cáo của Mazumdar và cộng sự, kết hợp SLET và ghép kết mạc tự thân (CAG) trong một thì đã đồng thời sửa chữa khuyết hổng kết mạc và tái tạo vùng rìa. Biểu mô hóa hoàn toàn sau 24 ngày phẫu thuật, và BCVA cải thiện lên 6/12p sau 24 tháng. 2)
Trong SLET thông thường, khuyết hổng kết mạc được để hở trên củng mạc hoặc che phủ bằng màng ối, nhưng thực hiện CAG đồng thời có thể mang lại sự che phủ kết mạc sớm và bề mặt nhãn cầu ổn định 2).
Trong tổng quan hệ thống của Shanbhag và cộng sự (1857 mắt), tỷ lệ thành công về giải phẫu tổng thể của ghép vùng rìa tự thân là 69%, và thành công chức năng là 61%. Theo kỹ thuật, SLET và CLAu cho kết quả tốt hơn đáng kể so với CLET. Tuy nhiên, có sự khác biệt đáng kể về chất lượng nghiên cứu và cỡ mẫu giữa các nhóm, cần thận trọng khi diễn giải. 3)
Trong tương lai, cần có các thử nghiệm ngẫu nhiên có đối chứng và tích lũy kết quả dài hạn. Các liệu pháp tế bào thế hệ tiếp theo, như mảnh biểu mô giác mạc có nguồn gốc từ tế bào iPS, vẫn đang trong giai đoạn nghiên cứu.
Mảnh tế bào biểu mô niêm mạc miệng nuôi cấy (CAOMECS) đã được báo cáo vào năm 2004, và hiệu quả của nó như một ghép tự thân cho LSCD hai mắt đã được xác nhận. Tuy nhiên, trong theo dõi dài hạn, tái đục đã được quan sát thấy ở một số trường hợp do sự xâm nhập mạch máu từ vùng ngoại vi giác mạc. Sự khác biệt về tính chất giữa biểu mô giác mạc và biểu mô niêm mạc miệng được cho là nguyên nhân, và việc sử dụng tế bào biểu mô giác mạc của chính bệnh nhân được coi là mong muốn hơn cho điều trị triệt để.
Nghiên cứu tái tạo giác mạc sử dụng nguồn tế bào khác ngoài tế bào gốc vùng rìa đang được tiến hành.
Sự hiện diện của tế bào tiền thân cũng đã được chứng minh trong mô đệm giác mạc, và nghiên cứu đang được tiến hành cho các liệu pháp mới đối với nội mô giác mạc, như bệnh loạn dưỡng giác mạc bọng nước.
Có, sản phẩm COMET Ocural® đã được bảo hiểm chi trả vào năm 2021. Tuy nhiên, chỉ có thể sử dụng tại các cơ sở có bác sĩ nhãn khoa là thành viên của Hiệp hội Giác mạc Nhật Bản và Hiệp hội Ghép giác mạc Nhật Bản và đã hoàn thành khóa đào tạo quy định. Chỉ định là thiếu hụt tế bào gốc vùng rìa mức độ trung bình đến nặng.