CLAu(結膜角膜緣自體移植)
眼表面再建術
1. 什麼是眼表重建術?
Section titled “1. 什麼是眼表重建術?”角膜上皮的幹細胞位於角膜和結膜交界處的角膜緣(limbus)。角膜緣的柵欄結構(Vogt柵欄,POV)作為幹細胞微環境,維持角膜上皮的恆定。
當這些角膜緣幹細胞廣泛受損時,會發生角膜緣幹細胞缺乏症(LSCD)。LSCD時角膜上皮無法再生,結膜上皮侵入角膜表面(結膜化)4),導致角膜混濁、淺層新生血管形成和視力障礙。
常規角膜移植對LSCD無效,因為移植片表面會再次結膜化而失敗3)。因此,需要眼表重建術來補充正常的角膜上皮幹細胞並穩定眼表。
重建手術的目標不是恢復視力,而是穩定眼表。如果角膜基質混濁仍然存在,在眼表穩定後分兩階段進行全層角膜移植術(PKP)或深板層角膜移植術(DALK)。
適用於角膜緣幹細胞廣泛受損、結膜上皮侵入角膜的患者。常見原因包括化學燒傷、Stevens-Johnson症候群、眼瘢痕性類天皰瘡、無虹膜症等。在結膜侵入僅限於周邊部的輕症病例中,首先進行觀察。
2. 主要症狀與臨床所見
Section titled “2. 主要症狀與臨床所見”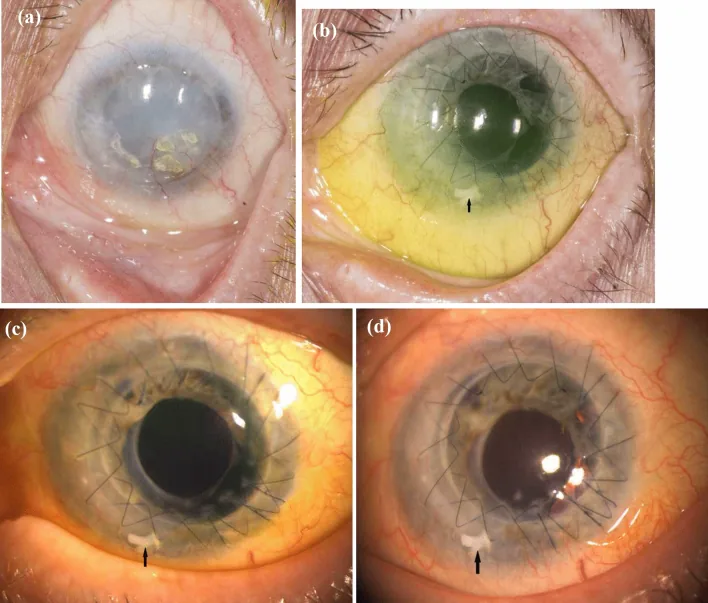
- 視力下降:因結膜化導致的角膜混濁而進行性惡化
- 異物感、眼痛:伴隨角膜上皮不穩定
- 畏光:角膜表面不規則引起的光散射
- 流淚:由慢性眼表炎症引起
臨床所見(醫師檢查確認的所見)
Section titled “臨床所見(醫師檢查確認的所見)”LSCD的嚴重程度根據Deng等人的國際分類1)分為以下三個階段。
| 分類 | 結膜化範圍 | 中央角膜 |
|---|---|---|
| 第I期 | 輪部受累<50% | 非侵襲性 |
| 第II期 | 輪部受累≥50% | 非侵襲性 |
| 第III期 | 全周性輪部受累 | 中央侵襲 |
主要臨床所見如下。
- Vogt柵欄(POV)消失:裂隙燈顯微鏡下無法觀察到輪部的柵欄狀結構。
- 結膜化:結膜上皮侵入角膜及角膜表層新生血管。
- 持續性上皮缺損:角膜上皮癒合延遲。
- 角膜基質疤痕:慢性炎症導致的混濁。
- 瞼球黏連:見於重症病例(SJS、眼類天皰瘡)。
3. 原因與風險因素
Section titled “3. 原因與風險因素”LSCD的原因多種多樣,但化學燒傷最為常見。在自體角膜緣移植的系統性回顧中,88%的患眼為化學燒傷3)。
主要原因如下所示。
- 化學燒傷(鹼/酸):最常見原因。鹼因pH升高而滲透至深層,廣泛破壞角膜緣幹細胞4)。多發生於工作場所,低收入族群多見4)。
- 熱燒傷:高溫金屬、火焰等導致的角膜熱凝固。
- Stevens-Johnson症候群(SJS)/ 中毒性表皮壞死鬆解症(TEN):急性期發炎導致角膜緣損傷。
- 眼瘢痕性類天皰瘡:慢性結膜炎和瘢痕化導致角膜緣幹細胞消失。
- 無虹膜症:與PAX6基因突變相關的先天性LSCD。
- 多次手術後:反覆的翼狀胬肉手術等導致角膜緣損傷。
- 隱形眼鏡佩戴:長期佩戴罕見但有報告。
4. 診斷與檢查方法
Section titled “4. 診斷與檢查方法”裂隙燈顯微鏡檢查
Section titled “裂隙燈顯微鏡檢查”這是最基本的診斷方法。評估Vogt柵欄(POV)的消失、結膜化的範圍以及淺層新生血管的程度。正常情況下,上方和下方的角膜緣POV易於觀察,但10歲以下和70歲以上者可能難以觀察。
可視化角膜上皮缺損的範圍。結膜化的區域呈現點狀染色模式。
採集角膜表面細胞進行免疫染色。角膜上皮標誌物細胞角蛋白3(CK3)/CK12的消失和結膜上皮標誌物CK13/MUC5AC的表現對LSCD的確診有用1)。
眼前段光學相干斷層掃描(AS-OCT)
Section titled “眼前段光學相干斷層掃描(AS-OCT)”可非侵入性評估角膜上皮厚度和結構的變化。結膜化區域顯示與正常角膜上皮不同的反射模式。
活體共軛焦顯微鏡
Section titled “活體共軛焦顯微鏡”可在細胞層級觀察POV結構和基底細胞形態。對角膜上皮和結膜上皮的鑑別也有用,但檢查設備僅限部分設施。
5. 標準治療方法
Section titled “5. 標準治療方法”治療策略的決定
Section titled “治療策略的決定”治療方法的選擇因單眼或雙眼而異。單眼LSCD可從健康眼的角膜緣採集自體組織,但雙眼病例無法使用自體角膜緣組織,因此使用口腔黏膜上皮等替代細胞來源。
SLET(簡易輪部上皮移植術)
CLET(培養輪部上皮移植術)
適應症:單眼(少量取樣)或活體捐贈者異體移植。
方法:輪部上皮細胞在體外培養後以片狀移植。
優點:可從微小組織製備大面積片狀移植物。
COMET(培養口腔黏膜上皮移植術)
不同術式的療效
Section titled “不同術式的療效”Shanbhag等人的系統性回顧3)對三種自體輪部幹細胞移植術進行了如下比較。
| 術式 | 解剖學成功率 | 功能性成功率 |
|---|---|---|
| CLAu | 69% | 60% |
| SLET | 78% | 69% |
| CLET | 61% | 52% |
分析:CLAu 22個病例系列(1023眼)、SLET 4項研究(253眼)、CLET 8項研究(581眼)。CLAu組88%、CLET/SLET組90%以上為化學燒傷。SLET和CLAu的解剖學成功率顯著高於CLET。3)
SLET + 結膜自體移植(CAG)
Section titled “SLET + 結膜自體移植(CAG)”Mazumdar等人報告了一例因鹼燒傷導致單眼LSCD的患者,採用SLET聯合結膜自體移植的一期手術進行治療2)。
24歲男性,鹼燒傷後III期LSCD。術後24天角膜上皮化完成,追蹤24個月最佳矯正視力(BCVA)達到6/12p。該病例顯示了一期手術同時修復結膜缺損和重建角膜緣的優勢。2)
如果眼表重建後角膜基質混濁仍然存在,則需進行全層角膜移植或DALK。為避免內皮型排斥反應,DALK更為可取。可能需要長期使用免疫抑制劑(環孢素、他克莫司)。
單眼病例可以從健康對側眼的角膜緣採集角膜上皮幹細胞。雙眼病例雙眼角膜緣均受損,無法採集角膜上皮幹細胞。因此,選擇使用口腔黏膜上皮等替代細胞源的培養移植(COMET)。
眼表重建的主要目的是穩定眼表,並不保證直接恢復視力。如果角膜實質混濁,需要在重建後進行角膜移植的兩階段治療。視力改善可能需要數月到一年以上。
6. 病理生理學與詳細發病機制
Section titled “6. 病理生理學與詳細發病機制”角膜緣幹細胞微環境的結構
Section titled “角膜緣幹細胞微環境的結構”角膜上皮幹細胞存在於角膜緣基底層Vogt柵欄內。Vogt柵欄由間質乳頭狀突起構成,富含血管和神經。這種微環境(微環境)調控幹細胞的自我更新和分化。
幹細胞通過不對稱分裂進行自我更新,同時產生瞬時擴增細胞(TAC)。TAC向角膜中心方向遷移、分裂和分化,最終成為角膜上皮細胞並從表面脫落。
LSCD的發病機制
Section titled “LSCD的發病機制”當角膜緣幹細胞受損時,以下病理過程會連鎖發生。
- 角膜上皮補充停止
- 結膜上皮侵入角膜表面(結膜化)
- 杯狀細胞出現在角膜上(MUC5AC陽性)
- 表層新生血管和慢性發炎
- 角膜基質瘢痕化
結膜化的角膜表面屏障功能下降,反覆出現持續性上皮缺損。持續的發炎也可能導致基質溶解或穿孔。
培養上皮片的製備技術
Section titled “培養上皮片的製備技術”在COMET(培養口腔黏膜上皮移植)中,溫度響應性培養皿是核心技術1)。培養皿表面的聚(N-異丙基丙烯醯胺)塗層在37°C時疏水,溫度降低後變為親水。這樣無需酶處理即可將細胞片從培養皿上剝離,從而在保持細胞間連接和基質的情況下進行移植1)。
利用幹細胞標誌物進行移植後評估
Section titled “利用幹細胞標誌物進行移植後評估”在PMC10219018的COMET病例中,對移植後的片和組織進行了免疫組織化學評估1)。
- p63:上皮幹細胞標誌物。移植片的基底細胞陽性
- p75NTR:神經營養因子受體。在幹/祖細胞中表達
- Ki-67:增殖標誌物。確認基底層的細胞分裂
- CK3:角膜上皮標誌物。評估移植後的上皮分化
- CK4/CK13:口腔黏膜上皮標誌物。確認移植物的來源
7. 最新研究與未來展望
Section titled “7. 最新研究與未來展望”日本起源的再生醫療產品
Section titled “日本起源的再生醫療產品”在日本,2021年6月,全球首個COMET產品**Ocural®**被納入健保1)。Ocural®適用於無眼瞼球黏連的雙側LSCD。對於伴有眼瞼球黏連的病例,則選擇Sakracy®1)。
Toshida等人報告了兩例Ocural®的初步結果。病例1為79歲男性(雙側III期LSCD),病例2也為雙側LSCD,兩例均確認移植成功。移植後的細胞片檢測到p63、p75NTR和Ki-67的表達,表明幹細胞特性和增殖能力得以維持。1)
對於單側LSCD,可使用Nepic®(培養的自體角膜緣上皮細胞片)1)。
Holoclar®(歐盟核准)
Section titled “Holoclar®(歐盟核准)”在歐洲,Holoclar®是首個作為歐盟藥品核准的培養自體角膜緣上皮移植產品1)。它是LSCD治療中再生醫學的先驅,與日本的Ocural®採用不同的方法(角膜緣上皮來源 vs 口腔黏膜上皮來源)。
SLET + CAG 單階段手術
Section titled “SLET + CAG 單階段手術”Mazumdar等人報告,將SLET與結膜自體移植(CAG)單階段聯合實施,可同時實現結膜缺損修復和角膜緣重建。術後24天完全上皮化,24個月時最佳矯正視力改善至6/12p。2)
傳統SLET中,結膜缺損處要麼暴露鞏膜,要麼用羊膜覆蓋,而同時進行CAG可能提供早期結膜覆蓋和穩定的眼表2)。
術式間療效比較
Section titled “術式間療效比較”Shanbhag等人的系統性回顧(1857隻眼)顯示,自體角膜緣移植總體解剖成功率為69%,功能成功率為61%。按術式分,SLET和CLAu的效果顯著優於CLET。但各組間研究品質和樣本數存在顯著差異,解釋時需謹慎。3)
未來需要累積隨機對照試驗和長期結果。下一代細胞療法,如iPS細胞來源的角膜上皮細胞片,也處於研究階段。
培養口腔黏膜上皮的長期挑戰
Section titled “培養口腔黏膜上皮的長期挑戰”培養的自體口腔黏膜上皮細胞片(CAOMECS)於2004年報導,已被證實作為雙側LSCD的自體移植有效。然而,長期觀察發現,部分病例因角膜周邊血管侵入導致再次混濁。原因被認為是角膜上皮與口腔黏膜上皮的性質差異,因此根治性治療更傾向於使用角膜上皮細胞本身。
替代幹細胞來源的研究
Section titled “替代幹細胞來源的研究”利用角膜緣幹細胞以外的細胞源進行角膜再生的研究正在進展中。
- 間質幹細胞(MSC):有報告將骨髓來源的MSC移植到人類羊膜上重建大鼠角膜表面。提示抑制發炎和血管新生而非上皮分化可能參與治療效果。脂肪來源的MSC經角膜基質內注射後已確認分化為功能性角膜基質細胞。
- 牙髓幹細胞:從乳牙中分離,表現角膜緣幹細胞標記物。在兔模型中顯示了眼表面重建,但在人類中的有效性尚未確認。
- 毛囊幹細胞:使用角膜和角膜緣基質來源的條件培養基在體外實驗中顯示了向角膜上皮表型的重新編程。
角膜基質中也存在前驅細胞,針對角膜內皮,如水泡性角膜病變等新治療方法的研究也在進行中。
是的,2021年COMET產品Ocural®已被納入健保。但僅限於擁有日本角膜學會和日本角膜移植學會會員資格並完成指定訓練的眼科醫生所在的機構。適應症為中度至重度角膜緣幹細胞缺乏症。
8. 參考文獻
Section titled “8. 參考文獻”- Toshida H, Seki T, Kuroda M, et al. Early Clinical Outcomes of the First Commercialized Human Autologous Ex Vivo Cultivated Oral Mucosal Epithelial Cell Sheet Transplantation for Limbal Stem Cell Deficiency. Int J Mol Sci. 2023;24(10):8926.
- Mazumdar S, Trehan HS, Agarwal T, et al. Autologous simple limbal stem cell transplantation with conjunctival autograft in a case of unilateral limbal stem cell deficiency secondary to alkali injury. BMJ Case Rep. 2024;17:e261555.
- Shanbhag SS, Nikpoor N, Patel CN, et al. Autologous limbal stem cell transplantation: a systematic review of clinical outcomes with different surgical techniques. Br J Ophthalmol. 2020;104:247-253.
- Trief D, Prescott C. Limbal stem cell deficiency. Ann Eye Sci. 2023;8:13.
