CLAu (การปลูกถ่ายลิมบัสและเยื่อบุตาตัวเอง)
ข้อบ่งชี้: LSCD ข้างเดียว
วิธีการ: เก็บเนื้อเยื่อลิมบัสและเยื่อบุตาจากตาข้างดีเป็นเวลา 2-4 ชั่วโมง และปลูกถ่ายไปยังลิมบัสของตาที่เป็นโรค
ข้อดี: ขั้นตอนเดียวและไม่ต้องใช้สถานที่เพาะเลี้ยง
สเต็มเซลล์ของเยื่อบุกระจกตาอยู่ที่ลิมบัส (limbus) ซึ่งเป็นรอยต่อระหว่างกระจกตาและเยื่อบุตา โครงสร้างรั้วของลิมบัส (Palisades of Vogt: POV) ทำหน้าที่เป็นแหล่งที่อยู่ ( microenvironment) ของสเต็มเซลล์และรักษาสมดุลของเยื่อบุกระจกตา
เมื่อสเต็มเซลล์ลิมบัสเหล่านี้ถูกทำลายอย่างกว้างขวาง จะเกิดภาวะขาดสเต็มเซลล์ลิมบัส (LSCD) ใน LSCD การสร้างใหม่ของเยื่อบุกระจกตาเป็นไปไม่ได้ และเยื่อบุตาจะรุกรานพื้นผิวกระจกตา (conjunctivalization) 4) ผลที่ตามมาคือ เกิดความขุ่นของกระจกตา หลอดเลือด新生ที่ผิว และการมองเห็นบกพร่อง
การปลูกถ่ายกระจกตาแบบทั่วไปไม่ได้ผลใน LSCD เนื่องจากพื้นผิวของ graft จะเกิด conjunctivalization อีกครั้งและล้มเหลว 3) ดังนั้น จึงจำเป็นต้องสร้างพื้นผิวตาขึ้นใหม่เพื่อเติมสเต็มเซลล์เยื่อบุกระจกตาปกติและทำให้พื้นผิวตาคงที่
เป้าหมายของการสร้างใหม่ไม่ใช่การฟื้นฟูการมองเห็น แต่คือ การทำให้ผิวตาคงที่ หากยังมีความขุ่นของเนื้อกระจกตาเหลืออยู่ จะทำการปลูกถ่ายกระจกตาทั้งชั้น (PKP) หรือการปลูกถ่ายกระจกตาชั้นลึก (DALK) แบบสองขั้นตอนหลังจากผิวตาคงที่แล้ว
ผู้ป่วยเป้าหมายคือผู้ที่มีความเสียหายอย่างกว้างขวางต่อสเต็มเซลล์บริเวณลิมบัสของกระจกตา โดยมีเยื่อบุตาลุกลามเข้าสู่กระจกตา สาเหตุทั่วไป ได้แก่ แผลไหม้จากสารเคมี, กลุ่มอาการสตีเวนส์-จอห์นสัน, เพมฟิกอยด์ที่ตา, และภาวะไม่มีม่านตา ในกรณีที่ไม่รุนแรงซึ่งการลุกลามของเยื่อบุตาจำกัดอยู่เฉพาะบริเวณรอบนอก จะทำการสังเกตอาการก่อน
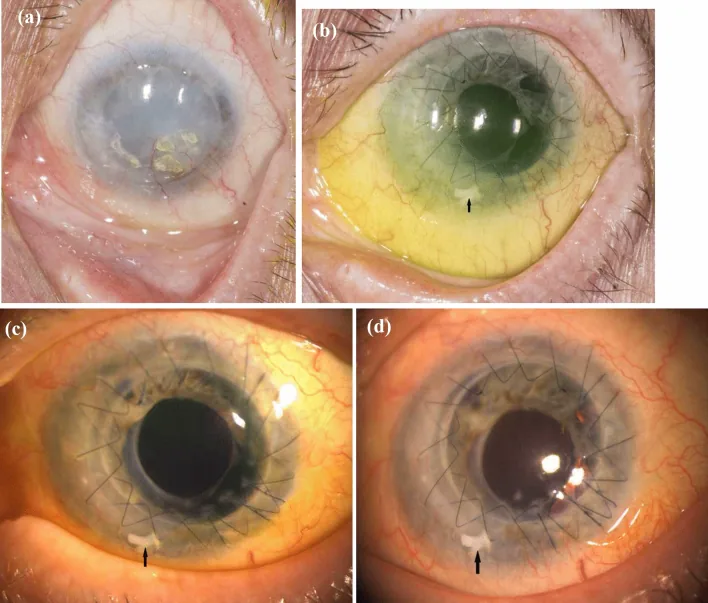
ความรุนแรงของ LSCD แบ่งออกเป็นสามระยะตามการจำแนกระหว่างประเทศของ Deng และคณะ 1)
| การจำแนก | ขอบเขตการถูกเยื่อบุตาคลุม | กระจกตาส่วนกลาง |
|---|---|---|
| ระยะที่ I | น้อยกว่า 50% ของลิมบัส | ไม่ลุกลาม |
| ระยะที่ II | 50% หรือมากกว่าของลิมบัส | ไม่ลุกลาม |
| ระยะที่ III | รอบทั้งหมด | ลุกลามเข้าสู่ศูนย์กลาง |
อาการแสดงทางคลินิกที่สำคัญมีดังนี้:
สาเหตุของ LSCD มีหลากหลาย แต่ที่พบบ่อยที่สุดคือ แผลไหม้จากสารเคมี ในการทบทวนวรรณกรรมอย่างเป็นระบบเกี่ยวกับการปลูกถ่ายลิมบัสแบบอัตโนมัติ พบว่า 88% ของดวงตาที่ได้รับผลกระทบเป็นแผลไหม้จากสารเคมี 3)
สาเหตุหลักแสดงไว้ด้านล่าง:
นี่เป็นวิธีการวินิจฉัยพื้นฐานที่สุด ประเมินการหายไปของ POV ขอบเขตของการเปลี่ยนเป็นเยื่อบุตา และระดับของเส้นเลือดใหม่ที่ผิว ปกติแล้ว POV จะสังเกตได้ง่ายที่ลิมบัสด้านบนและด้านล่าง แต่อาจสังเกตได้ยากในเด็กอายุต่ำกว่า 10 ปีและผู้สูงอายุที่อายุมากกว่า 70 ปี
เพื่อให้เห็นขอบเขตของความบกพร่องของเยื่อบุกระจกตา บริเวณที่มีการเปลี่ยนเป็นเยื่อบุตาจะแสดงรูปแบบการย้อมแบบจุด
เก็บเซลล์ผิวกระจกตาและทำการย้อมอิมมูโน การหายไปของไซโตเคราติน 3 (CK3)/CK12 ซึ่งเป็นเครื่องหมายของเยื่อบุกระจกตา และการปรากฏของเครื่องหมายของเยื่อบุตา CK13/MUC5AC มีประโยชน์ในการวินิจฉัยยืนยัน LSCD 1)
สามารถประเมินการเปลี่ยนแปลงความหนาและโครงสร้างของเยื่อบุกระจกตาแบบไม่รุกราน บริเวณที่มีการเปลี่ยนเป็นเยื่อบุตาจะแสดงรูปแบบการสะท้อนที่แตกต่างจากเยื่อบุกระจกตาปกติ
สามารถสังเกตโครงสร้าง POV และสัณฐานวิทยาของเซลล์ฐานในระดับเซลล์ นอกจากนี้ยังมีประโยชน์ในการแยกแยะเยื่อบุกระจกตาและเยื่อบุตา แต่อุปกรณ์มีจำกัดเฉพาะในบางสถานที่
การเลือกวิธีการรักษาแตกต่างกันอย่างมากขึ้นอยู่กับว่าเป็น ข้างเดียวหรือสองข้าง ใน LSCD ข้างเดียว สามารถเก็บเนื้อเยื่อลิมบัสจากตาข้างดีได้ แต่ในกรณีสองข้างไม่มีเนื้อเยื่อลิมบัส自体 จึงใช้แหล่งเซลล์อื่น เช่น เยื่อบุช่องปาก
CLAu (การปลูกถ่ายลิมบัสและเยื่อบุตาตัวเอง)
ข้อบ่งชี้: LSCD ข้างเดียว
วิธีการ: เก็บเนื้อเยื่อลิมบัสและเยื่อบุตาจากตาข้างดีเป็นเวลา 2-4 ชั่วโมง และปลูกถ่ายไปยังลิมบัสของตาที่เป็นโรค
ข้อดี: ขั้นตอนเดียวและไม่ต้องใช้สถานที่เพาะเลี้ยง
SLET (การปลูกถ่ายเยื่อบุลิมบัสแบบง่าย)
ข้อบ่งชี้: LSCD ข้างเดียว
วิธีการ: เก็บชิ้นเนื้อเยื่อลิมบัสขนาดเล็กจากตาที่แข็งแรง และปลูกถ่ายกระจายบนเยื่อหุ้มน้ำคร่ำ
ข้อดี: ปริมาณที่เก็บน้อย ภาระต่อตาที่แข็งแรงน้อย
CLET (การปลูกถ่ายเยื่อบุลิมบัสที่เพาะเลี้ยง)
ข้อบ่งชี้: ข้างเดียว (เก็บน้อย) หรือการปลูกถ่ายอัลโลจากผู้บริจาคที่มีชีวิต
วิธีการ: เพาะเลี้ยงเซลล์เยื่อบุลิมบัสนอกร่างกาย และปลูกถ่ายเป็นแผ่น
ข้อดี: สามารถสร้างแผ่นพื้นที่ขนาดใหญ่จากเนื้อเยื่อขนาดเล็กมาก
COMET (การปลูกถ่ายเยื่อบุช่องปากที่เพาะเลี้ยง)
ข้อบ่งชี้: LSCD สองข้าง
วิธีการ: เพาะเลี้ยงเซลล์เยื่อบุช่องปากของผู้ป่วยเองนอกร่างกาย และปลูกถ่ายเป็นแผ่น
ข้อดี: เนื่องจากเป็นการปลูกถ่ายตนเอง ปฏิกิริยาการปฏิเสธน้อย และสามารถใช้กับกรณีสองข้างได้
ในการทบทวนอย่างเป็นระบบโดย Shanbhag และคณะ 3) ได้เปรียบเทียบเทคนิคการปลูกถ่ายสเต็มเซลล์ลิมบัสแบบอัตโนมัติสามวิธีดังนี้
| เทคนิคการผ่าตัด | อัตราความสำเร็จทางกายวิภาค | อัตราความสำเร็จทางการทำงาน |
|---|---|---|
| CLAu | 69% | 60% |
| SLET | 78% | 69% |
| CLET | 61% | 52% |
การวิเคราะห์จาก 22 ชุดผู้ป่วย CLAu (1023 ตา), 4 การศึกษา SLET (253 ตา), 8 การศึกษา CLET (581 ตา) 88% ของผู้ป่วย CLAu และมากกว่า 90% ของ CLET/SLET เป็นแผลไหม้จากสารเคมี SLET และ CLAu มีอัตราความสำเร็จทางกายวิภาคสูงกว่า CLET อย่างมีนัยสำคัญ 3)
Mazumdar และคณะรายงานผู้ป่วย LSCD ข้างเดียวจากการบาดเจ็บจากด่าง ซึ่งรักษาด้วย SLET และการปลูกถ่ายเยื่อบุตาด้วยตนเองในขั้นตอนเดียว 2)
ชายอายุ 24 ปี LSCD ระยะ III หลังการบาดเจ็บจากด่าง การสร้างเยื่อบุกระจกตาเสร็จสมบูรณ์ในวันที่ 24 หลังผ่าตัด และบรรลุค่าสายตาที่ดีที่สุดที่แก้ไขแล้ว (BCVA) 6/12p ในการติดตามผล 24 เดือน การผ่าตัดขั้นตอนเดียวแสดงให้เห็นข้อดีของการซ่อมแซมข้อบกพร่องของเยื่อบุตาและการสร้างลิมบัสใหม่พร้อมกัน 2)
หากยังมีความขุ่นของสโตรมากระจกตาหลังการสร้างพื้นผิวลูกตาขึ้นใหม่ ให้เพิ่มการปลูกถ่ายกระจกตาทั้งชั้นหรือ DALK DALK เป็นที่ต้องการเพื่อหลีกเลี่ยงการปฏิเสธชั้น内皮 อาจจำเป็นต้องใช้ยากดภูมิคุ้มกันระยะยาว (cyclosporine, tacrolimus)
ในกรณีตาเดียว สามารถเก็บสเต็มเซลล์เยื่อบุกระจกตาจากลิมบัสของตาที่แข็งแรงข้างตรงข้ามได้ ในกรณีสองตา ลิมบัสของทั้งสองข้างเสียหาย จึงไม่สามารถเก็บสเต็มเซลล์เยื่อบุกระจกตาได้ ดังนั้นจึงเลือกการปลูกถ่ายเพาะเลี้ยงโดยใช้แหล่งเซลล์อื่น เช่น เยื่อบุช่องปาก (COMET)
เป้าหมายหลักของการสร้างพื้นผิวตาใหม่คือการทำให้พื้นผิวตาคงที่ ไม่ใช่การรับประกันการฟื้นฟูการมองเห็นโดยตรง หากมีต้อกระจกในชั้นสโตรมาของกระจกตา อาจจำเป็นต้องรักษาแบบสองขั้นตอนซึ่งรวมถึงการปลูกถ่ายกระจกตาหลังการสร้างใหม่ การมองเห็นที่ดีขึ้นอาจใช้เวลาหลายเดือนถึงมากกว่าหนึ่งปี
สเต็มเซลล์เยื่อบุกระจกตาอยู่ภายใน POV (palisades of Vogt) ในชั้นเบซอลของลิมบัส POV ประกอบด้วยส่วนยื่น papillary ของสโตรมา ซึ่งมีหลอดเลือดและเส้นประสาทมากมาย สภาพแวดล้อมจุลภาค (niche) นี้ควบคุมความสามารถในการสร้างตัวเองใหม่และการแบ่งตัวของสเต็มเซลล์
สเต็มเซลล์สร้างตัวเองใหม่ผ่านการแบ่งตัวแบบไม่สมมาตร ในขณะเดียวกันก็สร้าง เซลล์ขยายชั่วคราว (TAC) TAC จะย้ายไปยังศูนย์กลางของกระจกตาขณะแบ่งตัวและแยกความแตกต่าง ในที่สุดกลายเป็นเซลล์เยื่อบุกระจกตาและหลุดออกจากพื้นผิว
เมื่อสเต็มเซลล์ลิมบัสถูกทำลาย ภาวะทางพยาธิวิทยาต่อไปนี้จะเกิดขึ้นเป็นลูกโซ่
ผิวกระจกตาที่ถูกเยื่อบุตาครอบคลุมจะมีการทำงานของสิ่งกีดขวางลดลง ทำให้เกิดข้อบกพร่องของเยื่อบุผิวที่คงอยู่ การอักเสบที่ต่อเนื่องอาจนำไปสู่การละลายของสโตรมาหรือการทะลุ
ใน COMET (การปลูกถ่ายเยื่อบุช่องปากที่เพาะเลี้ยง) จานเพาะเลี้ยงที่ตอบสนองต่ออุณหภูมิ เป็นเทคโนโลยีหลัก 1) การเคลือบโพลี(N-ไอโซโพรพิลอะคริลาไมด์) บนพื้นผิวของจานเพาะเลี้ยงจะไม่ชอบน้ำที่ 37°C และเปลี่ยนเป็นชอบน้ำเมื่ออุณหภูมิลดลง ทำให้สามารถลอกแผ่นเซลล์ออกจากจานเพาะเลี้ยงได้โดยไม่ต้องใช้เอนไซม์ ทำให้สามารถปลูกถ่ายโดยคงการยึดเกาะระหว่างเซลล์และเมทริกซ์ไว้ 1)
ในกรณี COMET จาก PMC10219018 แผ่นเซลล์และเนื้อเยื่อหลังปลูกถ่ายได้รับการประเมินด้วยอิมมูโนฮิสโตเคมี 1)
ในญี่ปุ่น เมื่อเดือนมิถุนายน พ.ศ. 2564 ผลิตภัณฑ์ COMET ชนิดแรกของโลก Ocural® ได้รับการบรรจุในระบบประกันสุขภาพ 1) Ocural® มีข้อบ่งใช้สำหรับ LSCD สองตาที่ไม่มี Symblepharon (การยึดติดระหว่างเปลือกตาและลูกตา) สำหรับกรณีที่มี Symblepharon จะเลือกใช้ Sakracy® 1)
Toshida และคณะรายงานผลเบื้องต้นของผู้ป่วย 2 รายที่ใช้ Ocural® รายที่ 1 เป็นชายอายุ 79 ปี (LSCD สองตาระยะ III) รายที่ 2 ก็เป็น LSCD สองตาเช่นกัน และทั้งสองรายพบการติดของแผ่นเซลล์ หลังการปลูกถ่าย แผ่นเซลล์แสดงการแสดงออกของ p63, p75NTR, Ki-67 ซึ่งบ่งชี้ถึงการคงไว้ซึ่งลักษณะของสเต็มเซลล์และความสามารถในการแบ่งตัว 1)
สำหรับ LSCD ข้างเดียว สามารถใช้ Nepic® (แผ่นเซลล์เยื่อบุลิมบัสกระจกตาชนิดเพาะเลี้ยงจากเซลล์ตนเอง) ได้ 1)
ในยุโรป Holoclar® ได้รับการอนุมัติให้เป็นยาชนิดแรกของสหภาพยุโรปสำหรับการปลูกถ่ายเยื่อบุลิมบัสชนิดเพาะเลี้ยงจากเซลล์ตนเอง 1) เป็นผู้บุกเบิกการรักษาแบบฟื้นฟูสำหรับ LSCD โดยใช้แนวทางที่แตกต่างจาก Ocural® ของญี่ปุ่น (มาจากเยื่อบุลิมบัสเทียบกับมาจากเยื่อบุช่องปาก)
ในรายงานของ Mazumdar และคณะ การรวม SLET และการปลูกถ่ายเยื่อบุตาตนเอง (CAG) ในขั้นตอนเดียวสามารถซ่อมแซมข้อบกพร่องของเยื่อบุตาและสร้างลิมบัสขึ้นใหม่พร้อมกัน เยื่อบุผิวหายสนิทภายใน 24 วันหลังผ่าตัด และ BCVA ดีขึ้นเป็น 6/12p ที่ 24 เดือน 2)
ใน SLET แบบดั้งเดิม ข้อบกพร่องของเยื่อบุตาจะถูกปล่อยทิ้งไว้บนตาขาวหรือปิดด้วยเยื่อหุ้มน้ำคร่ำ แต่การทำ CAG พร้อมกันอาจช่วยให้ปิดเยื่อบุตาได้เร็วและมีพื้นผิวตาที่เสถียร 2)
ในการทบทวนอย่างเป็นระบบโดย Shanbhag และคณะ (1857 ตา) อัตราความสำเร็จทางกายวิภาคโดยรวมของการปลูกถ่ายลิมบัสตนเองคือ 69% และความสำเร็จทางการทำงานคือ 61% แยกตามเทคนิค SLET และ CLAu แสดงผลลัพธ์ที่ดีกว่าอย่างมีนัยสำคัญเมื่อเทียบกับ CLET อย่างไรก็ตาม มีความแตกต่างอย่างมีนัยสำคัญในคุณภาพการศึกษาและขนาดตัวอย่างระหว่างกลุ่ม จึงต้องใช้ความระมัดระวังในการตีความ 3)
ในอนาคต จำเป็นต้องมีการทดลองแบบสุ่มที่มีกลุ่มควบคุมและการสะสมผลลัพธ์ระยะยาว การบำบัดด้วยเซลล์รุ่นต่อไป เช่น แผ่นเซลล์เยื่อบุกระจกตาที่ได้จากเซลล์ iPS ยังอยู่ในขั้นตอนการวิจัย
แผ่นเซลล์เยื่อบุช่องปากที่เพาะเลี้ยง (CAOMECS) ได้รับการรายงานในปี พ.ศ. 2547 และยืนยันประสิทธิภาพในการปลูกถ่ายตนเองสำหรับ LSCD สองตา อย่างไรก็ตาม ในการติดตามผลระยะยาว พบว่ามีการขุ่นมัวซ้ำในบางกรณีเนื่องจากการบุกรุกของหลอดเลือดจากบริเวณรอบกระจกตา ความแตกต่างในคุณสมบัติระหว่างเยื่อบุกระจกตาและเยื่อบุช่องปากถูกเสนอว่าเป็นสาเหตุ และการใช้เซลล์เยื่อบุกระจกตาของผู้ป่วยเองถือว่าเหมาะสมกว่าสำหรับการรักษาให้หายขาด
กำลังมีการวิจัยเกี่ยวกับการสร้างกระจกตาขึ้นใหม่โดยใช้แหล่งเซลล์อื่นนอกเหนือจากสเต็มเซลล์ลิมบัส
นอกจากนี้ยังมีการแสดงการมีอยู่ของเซลล์ต้นกำเนิดในสโตรมาของกระจกตา และกำลังมีการวิจัยสำหรับการรักษาใหม่ๆ สำหรับเอ็นโดทีเลียมของกระจกตา เช่น โรคกระจกตาพุพอง
ใช่ ผลิตภัณฑ์ COMET Ocural® ได้รับการบรรจุในประกันในปี 2021 อย่างไรก็ตาม สามารถใช้ได้เฉพาะในสถานพยาบาลที่มีจักษุแพทย์ซึ่งเป็นสมาชิกของสมาคมกระจกตาแห่งญี่ปุ่นและสมาคมปลูกถ่ายกระจกตาแห่งญี่ปุ่น และผ่านการฝึกอบรมตามที่กำหนดเท่านั้น ข้อบ่งชี้คือภาวะพร่องสเต็มเซลล์ลิมบัสระดับปานกลางถึงรุนแรง