โรคกระจกตาพุพองเป็นภาวะที่เกิดอาการบวมน้ำถาวรในชั้นสโตรมาและเยื่อบุผิวกระจกตา จากความเสียหายของเซลล์เยื่อบุผนังกระจกตา
เมื่อความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา ลดลงต่ำกว่า 400-500 เซลล์/ตร.มม. ฟังก์ชันการสูบฉีดจะชดเชยไม่พอ ทำให้เกิดอาการบวมน้ำ
สาเหตุหลักคือหลังการผ่าตัดต้อกระจก (ตาเทียม ) และโรคฟุคส์เสื่อมที่เยื่อบุผนังกระจกตา
อาการที่ผู้ป่วยรู้สึกได้แก่ การมองเห็น ลดลง รู้สึกมีสิ่งแปลกปลอม และปวดตา โดยมีลักษณะแปรผันตามช่วงเวลา คือแย่ลงในตอนเช้าและดีขึ้นในตอนกลางวัน
การรักษาที่หายขาดคือการปลูกถ่ายเยื่อบุผนังกระจกตา (DMEK หรือ DSAEK ) และในกรณีที่มีความขุ่นของสโตรมารุนแรง จะเลือกปลูกถ่ายกระจกตา ทั้งชั้น
ยาหยอดตาที่ยับยั้ง ROCK และการฉีดเซลล์เยื่อบุผนังกระจกตา เพาะเลี้ยงเข้าสู่ช่องหน้าม่านตา เป็นวิธีการรักษาใหม่ที่ไม่พึ่งพาการปลูกถ่ายกระจกตา
โรคกระจกตาพุพอง (bullous keratopathy) เป็นภาวะที่เกิดอาการบวมน้ำแบบไม่สามารถกลับคืนได้ในชั้นสโตรมาและเยื่อบุกระจกตา เนื่องจากการทำลายของเซลล์เยื่อบุผนังกระจกตา และเมื่อดำเนินไปจะเกิดตุ่มน้ำ (bulla) ใต้เยื่อบุกระจกตา สาเหตุหลักของการมองเห็น ลดลงคืออาการบวมน้ำของสโตรมา แต่อาการปวดเกิดจากการแตกของตุ่มน้ำที่เยื่อบุกระจกตา
เยื่อบุผนังกระจกตา ทำหน้าที่รักษาปริมาณความชื้นและความหนาของกระจกตา ให้คงที่ผ่านการทำงานของปั๊มและหน้าที่เป็นสิ่งกีดขวางที่มีการซึมผ่านแบบเลือกได้ เมื่อความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา ลดลงต่ำกว่า 400-500 เซลล์/ตร.มม. การทำงานของปั๊มจะไม่เพียงพอ ทำให้เกิดอาการบวมน้ำของสโตรมา และเมื่อดำเนินไปจะเกิดอาการบวมน้ำของเยื่อบุกระจกตา และตุ่มน้ำ เนื่องจากเซลล์เยื่อบุผนังกระจกตา ไม่แบ่งตัวในช่องหน้าม่านตา ความเสียหายจึงไม่สามารถกลับคืนได้
การจำแนก สาเหตุที่พบบ่อย จากหัตถการ หลังผ่าตัดต้อกระจก (ตาเทียม /ตาไม่มีเลนส์), หลังการตัดม่านตาด้วยเลเซอร์ , การปฏิเสธหลังปลูกถ่ายกระจกตา เสื่อม/ dystrophy Fuchs endothelial dystrophy, posterior polymorphous corneal dystrophy (PPCD ), ICE syndrome อักเสบ Herpetic endothelialitis, cytomegalovirus endothelialitis, idiopathic endothelialitis บาดเจ็บ Descemet membrane rupture จากคีมคลอด, กระจกตา ฉีกขาด, การบาดเจ็บแบบทื่อ จากยา Amantadine, chlorpromazine, ยาหยอดตา ROCK inhibitor บางชนิด (เช่น netarsudil) เมแทบอลิซึม / ทั่วร่างกาย เบาหวาน, โรคเมือกโพลีแซ็กคาไรด์สะสม, ภาวะไขมันในเลือดสูงชนิด familial (LCAT deficiency, Tangier disease), โรคจอประสาทตา เสื่อมชนิด Schnyder
โรคกระจกตาพุพองจากเลนส์แก้วตาเทียม (pseudophakic bullous keratopathy: PBK) เกิดขึ้นในผู้ป่วยที่ได้รับการผ่าตัดต้อกระจก 1-2% และมักปรากฏชัดระหว่าง 8 เดือนถึง 7 ปีหลังผ่าตัด1) ด้วยความก้าวหน้าของเทคนิคการผ่าตัดต้อกระจก อัตราการเกิดโรคมีแนวโน้มลดลง แต่ยังคงเป็นข้อบ่งชี้หลักในการปลูกถ่ายกระจกตา ร่วมกับโรคจอประสาทตา เสื่อมชนิด Fuchs4,8)
ความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา ลดลงตามสรีรวิทยาตามอายุ ในทารกแรกเกิดอยู่ที่ 3,500-4,000 เซลล์/ตร.มม. ในวัย 20 ปีประมาณ 2,700 เซลล์/ตร.มม. และอายุมากกว่า 70 ปีลดลงเหลือเฉลี่ยประมาณ 2,200 เซลล์/ตร.มม. อัตราการลดลงทางสรีรวิทยาปกติคือ 0.5%/ปี แต่หลังผ่าตัดต้อกระจก จะเพิ่มขึ้นเป็นประมาณ 2%/ปี และหลังผ่าตัดต้อหิน เป็นประมาณ 10%/ปี
โรคจอประสาทตา เสื่อมชนิด Fuchs มีพื้นฐานทางพันธุกรรมแบบ autosomal dominant อัตราส่วนเพศชายต่อหญิงประมาณ 1:4 พบในผู้หญิงมากกว่า4) เดิมเชื่อว่าพบน้อยในคนญี่ปุ่นเมื่อเทียบกับคนผิวขาวและผิวดำ แต่ระยะก่อนหน้า คือ กระจกตา แบบจุด (cornea guttata) พบในผู้ป่วยก่อนผ่าตัดต้อกระจก 1.2% และมีการชี้ให้เห็นว่าอัตรานี้กำลังเพิ่มขึ้นในญี่ปุ่นตามอายุขัยที่ยืนยาวขึ้น
โรคกระจกตาพุพองเป็นสาเหตุหลักประการหนึ่งของความบกพร่องทางการมองเห็น จากโรคกระจกตา และเป็นข้อบ่งชี้หลักในการปลูกถ่ายกระจกตา ทั่วโลก เนื่องจากการผ่าตัดต้อกระจก เป็นการผ่าตัดตาที่ทำบ่อยที่สุดในโลก โรคกระจกตาพุพองจากเลนส์แก้วตาเทียม จึงมีความสำคัญทางสาธารณสุข ด้วยการพัฒนาเทคนิคการผ่าตัดที่รุกรานน้อยลง การปรับปรุงวัสดุวิสโคอีลาสติก และเทคโนโลยีลดพลังงานอัลตราซาวนด์ อัตราการเกิดโรคลดลงทุกปี แต่ก็ไม่เป็นศูนย์โดยสมบูรณ์ ในช่วงไม่กี่ปีที่ผ่านมา การเพิ่มขึ้นของการผ่าตัดต้อกระจกในผู้สูงอายุ มาก และการมีผู้ป่วยโรคจอประสาทตา เสื่อมชนิด Fuchs ก่อนผ่าตัด ได้รับการยอมรับอีกครั้งว่าเป็นปัจจัยเสี่ยง
ข้อบ่งชี้หลักในการปลูกถ่ายกระจกตา ทั่วโลกคือโรคจอประสาทตา เสื่อมชนิด Fuchs และโรคกระจกตาพุพองจากเลนส์แก้วตาเทียม ซึ่งครองอันดับต้นๆ8) ในญี่ปุ่น มีการขาดแคลนผู้บริจาคกระจกตา เรื้อรัง และการพึ่งพาผู้บริจาคจากต่างประเทศในระดับสูงก็เป็นลักษณะเฉพาะ ตามสถิติในประเทศล่าสุด ประมาณ 40-50% ของการปลูกถ่ายกระจกตา ทั้งหมดเป็นโรคกระจกตาพุพอง (รวมถึงจากเลนส์แก้วตาเทียม และไม่มีเลนส์แก้วตา ) และแม้ว่าจำนวนสัมบูรณ์จะลดลงตามการผ่าตัดต้อกระจก ที่รุกรานน้อยลง แต่ก็ยังคงเป็นข้อบ่งชี้หลัก โรคกระจกตาพุพองหลังการตัดม่านตาด้วยเลเซอร์ (LI) เคยพบได้บ่อยในญี่ปุ่น แต่ลดลงตามการเปลี่ยนไปสู่การผ่าตัดต้อกระจก เชิงป้องกัน
Q
โรคกระจกตาพุพองสามารถหายได้เองหรือไม่?
A
ไม่ โรคกระจกตาพุพอง (Bullous keratopathy) เป็นภาวะที่เกิดจากความเสียหายที่ไม่สามารถฟื้นฟูได้ของเซลล์เยื่อบุผิวดำนอกของกระจกตา และไม่สามารถหายได้เอง เนื่องจากเซลล์เยื่อบุผิวดำนอกของกระจกตา ในมนุษย์มีการแบ่งตัวและสร้างใหม่ได้ยากมาก เซลล์ที่สูญเสียไปจะไม่กลับคืนมา การรักษาที่หายขาดคือการปลูกถ่ายเยื่อบุผิวดำนอกกระจกตา และในช่วงไม่กี่ปีที่ผ่านมา การแพทย์เชิงฟื้นฟูโดยใช้เซลล์เยื่อบุผิวดำนอกที่เพาะเลี้ยงก็กำลังก้าวหน้าเช่นกัน
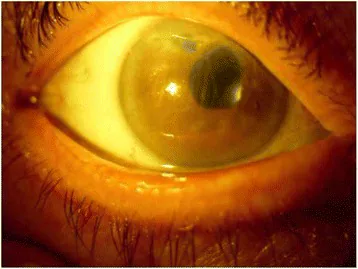
ภาพกระจกตาบวมน้ำ Pacella F, Agostinelli E, Carlesimo SC, et al. J Med Case Rep. 2016;10:282. Figure 2. PM
CI D: PMC5062904. License: CC BY.
ภาพทางคลินิกของผู้ป่วยหนักที่กระจกตา ทั้งหมดขุ่นมัวแบบกระจาย ทำให้มองเห็นขอบม่านตา และรายละเอียดของม่านตา ได้ยาก ความขุ่นจากอาการบวมน้ำของชั้นสโตรมากระจายไปทั่วส่วนหน้าของดวงตา
อาการที่ผู้ป่วยรู้สึกได้ของโรคกระจกตาพุพองจะแตกต่างกันไปตามระดับของอาการบวมน้ำและชั้นที่ได้รับผลกระทบ
การมองเห็น ลดลงการมองเห็น ลดลงในตอนเช้าและดีขึ้นในตอนกลางวัน (การเปลี่ยนแปลงในรอบวัน) ขณะหลับตา การระเหยของน้ำตาจะลดลง ทำให้เกิดการสะสมของอาการบวมน้ำ และหลังจากลืมตา อาการบวมน้ำจะค่อยๆ ลดลง เมื่อดำเนินไป จะเกิดการมองเห็น ลดลงอย่างต่อเนื่องและไม่สามารถฟื้นฟูได้ปวดตา ความรู้สึกเหมือนมีสิ่งแปลกปลอม : เกิดจากข้อบกพร่องของเยื่อบุผิวจากการแตกของตุ่มน้ำหรือความไม่เรียบของผิวกระจกตา กลัวแสงและน้ำตาไหล : เกิดจากความไม่สม่ำเสมอทางแสงของผิวกระจกตา และการกระตุ้นเส้นประสาทไทรเจมินัล การเริ่มต้นอย่างช้าๆ : ดำเนินไปอย่างค่อยเป็นค่อยไปในช่วงหลายสัปดาห์ถึงหลายเดือน ดังนั้นผู้ป่วยอาจปรับตัวได้ค่อนข้างดี
อาการแสดงที่กระจกตา
อาการบวมน้ำของชั้นสโตรมากระจกตา : แสดงเป็นกระจกตา ขุ่นมัวคล้ายกระจกฝ้า ความหนาของกระจกตา เพิ่มขึ้นอย่างมาก ในบางรายอาจเกิน 800 ไมโครเมตร
รอยย่นของเยื่อหุ้มเดสเซเมท : เกิดรอยย่นบนผิวด้านหลังของกระจกตา จากการทำงานผิดปกติของเยื่อบุผิวดำนอก เป็นตัวบ่งชี้ที่สำคัญของความเสียหายของเยื่อบุผิวดำนอก
ตุ่มน้ำใต้เยื่อบุผิว (bullae) : ในรายที่ลุกลาม จะเกิดตุ่มน้ำขนาดใหญ่ และการแตกทำให้เกิดข้อบกพร่องของเยื่อบุผิวและความเจ็บปวด
แผลเป็นในสโตรมาและการบุกรุกของหลอดเลือด : เมื่อเรื้อรัง จะเกิดการบุกรุกของหลอดเลือดจากส่วนรอบนอกและความขุ่นแบบแผลเป็น ซึ่งเป็นสาเหตุหนึ่งของการมองเห็น ลดลง
ลักษณะเฉพาะตามสาเหตุ
Fuchs endothelial dystrophy : เริ่มจาก guttae ตรงกลาง ลุกลามเป็นลักษณะ beaten-metal appearance ตรวจพบเป็นจุดดำใน specular microscopy
Pseudophakic : ตรวจสอบชนิดและตำแหน่งของเลนส์แก้วตาเทียม IOL ห้องหน้าความเสี่ยงสูง ประเมินสภาพเอนโดทีเลียมของตาข้างตรงข้ามด้วย
Disciform edema : อาการบวมน้ำสโตรมาเฉพาะที่รูปวงกลมและคราบตะกอนหลังกระจกตา คล้ายไขมันหมู บ่งชี้到她 herpetic endothelitis
Diffuse edema : อาการบวมน้ำจากลิมบัส ถึงลิมบัส สงสัย toxic anterior segment syndrome (TASS ) หรือพิษจากยา7)
ในการตรวจด้วย slit-lamp หากพบสโตรมาบวมน้ำโดยไม่มีอาการอักเสบ ให้คิดถึงความผิดปกติของเอนโดทีเลียมก่อน อาการบวมน้ำสโตรมาหลังผ่าตัดลูกตามักรุนแรงใกล้แผลผ่าตัด และยังพบสโตรมาบวมน้ำรอบๆ รอยแทรกซึมใน keratitis ติดเชื้อ การย้อมฟลูออเรสซีน จะเห็นตุ่มน้ำเยื่อบุผิวเป็นจุดดำ
สัญญาณที่บ่งชี้ความผิดปกติของเอนโดทีเลียม ได้แก่ คราบตะกอนสีเทาหรือน้ำตาลบนผิวเอนโดทีเลียมใกล้กลางกระจกตา เมื่อคราบตะกอนขยายและรวมตัวกัน จะเกิดลักษณะเฉพาะที่เรียกว่า beaten-metal appearance และตรวจพบเป็นจุดดำในการสะท้อนแบบกระจกหรือกล้องจุลทรรศน์เอนโดทีเลียม
การดำเนินของ bullous keratopathy โดยทั่วไปสามารถเข้าใจได้ในระยะต่อไปนี้
ระยะการทำงานของเอนโดทีเลียมลดลง : ความหนากระจกตา เพิ่มขึ้นเล็กน้อย อาการจำกัดเฉพาะตามัวในตอนเช้าระยะสโตรมาบวมน้ำ : รอยย่นของ Descemet membrane, สโตรมาบวมน้ำต่อเนื่อง, การมองเห็น ลดลงเรื่อยๆระยะเยื่อบุผิวบวมน้ำ : การเกิดไมโครซีสต์ของเยื่อบุผิว, กลัวแสงและความรู้สึกสิ่งแปลกปลอมเพิ่มขึ้นระยะเกิดตุ่มน้ำ : การเกิดตุ่มน้ำใต้เยื่อบุผิว (bulla), เมื่อแตกจะเกิดปวดตา อย่างรุนแรงและข้อบกพร่องของเยื่อบุผิวระยะแผลเป็น : แผลเป็นใต้เยื่อบุผิว การบุกรุกของหลอดเลือด และความขุ่นของสโตรมาดำเนินไปเนื่องจากการเรื้อรัง
กลยุทธ์การรักษาแตกต่างกันในแต่ละระยะ จนถึงระยะบวมน้ำของสโตรมา สามารถสังเกตด้วยการรักษาแบบประคับประคองหรือการใช้ยา แต่หลังจากระยะการเกิดตุ่มน้ำ จำเป็นต้องจัดการความปวดและพิจารณาการปลูกถ่ายเอ็นโดทีเลียม
Q
ทำไมการมองเห็นลดลงในตอนเช้า?
A
เมื่อการทำงานของเอ็นโดทีเลียมกระจกตา ลดลง ในระหว่างการหลับตา (นอนหลับ) การระเหยของน้ำตาลดลงและอาการบวมน้ำของกระจกตา สะสมได้ง่าย ในระหว่างวัน การระเหยของน้ำตาจะดึงน้ำออกจากกระจกตา ทำให้อาการบวมน้ำลดลงและการมองเห็น ดีขึ้น รูปแบบนี้เป็นที่รู้จักว่าเป็นอาการทั่วไปของโรคกระจกตาพุพอง (bullous keratopathy) และโรค Fuchs endothelial dystrophy ในระยะเริ่มต้น
เซลล์เอ็นโดทีเลียมของกระจกตา ไม่แบ่งตัวหรือเพิ่มจำนวนในร่างกาย ความเสียหายเฉพาะที่ได้รับการซ่อมแซมโดยการขยายตัวและการย้ายที่ของเซลล์ข้างเคียง แต่เมื่อความหนาแน่นลดลงต่ำกว่าเกณฑ์ที่กำหนด จะเกิดการชดเชยที่ไม่สามารถกลับคืนได้ สาเหตุของโรคกระจกตาพุพองมีหลากหลาย: จากการรักษาทางการแพทย์, เสื่อม, บาดเจ็บ, อักเสบ, จากยา ที่พบบ่อยที่สุดคือ โรคกระจกตาพุพองชนิด pseudophakic (PBK) และโรค Fuchs endothelial dystrophy
ความเสี่ยงถูกกำหนดโดยปัจจัยก่อนและหลังการผ่าตัดต้อกระจก
ปัจจัยก่อนผ่าตัด : ความหนาแน่นเซลล์เอ็นโดทีเลียมต่ำ, อายุมาก, การมีโรค Fuchs endothelial dystrophy ร่วม, ช่องหน้าตื้น, ความหนากระจกตา ส่วนกลางก่อนผ่าตัด ≥600–640 μm เพิ่มความเสี่ยงของอาการบวมน้ำที่ไม่สามารถกลับคืนได้1) ปัจจัยระหว่างผ่าตัด : พลังงานอัลตราซาวนด์มากเกินไป, การสัมผัสเอ็นโดทีเลียมกับเครื่องมือหรือ IOL , การแตกของแคปซูลหลัง, การย้อยของวุ้นตา , การยืดเวลาผ่าตัด2) ปัจจัยหลังผ่าตัด : การอักเสบเรื้อรัง, การเคลื่อนของ IOL , เศษนิวเคลียส, ต้อหินทุติยภูมิ
IOL ช่องหน้า (ACIOL ) มีรายงานว่าทำให้เกิด PBK ในประมาณ 14% ของกรณี และถือว่ามีความเสี่ยงสูงกว่า IOL ช่องหลัง3) อัตราการสูญเสียเซลล์เอ็นโดทีเลียมหลังผ่าตัดเร่งขึ้นเป็นประมาณ 2.5%/ปี เทียบกับ 0.6%/ปีปกติ หรือประมาณ 4 เท่า และมีรายงานการลดลงประมาณ 11% ที่ 5 ปี และ 18.7% ที่ 10 ปีหรือมากกว่าหลังผ่าตัดเมื่อเทียบกับก่อนผ่าตัด
ในตาที่มีความเสี่ยงสูง แนะนำมาตรการต่อไปนี้
วัดความหนาแน่นเซลล์เอ็นโดทีเลียมของกระจกตา ด้วยกล้องจุลทรรศน์สเปคูลาร์ก่อนผ่าตัดและประเมินความเสี่ยง
ใช้สารหนืดชนิดกระจายตัว (dispersive OVD ) อย่างเพียงพอเพื่อปกป้องเอ็นโดทีเลียม
ใช้เทคนิคซอฟต์เชลล์ (soft-shell technique)
พิจารณาเทคนิคที่ประหยัดพลังงานอัลตราซาวนด์ (เช่น วิธีพรีชอป)
ในกรณีที่มีความเสี่ยงสูง เทคนิคที่ไม่ใช้อัลตราซาวนด์ (ECCE , SICS) ก็เป็นทางเลือก 2)
โรคเอ็นโดทีเลียมที่ลุกลามทั้งสองข้างโดยมีพื้นฐานทางพันธุกรรมแบบ autosomal dominant ทำให้เกิดกัตเท (guttae) ที่บริเวณกลางกระจกตา และค่อยๆ แผ่ไปยังส่วนรอบนอก 4) โดยปกติจะไม่มีอาการก่อนอายุ 50 ปี และดำเนินไปอย่างช้าๆ เมื่อดำเนินไป การทำงานของสิ่งกีดขวางและปั๊มของเอ็นโดทีเลียมจะลดลง นำไปสู่โรคกระจกตาพุพอง
หลังการตัดม่านตาด้วยเลเซอร์ : พลังงานเลเซอร์อาร์กอนทำให้เซลล์เอ็นโดทีเลียมเสียหายโดยตรง คนญี่ปุ่นมักมีมุมแคบ ดังนั้นการลดลงของเซลล์เอ็นโดทีเลียมหลังทำหัตถการจึงเป็นปัญหาหลังการเชื่อมขวางกระจกตา (CXL ) : มีรายงานอาการบวมน้ำที่กระจกตา ที่เกิดขึ้นช้าเป็นภาวะแทรกซ้อนที่พบได้ยาก Vandevenne และคณะรายงานกรณีผู้ป่วยที่มีอาการบวมน้ำที่กระจกตา แบบไมโครซิสติก 4 เดือนหลังการเชื่อมขวางแบบเฉพาะสำหรับโรคกระจกตา รูปกรวยที่ลุกลาม โดยความหนาแน่นของเซลล์เอ็นโดทีเลียมลดลงจาก 2,414 เป็น 1,514 เซลล์/ตร.มม. (ลดลง 37%) แต่หายได้เองภายใน 1 เดือน 5) จากยา : อะแมนทาดีน (ทำให้เสียหายถาวรเมื่อใช้เป็นเวลานาน), คลอร์โปรมาซีน, ยาทองคำ, ยายับยั้ง ROCK เนทาร์ซูดิล Chu และคณะรายงานหญิงอายุ 79 ปีที่มีอาการบวมน้ำรุนแรง 5 วันหลังจากเริ่มใช้เนทาร์ซูดิล โดยความหนาของกระจกตา เพิ่มขึ้นจาก 557 เป็น 808 ไมโครเมตร และฟื้นตัวสมบูรณ์หลังจากหยุดยา 4 เดือนและใช้ยาหยอดน้ำเกลือไฮเปอร์โทนิกและสเตียรอยด์ 6) กลุ่มอาการพิษของส่วนหน้าดวงตา (TASS ) : การอักเสบที่ไม่ติดเชื้อเนื่องจากความเป็นพิษของน้ำยาล้างตาหรือการฉีดยาเข้าช่องหน้าดวงตาผิดพลาด Arici และคณะรายงานกรณีผู้ป่วยที่มีอาการบวมน้ำที่กระจกตา แบบกระจายหลังการผ่าตัดต้อเนื้อ โดยไม่มีภาวะแทรกซ้อน โดยสงสัยว่ามีความเป็นพิษของ PVP-I ต่อเอ็นโดทีเลียมกระจกตา อาการบวมน้ำหายไปภายใน 2 สัปดาห์ด้วยการหยอดเดกซาเมทาโซนเข้มข้น แต่ความหนาแน่นของเซลล์เอ็นโดทีเลียมหลังจาก 1 ปีลดลงเหลือ 1,001 เซลล์/ตร.มม. 7) การเสื่อมของวงแหวนโซเมอร์ริง : หลังจาก 20-30 ปีหลังการผ่าตัดต้อกระจก อนุภาคที่กลายเป็นปูนจากเศษเลนส์ที่เหลือจะหลุดออกและเกาะบนเอ็นโดทีเลียมกระจกตา การบาดเจ็บ / การคลอดด้วยคีม : การแตกของเยื่อเดสเซเม็ททำให้เกิดความผิดปกติของเอ็นโดทีเลียม การบาดเจ็บที่เกิดขึ้นตั้งแต่แรกเกิดอาจแสดงอาการหลังจากเวลาผ่านไปนานกลุ่มอาการ ICE (Iridocorneal Endothelial Syndrome)ม่านตา ฝ่อ, รูม่านตา เบี่ยง, และพังผืดยึดม่านตา ส่วนปลายด้านหน้า โดยเซลล์เอ็นโดทีเลียมที่ผิดปกติจะแผ่กระจายไปบนผิวด้านหลังของกระจกตา ทำให้เกิดอาการบวมน้ำต้อหินทุติยภูมิ ความดันลูกตา สูงเรื้อรังเพิ่มภาระต่อปั๊มเอ็นโดทีเลียม และเร่งการลดลงของเซลล์เอ็นโดทีเลียมในระยะยาวการใส่คอนแทคเลนส์เป็นเวลานาน : ภาวะขาดออกซิเจนเรื้อรังทำให้เกิดความผิดปกติทางสัณฐานวิทยาของเซลล์เอนโดทีเลียม (polymegethism, pleomorphism) ซึ่งเป็นความเสี่ยงต่อการเสื่อมสมรรถภาพในอนาคตโรคเบาหวาน : เกี่ยวข้องกับการทำงานของเซลล์เอนโดทีเลียมที่ลดลงและความเสี่ยงที่เพิ่มขึ้นของภาวะแทรกซ้อนหลังการผ่าตัด
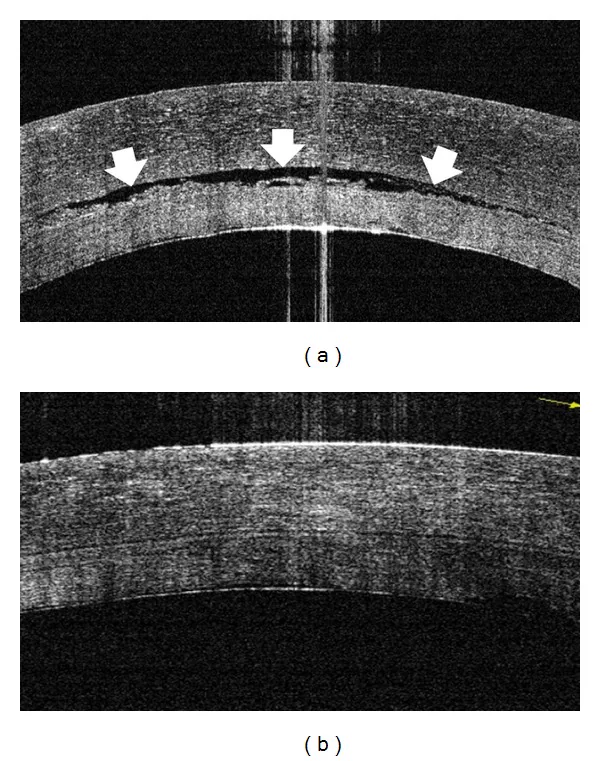
ภาพ OCT ของโรคกระจกตาพุพอง ISRN Ophthalmol. 2014;2014:562062. Figure 4. PM
CI D: PMC3929380. License: CC BY.
OCT ส่วนหน้าช่วยเปรียบเทียบการสะสมของเหลวใต้เยื่อบุผิวและอาการบวมน้ำของกระจกตา ก่อนและหลังการปรับปรุง เป็นภาพแทนการเปลี่ยนแปลงโครงสร้างในโรคกระจกตาพุพอง
การวินิจฉัยโรคกระจกตาพุพองขึ้นอยู่กับผลการตรวจทางคลินิก และประเมินการทำงานของเอนโดทีเลียมและระดับอาการบวมน้ำด้วยการตรวจเสริม
นี่คือการตรวจพื้นฐานที่สุด ประเมินขอบเขตและความลึกของความขุ่นของกระจกตา ด้วยการส่องผ่านแสง และยืนยันการแพร่กระจายของอาการบวมน้ำของเยื่อบุผิวด้วยวิธีการกระจายแสงจากตาขาว การใช้วิธีการสะท้อนแบบกระจก ในกรณีของ Fuchs สามารถสังเกตลักษณะ beaten-metal บนพื้นผิวเอนโดทีเลียมได้
รูปแบบของอาการบวมน้ำมีประโยชน์ในการประมาณสาเหตุ อาการบวมน้ำแบบกระจายบ่งชี้ถึง TASS หรือพิษจากยา อาการบวมน้ำเฉพาะที่บ่งชี้ถึงการลอกของเยื่อเดสเซเมตหรือการสัมผัสเครื่องมือ และอาการบวมน้ำแบบแผ่นกลมบ่งชี้ถึงเยื่อบุกระจกตา อักเสบจากเริม ในตาที่ปลูกถ่ายกระจกตา อาการบวมน้ำแบบ compartment และการสะสมที่ผิวหลังกระจกตา (เส้น Khodadoust) บ่งชี้ถึงปฏิกิริยาการปฏิเสธ
เป็นการตรวจหลักเพื่อประเมินความหนาแน่นและสัณฐานวิทยาของเซลล์เอนโดทีเลียมของกระจกตา
ตัวชี้วัด ค่าปกติ ค่าผิดปกติ ความหนาแน่นของเซลล์ 2,200–4,000 เซลล์/ตร.มม. ขึ้นอยู่กับอายุ ต่ำกว่า 500 เซลล์/ตร.มม. ทำให้รักษาความใสได้ยาก ค่า CV (สัมประสิทธิ์ความแปรปรวน) 0.2–0.3 0.35 ขึ้นไป ร้อยละของเซลล์รูปหกเหลี่ยม 60–70% น้อยกว่า 50%
ในกรณีที่ไม่รุนแรง มีประโยชน์สำหรับการประเมินก่อนผ่าตัด แต่ในกรณีที่มีอาการบวมน้ำรุนแรง การถ่ายภาพจะทำได้ยาก ในกรณีดังกล่าว กล้องจุลทรรศน์สเปกคิวลาร์แบบสัมผัสหรือกล้องจุลทรรศน์คอนโฟคอล มีประโยชน์
จำเป็นสำหรับการประเมินปริมาณอาการบวมน้ำ การวัดความหนาด้วยคลื่นเสียงความถี่สูงเป็นการตรวจที่รวดเร็วและเป็นมาตรฐาน ในขณะที่ OCT ส่วนหน้าด้วยแสงและการถ่ายภาพ Scheimpflug ช่วยให้วัดแบบไม่สัมผัสได้หลายตำแหน่ง 9)
สามารถมองเห็นชั้นต่างๆ ของกระจกตา ได้ด้วยความละเอียดสูง และประเมินขอบเขตของตุ่มน้ำใต้เยื่อบุผิว ความหนาของสโตรมา และความผิดปกติของเยื่อหุ้มเดสเซเม็ทได้อย่างละเอียด มีประโยชน์ในการระบุความผิดปกติของโครงสร้างที่ยากต่อการยืนยันด้วยกล้องจุลทรรศน์ชนิดกรีด 9) สามารถประยุกต์ใช้ได้อย่างกว้างขวาง รวมถึงการประเมินหลังผ่าตัด การตรวจหาการลอกตัวของเยื่อหุ้มเดสเซเม็ท การกำหนดขอบเขตของอาการบวมน้ำของเยื่อบุผิว และการตรวจสอบสถานะการยึดติดของกราฟต์ OCT ส่วนหน้าด้วยแสงไม่สัมผัสและลดภาระของผู้ป่วย และยังเหมาะสำหรับการติดตามผลเป็นระยะ
ในกรณีที่กระจกตาบวมน้ำ รุนแรงซึ่งประเมินด้วยกล้องจุลทรรศน์สเปกคิวลาร์ได้ยาก กล้องจุลทรรศน์คอนโฟคอล มีประโยชน์ สามารถสังเกตรูปร่างของเซลล์เยื่อบุผนังกระจกตา ได้โดยตรง และประเมินความหนาแน่นของเซลล์และความหลากหลายของรูปร่าง ในการวิจัย ยังใช้สังเกตข่ายประสาท เคอราโตไซต์ และเซลล์ภูมิคุ้มกัน
ในผู้สูงอายุที่เข้ารับการผ่าตัดต้อกระจก นอกจากการลดลงตามธรรมชาติเนื่องจากอายุที่เพิ่มขึ้นแล้ว โรคทางระบบที่เกิดร่วมและประวัติการผ่าตัดตาหรือการบาดเจ็บก่อนหน้ายังส่งผลต่อสภาพของเซลล์เยื่อบุผนังกระจกตา จากผลการตรวจด้วยกล้องจุลทรรศน์สเปกคิวลาร์ที่ได้ก่อนผ่าตัด จะประมาณการพยากรณ์โรคของการผ่าตัดและความเสี่ยงในการเกิดโรคกระจกตาพุพอง โดยเฉพาะในกรณีที่มีความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา ต่ำกว่า 1,000 เซลล์/ตร.มม. ค่า CV 0.4 ขึ้นไป และร้อยละของเซลล์รูปหกเหลี่ยมน้อยกว่า 40% ความเสี่ยงของการเสื่อมสภาพหลังผ่าตัดจะสูง ซึ่งจำเป็นต้องปรับเปลี่ยนเทคนิคการผ่าตัด เช่น การใช้สารหนืดหยุ่นอย่างเพียงพอ การลดพลังงานคลื่นเสียงความถี่สูงให้น้อยที่สุด และการจัดการกับนิวเคลียสที่แข็ง
เมื่อสงสัยโรคกระจกตาพุพอง (bullous keratopathy) การวินิจฉัยแยกโรคที่สำคัญมีดังนี้:
Fuchs endothelial dystrophy : มี guttae ที่กระจกตา ประวัติครอบครัว และเป็นสองตาPosterior polymorphous corneal dystrophy (PPCD ) : ถ่ายทอดทาง autosomal dominant, รอยโรคคล้ายพุพองIridocorneal endothelial (ICE) syndrome : เป็นข้างเดียว, ร่วมกับม่านตา ฝ่อและรูม่านตา เบี่ยงHerpetic หรือ cytomegalovirus corneal endotheliitis : วินิจฉัยยืนยันด้วย PCR ของ aqueous humorAcute hydrops ใน keratoconus : วินิจฉัยได้จากประวัติCorneal edema หลัง acute angle-closure glaucoma : ประวัติการกำเริบและการตรวจตาข้างตรงข้ามEndothelial rejection หลังปลูกถ่ายกระจกตา : Khodadoust line, ประวัติการปลูกถ่าย
การรักษาโรคกระจกตาพุพองผสมผสานการรักษาทางยาและการผ่าตัดตามความสามารถในการฟื้นตัวของความเสียหายของ endothelial และความต้องการทางการมองเห็น
การรักษายึดหลักสี่ประการ: “การกำจัดสาเหตุ”, “การรักษาและฟื้นฟูการทำงานของ endothelial”, “การลดอาการบวมและปวด” และ “การฟื้นฟูการมองเห็น ”. ในระยะที่ความเสียหายของ endothelial สามารถฟื้นตัวได้ (จากการอักเสบ ยา หรือชั่วคราวหลังผ่าตัด) การแก้ไขสาเหตุสามารถทำให้อาการบวมดีขึ้นได้ ในระยะที่ไม่สามารถฟื้นตัวได้ การจัดการตามอาการแบบประคับประคองและการผ่าตัดรักษาแบบรุนแรงเป็นหลัก
การรักษาแบบประคับประคองทำเป็นสะพานไปสู่การปลูกถ่าย endothelial หรือเป็นการรักษาตามอาการในกรณีที่ผ่าตัดยาก
ยาหยอดตาโซเดียมคลอไรด์ 5% และยาทาตาโซเดียมคลอไรด์ 6% : ทำให้ชั้นน้ำตาเป็นไฮเปอร์โทนิกเพื่อดึงน้ำออกจากกระจกตา โดยออสโมซิส การทายาก่อนนอนมีประโยชน์ในการลดการสะสมของอาการบวมน้ำในเวลากลางคืน ผลจำกัดเฉพาะอาการบวมน้ำที่เยื่อบุผิว ส่วนอาการบวมน้ำที่สโตรมาได้ผลน้อยคอนแทคเลนส์ชนิดนิ่มเพื่อการรักษา (BCL) : มีประโยชน์ในการบรรเทาอาการปวดจากการแตกของตุ่มน้ำที่เยื่อบุผิว เนื่องจากมีความเสี่ยงต่อการเกิดกระจกตา อักเสบติดเชื้อ จึงแนะนำให้ตรวจติดตามเป็นระยะและใช้ยาหยอดตาปฏิชีวนะป้องกันยาหยอดตาสเตียรอยด์ : ใช้เมื่อมีการอักเสบ อาจเพิ่มกิจกรรมของปั๊ม Na⁺/K⁺-ATPase ของเอ็นโดทีเลียมยาลดความดันลูกตา : ใช้เมื่อมีความดันลูกตา สูง อย่างไรก็ตาม การใช้ยาในกลุ่มยับยั้งคาร์บอนิกแอนไฮเดรสเฉพาะที่อาจรบกวนการทำงานของปั๊มเอ็นโดทีเลียม ดังนั้นจึงไม่ใช่ทางเลือกแรกในกรณีที่เอ็นโดทีเลียมทำงานผิดปกติ ควรระมัดระวังกับยาในกลุ่มพรอสตาแกลนดินเนื่องจากอาจก่อให้เกิดการอักเสบวิธีใช้ไดร์เป่าผม : วิธีง่ายๆ ในตอนเช้าโดยเป่าลมร้อนจากไดร์เป่าผมไปยังผิวกระจกตา เพื่อส่งเสริมการระเหยและเร่งการมองเห็น ที่ดีขึ้นในระหว่างวันการปลูกถ่ายเยื่อหุ้มน้ำคร่ำและการเจาะสโตรมาส่วนหน้า (ASP ) : เพื่อบรรเทาอาการปวดที่ดื้อต่อการรักษาและส่งเสริมการสร้างเยื่อบุผิวชั้นผิวใหม่
ยายับยั้ง Rho-associated coiled-coil forming kinase (ROCK) ส่งเสริมการเพิ่มจำนวน การย้ายที่ และการยึดเกาะของเซลล์เอ็นโดทีเลียมกระจกตา และยับยั้งการตายของเซลล์แบบอะพอพโทซิส Erdinest และคณะรายงานผู้ป่วย PBK 3 รายที่ไม่ตอบสนองต่อการรักษาแบบอนุรักษ์นิยมตามปกติ ได้รับยาหยอดตา ripasudil 0.4% วันละสามครั้งเป็นเวลา 3-11 เดือน และทุกรายมีความหนากระจกตา ส่วนกลางลดลงและการมองเห็น ที่ดีขึ้นเมื่อแก้ไขแล้ว และหลีกเลี่ยงการปลูกถ่ายกระจกตา 10) ในรายที่ 3 ความขุ่นของสโตรมาหายไปอย่างสมบูรณ์หลังจากรักษา 11 เดือน ความหนากระจกตา ส่วนกลางลดลงจาก 582 μm เหลือ 540 μm และการมองเห็น ดีขึ้นจาก 0.3 logMAR เป็น 0.04 logMAR
นอกจากนี้ยังมีรายงานว่าการให้ ripasudil ในช่วงผ่าตัดช่วยลดอัตราการสูญเสียเซลล์เอ็นโดทีเลียม 12 เดือนหลังการผ่าตัดต้อกระจก ในตาที่มีความเสี่ยงสูง โดยกลุ่ม ripasudil อยู่ที่ 4.5% เทียบกับกลุ่มควบคุมที่ 12.8% ซึ่งบ่งชี้ถึงศักยภาพในการใช้ป้องกัน 1)
การรักษาที่หายขาดสำหรับความผิดปกติของเอ็นโดทีเลียมกระจกตา ที่ไม่สามารถกลับคืนได้คือการปลูกถ่ายกระจกตา
การผ่าตัดปลูกถ่ายเอ็นโดทีเลียมกระจกตา (DSAEK และ DMEK)
DSAEK กระจกตา ผู้บริจาคพร้อมสโตรมาส่วนหลัง 50-100 μm ไม่ต้องเย็บ ทำให้สายตาเอียง น้อยกว่าและทนทานต่อการบาดเจ็บได้ดีกว่า
DSAEK บางพิเศษ (UT-DSAEK )การมองเห็น ใกล้เคียงกับ DMEK
DMEK การมองเห็น รวดเร็วและดี อัตราการปฏิเสธต่ำ
ข้อบ่งชี้ : โดยหลักการแล้ว ตาเทียม (pseudophakic) และกรณีที่ความขุ่นของสโตรมาไม่รุนแรงเหมาะสม มีข้อจำกัดในตาที่ไม่มีม่านตา หรือมีพังผืดยึดม่านตา ส่วนหน้ากว้าง
การปลูกถ่ายกระจกตาแบบทะลุ (PK)
ข้อบ่งชี้ : เลือกใช้ในกรณีที่มีแผลเป็นที่สโตรมาหรือการบุกรุกของหลอดเลือดรุนแรงจนไม่สามารถคาดหวังการมองเห็น ที่ดีขึ้นได้ด้วยการปลูกถ่ายเอ็นโดทีเลียมเพียงอย่างเดียว
ลักษณะ : ความเสี่ยงต่อการปฏิเสธ graft หลังผ่าตัดสูงกว่าการปลูกถ่ายเอ็นโดทีเลียม และต้องใช้ยาหยอดตาสเตียรอยด์ ในระยะยาว
ข้อควรระวัง : ความแข็งแรงของกระจกตา ลดลงหลังผ่าตัด และมีแนวโน้มที่จะเกิดการแยกของแผลจากการบาดเจ็บแบบทื่อ
ในการวิเคราะห์อภิมานของ Sela และคณะ (8 การศึกษา รวม 3 RCT, 2 การศึกษาแบบตาเดียวกัน, และ 3 การศึกษาแบบ cohort รวม 376 ตา: DMEK 187 ตา, UT-DSAEK 189 ตา) พบว่า logMAR BCVA ที่ 12 เดือนดีกว่าอย่างมีนัยสำคัญในกลุ่ม DMEK (ผลต่างเฉลี่ย −0.06; ช่วงความเชื่อมั่น 95%: −0.10 ถึง −0.02)8) ในทางกลับกัน ความถี่ของการต้องเติมอากาศซ้ำ (rebubbling) คือ 19.79% ใน DMEK และ 8.99% ใน UT-DSAEK ซึ่งสูงกว่าอย่างมีนัยสำคัญในฝั่ง DMEK (OR 2.76; ช่วงความเชื่อมั่น 95%: 1.46 ถึง 5.22)8) ที่น่าสนใจคือ ใน DSAEK ที่มีความหนาของ graft น้อยกว่า 70 μm ไม่พบความแตกต่างที่มีนัยสำคัญใน BCVA ซึ่งบ่งชี้ว่าการทำให้บางลงอาจลดความแตกต่างระหว่างสองวิธี8)
ตัวชี้วัด PK DSAEK /UT-DSAEK DMEK BCVA ที่ 12 เดือน ฟื้นตัวช้า UT-DSAEK ดี ดีที่สุด8) การเติมอากาศซ้ำ (Rebubbling) ไม่จำเป็น ประมาณ 9% ประมาณ 20%8) อัตราการปฏิเสธใน 5 ปี ประมาณ 22% ประมาณ 22% ประมาณ 2.8%9) อัตราความล้มเหลวของกราฟต์ ต่ำ ปานกลาง ค่อนข้างสูง3,9) ความต้านทานต่อการบาดเจ็บหลังผ่าตัด ต่ำ ดี ดี
หากอาการบวมน้ำไม่ดีขึ้นหลังจาก 6 เดือนหลังผ่าตัด ถือว่ามีภาวะ decompensation ของเซลล์เยื่อบุผนังกระจกตา และเป็นข้อบ่งชี้ในการปลูกถ่ายเยื่อบุผนังกระจกตา 9) แม้ในตาที่ซับซ้อน เช่น ไมโครคอร์เนีย หรือมี ACIOL ค้างอยู่ ก็สามารถทำ DSAEK ได้ และมีรายงานการฟื้นฟูการมองเห็น ที่ดีโดยไม่ต้องเปลี่ยน IOL 3)
การเลือกระหว่าง DMEK และ DSAEK ขึ้นอยู่กับการมีตาที่ซับซ้อนในผู้ป่วย ประสบการณ์ของศัลยแพทย์ การพยากรณ์การมองเห็น ที่คาดหวัง และระบบการจัดการหลังผ่าตัด ในตาที่ซับซ้อน (ข้อบกพร่องของม่านตา กว้าง, IOL ในช่องหน้าม่านตา , ประวัติการผ่าตัดน้ำวุ้นตา , ตาที่มีท่อระบายต้อหิน , ตาไม่มีเลนส์) การคลี่และวางตำแหน่งกราฟต์ทำได้ยาก ดังนั้น DSAEK (หรือ DSAEK บางพิเศษ) จึงปลอดภัยกว่า 3,8) ในทางกลับกัน ในกรณีที่ไม่มีภาวะแทรกซ้อน DMEK ให้ข้อดีของการฟื้นฟูการมองเห็น เร็วขึ้นและอัตราการปฏิเสธต่ำกว่า 9)
ในการจัดการหลังผ่าตัด จะทำการอุดช่องหน้าม่านตา ด้วยอากาศหรือแก๊ส (เช่น SF6 หรือ C3F8) เพื่อให้กราฟต์แนบสนิทกับสโตรมาชั้นหลัง ผู้ป่วยจะถูกขอให้นอนหงายเป็นเวลาหลายวันหลังผ่าตัด และหากเกิดการหลุดลอกของกราฟต์ จะทำการฉีดอากาศซ้ำ (rebubbling) ยาหยอดตาสเตียรอยด์ จะใช้ต่อเนื่องเป็นเวลาหลายเดือนถึงมากกว่าหนึ่งปีเพื่อป้องกันการปฏิเสธ จากนั้นจึงคงการรักษาด้วยขนาดต่ำ
Kinoshita และคณะได้พัฒนาการบำบัดโดยการฉีดเซลล์เยื่อบุผนังกระจกตา มนุษย์ที่เพาะเลี้ยงร่วมกับสารยับยั้ง ROCK Y-27632 เข้าไปในช่องหน้าม่านตา มีรายงานว่า 10 ใน 11 ตาที่เป็นโรคกระจกตา พอง (bullous keratopathy) ยังคงความใสของกระจกตา หลังจาก 5 ปี โดยมีความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา เฉลี่ย 1,257 เซลล์/ตร.มม. 14) การบำบัดนี้ได้รับการอนุมัติให้ผลิตและจำหน่ายในญี่ปุ่นในปี 2022 หลังจากการทดลองทางคลินิกระยะ II/III และได้รับความสนใจจากนานาชาติในฐานะเวชศาสตร์ฟื้นฟูเพื่อชดเชยการขาดแคลนกระจกตา บริจาค 1,14)
ขั้นตอนของการบำบัดนี้คือการแยกและเพาะเลี้ยงเซลล์เยื่อบุผนังกระจกตา จากกระจกตา บริจาค จากนั้นฉีดสารแขวนลอยเซลล์ที่เติมสารยับยั้ง ROCK Y-27632 เข้าไปในช่องหน้าม่านตา หลังการฉีด จะรักษาท่าคว่ำหน้า (หันหน้าลง) เป็นเวลาหลายชั่วโมงเพื่อให้เซลล์ตกตะกอนและยึดติดกับพื้นผิวเยื่อบุผนังกระจกตา ด้วยแรงโน้มถ่วง เมื่อเทียบกับการปลูกถ่ายเยื่อบุผนังกระจกตา แบบดั้งเดิม แผลมีขนาดเล็กกว่า และสามารถรักษาหลายกรณีจากกระจกตา บริจาคชิ้นเดียว จึงมีความสำคัญอย่างยิ่งในการใช้กระจกตา บริจาคอย่างมีประสิทธิภาพ
แผนการรักษาจะพิจารณาจากการประเมินที่ครอบคลุมถึงระดับความก้าวหน้าของอาการบวมน้ำ ความหนาแน่นของเซลล์เยื่อบุผนังกระจกตา ความต้องการด้านการมองเห็น โรคร่วม สภาพร่างกายโดยรวม และความต้องการของผู้ป่วย ในกรณีที่ไม่รุนแรงและระยะเริ่มต้น จะสังเกตอาการด้วยการรักษาแบบประคับประคองหรือยาหยอดตาที่ยับยั้ง ROCK ในกรณีปานกลางถึงรุนแรง จะพิจารณาการปลูกถ่ายเยื่อบุผนังกระจกตา ในกรณีรุนแรงที่มีความขุ่นของสโตรมาหรือการบุกรุกของหลอดเลือด จะเลือกการปลูกถ่ายกระจกตา ทั้งชั้น แม้ในกรณีที่เหมาะสมกับการผ่าตัด หากอาการหลักคือปวดและการพยากรณ์การมองเห็น ไม่ดี การปลูกถ่ายเยื่อหุ้มน้ำคร่ำหรือ PTK เพื่อการรักษาจะมีประโยชน์เป็นการรักษาตามอาการ
ในกรณีที่ไม่มีความหวังในการมองเห็น ดีขึ้นและมีอาการปวดรุนแรงจากตุ่มน้ำ จะเลือกทำการเจาะสโตรมาชั้นหน้า (ASP ), การตัดกระจกตา ด้วยเลเซอร์เอ็กไซเมอร์เพื่อการรักษา (PTK ) หรือการปลูกถ่ายเยื่อหุ้มน้ำคร่ำเพื่อบรรเทาอาการปวด
กระจกตา
ภาวะแทรกซ้อนหลักหลังการปลูกถ่ายเอ็นโดทีเลียมกระจกตา ได้แก่ การหลุดลอกของกราฟต์ (ต้องฉีดอากาศซ้ำ), กราฟต์ล้มเหลว, ปฏิกิริยาการปฏิเสธ, การอุดตันรูม่านตา จากอากาศ, และการเจริญของเยื่อบุผิวผิดที่ซึ่งพบได้น้อย การตรวจพบตั้งแต่เนิ่นๆ และการจัดการที่เหมาะสมเป็นตัวกำหนดพยากรณ์การมองเห็น การติดตามผลอย่างสม่ำเสมอและการให้ความรู้แก่ผู้ป่วยเป็นสิ่งจำเป็นหลังผ่าตัด
Q
สามารถหลีกเลี่ยงการปลูกถ่ายกระจกตาได้ด้วยยาหยอดตาที่ยับยั้ง ROCK หรือไม่?
A
ในโรคกระจกตาพุพองชนิดไม่รุนแรงถึงปานกลาง มีรายงานการปรับปรุงของอาการบวมน้ำที่กระจกตา และการชะลอหรือหลีกเลี่ยงการปลูกถ่ายกระจกตา ด้วยยาหยอดตาที่ยับยั้ง ROCK (ริพาซูดิล) อย่างไรก็ตาม ผลมีจำกัดในกรณีที่ลุกลามซึ่งเซลล์เอ็นโดทีเลียมลดลงอย่างรุนแรง ปัจจุบันยาหยอดยับยั้ง ROCK ยังไม่ได้รับการยอมรับว่าเป็นการรักษามาตรฐาน และเสาหลักของการรักษาให้หายขาดคือการปลูกถ่ายเอ็นโดทีเลียมกระจกตา โปรดปรึกษาแพทย์เพื่อเลือกการรักษาที่เหมาะสมกับสภาพโรคของแต่ละบุคคล
Q
การรักษาด้วยการฉีดเซลล์เอ็นโดทีเลียมกระจกตาที่เพาะเลี้ยงสามารถรับได้ในญี่ปุ่นหรือไม่?
A
ใช่ การรักษาด้วยการฉีดเซลล์เอ็นโดทีเลียมกระจกตา ที่เพาะเลี้ยงได้รับการอนุมัติให้วางตลาดในญี่ปุ่นในปี 2022 อย่างไรก็ตาม สถานพยาบาลที่สามารถดำเนินการได้มีจำกัด และมีเกณฑ์บ่งชี้ การรักษานี้ไม่เหมาะกับผู้ป่วยโรคกระจกตาพุพองทุกราย จำเป็นต้องปรึกษาแพทย์เพื่อพิจารณาความเป็นไปได้ ในภาวะที่ขาดแคลนกระจกตา บริจาคอย่างรุนแรง การรักษานี้คาดว่าจะพัฒนาเป็นเวชศาสตร์ฟื้นฟูที่มาจากญี่ปุ่น
กระจกตา รักษาความใสโดยการรักษาปริมาณน้ำประมาณ 78% (การลดอาการบวม) ภาวะขาดน้ำสัมพัทธ์นี้คงอยู่โดยสมดุลของปัจจัยห้าประการดังต่อไปนี้
แรงดันบวมของสโตรมา (SP) : ประมาณ 50 มิลลิเมตรปรอท ไกลโคซามิโนไกลแคนในสโตรมากระจกตา ทำให้เนื้อเยื่อขยายตัวโดยการผลักกันของประจุลบ ดึงของเหลวเข้าไปหน้าที่กั้นของเยื่อบุผิว : รอยต่อแน่นของเยื่อบุผิวมีความต้านทานต่อการไหลของน้ำประมาณสองเท่าของเอ็นโดทีเลียมกระจกตา หน้าที่ปั๊มของเอ็นโดทีเลียม : การลำเลียงแบบแอคทีฟขับของเหลวออกจากสโตรมากระจกตา ไปยังอารมณ์ขันในช่องหน้าม่านตา การระเหยของน้ำตา : การดึงน้ำออกจากผิวกระจกตา โดยออสโมซิสความดันลูกตา (IOP )ความดันลูกตา เกินแรงดันบวมของสโตรมา จะเกิดการเคลื่อนที่ของของเหลวไปข้างหน้า
การควบคุมน้ำของเอ็นโดทีเลียมกระจกตา อธิบายโดยกลไกปั๊ม-รั่วที่เสนอโดย Maurice เซลล์เอ็นโดทีเลียมขับเคลื่อนฟลักซ์ไอออนสุทธิจากสโตรมาของกระจกตา ไปยังช่องหน้าม่านตา ผ่านกลไกการลำเลียงแบบแอคทีฟปฐมภูมิและทุติยภูมิ ทำให้เกิดการไล่ระดับออสโมติก การทำงานของปั๊มนี้ขึ้นอยู่กับ HCO₃⁻ และ Cl⁻ เป็นหลัก โดยมี Na⁺/K⁺-ATPase เป็นแกนกลาง 11)
ความดันดูดซับ IP ในตาปกติแสดงเป็น IP = IOP − SP โดยปกติจะเป็นความดันลบประมาณ −35 ถึง −45 มิลลิเมตรปรอท ในภาวะเอ็นโดทีเลียมทำงานผิดปกติ ความชื้นในสโตรมาจะเพิ่มขึ้นและ SP ลดลง และเมื่อดำเนินต่อไป SP จะต่ำกว่า IOP และ IP กลายเป็นความดันบวก ในภาวะความดันบวก น้ำจะถูกปั๊มออกจากสโตรมาไปยังด้านเยื่อบุผิว ทำให้เกิดอาการบวมน้ำที่เยื่อบุผิวและตุ่มน้ำ ในทางกลับกัน ในภาวะความดันลูกตาสูง (มากกว่าประมาณ 50 มิลลิเมตรปรอท) แม้ว่าเอ็นโดทีเลียมจะปกติ น้ำในช่องหน้าม่านตา สามารถถูกดันเข้าไปในชั้นเยื่อบุผิวทำให้เกิดอาการบวมน้ำที่เยื่อบุผิว แต่ในกรณีนี้ SP ไม่เปลี่ยนแปลงและไม่มีอาการบวมน้ำที่สโตรมาร่วมด้วย
ตามรายงานของ Tone และคณะ ในระยะเริ่มต้นของโรคเสื่อมเอ็นโดทีเลียมกระจกตา ฟุคส์ พบว่ามีการเพิ่มขึ้นแบบชดเชยของความหนาแน่น Na⁺/K⁺-ATPase แต่เมื่อโรคดำเนินไป ความหนาแน่นจะลดลงเรื่อยๆ 11) การตรวจ PCR แบบเรียลไทม์ตรวจพบการลดลงอย่างมีนัยสำคัญของความหนาแน่น Na⁺/K⁺-ATPase ในกรณีที่ดำเนินไปมาก ซึ่งยืนยันความล้มเหลวของการทำงานของปั๊มเอ็นโดทีเลียมร่วมกับการลดลงของ MCT1 และ MCT4 การเพิ่มขึ้นของการซึมผ่านของเอ็นโดทีเลียมกระจกตา (ความผิดปกติของสิ่งกีดขวาง) ยังแสดงให้เห็นว่าเกิดขึ้นก่อนความผิดปกติของปั๊ม 11)
การลดลงของเซลล์เอ็นโดทีเลียมหลังการผ่าตัดต้อกระจก เกิดขึ้นจากหลายกลไก การสัมผัสกับเครื่องมือและเลนส์แก้วตาเทียม ระหว่างการผ่าตัด และความเสียหายทางกลและทางกายภาพจากพลังงานอัลตราซาวนด์เป็นสาเหตุหลัก และการบาดเจ็บของม่านตา จะเพิ่มความเข้มข้นของไซโตไคน์อักเสบในช่องหน้าม่านตา ซึ่งเร่งการลดลงของเอ็นโดทีเลียมในระยะยาว 1,2)
หากเกิดอาการบวมน้ำที่กระจกตา เมื่อมีเลนส์แก้วตาเทียม แม้ว่าจะมี guttae ที่เอ็นโดทีเลียมกระจกตา ก็จะถูกกำหนดให้เป็นโรคกระจกตาพุพองหลังผ่าตัด แตกต่างจากโรคเสื่อมเอ็นโดทีเลียมกระจกตา ฟุคส์ ในโรคกระจกตาพุพองหลังผ่าตัด อาการบวมน้ำที่กระจกตา มักเริ่มจากบริเวณรอบนอกและดำเนินไปสู่ศูนย์กลาง
เมื่อความหนาแน่นของเซลล์เอ็นโดทีเลียมกระจกตา ลดลงต่ำกว่าประมาณ 2,000 เซลล์/ตร.มม. การซึมผ่านจะเพิ่มขึ้นทีละน้อย แต่ภาวะแห้ง (deturgescence) จะคงอยู่จนถึงประมาณ 500–400 เซลล์/ตร.มม. ด้วยกลไกปั๊มชดเชย หากต่ำกว่าเกณฑ์นี้ มีแนวโน้มสูงที่จะดำเนินไปสู่โรคกระจกตาพุพอง อย่างไรก็ตาม เกณฑ์นี้แตกต่างกันไปในแต่ละบุคคล และการเกิดอาการบวมน้ำขึ้นอยู่กับการทำงานของเอ็นโดทีเลียมของแต่ละคนแม้ว่าความหนาแน่นของเซลล์จะเท่ากัน
เซลล์เอนโดทีเลียมของกระจกตา แทบจะไม่มีการแบ่งตัวในสภาพแวดล้อมของช่องหน้าม่านตา และเมื่อเกิดข้อบกพร่อง จะถูกปกคลุมโดยการขยายตัวและการย้ายที่ของเซลล์รอบข้าง ในกระบวนการซ่อมแซมนี้ พื้นที่เซลล์เพิ่มขึ้น และความแตกต่างของรูปร่าง (pleomorphism) และความแตกต่างของขนาด (polymegethism) ปรากฏชัดเจน ด้วยกล้องจุลทรรศน์สเปคิวลาร์ การเปลี่ยนแปลงเหล่านี้จะถูกวัดเชิงปริมาณเป็นการเพิ่มขึ้นของค่าสัมประสิทธิ์ความแปรปรวน (CV) และการลดลงของเปอร์เซ็นต์เซลล์หกเหลี่ยม ตราบใดที่ความหนาแน่นของเซลล์ยังสูง การทำงานของปั๊มจะยังคงอยู่ แต่เมื่อถึงขีดจำกัดของการชดเชย จะเกิดการเปลี่ยนผ่านอย่างรวดเร็วไปสู่อาการบวมน้ำ การเสื่อมของการทำงานของเอนโดทีเลียมอาจเกิดขึ้นก่อนการลดลงของความหนาแน่น ดังนั้นค่าสัมบูรณ์ของความหนาแน่นเพียงอย่างเดียวไม่สามารถทำนายการเกิดโรคกระจกตาพุพองได้อย่างสมบูรณ์
การอักเสบเรื้อรังในช่องหน้าม่านตา หลังการผ่าตัดต้อกระจก หรือการผ่าตัดลูกตาอื่นๆ มีส่วนทำให้เซลล์เอนโดทีเลียมลดลงเรื้อรังผ่านไซโตไคน์อักเสบ (TNF -α, IL-1, IL-6) ไซโตไคน์เหล่านี้เหนี่ยวนำให้เกิดอะพอพโทซิส ของเซลล์เอนโดทีเลียม ลดทั้งการทำงานของสิ่งกีดขวางและการทำงานของปั๊ม การอักเสบที่คงอยู่หลังการผ่าตัดเป็นปัจจัยเสี่ยงสำคัญของ PBK 1)
เนื้อหาต่อไปนี้เป็นการรักษาที่ยังอยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป นำเสนอเป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับความก้าวหน้าทางการแพทย์ในอนาคต
EndoArt (บริษัท EyeYon Medical) เป็นชั้นเอนโดทีเลียมเทียมรูปโดมขนาดเส้นผ่านศูนย์กลาง 6.0 มม. และหนา 50 ไมครอน ซึ่งเข้ากับความโค้งของผิวด้านหลังกระจกตา ทำจากวัสดุอะคริลิกที่ชอบน้ำ และถูกใส่เข้าไปในช่องหน้าม่านตา ด้วยเทคนิคเดียวกับ DMEK เนื่องจากเป็นวัสดุที่ไม่ใช่ชีวภาพ จึงไม่จำเป็นต้องใช้การบำบัดกดภูมิคุ้มกัน และสามารถเก็บรักษาได้ในระยะยาว Auffarth และคณะรายงานการปลูกถ่าย EndoArt ในผู้ป่วยกระจกตาบวมน้ำ เรื้อรัง 2 ราย โดยความหนาของกระจกตา ลดลงจาก 730 เป็น 526 ไมครอนในรายที่ 1 และจาก 761 เป็น 457 ไมครอนในรายที่ 2 และคงที่ที่ 17 เดือน 12) ได้รับการกำหนดให้เป็นนวัตกรรมการรักษาที่ก้าวล้ำจาก FDA ของสหรัฐอเมริกา และคาดว่าจะนำไปใช้ในตาที่ซับซ้อน (ไม่มีม่านตา , หลังการตัดวุ้นตา , ตาที่มีท่อระบาย)
DSO เป็นขั้นตอนที่กำจัดเฉพาะเยื่อเดสเซเม็ตส่วนกลางเท่านั้น โดยให้เซลล์เอนโดทีเลียมที่แข็งแรงบริเวณรอบนอกเคลื่อนย้ายและสร้างใหม่เข้าสู่ส่วนกลางเพื่อลดอาการบวมน้ำของกระจกตา ข้อบ่งชี้หลักคือกรณีเริ่มต้นของโรคจอประสาทตา เสื่อมชนิด Fuchs แต่เมื่อเร็ว ๆ นี้มีการรายงานการประยุกต์ใช้ในอาการบวมน้ำของกระจกตา เฉพาะที่ เช่น การสัมผัสท่อ MIGS Khan และ Lin รายงานกรณีอาการบวมน้ำของกระจกตา หลังจากการหลุดลอกของเยื่อเดสเซเม็ตหลังหยุดการใส่อุปกรณ์ MIGS ซึ่งทำ DSO อาการบวมลดลงหลังจาก 6 สัปดาห์ของการตัดเยื่อเดสเซเม็ตแบบเยื้องศูนย์ และความหนาแน่นของเซลล์เอนโดทีเลียมส่วนกลางฟื้นตัวจากตรวจไม่พบเป็น 975 เซลล์/ตร.มม.13) การใช้ยาหยอดตาที่ยับยั้ง ROCK (ripasudil, netarsudil) เป็นการรักษาเสริมกำลังอยู่ระหว่างการศึกษา
สำหรับโรคจอประสาทตา เสื่อมชนิด Fuchs มีการวิจัยพื้นฐานเกี่ยวกับโอลิโกนิวคลีโอไทด์ antisense ที่มุ่งเป้าไปที่การขยายซ้ำ CTG ในยีน TCF 4 และการบำบัดระดับโมเลกุลที่มุ่งเป้าไปที่วิถีความเครียดออกซิเดชัน ความผิดปกติของวิถีความเครียดออกซิเดชัน (การลดลงของสัญญาณ Nrf2/NQO1, ความผิดปกติของไมโตคอนเดรีย) ได้รับการแสดงว่ามีส่วนเกี่ยวข้องกับการตายของเซลล์ และกำลังศึกษาการประยุกต์ใช้ยาป้องกันไมโตคอนเดรียและสารต้านอนุมูลอิสระ
นอกเหนือจากการบำบัดด้วยการฉีดเซลล์เอนโดทีเลียมกระจกตา ที่เพาะเลี้ยงซึ่งมีต้นกำเนิดจากญี่ปุ่นแล้ว การวิจัยที่ใช้เซลล์เอนโดทีเลียมกระจกตา ที่ได้จากเซลล์ iPS หรือสเต็มเซลล์ก็กำลังก้าวหน้าในประเทศอื่น ๆ มีความเป็นไปได้ในการรักษาดวงตาหลายดวงจากตาผู้บริจาคเพียงดวงเดียว ซึ่งคาดหวังให้เป็นทางออกสำหรับการขาดแคลนผู้บริจาคกระจกตา ทั่วโลก1,14) นอกจากนี้ การทดลองทางคลินิกกำลังดำเนินการเกี่ยวกับผลระยะยาวและความปลอดภัยของยายับยั้ง ROCK การประเมินเชิงปริมาณของการเคลื่อนที่ของเซลล์เอนโดทีเลียม และความเข้มข้นและระยะเวลาที่เหมาะสม
เพื่อทำนายการดำเนินของโรคกระจกตาพุพองและประเมินการตอบสนองต่อการรักษา กำลังศึกษาการเปลี่ยนแปลงตามเวลาของความหนากระจกตา ส่วนกลาง ความหนาแน่นของเซลล์เอนโดทีเลียม การตรวจหาอาการบวมน้ำของเยื่อบุผิวและไมโครซีสต์โดยใช้ OCT ส่วนหน้า และความเข้มข้นของไซโตไคน์ในน้ำตา การปรับปรุงความแม่นยำของการประเมินก่อนผ่าตัดคาดว่าจะช่วยกำหนดกลยุทธ์การรักษาที่เหมาะสมที่สุดสำหรับผู้ป่วยแต่ละราย (การรักษาแบบประคับประคองต่อเนื่อง ยาหยอดตายับยั้ง ROCK การปลูกถ่ายเอนโดทีเลียม การผ่าตัดเปลี่ยนกระจกตา แบบทะลุ) ได้ตั้งแต่เนิ่น ๆ
โรคกระจกตาพุพองมักดำเนินไปทั้งสองข้าง และผลกระทบต่อการมองเห็น ในชีวิตประจำวันมีมาก การมองเห็น ลดลงในตอนเช้ารบกวนงานบ้านและการเดินทาง และเมื่อดำเนินไป การอ่าน การขับรถ และงานที่ต้องใช้รายละเอียดกลายเป็นเรื่องยาก ในช่วงไม่กี่ปีที่ผ่านมา ความพยายามในการประเมินผลลัพธ์ที่รายงานโดยผู้ป่วย (PROMs) ที่เกี่ยวข้องกับการมองเห็น ก่อนและหลังการผ่าตัดกำลังก้าวหน้า และระดับการปรับปรุงคุณภาพชีวิตที่เกี่ยวข้องกับการมองเห็น ถูกใช้เป็นตัวบ่งชี้ในการเลือกการรักษาอย่างเป็นกลาง8) การประเมินคุณภาพชีวิตโดยใช้แบบสอบถามการมองเห็น -14 หรือ NEI VFQ-25 ก่อนและหลังการปลูกถ่ายเอนโดทีเลียมแสดงให้เห็นว่ากลุ่ม DMEK มีแนวโน้มที่จะปรับปรุงมากกว่า8)
การรักษาโรคกระจกตาพุพอง (bullous keratopathy) มีความหลากหลายมากขึ้น ตั้งแต่การปลูกถ่ายกระจกตา ทั้งชั้นหรือเฉพาะชั้น内皮โดยใช้กระจกตา จากผู้บริจาค ไปจนถึงการรักษาด้วยเซลล์แบบเลือกสรร การรักษาด้วยยา และอุปกรณ์内皮เทียม การฉีดเซลล์内皮กระจกตา ที่เพาะเลี้ยงเข้าไปในช่องหน้าม่านตา ซึ่งเป็นนวัตกรรมของญี่ปุ่น ถือเป็นผู้บุกเบิกและได้รับความสนใจในฐานะทางออกสำหรับการขาดแคลนกระจกตา ผู้บริจาคทั่วโลก ด้วยการขยายขอบเขตการใช้ยาหยอดตาที่ยับยั้ง ROCK การเผยแพร่ EndoArt ในทางคลินิก การขยายข้อบ่งชี้ของ DSO และการนำยีนบำบัดมาใช้จริง คาดว่าตัวเลือกการรักษาจะกว้างขึ้นอีกในทศวรรษหน้า เป้าหมายคือการลดความจำเป็นในการปลูกถ่ายกระจกตา และปรับปรุงการมองเห็น และคุณภาพชีวิตของผู้ป่วยอย่างมีนัยสำคัญผ่านการวินิจฉัยตั้งแต่เนิ่นๆ และกลยุทธ์การรักษาเป็นขั้นตอน
Jukić A, Pavan J, Čapić Ivančić B, et al. RhoKinase (ROCK) Inhibition as a Therapeutic Strategy for Pseudophakic Bullous Keratopathy: A Comprehensive Review. J Clin Med. 2025;14(17):6093.
European Society of Cataract and Refractive Surgeons. ESCRS Clinical Guidelines for Cataract Surgery. 2024.
Singhal A, Kaushik J, Singh A, et al. Descemet Stripping Endothelial Keratoplasty in Microcornea for Pseudophakic Bullous Keratopathy With Anterior Chamber Intraocular Lens. Cureus. 2021;13(11):e19262.
Matthaei M, Hribek A, Clahsen T, Bachmann B, Cursiefen C, Jun AS. Fuchs Endothelial Corneal Dystrophy: Clinical, Genetic, Pathophysiologic, and Therapeutic Aspects. Annu Rev Vis Sci. 2019;5:151-175.
Vandevenne MMS , Berendschot TTJM, Visser N, Dickman MM, Nuijts RMMA. Late-onset corneal edema after customized crosslinking for progressive keratoconus. Am J Ophthalmol Case Rep. 2024;35:102090.
Chu MJ, Song M, Palmares T, Song A, Song J. Rhopressa-induced corneal edema: a case report. J Med Case Rep. 2021;15:182.
Arici C, Mergen B, Kılıçarslan O, Ağaçhan A, Tülü Aygün B, Özdamar A. Diffuse corneal edema after uneventful pterygium surgery: toxic anterior segment syndrome or toxic keratopathy? Turk J Ophthalmol. 2022;52:69-71.
Sela TC, Iflah M, Muhsen K, Zahavi A. Descemet membrane endothelial keratoplasty compared with ultrathin Descemet stripping automated endothelial keratoplasty: a meta-analysis. BMJ Open Ophthalmol. 2023;8:e001397.
American Academy of Ophthalmology Cornea/External Disease PPP Panel. Corneal Edema and Opacification Preferred Practice Pattern. Ophthalmology. 2019.
Erdinest N, Shemesh N, Weill Y, et al. Managing pseudophakic bullous keratopathy with a topical rho kinase inhibitor: a case series. J Med Case Rep. 2025;19:214.
Tone SO, Kocaba V, Böhm M, Wylegala A, White TL, Jurkunas UV. Fuchs endothelial corneal dystrophy: the vicious cycle of Fuchs pathogenesis. Prog Retin Eye Res. 2021;80:100863.
Auffarth GU, Son HS , Koch M, et al. Implantation of an artificial endothelial layer for treatment of chronic corneal edema. Cornea. 2021;40:1633-1638.
Khan NC, Lin CC. Descemet stripping only for Descemet’s membrane detachment and sectoral corneal edema. Am J Ophthalmol Case Rep. 2023;29:101784.
Kinoshita S, Koizumi N, Okumura N, et al. Injection of Cultured Cells with a ROCK Inhibitor for Bullous Keratopathy. N Engl J Med. 2018;378(11):995-1003.