CLAu (پیوند اتولوگ ملتحمه-لیمبوس)
اندیکاسیون: LSCD یک طرفه
روش: برداشت بافت به مدت ۲ تا ۴ ساعت از لیمبوس و ملتحمه چشم سالم و پیوند به لیمبوس چشم مبتلا
مزایا: یک مرحله جراحی کامل میشود و نیازی به مرکز کشت نیست
سلولهای بنیادی اپیتلیوم قرنیه در لیمبوس (limbus)، مرز بین قرنیه و ملتحمه، قرار دارند. ساختارهای حصارمانند لیمبوس (palisades of Vogt: POV) به عنوان جایگاه (نیچ) سلولهای بنیادی عمل کرده و هموستاز اپیتلیوم قرنیه را حفظ میکنند.
آسیب گسترده به این سلولهای بنیادی لیمبال منجر به کمبود سلولهای بنیادی لیمبال (limbal stem cell deficiency: LSCD) میشود. در LSCD، بازسازی اپیتلیوم قرنیه غیرممکن شده و اپیتلیوم ملتحمه به سطح قرنیه حمله میکند (ملتحمهای شدن) 4). در نتیجه، کدورت قرنیه، عروقزایی سطحی و اختلال بینایی پیشرفت میکند.
پیوند معمولی قرنیه در LSCD مؤثر نیست و سطح پیوند دوباره ملتحمهای شده و دچار نارسایی میشود 3). بنابراین، برای تأمین سلولهای بنیادی اپیتلیوم قرنیه طبیعی و تثبیت سطح چشم، بازسازی سطح چشم ضروری است.
هدف بازسازی، بهبود بینایی نیست، بلکه تثبیت سطح چشم است. اگر کدورت استرومای قرنیه باقی بماند، پس از تثبیت سطح چشم، پیوند کامل قرنیه (PKP) یا پیوند لایهای عمیق قرنیه (DALK) در دو مرحله انجام میشود.
بیمارانی که سلولهای بنیادی لیمبوس قرنیه به طور گسترده آسیب دیده و اپیتلیوم ملتحمه به قرنیه入侵 کرده است، کاندید این عمل هستند. علل شایع شامل سوختگی شیمیایی، سندرم استیونز-جانسون، پمفیگوئید چشمی، و آنیریدیا میباشد. در موارد خفیف که تهاجم ملتحمه محدود به محیط است، ابتدا پیگیری انجام میشود.
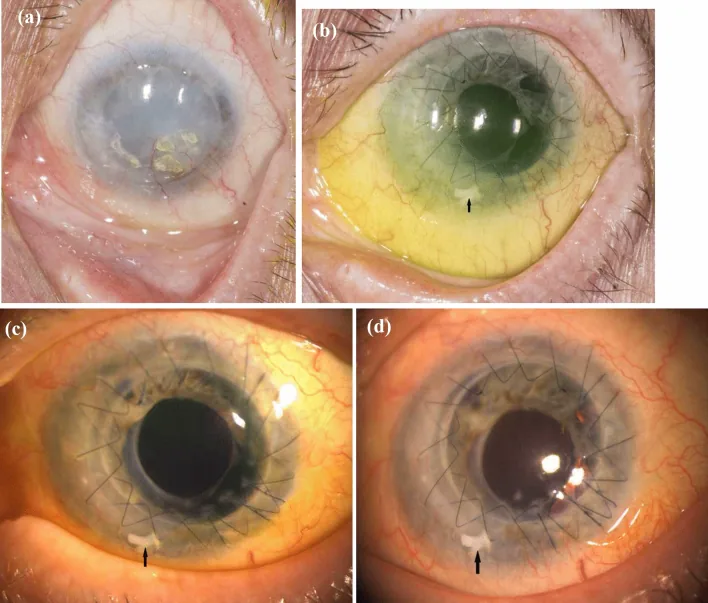
شدت LSCD بر اساس طبقهبندی بینالمللی Deng و همکاران 1) به سه درجه زیر تقسیم میشود.
| طبقهبندی | وسعت ملتحمهای شدن | قرنیه مرکزی |
|---|---|---|
| مرحله I | کمتر از 50% لیمبوس | غیرتهاجمی |
| مرحله II | 50% یا بیشتر لیمبوس | غیرتهاجمی |
| مرحله III | درگیر کل محیط | تهاجم مرکزی |
یافتههای بالینی اصلی به شرح زیر است:
علل LSCD متنوع هستند، اما سوختگی شیمیایی شایعترین علت است. در یک مرور سیستماتیک از پیوند لیمبوس اتولوگ، 88٪ از چشمهای مورد مطالعه دچار سوختگی شیمیایی بودند3).
علل اصلی در زیر آورده شده است.
این اساسیترین روش تشخیصی است. ناپدید شدن POV، وسعت ملتحمهای شدن و میزان عروقزایی سطحی ارزیابی میشود. به طور طبیعی، POV در لیمبوس فوقانی و تحتانی به راحتی قابل مشاهده است، اما در افراد زیر 10 سال و بالای 70 سال ممکن است مشاهده آن دشوار باشد.
برای تجسم ناحیه نقص اپیتلیال قرنیه استفاده میشود. نواحی ملتحمهای شده الگوی رنگآمیزی نقطهای نشان میدهند.
سلولهای سطح قرنیه جمعآوری شده و رنگآمیزی ایمنی انجام میشود. از بین رفتن سیتوکراتین 3 (CK3)/CK12 به عنوان نشانگر اپیتلیال قرنیه و بیان CK13/MUC5AC به عنوان نشانگر اپیتلیال ملتحمه برای تشخیص قطعی LSCD مفید است1).
میتواند ضخامت و تغییرات ساختاری اپیتلیوم قرنیه را به صورت غیرتهاجمی ارزیابی کند. نواحی ملتحمهای شده الگوی بازتابی متفاوتی نسبت به اپیتلیوم طبیعی قرنیه نشان میدهند.
میتوان ساختارهای POV و مورفولوژی سلولهای پایه را در سطح سلولی مشاهده کرد. همچنین برای تمایز بین اپیتلیوم قرنیه و ملتحمه مفید است، اما تجهیزات معاینه فقط در مراکز محدودی موجود است.
انتخاب روش درمان بسته به یک طرفه یا دو طرفه بودن بیماری تفاوت زیادی دارد. در LSCD یک طرفه، میتوان بافت اتولوگ از لیمبوس چشم سالم برداشت، اما در موارد دو طرفه، بافت لیمبال اتولوگ در دسترس نیست، بنابراین از منابع سلولی جایگزین مانند اپیتلیوم مخاط دهان استفاده میشود.
CLAu (پیوند اتولوگ ملتحمه-لیمبوس)
اندیکاسیون: LSCD یک طرفه
روش: برداشت بافت به مدت ۲ تا ۴ ساعت از لیمبوس و ملتحمه چشم سالم و پیوند به لیمبوس چشم مبتلا
مزایا: یک مرحله جراحی کامل میشود و نیازی به مرکز کشت نیست
SLET (پیوند اپیتلیوم لیمبال ساده)
اندیکاسیون: LSCD یک طرفه
روش: برداشت قطعه کوچکی از بافت لیمبال از چشم سالم و پیوند آن به صورت پراکنده روی آمنیون
مزایا: برداشت کم و فشار کم بر چشم سالم
CLET (پیوند اپیتلیوم لیمبال کشت داده شده)
اندیکاسیون: یک طرفه (برداشت کم) یا آلوگرافت از دهنده زنده
روش: کشت سلولهای اپیتلیال لیمبال در خارج از بدن و پیوند به صورت ورقه
مزایا: امکان ساخت ورقه بزرگ از بافت بسیار کوچک
COMET (پیوند اپیتلیوم مخاط دهان کشت داده شده)
اندیکاسیون: LSCD دو طرفه
روش: کشت سلولهای اپیتلیال مخاط دهان خود بیمار و پیوند به صورت ورقه
مزایا: به دلیل پیوند خودی، واکنش رد کم و قابل استفاده در موارد دو طرفه
در مرور سیستماتیک Shanbhag و همکاران3)، سه روش پیوند سلولهای بنیادی لیمبال خودی به شرح زیر مقایسه شده است.
| روش جراحی | موفقیت آناتومیک | موفقیت عملکردی |
|---|---|---|
| CLAu | ۶۹٪ | ۶۰٪ |
| SLET | ۷۸٪ | ۶۹٪ |
| CLET | ۶۱٪ | ۵۲٪ |
تحلیل ۲۲ سری موردی CLAu (۱۰۲۳ چشم)، ۴ مطالعه SLET (۲۵۳ چشم)، ۸ مطالعه CLET (۵۸۱ چشم). ۸۸٪ موارد CLAu و بیش از ۹۰٪ موارد CLET/SLET ناشی از سوختگی شیمیایی بودند. SLET و CLAu موفقیت آناتومیک بهطور معنیداری بالاتری نسبت به CLET داشتند. 3)
مزومدار و همکاران موردی از LSCD یکطرفه ناشی از آسیب قلیایی را گزارش کردند که در آن SLET و پیوند خودی ملتحمه بهصورت یکمرحلهای انجام شد. 2)
مرد ۲۴ ساله، LSCD مرحله III پس از آسیب قلیایی. اپیتلیالسازی قرنیه ۲۴ روز پس از جراحی کامل شد و در ۲۴ ماه پیگیری، بهترین corrected visual acuity (BCVA) 6/12p حاصل شد. مزیت ترمیم همزمان نقص ملتحمه و بازسازی لیمبوس در جراحی یکمرحلهای نشان داده شد. 2)
در صورت باقیماندن کدورت استرومای قرنیه پس از بازسازی سطح چشم، پیوند تماملایه قرنیه یا DALK اضافه میشود. برای جلوگیری از رد اندوتلیال، DALK ترجیح داده میشود. ممکن است مصرف طولانیمدت داروهای سرکوبکننده ایمنی (سیکلوسپورین، تاکرولیموس) لازم باشد.
در موارد یکطرفه، میتوان سلولهای بنیادی اپیتلیال قرنیه را از لیمبوس چشم سالم مقابل برداشت. در موارد دوطرفه، لیمبوس هر دو چشم آسیب دیده است، بنابراین نمیتوان سلولهای بنیادی اپیتلیال قرنیه را برداشت. به همین دلیل، پیوند کشتشده با استفاده از منابع سلولی جایگزین مانند اپیتلیوم مخاط دهان (COMET) انتخاب میشود.
هدف اصلی بازسازی سطح چشم، تثبیت سطح چشم است و بهبود مستقیم بینایی را تضمین نمیکند. اگر استرومای قرنیه کدر باشد، درمان دو مرحلهای شامل پیوند قرنیه پس از بازسازی لازم است. بهبود بینایی ممکن است چند ماه تا بیش از یک سال طول بکشد.
سلولهای بنیادی اپیتلیال قرنیه در لایه پایه لیمبوس درون برآمدگیهای پالیزادی (POV) قرار دارند. POV از برجستگیهای پاپیلاری استروما تشکیل شده و سرشار از عروق و اعصاب است. این ریزمحیط (نیچ) خودنوسازی و تمایز سلولهای بنیادی را کنترل میکند.
سلولهای بنیادی از طریق تقسیم نامتقارن خودنوسازی میکنند و در عین حال سلولهای تقویتکننده گذرا (TAC) تولید میکنند. TACها در حین حرکت به سمت مرکز قرنیه تقسیم و تمایز مییابند و در نهایت به سلولهای اپیتلیال قرنیه تبدیل شده و از سطح جدا میشوند.
هنگامی که سلولهای بنیادی لیمبوس آسیب میبینند، شرایط زیر به صورت زنجیرهای پیشرفت میکند:
سطح قرنیه ملتحمهای شده عملکرد سد را کاهش میدهد و نقص اپیتلیال پایدار مکرر رخ میدهد. تداوم التهاب ممکن است منجر به ذوب استروما یا سوراخ شدن شود.
در COMET (پیوند اپیتلیوم مخاط دهان کشتشده)، ظروف کشت پاسخدهنده به دما فناوری اصلی هستند1). پوشش پلی (N-ایزوپروپیلآکریلآمید) روی سطح ظرف کشت در دمای 37 درجه سانتیگراد آبگریز و با کاهش دما آبدوست میشود. این امر امکان جداسازی لایه سلولی از ظرف کشت بدون درمان آنزیمی را فراهم میکند و پیوند با حفظ اتصالات بین سلولی و ماتریکس امکانپذیر است1).
در موارد COMET از PMC10219018، لایه و بافت پیوندی با ایمونوهیستوشیمی ارزیابی شد1).
در ژاپن، در ژوئن 2021، اولین محصول COMET در جهان به نام Ocural® تحت پوشش بیمه قرار گرفت 1). Ocural® برای LSCD دوطرفه بدون Symblepharon (چسبندگی پلک به کره چشم) مناسب است. برای موارد همراه با Symblepharon، از Sakracy® استفاده میشود 1).
توشیدا و همکاران نتایج اولیه دو مورد از Ocural® را گزارش کردند. مورد اول یک مرد 79 ساله (LSCD مرحله III دوطرفه) و مورد دوم نیز LSCD دوطرفه بود که در هر دو پیوند موفقیتآمیز بود. در لایههای پیوندی پس از جراحی، بیان p63، p75NTR و Ki-67 تأیید شد که نشاندهنده حفظ ویژگیهای سلولهای بنیادی و توانایی تکثیر است. 1)
برای LSCD یک طرفه، Nepic® (لایه سلولهای اپیتلیال لیمبوس اتولوگ کشتشده) قابل استفاده است 1).
در اروپا، Holoclar® به عنوان اولین پیوند اپیتلیال لیمبوس اتولوگ کشتشده به عنوان یک داروی اتحادیه اروپا تأیید شد 1). این محصول پیشگام پزشکی بازساختی در درمان LSCD است و رویکرد متفاوتی (مشتق از اپیتلیوم لیمبوس در مقابل اپیتلیوم مخاط دهان) نسبت به Ocural® ژاپنی دارد.
در گزارش مازومدار و همکاران، انجام همزمان SLET و پیوند اتولوگ ملتحمه (CAG) در یک مرحله، ترمیم نقص ملتحمه و بازسازی لیمبوس را به طور همزمان محقق کرد. اپیتلیالسازی کامل در روز 24 پس از جراحی رخ داد و BCVA در 24 ماه به 6/12p بهبود یافت. 2)
در SLET سنتی، ناحیه نقص ملتحمه یا به صورت صلبیه در معرض باقی میماند یا با آمنیون پوشانده میشود، اما انجام همزمان CAG ممکن است پوشش زودهنگام ملتحمه و سطح پایدار چشم را فراهم کند 2).
در مرور سیستماتیک شانباگ و همکاران (1857 چشم)، نرخ موفقیت آناتومیک کلی برای پیوند اتولوگ لیمبوس 69% و نرخ موفقیت عملکردی 61% بود. از نظر روش جراحی، SLET و CLAu نتایج بهتری نسبت به CLET نشان دادند. با این حال، کیفیت مطالعات و حجم نمونه بین گروهها تفاوت معنیداری داشت و تفسیر نتایج نیاز به احتیاط دارد. 3)
در آینده، کارآزماییهای تصادفی کنترلشده و جمعآوری نتایج بلندمدت ضروری است. درمانهای سلولی نسل بعدی مانند لایههای سلولهای اپیتلیال قرنیه مشتق از سلولهای iPS نیز در مرحله تحقیقاتی قرار دارند.
لایه سلولهای اپیتلیال مخاط دهان کشتشده (CAOMECS) در سال 2004 گزارش شد و اثربخشی آن به عنوان پیوند اتولوگ برای LSCD دوطرفه تأیید شده است. با این حال، در پیگیری طولانیمدت، در برخی موارد کدورت مجدد به دلیل نفوذ عروق از ناحیه اطراف قرنیه مشاهده شده است. تفاوت در ویژگیهای اپیتلیوم قرنیه و اپیتلیوم مخاط دهان به عنوان علت احتمالی مطرح شده است و استفاده از سلولهای اپیتلیال قرنیه خود بیمار برای درمان ریشهای مطلوبتر در نظر گرفته میشود.
تحقیقات در زمینه بازسازی قرنیه با استفاده از منابع سلولی غیر از سلولهای بنیادی لیمبوس در حال پیشرفت است.
وجود سلولهای پیشساز در استرومای قرنیه نیز نشان داده شده است و تحقیقات در مورد اندوتلیوم قرنیه به عنوان یک درمان جدید برای کراتوپاتی تاولی و غیره در حال پیشرفت است.
بله، در سال 2021 محصول COMET به نام Ocural® تحت پوشش بیمه قرار گرفت. با این حال، فقط در مراکزی قابل استفاده است که چشمپزشک متخصص عضو انجمن قرنیه ژاپن و انجمن پیوند قرنیه ژاپن بوده و دوره آموزشی مشخصی را گذرانده باشد. اندیکاسیون آن کمبود سلول بنیادی لیمبوس با شدت متوسط تا شدید است.