انعدام القزحية المعزول
التكرار: حوالي ثلثي الحالات.
نمط الوراثة: جسمي سائد (AD).
الخصائص: ناتج عن طفرة في جين PAX6. لا يصاحبه أعراض جهازية. الاختراق كامل ولكن التعبير متغير.

انعدام القزحية (Aniridia) هو مرض خلقي نادر يتميز بنقص تنسج أو غياب القزحية بدرجات متفاوتة. اسم “انعدام القزحية” هو تسمية خاطئة، حيث يمكن دائمًا رؤية أجزاء من نسيج القزحية تقريبًا باستخدام تنظير الزاوية (gonioscopy) أو المجهر الحيوي بالموجات فوق الصوتية (UBM).
يبلغ معدل الانتشار حوالي 1/40,000 إلى 1/100,000، ولم يتم الإبلاغ عن اختلافات عرقية أو جنسية ملحوظة 1). في التصنيف الدولي للأمراض (ICD-10)، يُصنف تحت رمز Q13.1.
إنه مرض يصيب العين بأكملها (pan-ocular) لا يؤثر فقط على القزحية، بل أيضًا على القرنية، العدسة، زاوية العين، النقرة، والعصب البصري 1)، ويظهر بمضاعفات عينية متعددة تهدد البصر. يكون تشخيص البصر سيئًا بشكل عام، وغالبًا ما تبقى حدة البصر المصححة حوالي 0.1. يختفي رد فعل الحدقة (pupillary reflex) ولكن يبقى رد فعل التكيف (accommodation) محفوظًا، وتكون الحالة ثنائية الجانب في 60-90% من الحالات.
تم التعرف على الأنماط الظاهرية الثلاثة التالية.
انعدام القزحية المعزول
التكرار: حوالي ثلثي الحالات.
نمط الوراثة: جسمي سائد (AD).
الخصائص: ناتج عن طفرة في جين PAX6. لا يصاحبه أعراض جهازية. الاختراق كامل ولكن التعبير متغير.
متلازمة WAGR
التكرار: جزء من الحالات المتفرقة.
نمط الوراثة: حذف متجاور لجيني PAX6 وWT1.
الخصائص: يرافقه ورم ويلمز، تشوهات الجهاز البولي التناسلي، وتأخر عقلي. خطر الورم يصل إلى 50%.
متلازمة غيليسبي
التكرار: حوالي 2% من الحالات.
نمط الوراثة: طفرة في جين ITPR1.
الخصائص: يرافقه رنح مخيخي وإعاقة ذهنية. يتميز بشذوذ قزحي محدد يتمثل في حدقة ثابتة ومتوسعة 3).
يشكل انعدام القزحية المتفرق حوالي ثلث الحالات الكلية، وينتج عن حذف de novo في 11p13 يشمل PAX6. إذا امتد الحذف ليشمل جين WT1 المجاور، فإنه يسبب متلازمة WAGR 1). 25-30% من حالات انعدام القزحية المتفرق يصابون بورم ويلمز، ويبلغ الخطر النسبي 67.
PAX6 هو الجين الرئيسي المتحكم في تكوين العين، ويشارك في تطور العين، الأنبوب العصبي، البصلة الشمية، جزر لانغرهانس في البنكرياس، والظهارة الشمية. يحدث المرض بسبب فقدان وظيفة أليل واحد (haploinsufficiency)، وعند شذوذ الأليلين يكون مميتًا للجنين. في عام 2017، تم تصنيفه كمرض نادر محدد بموجب قانون الأمراض النادرة، ويصبح مؤهلاً للإعانات الطبية إذا كانت شدته من الدرجة الثالثة أو أعلى (انظر قسم التشخيص والفحص للتفاصيل) 7).
تمثل الحالات المتفرقة (الطفرات الجديدة) حوالي ثلث الحالات، ويمكن أن تحدث دون تاريخ عائلي. في الحالات المتفرقة، هناك احتمال لمتلازمة WAGR، لذلك من المهم إجراء الفحص الجيني وفحص الموجات فوق الصوتية للبطن للكشف عن ورم ويلمز.
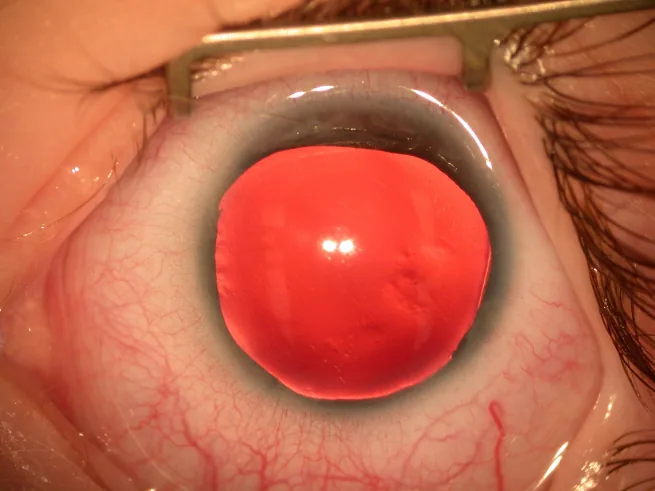
يتم اكتشاف معظم حالات انعدام القزحية عند الولادة بسبب شذوذ القزحية والحدقة، أو في مرحلة الرضاعة بسبب الرأرأة.
يختلف النمط الظاهري بين العائلات وداخل العائلة الواحدة، لكن الفرق بين العين اليمنى واليسرى عادة ما يكون صغيرًا.
بسبب نقص تنسج النقرة بشكل أساسي، غالبًا ما تكون حدة البصر المصححة حوالي 0.1-0.2. يكون تشخيص البصر سيئًا بشكل خاص في حالة وجود نقص تنسج البقعة الصفراء. تصحيح الانكسار ورعاية ضعف البصر منذ الطفولة المبكرة مهمان للنمو البصري.
نظرًا لأن PAX6 يُعبر عنه أيضًا في الجهاز العصبي المركزي وجزر لانغرهانس في البنكرياس والظهارة الشمية، فقد تحدث المضاعفات خارج العين التالية 8).
العوامل الحاسمة في تحديد الوظيفة البصرية هي الجلوكوما، نقص تنسج البقعة، الرأرأة، اعتلال القرنية، إعتام عدسة العين، وتشوهات القزحية. نظرًا لأن تلف المجال البصري وضعف البصر الناجم عن الجلوكوما لا رجعة فيه، فإن إدارة ضغط العين هي الأهم في المتابعة8).
معظم حالات انعدام القزحية الخلقي ناتجة عن طفرات متغايرة الزيجوت في جين PAX6 الموجود على الذراع القصير للكروموسوم 11 (11p13). آلية المرض الرئيسية هي نقص الجرعة (haploinsufficiency)1).
جين PAX6 هو جين تحكم رئيسي في تكوين العين، ويلعب دورًا مهمًا في تطور العين والأنبوب العصبي والبصلة الشمية والبنكرياس. يتطلب التطور الطبيعي للعين نسختين من PAX6، وفقدان وظيفة نسخة واحدة فقط يؤدي إلى انعدام القزحية1).
في دراسة جماعية للمرضى الصينيين، تم تحديد طفرات مسببة في جين PAX6 في 96.9% من الحالات1). في انعدام القزحية النموذجي، يتم اكتشاف طفرات تحفز تحلل mRNA المعتمد على الطفرات غير المنطقية (NMD) أو حذف كبير في 96% من الحالات1).
من الناحية المرضية، هناك نقص في العضلات الملساء مع بقاء جذر القزحية، ويلاحظ نقص تطور الزاوية. هناك خلل وظيفي في الخلايا الجذعية الظهارية للقرنية، مما يؤدي إلى تشوهات في الظهارة وغشاء بومان، وتشكل غشاء وعائي كثيف (pannus).
فيما يلي تفصيل طفرات PAX6 المسببة لنمط انعدام القزحية.
| نوع الطفرة | التكرار |
|---|---|
| طفرة غير منطقية (nonsense) | حوالي 39% |
| طفرة إزاحة الإطار (frameshift) | حوالي 25% |
| طفرة في موقع الوصل (splice site) | حوالي 13% |
| طفرة مغلطة (missense) | حوالي 12% |
الطفرات المستمرة (طفرات تمديد الطرف الكربوكسيلي) تمثل حوالي 5%، حيث يتحول كودون التوقف إلى كودون ترجمة مما يؤدي إلى إنتاج بروتين PAX6 ممتد بشكل غير طبيعي 6). غالبًا ما ترتبط طفرات تمديد الطرف الكربوكسيلي بنقص تنسج القزحية الشديد وضعف البصر الشديد 1)6).
الطفرات الجينية غالبًا ما تكون من النوع PTC، كما توجد تقارير عن طفرات مغلطة 7). فيما يتعلق بفائدة الفحص الجيني، يمكن اكتشاف طفرات في حوالي 85% من حالات انعدام القزحية المعزول باستخدام تسلسل سانجر أو NGS. بالإضافة إلى ذلك، يمكن اكتشاف حذف داخل جين PAX6 أو في المنطقة المنظمة له (cis-regulatory) في حوالي 15% من الحالات باستخدام MLPA أو CMA 8).
حدد Wang (2023) طفرة إزاحة الإطار c.640_646del (p.R214Pfs*28) الجديدة، وأبلغ عن حالة أظهرت غيابًا كاملاً للقزحية، ونقص تنسج النقرة، وانحراف العدسة، وانفصال الشبكية 1).
حدد Ratna وزملاؤه (2022) طفرة مستمرة c.1268A>T (p.*423L) في عائلة هندية. أظهر المصابون انعدام قزحية كامل، ورأرأة، ونقص تنسج النقرة، وAAK، وخلع جزئي علوي للعدسة، وقصر نظر شديد، وضمور العصب البصري، مما يشير إلى نمط ظاهري شديد ناتج عن طفرة تمديد الطرف الكربوكسيلي 6).
في حالات انعدام القزحية المتفرقة، يؤدي الحذف الكبير الذي يشمل جين WT1 بالإضافة إلى PAX6 إلى متلازمة WAGR. يصل خطر ورم ويلمز إلى 50% في حالة وجود حذف WT1 1). إذا كان هناك اشتباه بمتلازمة WAGR، يمكن تأكيد نقص PAX6 وWT1 من خلال الفحص الجيني، مما يتيح تقييم خطر ورم ويلمز ومتابعة تأخر النمو 8). يعد تقييم منطقة WT1 عن طريق الفحص الجيني أمرًا ضروريًا، ويُذكر أن 30% من الحالات المتفرقة تصاب بورم ويلمز قبل سن 5 سنوات. نظرًا لموقع جين WT1 بالقرب من PAX6، يؤدي حذف الذراع القصير للكروموسوم 11 (حذف 11p13) الذي يشمل كلا الجينين إلى انعدام القزحية المصاحب لورم ويلمز.
تحدث متلازمة غيليسبي بسبب طفرات سلبية سائدة متغايرة أو طفرات ثنائية الأليل في جين ITPR1 3). تم الإبلاغ عن 37 حالة مؤكدة جزيئيًا حتى الآن، ويُعرف بقايا Gly2554 كنقطة ساخنة 3).
بناءً على معايير تشخيص انعدام القزحية (2020)، يتم التأكيد وفقًا للمعايير التالية7).
أ. الأعراض
ب. النتائج الفحصية
ج. الأمراض التي يجب تمييزها
هـ. الفحص الجيني: طفرة مرضية في جين PAX6 أو حذف في المنطقة 11p13
فئات التشخيص7):
تم تحديد تصنيف الشدة لتأهيل الأمراض المستعصية في أربع درجات على النحو التالي7).
| الشدة | التعريف |
|---|---|
| الدرجة الأولى | إصابة عين واحدة، والعين الأخرى سليمة |
| الدرجة الثانية | إصابة كلتا العينين، أفضل حدة بصر مصححة ≥ 0.3 |
| الدرجة الثالثة | إصابة كلتا العينين، أفضل حدة بصر مصححة ≥ 0.1 وأقل من 0.3 |
| الدرجة الرابعة | إصابة كلتا العينين، أفضل حدة بصر مصححة < 0.1 |
حتى في الدرجات من الأولى إلى الثالثة، إذا كان هناك تضيق في المجال البصري بسبب الجلوكوما أو غيره (المجال البصري المتبقي المركزي ≤ 20 درجة بمخطط Goldmann I/4)، تنتقل الحالة إلى درجة شدة أعلى. الدرجة الثالثة فما فوق مؤهلة للحصول على دعم التكاليف الطبية 7).
التشخيص السريري سهل إذا تم تأكيد غياب القزحية أو عدم اكتمالها باستخدام المصباح الشقي. يتم تقييم الأنسجة القزحية المتبقية باستخدام تنظير الزاوية أو المجهر فوق الصوتي الحيوي. يتم أيضًا التحقق من وجود تشوهات في زاوية الغرفة الأمامية.
يتم تقييم المضاعفات العينية التالية بشكل منهجي:
الهدف الأهم في التقييم الوراثي لانعدام القزحية هو التأكد مما إذا كان حذف PAX6 يمتد ليشمل جين WT11). يتم تقييم الطفرات والحذف في منطقتي PAX6 وWT1 باستخدام تحليل الإكسوم الكامل أو تقنية MLPA1)2).
في حالات انعدام القزحية المتفرقة، يرتبط تقييم خطر ورم ويلمز الناتج عن حذف جين WT1 بشكل مباشر بالبقاء على قيد الحياة1). حتى في الحالات العائلية، نظرًا لتنوع النمط الظاهري، يُوصى بالتشخيص الجيني المؤكد والاستشارة الوراثية.
لا يوجد علاج جذري لانعدام القزحية. يركز العلاج على رعاية ضعف البصر لتحقيق أقصى استفادة من الرؤية المتبقية، والعلاج الفردي لكل مضاعفة. توصي الإرشادات السريرية (2021) بناءً على 6 أسئلة سريرية8).
السؤال السريري 1: يُوصى بعدم إجراء زراعة القرنية لعتمة حمة القرنية بشكل ضعيف8).
قد تؤدي زراعة القرنية إلى تحسن مؤقت في الرؤية، لكن التحسن محدود بسبب المضاعفات مثل نقص تنسج البقعة. على المدى الطويل، يكون تشخيص الرؤية سيئًا بسبب تقدم الجلوكوما وفشل الطعم.
س2: يوصى بشكل ضعيف بإجراء الجراحة لعلاج نقص الخلايا الجذعية الظهارية القرنية 8).
س3: يوصى بشكل ضعيف بإجراء جراحة الساد 8).
يحدث الساد في 50-85% من الحالات قبل سن 20 عامًا. يتم التخطيط للجراحة بناءً على شدة العتامة ورهاب الضوء. تشير التقارير إلى تحسن الرؤية في 66-100% من الحالات الجراحية، ولكن يجب ملاحظة النقاط التالية.
نظرًا لضعف الألياف الناحلة (Zinn)، فإن إدخال العدسة داخل العين يتطلب مؤشرات حذرة.
أجرى هو وزملاؤه (2024) عملية استحلاب العدسة بمساعدة الإضاءة الخلفية الثريا لحالتين من انعدام القزحية الخلقي المصحوب باعتلال القرنية القزحي الشديد. نظرًا لصعوبة الرؤية الجراحية المعتادة بسبب عتامة القرنية، أتاحت الإضاءة الخلفية رؤية واضحة للعدسة والمحفظة الأمامية، وتحسنت حدة البصر المصححة إلى 20/200 و20/1000 بعد 3 أسابيع من الجراحة 4).
سؤال سريري 4: يوصى بشدة بإجراء علاج الجلوكوما 8).
بعد ظهور الجلوكوما، تتم الإدارة وفقًا للخوارزمية المكونة من 5 خطوات التالية.
العلاج الدوائي: حاصرات بيتا، محفزات الجهاز العصبي الودي، والأدوية المرتبطة بالبروستاجلاندين فعالة. يُمنع استخدام بريمونيدين (محفز مستقبلات ألفا الأدرينالية) للأطفال دون سن الثانية بسبب خطر تثبيط الجهاز العصبي المركزي. في حالة القلق من تلف ظهارة القرنية، استخدم مستحضرات خالية من المواد الحافظة.
جراحة إعادة بناء مسار التصريف (بضع الزاوية، بضع التربيق): يوصى بها كجراحة أولى 16). هناك تقارير عن بضع الزاوية الوقائي. ومع ذلك، قد تكون غير فعالة في الحالات التي تغطي فيها القزحية المتبقية التربيق.
جراحة الترشيح (استئصال التربيق): تقتصر التقارير على حالات قليلة ومتوسطة وقصيرة المدى. تميل النتائج إلى أن تكون ضعيفة في عيون الأطفال، ويصل تسرب العين بعد الجراحة إلى حوالي 25% 13). هناك أيضًا تقارير عن الجلوكوما الخبيثة بعد الجراحة.
جراحة زرع تحويلة الجلوكوما (جراحة تحويلة أنبوبية): يمكن استخدام أجهزة من نوع Baerveldt وAhmed. يُوصى بإدخال الأنبوب في العيون التي تحتوي على عدسة طبيعية في اتجاه مماسي وليس نحو مركز القرنية. يمكن توقع تحكم جيد في ضغط العين.
تخثير الجسم الهدبي: الملاذ الأخير. هناك تقارير عن أن التجميد التخثري للجسم الهدبي أدى إلى تسرب العين في العديد من الحالات. نظرًا لوجود نقص تنسج في الجسم الهدبي، فإن خطر تسرب العين أعلى منه في العيون السليمة.
نظرًا لوجود تشوهات في تطور زاوية العين، يلزم اتباع نهج مختلف عن الجلوكوما مفتوحة الزاوية المعتادة. في البداية، يتم اختيار جراحة إعادة بناء مسار التصريف، ثم جراحة تحويلة أنبوبية كخيار جيد. يُمنع استخدام بريمونيدين للأطفال دون سن الثانية، كما أن استخدام مضادات الأيض قد يؤدي إلى تفاقم AAK، لذا يتطلب الأمر حذرًا في اتخاذ القرار 8).
CQ5: يُوصى بشدة بتقديم رعاية ضعف البصر 8).
تصحيح الانكسار هو الأساس، ويُقدر معدل الإصابة بقصر النظر بأكثر من 64%.
CQ6: يُوصى بشدة بعلاج رهاب الضوء 8).
يمكن لمعظم المرضى الالتحاق بالمدارس العادية، لكنهم يحتاجون إلى دعم مثل الكتب المدرسية الموسعة والأجهزة اللوحية وحوامل القراءة. كما يمكن الاستفادة من فصول ضعاف البصر أو استشارات التربية والتعليم من مدارس المكفوفين ومدارس الدعم البصري الخاصة.
منذ أبريل 2017، تم تصنيف هذا المرض كمرض نادر محدد، وبالتالي حتى إذا لم يحصل المريض على بطاقة إعاقة جسدية، فإنه يصبح مؤهلاً للحصول على دعم التكاليف الطبية وتوفير الأجهزة التعويضية إذا كانت شدته من الدرجة الثالثة أو أعلى 7). تشمل الأجهزة التعويضية المؤهلة النظارات الطبية، النظارات الواقية من الضوء، العدسات اللاصقة (بما في ذلك تلك المزودة بقزحية اصطناعية)، نظارات ضعاف البصر، عصا الأمان للمكفوفين، والعين الاصطناعية.
يمتد جين PAX6 على 22 كيلو قاعدة من الحمض النووي الجينومي ويتضمن 14 إكسونًا، ويشفر 422 حمضًا أمينيًا 1). يحتوي على نطاقين رابطين للحمض النووي (النطاق المزدوج ونطاق الهوميو المزدوج)، ويعمل نطاق PST (الغني بالبرولين والسيرين والثريونين) في الطرف الكربوكسيلي كمنشط للنسخ.
ينظم PAX6 تكاثر الخلايا وتمايزها وهجرتها والتصاقها، وتشمل أهدافه جين PAX6 نفسه بالإضافة إلى الجينات المشفرة لبلورات العدسة وكيراتين القرنية. يستمر التعبير الجيني في شبكية العين والعدسة والقرنية لدى البالغين. جين PAX6 هو أحد الجينات الرئيسية المنظمة لتمايز الأعضاء خلال المرحلة الجنينية.
معظم طفرات PAX6 تسبب نقص الجرعة عبر تحلل الحمض النووي الريبوزي الرسول المعتمد على الطفرات غير المنطقية (NMD) 1). الطفرات التي تُحدث كودون توقف مبكر (PTC) (الطفرات غير المنطقية، طفرات الإزاحة الإطارية، ومعظم طفرات الوصل) تؤدي إلى النمط الظاهري النموذجي لانعدام القزحية.
من ناحية أخرى، إذا كان PTC يقع في الإكسون الأخير أو ضمن 50 زوجًا قاعديًا من نهاية الإكسون قبل الأخير، فقد يفلت من NMD ويُترجم البروتين المبتور مما يؤدي إلى نمط ظاهري شديد 1).
تم الإبلاغ عن حالة نادرة لطفرة غير منطقية في PAX6 c.282C>A (p.Cys94*) مصاحبة لتثلث الصبغي 21 في نفس المريض. حدثت طفرة PAX6 بشكل جديد (de novo) وأدت إلى انعدام القزحية الكامل في كلتا العينين، الجلوكوما الخلقية، AAK، ونقص تنسج النقرة 2).
على الرغم من عدم وجود ارتباط واضح بين النمط الجيني والنمط الظاهري، إلا أن بعض الاتجاهات معروفة 1).
في سلسلة تنظير زاوية غرفة العين التي أجراها Grant وWalton، أظهرت النتائج أن سدى القزحية يمتد للأمام فوق الشبكة التربيقية مكونًا التصاقًا يشبه الالتصاق، ثم يتطور تدريجيًا إلى طبقة رقيقة تؤدي في النهاية إلى انسداد الزاوية 14). هذه الآلية هي السبب الرئيسي لتطور الجلوكوما. من الناحية المرضية، يكمن الأساس في نقص العضلات الملساء مع بقاء جذر القزحية ونقص تطور الزاوية.
ينتج AAK بشكل رئيسي عن نقص الخلايا الجذعية الحوفية (LSCD)، ولكن يلعب أيضًا دورًا في التمايز غير الطبيعي للظهارة القرنية، وضعف الالتصاق، وارتشاح الخلايا الملتحمية، ونقص إنتاج الدموع. يؤدي نقص المصفوفة المعدنية البروتيناز 9 (MMP-9) المنظم بواسطة PAX6 إلى تراكم الفيبرين وارتشاح الخلايا الالتهابية، مما يسبب اضطرابًا في ترتيب الكولاجين في السدى وفقدان الشفافية.
يصنف AAK إلى 5 مراحل. في المرحلة الأولى، يكون هناك شذوذ في الظهارة المحيطية فقط. في المرحلة الثانية، تغيرات ظهارية جاذبة للمركز (لم تصل إلى المركز). في المرحلة الثالثة، تغيرات ظهارية في مركز القرنية وأوعية دموية سطحية محيطية. في المرحلة الرابعة، أوعية دموية سطحية في القرنية بأكملها. في المرحلة الخامسة، شذوظ ظهاري في القرنية بأكملها وتندب في السدى العميق 10).
هناك علاقة بين حالة طفرة PAX6 وتطور AAK. في المرضى الذين يعانون من طفرات PTC أو التمديد الطرفي C، يتطور AAK بشكل يعتمد على العمر، بينما في الأنماط الطفرية الأخرى، قد يظهر اعتلال قرنية غير تقدمي 11).
تحدث متلازمة غيليسبي بسبب طفرات في جين ITPR1 3). ينتمي ITPR1 إلى عائلة مستقبلات IP3 ويشكل قنوات إطلاق Ca²⁺، ويتمركز في الشبكة الإندوبلازمية. تؤثر الطفرات السلبية السائدة على تكوين وصيانة العضلة العاصرة للقزحية، مما يؤدي إلى نقص تنسج القزحية المميز حول الحدقة وتوسع حدقة ثابت.
في مراجعة أدبيات متلازمة غيليسبي التي أجراها Ciaccio وآخرون (2024)، من تحليل 33 حالة مؤكدة جزيئيًا، تبين أن التطور الحركي يتأخر ولكنه يتحسن بمرور الوقت، وأن الإعاقة الذهنية لا توجد في جميع الحالات (17% لديهم ذكاء طبيعي)، وأن العلامات العصبية غير تقدمية 3).
مع انتشار تقنية تحليل الإكسوم الكامل، يستمر تحديد طفرات PAX6 الجديدة. في قاعدة بيانات طفرات PAX6 البشرية، تم تسجيل 491 طفرة حتى عام 2018، وتم الإبلاغ عن حوالي 250 طفرة جديدة منذ ذلك الحين 1). كما يتم تحديد طفرات في المناطق غير المشفرة كسبب لانعدام القزحية، مما يعطي أملاً في تفسير الحالات التي لم يتم تشخيصها بالاختبارات التقليدية 9).
في حالات جراحة الساد المصحوبة باعتلال القرنية الشديد المرتبط بانعدام القزحية، تكون تقنية التصور بمساعدة الإضاءة الخلفية الثريا مفيدة 4). تتيح هذه التقنية إجراء استحلاب العدسة بأمان حتى في المرضى الذين يعانون من اعتلال القرنية الشديد من الدرجة 3-4، وقد لوحظ تحسن في حدة البصر بعد الجراحة.
يتضح أن أنماط تطور اعتلال القرنية المرتبط بانعدام القزحية تختلف باختلاف نوع طفرة PAX6. مع انخفاض تكلفة الاختبارات الجينية، أصبح التنبؤ بالمسار السريري بناءً على نوع الطفرة والتدخل المبكر خيارات عملية.
في حالات انعدام القزحية المصاحب لمتلازمة داون، تم الإبلاغ عن مسار سريري خفيف نسبياً على الرغم من وجود المرضين معاً 2). فهم تأثير coexistence of multiple genetic disorders على النمط الظاهري قد يوفر رؤى مهمة للطب الشخصي في المستقبل.
يتم دراسة تطبيق عقار أتالورين (ataluren) المحفز لتجاوز كودون التوقف المبكر في طفرات PTC لعلاج انعدام القزحية على المستوى الأساسي 8). بالنسبة للعلاج الجيني لـ PAX6، تجري أبحاث أساسية على استبدال الجين باستخدام ناقل AAV-PAX6 في نموذج فأر مصاب بطفرات Sey. من المتوقع أن تتطور هذه الأبحاث إلى تجارب سريرية في المستقبل.
تُجرى تجارب سريرية على زرع صفائح الخلايا الظهارية القرنية المشتقة من الخلايا الجذعية المحفزة (iPS) محلياً ودولياً، مما يلفت الانتباه كعلاج جديد لاعتلال القرنية المرتبط بانعدام القزحية 8). بالنسبة للقزحية الاصطناعية (مثل CustomFlex Artificial Iris)، تتراكم خبرات الاستخدام في الخارج. العدسات اللاصقة المزودة بقزحية اصطناعية كأجهزة تعويضية مشمولة بالتأمين الصحي.
في الإرشادات السريرية (2021)، تم تحديد تجميع بيانات السجلات واسعة النطاق في اليابان لفهم الوضع الفعلي، ومراجعة الإرشادات بناءً على تحسين جودة الأدلة كقضايا مهمة للمستقبل 8). من المتوقع تحسين التنبؤ بتطور اعتلال القرنية المرتبط بانعدام القزحية بناءً على الطفرات الجينية الفردية وتحسين التدخل المبكر.