Aniridia Terisolasi
Frekuensi: Sekitar 2/3 dari total kasus.
Pola pewarisan: Autosomal dominan (AD).
Karakteristik: Disebabkan oleh mutasi gen PAX6. Tanpa gejala sistemik. Penetrasi lengkap tetapi ekspresivitas bervariasi.

Aniridia adalah penyakit bawaan langka yang ditandai dengan hipoplasia atau defek iris dalam berbagai derajat. Nama “aniridia” adalah istilah yang keliru, karena fragmen jaringan iris hampir selalu dapat diamati dengan gonioskopi atau mikroskop ultrasonik (UBM).
Prevalensi sekitar 1/40.000 hingga 1/100.000, tanpa perbedaan ras atau jenis kelamin yang signifikan 1). Dalam ICD-10, diklasifikasikan sebagai Q13.1.
Ini adalah penyakit pan-okular yang tidak hanya mempengaruhi iris tetapi juga kornea, lensa, sudut bilik mata, fovea, dan saraf optik 1), dengan berbagai komplikasi okular yang mengancam penglihatan. Prognosis penglihatan umumnya buruk, dengan ketajaman terkoreksi sekitar 0,1. Refleks pupil menghilang tetapi refleks akomodasi tetap ada, dan 60-90% kasus bilateral.
Tiga fenotipe berikut telah diidentifikasi.
Aniridia Terisolasi
Frekuensi: Sekitar 2/3 dari total kasus.
Pola pewarisan: Autosomal dominan (AD).
Karakteristik: Disebabkan oleh mutasi gen PAX6. Tanpa gejala sistemik. Penetrasi lengkap tetapi ekspresivitas bervariasi.
Sindrom WAGR
Frekuensi: Sebagian dari kasus sporadis.
Pola pewarisan: Delesi bersebelahan dari PAX6 dan WT1.
Karakteristik: Disertai tumor Wilms, kelainan urogenital, dan retardasi mental. Risiko tumor hingga 50%.
Sindrom Gillespie
Frekuensi: Sekitar 2% dari total kasus.
Pola pewarisan: Mutasi gen ITPR1.
Karakteristik: Disertai ataksia serebelar dan disabilitas intelektual. Ditandai dengan kelainan iris spesifik berupa pupil yang tetap dan melebar 3).
Aniridia sporadis mencakup sekitar 1/3 dari total kasus, disebabkan oleh delesi de novo pada 11p13 yang mencakup PAX6. Jika delesi meluas hingga mencakup gen WT1 yang berdekatan, hal ini menyebabkan sindrom WAGR 1). 25-30% dari aniridia sporadis mengembangkan tumor Wilms, dengan risiko relatif 67.
PAX6 adalah gen master kontrol pembentukan mata, dan terlibat dalam perkembangan mata, tabung saraf, bulbus olfaktorius, pulau Langerhans pankreas, dan epitel olfaktorius. Penyakit terjadi karena kehilangan fungsi satu alel (haploinsufisiensi), dan jika kedua alel abnormal, menyebabkan kematian janin. Pada tahun 2017, ditetapkan sebagai penyakit langka tertentu berdasarkan Undang-Undang Penyakit Langka, dan jika tingkat keparahan III atau lebih (lihat bagian diagnosis dan pemeriksaan untuk detail), memenuhi syarat untuk subsidi biaya medis 7).
Kasus sporadis (mutasi baru) mencakup sekitar sepertiga dari seluruh kasus, dan dapat terjadi tanpa riwayat keluarga. Pada kasus sporadis, ada kemungkinan sindrom WAGR, sehingga pemeriksaan genetik dan skrining tumor Wilms dengan USG abdomen penting dilakukan.
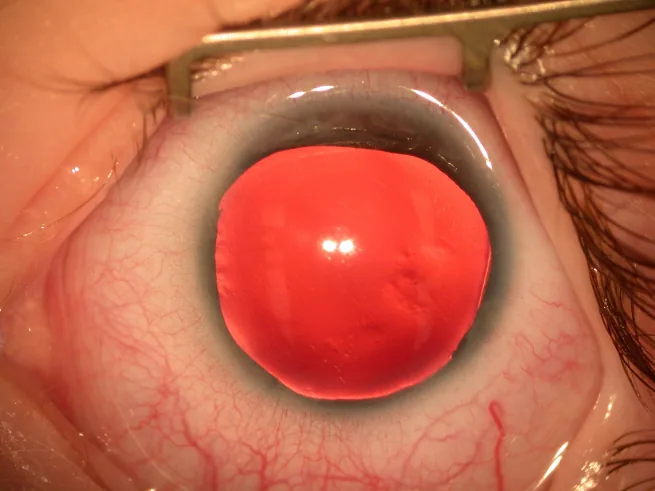
Sebagian besar kasus aniridia ditemukan saat lahir karena kelainan iris/pupil, atau pada masa bayi karena nistagmus.
Fenotipe bervariasi antar keluarga dan dalam satu keluarga, namun perbedaan antara mata kanan dan kiri biasanya kecil.
Terutama karena hipoplasia fovea, ketajaman penglihatan terkoreksi sering sekitar 0,1-0,2. Prognosis penglihatan sangat buruk jika disertai hipoplasia makula. Koreksi refraksi dan perawatan low vision sejak bayi penting untuk perkembangan penglihatan.
Karena PAX6 juga diekspresikan di sistem saraf pusat, pulau Langerhans pankreas, dan epitel olfaktorius, komplikasi ekstraokular berikut dapat terjadi 8).
Faktor penentu fungsi penglihatan adalah glaukoma, hipoplasia makula, nistagmus, keratopati, katarak, dan kelainan iris. Karena kerusakan lapang pandang dan gangguan penglihatan akibat glaukoma bersifat ireversibel, manajemen tekanan intraokular adalah yang terpenting dalam pemantauan8).
Sebagian besar aniridia kongenital disebabkan oleh mutasi heterozigot pada gen PAX6 yang terletak di lengan pendek kromosom 11 (11p13). Mekanisme utama penyakit ini adalah haploinsufisiensi1).
Gen PAX6 adalah gen master kontrol pembentukan mata, yang berperan penting dalam perkembangan mata, tabung saraf, bulbus olfaktorius, dan pankreas. Perkembangan mata normal memerlukan dua salinan PAX6, dan kehilangan fungsi satu salinan saja sudah menyebabkan aniridia1).
Dalam studi kohort pasien Tionghoa, mutasi penyebab pada gen PAX6 diidentifikasi pada 96,9% kasus1). Pada aniridia tipikal, mutasi yang menginduksi degradasi mRNA yang bergantung pada mutasi nonsense (NMD) atau delesi besar terdeteksi pada 96% kasus1).
Secara patologis, terdapat defisiensi otot polos dengan sisa akar iris, dan ditemukan disgenesis sudut. Terdapat disfungsi sel punca epitel kornea, menyebabkan kelainan pada epitel dan membran Bowman, serta pembentukan pannus yang kaya pembuluh darah.
Berikut adalah rincian mutasi PAX6 yang menyebabkan fenotip aniridia.
| Tipe Mutasi | Frekuensi |
|---|---|
| Mutasi nonsense | Sekitar 39% |
| Mutasi frameshift | Sekitar 25% |
| Mutasi splice site | Sekitar 13% |
| Mutasi missense | Sekitar 12% |
Mutasi run-on (mutasi perpanjangan ujung C) mencakup sekitar 5%, di mana kodon stop diubah menjadi kodon translasi sehingga menghasilkan protein PAX6 yang memanjang secara abnormal 6). Mutasi perpanjangan ujung C sering disertai dengan hipoplasia iris yang parah dan gangguan penglihatan berat 1)6).
Mutasi genetik sebagian besar berupa mutasi tipe PTC, dan ada juga laporan mutasi missense 7). Mengenai kegunaan pemeriksaan genetik, sekuensing Sanger atau NGS dapat mendeteksi mutasi pada hampir 85% kasus aniridia terisolasi. Selain itu, MLPA atau CMA dapat mendeteksi delesi dalam gen PAX6 atau daerah cis-regulator pada hampir 15% kasus 8).
Wang (2023) mengidentifikasi mutasi pergeseran kerangka baca baru c.640_646del (p.R214Pfs*28) dan melaporkan kasus yang menunjukkan defek iris total, hipoplasia fovea, dislokasi lensa, dan ablasi retina 1).
Ratna dkk. (2022) mengidentifikasi mutasi run-on c.1268A>T (p.*423L) pada sebuah keluarga India. Individu yang terkena menunjukkan aniridia total, nistagmus, hipoplasia fovea, AAK, subluksasi lensa superior, miopia tinggi, dan atrofi saraf optik, menunjukkan fenotip berat akibat mutasi perpanjangan ujung C 6).
Pada aniridia sporadik, delesi besar yang mencakup gen WT1 selain PAX6 menyebabkan sindrom WAGR. Risiko tumor Wilms mencapai 50% jika terdapat delesi WT1 1). Jika dicurigai sindrom WAGR, pemeriksaan genetik dapat mengonfirmasi defisiensi PAX6 dan WT1, memungkinkan penilaian risiko tumor Wilms dan pemantauan keterlambatan perkembangan 8). Evaluasi daerah WT1 melalui tes genetik sangat penting, dan 30% kasus sporadik dilaporkan mengembangkan tumor Wilms sebelum usia 5 tahun. Karena gen WT1 terletak di dekat PAX6, delesi lengan pendek kromosom 11 (delesi 11p13) yang mencakup kedua gen menyebabkan aniridia disertai tumor Wilms.
Sindrom Gillespie disebabkan oleh mutasi dominan negatif heterozigot atau mutasi bialelik pada gen ITPR1 3). Hingga saat ini, 37 kasus telah dikonfirmasi secara molekuler, dan residu Gly2554 dikenal sebagai titik panas 3).
Berdasarkan kriteria diagnosis aniridia (2020), diagnosis ditegakkan dengan kriteria berikut7).
A. Gejala
B. Temuan Pemeriksaan
C. Penyakit yang Perlu Dibedakan
E. Pemeriksaan genetik: Mutasi patogen pada gen PAX6 atau delesi pada wilayah 11p13
Kategori diagnosis7):
Klasifikasi keparahan untuk penetapan penyakit langka ditetapkan dalam empat tingkatan sebagai berikut7).
| Keparahan | Definisi |
|---|---|
| Derajat I | Satu mata terkena, mata lainnya normal |
| Derajat II | Kedua mata terkena, visus terkoreksi terbaik ≥ 0,3 |
| Derajat III | Kedua mata terkena, visus terkoreksi terbaik ≥ 0,1 dan < 0,3 |
| Derajat IV | Kedua mata terkena, visus terkoreksi terbaik < 0,1 |
Bahkan pada derajat I–III, jika terdapat penyempitan lapang pandang akibat glaukoma atau lainnya (lapang pandang sentral tersisa ≤ 20 derajat dengan target Goldmann I/4), maka derajat keparahan naik satu tingkat. Derajat III atau lebih tinggi memenuhi syarat untuk subsidi biaya medis 7).
Diagnosis klinis mudah jika tidak adanya atau hipoplasia iris dikonfirmasi dengan slit lamp. Sisa jaringan iris dievaluasi dengan gonioskopi atau mikroskop ultrasonik biomikroskopi. Kelainan perkembangan sudut bilik mata depan juga diperiksa.
Komplikasi mata berikut dievaluasi secara sistematis:
Tujuan terpenting dalam evaluasi genetik aniridia adalah memastikan apakah delesi PAX6 meluas hingga mencakup gen WT11). Mutasi dan delesi pada daerah PAX6 dan WT1 dievaluasi menggunakan whole exome sequencing atau MLPA1)2).
Pada aniridia sporadis, penilaian risiko tumor Wilms akibat delesi gen WT1 berkaitan langsung dengan prognosis hidup1). Meskipun familial, karena variabilitas fenotipe, diagnosis pasti melalui tes genetik dan konseling genetik dianjurkan.
Tidak ada terapi kuratif untuk aniridia. Perawatan berfokus pada perawatan low vision untuk memaksimalkan sisa penglihatan dan penanganan individual untuk setiap komplikasi. Pedoman klinis (2021) memberikan rekomendasi berdasarkan 6 pertanyaan klinis8).
CQ1: Direkomendasikan secara lemah untuk tidak melakukan transplantasi kornea pada kekeruhan stroma kornea8).
Transplantasi kornea dapat memberikan perbaikan penglihatan jangka pendek, namun perbaikannya terbatas karena komplikasi seperti hipoplasia makula. Dalam jangka panjang, prognosis penglihatan buruk akibat progresi glaukoma dan kegagalan graft.
CQ2: Operasi untuk defisiensi sel punca epitel kornea direkomendasikan secara lemah 8).
CQ3: Operasi katarak direkomendasikan secara lemah 8).
Katarak terjadi pada 50-85% kasus sebelum usia 20 tahun. Operasi direncanakan berdasarkan tingkat kekeruhan dan fotofobia. Dilaporkan perbaikan penglihatan pada 66-100% kasus operasi, namun perlu diperhatikan hal-hal berikut.
Karena zonula Zinn rapuh, pemasangan lensa intraokular memerlukan indikasi yang hati-hati.
Hu dkk. (2024) melakukan fakoemulsifikasi dengan bantuan pencahayaan belakang chandelier pada dua kasus aniridia kongenital dengan AAK berat. Visualisasi intraoperatif biasa sulit karena kekeruhan kornea, namun pencahayaan dari belakang memungkinkan visualisasi lensa dan kapsul anterior yang jelas, dan ketajaman visual terkoreksi membaik menjadi 20/200 dan 20/1000 pada 3 minggu pasca operasi 4).
CQ4: Terapi glaukoma sangat direkomendasikan untuk dilakukan 8).
Setelah onset glaukoma, manajemen dilakukan berdasarkan algoritma 5 langkah berikut.
Terapi obat: Beta-blocker, stimulan simpatis, dan obat terkait prostaglandin efektif. Brimonidin (stimulan reseptor alfa-adrenergik) dikontraindikasikan pada anak di bawah 2 tahun karena risiko depresi sistem saraf pusat. Jika ada kekhawatiran kerusakan epitel kornea, gunakan sediaan bebas pengawet.
Operasi rekonstruksi saluran keluar (goniotomi, trabekulotomi): Direkomendasikan sebagai operasi pertama 16). Ada laporan tentang goniotomi profilaksis. Namun, mungkin tidak efektif pada kasus di mana iris residual menutupi trabekulum.
Operasi filtrasi (trabekulektomi): Hanya ada laporan kasus kecil dan jangka pendek. Hasil cenderung buruk pada mata anak-anak, dan kebocoran bola mata pasca operasi mencapai sekitar 25% 13). Ada juga laporan glaukoma maligna pasca operasi.
Operasi implan glaukoma (operasi shunt tuba): Perangkat tipe Baerveldt dan Ahmed dapat digunakan. Pada mata yang masih memiliki lensa alami, disarankan memasukkan tuba secara tangensial, bukan ke arah tengah kornea. Kontrol tekanan intraokular yang baik dapat diharapkan.
Siklofotokoagulasi: Pilihan terakhir. Ada laporan bahwa kriokoagulasi badan siliar menyebabkan kebocoran bola mata pada banyak kasus. Karena adanya hipoplasia badan siliar, risiko kebocoran bola mata lebih tinggi daripada mata normal.
Karena adanya kelainan perkembangan sudut bilik mata, diperlukan pendekatan yang berbeda dari glaukoma sudut terbuka biasa. Pada awalnya, pilih operasi rekonstruksi saluran keluar, kemudian operasi shunt tabung menjadi pilihan yang baik. Brimonidine dikontraindikasikan pada anak di bawah 2 tahun, dan penggunaan obat antimetabolit dapat memperburuk AAK, sehingga diperlukan pertimbangan yang hati-hati 8).
CQ5: Perawatan low vision sangat direkomendasikan 8).
Koreksi refraksi adalah dasar, dan tingkat komplikasi miopia dilaporkan lebih dari 64%.
CQ6: Pengobatan fotofobia sangat direkomendasikan 8).
Sebagian besar pasien dapat bersekolah di sekolah reguler, namun memerlukan dukungan seperti buku teks yang diperbesar, tablet, dan rak buku. Alternatifnya, mereka dapat mengikuti kelas tunanetra atau memanfaatkan konsultasi pengasuhan dan pendidikan dari sekolah tunanetra dan sekolah dukungan penglihatan khusus.
Sejak April 2017, penyakit ini telah ditetapkan sebagai penyakit langka yang ditunjuk, sehingga meskipun pasien belum memiliki kartu disabilitas fisik, jika tingkat keparahannya derajat III atau lebih, mereka memenuhi syarat untuk mendapatkan subsidi biaya pengobatan dan penyediaan alat bantu 7). Alat bantu yang memenuhi syarat meliputi kacamata korektif, kacamata pelindung cahaya, lensa kontak (termasuk yang dilengkapi iris buatan), kacamata low vision, tongkat pengaman tunanetra, dan mata palsu.
Gen PAX6 membentang sepanjang 22 kb DNA genomik yang mencakup 14 ekson, dan mengkode 422 asam amino 1). Gen ini memiliki dua domain pengikat DNA (paired domain dan paired-type homeodomain), dan domain PST (kaya prolin, serin, treonin) di ujung C berfungsi sebagai aktivator transkripsi.
PAX6 mengatur proliferasi, diferensiasi, migrasi, dan adhesi sel, dan targetnya meliputi PAX6 itu sendiri serta gen yang mengkode kristalin lensa dan keratin kornea. Ekspresinya berlanjut di retina, lensa, dan kornea orang dewasa. Gen PAX6 adalah salah satu gen master kontrol yang mengatur diferensiasi organ selama masa embrio.
Sebagian besar mutasi PAX6 menyebabkan haploinsufisiensi melalui degradasi mRNA yang bergantung pada nonsense-mediated decay (NMD) 1). Mutasi yang memperkenalkan kodon stop prematur (PTC) (mutasi nonsense, mutasi pergeseran bingkai, dan sebagian besar mutasi sambungan) menghasilkan fenotip aniridia yang khas.
Di sisi lain, jika PTC terletak di ekson terakhir atau dalam 50 bp dari ujung ekson kedua terakhir, mutasi tersebut dapat lolos dari NMD dan menghasilkan protein terpotong yang dapat menyebabkan fenotip yang parah 1).
Telah dilaporkan kasus langka mutasi nonsense PAX6 c.282C>A (p.Cys94*) yang terjadi bersamaan dengan trisomi 21 pada pasien yang sama. Mutasi PAX6 terjadi secara de novo dan menyebabkan aniridia bilateral total, glaukoma kongenital, AAK, dan hipoplasia fovea 2).
Meskipun korelasi genotip-fenotip yang jelas belum ditetapkan, beberapa kecenderungan diketahui 1).
Dalam seri gonioskopi Grant dan Walton, ditunjukkan bahwa stroma iris meluas ke anterior di atas trabekula membentuk perlekatan seperti sinekia, yang secara bertahap menjadi seperti lembaran dan akhirnya menyebabkan oklusi sudut 14). Mekanisme ini merupakan faktor utama terjadinya glaukoma. Secara patologis, dasar dari kondisi ini adalah defek otot polos dengan sisa akar iris dan disgenesis sudut.
AAK terutama disebabkan oleh defisiensi sel punca limbal (LSCD), namun juga melibatkan diferensiasi abnormal epitel kornea, adhesi abnormal, infiltrasi sel konjungtiva, dan produksi air mata yang tidak mencukupi. Defisiensi matriks metaloproteinase 9 (MMP-9) yang diatur oleh PAX6 menyebabkan akumulasi fibrin dan infiltrasi sel inflamasi, yang mengakibatkan gangguan susunan kolagen stroma dan hilangnya transparansi.
AAK diklasifikasikan menjadi 5 tahap. Tahap I: kelainan epitel perifer saja. Tahap II: perubahan epitel sentripetal (belum mencapai pusat). Tahap III: perubahan epitel kornea sentral dan neovaskularisasi superfisial perifer. Tahap IV: neovaskularisasi superfisial seluruh kornea. Tahap V: kelainan epitel seluruh kornea dan sikatrik stroma dalam 10).
Terdapat hubungan antara status mutasi PAX6 dan progresi AAK. Pada pasien dengan mutasi PTC atau perpanjangan terminal-C, AAK berkembang secara tergantung usia, sedangkan pada tipe mutasi lain, dapat terjadi keratopati non-progresif 11).
Sindrom Gillespie disebabkan oleh mutasi pada gen ITPR1 3). ITPR1 adalah anggota keluarga reseptor IP3 yang membentuk saluran pelepasan Ca²⁺ dan terlokalisasi di retikulum endoplasma. Mutasi dominan negatif mempengaruhi pembentukan dan pemeliharaan sfingter pupil, menyebabkan hipoplasia iris spesifik di sekitar pupil dan midriasis fiks.
Dalam tinjauan literatur sindrom Gillespie oleh Ciaccio dkk. (2024), dari analisis 33 kasus yang dikonfirmasi secara molekuler, ditemukan bahwa perkembangan motorik tertunda tetapi membaik seiring waktu, kecacatan intelektual tidak terjadi pada semua kasus (17% memiliki inteligensi normal), dan tanda neurologis bersifat non-progresif 3).
Dengan meluasnya teknologi analisis eksom lengkap, identifikasi mutasi PAX6 baru terus berlanjut. Pada basis data Mutasi PAX6 Manusia, tercatat 491 mutasi pada tahun 2018, dan sekitar 250 mutasi baru telah dilaporkan sejak saat itu 1). Mutasi pada daerah nonkoding juga mulai diidentifikasi sebagai penyebab aniridia, sehingga diharapkan dapat menjelaskan kasus yang tidak terdiagnosis dengan pemeriksaan konvensional 9).
Pada operasi katarak dengan AAK berat, teknik visualisasi dengan bantuan pencahayaan retroiluminasi chandelier berguna 4). Teknik ini memungkinkan fakoemulsifikasi yang aman bahkan pada pasien dengan AAK derajat 3-4, dan perbaikan ketajaman penglihatan pascaoperasi telah dilaporkan.
Menjadi jelas bahwa pola perkembangan AAK berbeda tergantung pada jenis mutasi PAX6. Dengan menurunnya biaya tes genetik, prediksi perjalanan klinis berdasarkan tipe mutasi dan intervensi dini menjadi pilihan yang realistis.
Pada kasus aniridia yang menyertai trisomi 21, telah dilaporkan perjalanan yang relatif ringan meskipun kedua penyakit tersebut ada 2). Memahami dampak koeksistensi beberapa kelainan genetik pada fenotip dapat memberikan wawasan penting untuk pengobatan personal di masa depan.
Penerapan obat read-through (ataluren) untuk mutasi tipe PTC pada aniridia sedang diteliti pada tingkat penelitian dasar 8). Untuk terapi gen PAX6, penelitian dasar tentang penggantian gen menggunakan vektor AAV-PAX6 pada model tikus mutan Sey sedang berlangsung. Diharapkan akan berkembang ke uji klinis di masa depan.
Uji klinis transplantasi lembaran sel epitel kornea yang berasal dari sel iPS sedang dilakukan di dalam dan luar negeri, dan menarik perhatian sebagai terapi baru untuk AAK 8). Untuk iris buatan (seperti CustomFlex Artificial Iris), pengalaman penggunaan di luar negeri terus bertambah. Lensa kontak dengan iris buatan sebagai alat bantu tercakup dalam asuransi.
Dalam pedoman praktik klinis (2021), pengumpulan data registri skala besar di Jepang untuk memahami situasi aktual dan revisi pedoman berdasarkan peningkatan kualitas bukti ditetapkan sebagai isu penting di masa depan 8). Diharapkan optimalisasi prediksi perkembangan AAK berdasarkan mutasi gen individu dan intervensi dini.