ภาวะไม่มีม่านตาแบบเดี่ยว
ความถี่: ประมาณ 2 ใน 3 ของทั้งหมด
รูปแบบการถ่ายทอด: ถ่ายทอดแบบออโตโซมอลโดมิแนนต์ (AD)
ลักษณะ: เกิดจากการกลายพันธุ์ของยีน PAX6 ไม่มีอาการทางระบบ การแทรกซึมสมบูรณ์แต่การแสดงออกหลากหลาย

ภาวะไม่มีม่านตา (Aniridia) เป็นโรคประจำตัวที่พบได้ยาก โดยมีลักษณะของม่านตาที่เจริญไม่เต็มที่หรือบกพร่องในระดับต่างๆ ชื่อ “ภาวะไม่มีม่านตา” เป็นการเรียกที่คลาดเคลื่อน เนื่องจากสามารถมองเห็นชิ้นส่วนของเนื้อเยื่อม่านตาได้เกือบทุกครั้งโดยใช้กล้องสอดตรวจมุมตา (gonioscopy) หรือกล้องจุลทรรศน์อัลตราซาวนด์ (UBM)
ความชุกประมาณ 1/40,000 ถึง 1/100,000 โดยไม่มีรายงานความแตกต่างทางเชื้อชาติหรือเพศอย่างมีนัยสำคัญ 1) ใน ICD-10 จัดอยู่ในรหัส Q13.1
เป็นโรคที่ส่งผลกระทบต่อลูกตาทั้งหมด (pan-ocular) ไม่เพียงแต่ม่านตาเท่านั้น แต่ยังรวมถึงกระจกตา เลนส์แก้วตา มุมตา (angle) รอยบุ๋มจอตา (fovea) และเส้นประสาทตา 1) โดยมีภาวะแทรกซ้อนทางตาหลายอย่างที่คุกคามการมองเห็น การพยากรณ์โรคทางสายตาโดยทั่วไปไม่ดี โดยสายตาที่แก้ไขแล้วมักอยู่ที่ประมาณ 0.1 ปฏิกิริยารูม่านตาหายไป แต่ปฏิกิริยาการปรับโฟกัส (accommodation) ยังคงอยู่ และ 60-90% ของกรณีเป็นทั้งสองข้าง
ฟีโนไทป์สามแบบต่อไปนี้ได้รับการยอมรับ
ภาวะไม่มีม่านตาแบบเดี่ยว
ความถี่: ประมาณ 2 ใน 3 ของทั้งหมด
รูปแบบการถ่ายทอด: ถ่ายทอดแบบออโตโซมอลโดมิแนนต์ (AD)
ลักษณะ: เกิดจากการกลายพันธุ์ของยีน PAX6 ไม่มีอาการทางระบบ การแทรกซึมสมบูรณ์แต่การแสดงออกหลากหลาย
กลุ่มอาการ WAGR
ความถี่: ส่วนหนึ่งของผู้ป่วยประปราย
รูปแบบการถ่ายทอด: การขาดหายของยีน PAX6 และ WT1 ที่อยู่ติดกัน
ลักษณะ: ร่วมกับเนื้องอกวิล์มส์ ความผิดปกติของระบบสืบพันธุ์และทางเดินปัสสาวะ และภาวะปัญญาอ่อน ความเสี่ยงเนื้องอกสูงถึง 50%
กลุ่มอาการกิลเลสพี
ความถี่: ประมาณ 2% ของทั้งหมด
รูปแบบการถ่ายทอด: การกลายพันธุ์ของยีน ITPR1
ลักษณะ: ร่วมกับภาวะเสียการทรงตัวจากสมองน้อยและความบกพร่องทางสติปัญญา มีความผิดปกติของม่านตาที่จำเพาะคือรูม่านตาคงที่และขยาย 3)
ภาวะไม่มีม่านตาแบบประปรายคิดเป็นประมาณ 1 ใน 3 ของทั้งหมด เกิดจากการขาดหายของยีนแบบ de novo ที่ตำแหน่ง 11p13 ซึ่งรวมถึง PAX6 หากการขาดหายขยายไปถึงยีน WT1 ที่อยู่ติดกัน จะทำให้เกิดกลุ่มอาการ WAGR 1) ผู้ป่วยภาวะไม่มีม่านตาแบบประปราย 25-30% จะเกิดเนื้องอกวิล์มส์ โดยมีความเสี่ยงสัมพัทธ์เท่ากับ 67
PAX6 เป็นยีนควบคุมหลักของการสร้างดวงตา เกี่ยวข้องกับการพัฒนาของตา ท่อประสาท ปุ่มรับกลิ่น เกาะเล็กแลงเกอร์ฮานส์ในตับอ่อน และเยื่อบุรับกลิ่น โรคนี้เกิดจากการสูญเสียการทำงานของอัลลีลหนึ่ง (haploinsufficiency) และหากอัลลีลทั้งสองผิดปกติจะทำให้ทารกในครรภ์เสียชีวิต ในปี 2017 โรคนี้ถูกกำหนดให้เป็นโรคหายากเฉพาะตามกฎหมายโรคหายาก และผู้ป่วยที่มีความรุนแรงระดับ III ขึ้นไป (ดูรายละเอียดในหัวข้อการวินิจฉัยและการตรวจ) จะมีสิทธิ์ได้รับเงินช่วยเหลือค่ารักษาพยาบาล 7)
ผู้ป่วยแบบประปราย (การกลายพันธุ์ใหม่) คิดเป็นประมาณ 1 ใน 3 ของทั้งหมด และสามารถเกิดขึ้นได้โดยไม่มีประวัติครอบครัว ในผู้ป่วยแบบประปราย มีความเป็นไปได้ของกลุ่มอาการ WAGR ดังนั้นการตรวจทางพันธุกรรมและการอัลตราซาวด์ช่องท้องเพื่อคัดกรองเนื้องอกวิลมส์จึงมีความสำคัญ
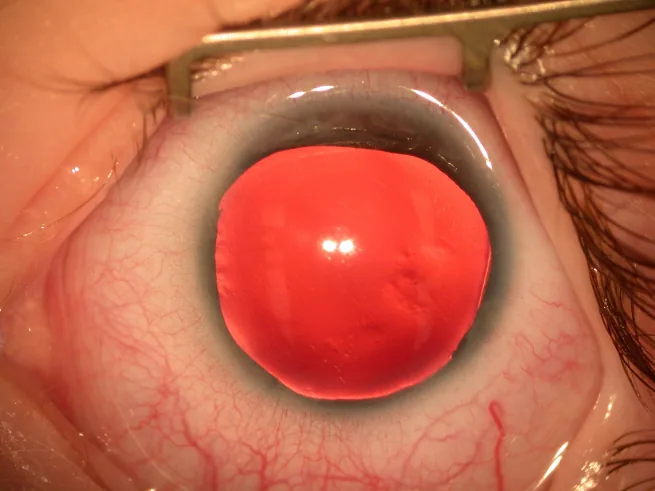
ผู้ป่วยภาวะไม่มีม่านตาส่วนใหญ่จะถูกตรวจพบตั้งแต่แรกเกิดเนื่องจากความผิดปกติของม่านตา/รูม่านตา หรือในวัยทารกเนื่องจากอาตา
ฟีโนไทป์แตกต่างกันระหว่างครอบครัวและภายในครอบครัวเดียวกัน แต่ความแตกต่างระหว่างตาขวาและตาซ้ายมักมีน้อย
สาเหตุหลักมาจาก foveal hypoplasia ค่าสายตาที่แก้ไขแล้วมักอยู่ที่ประมาณ 0.1-0.2 การพยากรณ์โรคการมองเห็นแย่เป็นพิเศษหากมี macular hypoplasia ร่วมด้วย การแก้ไขค่าสายตาและการดูแลสายตาเลือนรางตั้งแต่ทารกมีความสำคัญต่อพัฒนาการทางสายตา
เนื่องจาก PAX6 ยังแสดงออกในระบบประสาทส่วนกลาง เกาะ Langerhans ของตับอ่อน และเยื่อบุรับกลิ่น จึงอาจเกิดภาวะแทรกซ้อนนอกตาต่อไปนี้ 8)
ปัจจัยสำคัญที่กำหนดการทำงานของการมองเห็นคือ โรคต้อหิน, ภาวะจอประสาทตาส่วนกลางเจริญไม่เต็มที่, อาตา, โรคกระจกตา, ต้อกระจก และความผิดปกติของม่านตา เนื่องจากความเสียหายของลานสายตาและการมองเห็นที่บกพร่องจากโรคต้อหินนั้นไม่สามารถฟื้นคืนได้ การจัดการความดันลูกตาจึงสำคัญที่สุดในการติดตามผล8)
ภาวะไม่มีม่านตาตั้งแต่กำเนิดส่วนใหญ่เกิดจากการกลายพันธุ์แบบเฮเทอโรไซกัสในยีน PAX6 ซึ่งอยู่บนแขนสั้นของโครโมโซมคู่ที่ 11 (11p13) กลไกหลักของโรคคือภาวะแฮพลอยด์ไม่เพียงพอ (haploinsufficiency)1)
ยีน PAX6 เป็นยีนควบคุมหลักของการสร้างดวงตา มีบทบาทสำคัญในการพัฒนาของดวงตา ท่อประสาท ป่องรับกลิ่น และตับอ่อน การพัฒนาดวงตาตามปกติต้องใช้ PAX6 จำนวน 2 ชุด และการสูญเสียการทำงานเพียงชุดเดียวก็ทำให้เกิดภาวะไม่มีม่านตาได้1)
ในการศึกษาแบบกลุ่มผู้ป่วยชาวจีน พบการกลายพันธุ์ที่เป็นสาเหตุในยีน PAX6 ใน 96.9% ของผู้ป่วย1) ในภาวะไม่มีม่านตาทั่วไป การกลายพันธุ์ที่เหนี่ยวนำให้เกิดการสลาย mRNA ที่ขึ้นกับการกลายพันธุ์แบบ nonsense (NMD) หรือการขาดหายไปเป็นบริเวณกว้าง ตรวจพบใน 96% ของผู้ป่วย1)
ทางพยาธิวิทยา พบการขาดกล้ามเนื้อเรียบโดยมีรากม่านตาหลงเหลืออยู่ และพบความผิดปกติของการพัฒนาของมุมตา มีความผิดปกติของเซลล์ต้นกำเนิดเยื่อบุกระจกตา ทำให้เกิดความผิดปกติของเยื่อบุผิวและเยื่อโบว์แมน และเกิดพานนัส (pannus) ที่มีหลอดเลือดมาก
รายละเอียดของการกลายพันธุ์ของ PAX6 ที่ทำให้เกิดฟีโนไทป์ของภาวะไม่มีม่านตามีดังนี้
| ชนิดของการกลายพันธุ์ | ความถี่ |
|---|---|
| การกลายพันธุ์แบบ nonsense | ประมาณ 39% |
| การกลายพันธุ์แบบ frameshift | ประมาณ 25% |
| การกลายพันธุ์ที่ตำแหน่ง splice site | ประมาณ 13% |
| การกลายพันธุ์แบบมิสเซนส์ (missense) | ประมาณ 12% |
การกลายพันธุ์แบบรันออน (run-on) หรือการกลายพันธุ์แบบต่อปลาย C (C-terminal extension) คิดเป็นประมาณ 5% โดยที่โคดอนหยุดถูกเปลี่ยนเป็นโคดอนแปลรหัส ทำให้เกิดโปรตีน PAX6 ที่ยาวผิดปกติ 6) การกลายพันธุ์แบบต่อปลาย C มักมาพร้อมกับภาวะม่านตาพัฒนาน้อยผิดปกติอย่างรุนแรงและความบกพร่องทางการมองเห็นระดับสูง 1)6).
การกลายพันธุ์ทางพันธุกรรมส่วนใหญ่เป็นชนิด PTC และมีรายงานการกลายพันธุ์แบบมิสเซนส์ด้วยเช่นกัน 7) ในด้านประโยชน์ของการตรวจทางพันธุกรรม การหาลำดับดีเอ็นเอแบบแซงเกอร์หรือ NGS สามารถตรวจพบการกลายพันธุ์ในเกือบ 85% ของผู้ป่วยภาวะไม่มีม่านตาแบบแยกเดี่ยว นอกจากนี้ MLPA หรือ CMA สามารถตรวจพบการขาดหายของยีน PAX6 หรือบริเวณควบคุมซิส (cis-regulatory) ในเกือบ 15% ของผู้ป่วย 8).
Wang (2023) ระบุการกลายพันธุ์แบบเฟรมชิฟต์ชนิดใหม่ c.640_646del (p.R214Pfs*28) และรายงานผู้ป่วยที่แสดงภาวะไม่มีม่านตาโดยสมบูรณ์ ภาวะฟอฟีอาพัฒนาน้อยผิดปกติ เลนส์เคลื่อน และจอประสาทตาลอก 1).
Ratna และคณะ (2022) ระบุการกลายพันธุ์แบบรันออน c.1268A>T (p.*423L) ในครอบครัวชาวอินเดีย ผู้ป่วยแสดงภาวะไม่มีม่านตาโดยสมบูรณ์ อาตา ภาวะฟอฟีอาพัฒนาน้อยผิดปกติ AAK เลนส์เคลื่อนขึ้นด้านบนบางส่วน สายตาสั้นรุนแรง และเส้นประสาทตาฝ่อ แสดงถึงฟีโนไทป์รุนแรงจากการกลายพันธุ์แบบต่อปลาย C 6).
ในภาวะไม่มีม่านตาแบบประปราย การขาดหายขนาดใหญ่ที่รวมถึงยีน WT1 นอกเหนือจาก PAX6 ทำให้เกิดกลุ่มอาการ WAGR ความเสี่ยงของเนื้องอกวิล์มส์สูงถึง 50% หากมีการขาดหายของ WT1 1) หากสงสัยกลุ่มอาการ WAGR การตรวจทางพันธุกรรมสามารถยืนยันการขาด PAX6 และ WT1 ทำให้สามารถประเมินความเสี่ยงเนื้องอกวิล์มส์และติดตามพัฒนาการล่าช้าได้ 8) การประเมินบริเวณ WT1 โดยการตรวจทางพันธุกรรมเป็นสิ่งจำเป็น และ 30% ของผู้ป่วยแบบประปรายจะเกิดเนื้องอกวิล์มส์ก่อนอายุ 5 ปี เนื่องจากยีน WT1 อยู่ใกล้กับ PAX6 การขาดหายของแขนสั้นของโครโมโซมคู่ที่ 11 (การขาดหาย 11p13) ที่รวมทั้งสองยีนทำให้เกิดภาวะไม่มีม่านตาร่วมกับเนื้องอกวิล์มส์
กลุ่มอาการกิลเลสปีเกิดจากการกลายพันธุ์แบบเด่นเชิงลบแบบเฮเทอโรไซกัสหรือการกลายพันธุ์แบบสองอัลลีลในยีน ITPR1 3) จนถึงปัจจุบัน มีรายงานผู้ป่วยที่ได้รับการยืนยันทางโมเลกุล 37 ราย และกรดอะมิโน Gly2554 เป็นที่รู้จักในฐานะจุดร้อน 3).
ตามเกณฑ์การวินิจฉัยภาวะไม่มีม่านตา (พ.ศ. 2563) การวินิจฉัยจะยืนยันตามเกณฑ์ต่อไปนี้7).
ก. อาการ
ข. ผลการตรวจ
ค. โรคที่ควรแยก
จ. การตรวจทางพันธุกรรม: การกลายพันธุ์ที่ก่อโรคในยีน PAX6 หรือการขาดหายของบริเวณ 11p13
ประเภทการวินิจฉัย7):
การจำแนกความรุนแรงสำหรับการรับรองโรคหายากถูกกำหนดเป็นสี่ระดับดังนี้7).
| ความรุนแรง | คำจำกัดความ |
|---|---|
| ระดับ I | ตาข้างหนึ่งเป็นโรค ตาอีกข้างปกติ |
| ระดับ II | ตาทั้งสองข้างได้รับผลกระทบ ค่าสายตาแก้ไขที่ดีที่สุด ≥ 0.3 |
| ระดับ III | ตาทั้งสองข้างได้รับผลกระทบ ค่าสายตาแก้ไขที่ดีที่สุด ≥ 0.1 และ < 0.3 |
| ระดับ IV | ตาทั้งสองข้างได้รับผลกระทบ ค่าสายตาแก้ไขที่ดีที่สุด < 0.1 |
แม้ในระดับ I–III หากมีการตีบของลานสายตาจากโรคต้อหินหรืออื่นๆ (ลานสายตาส่วนกลางที่เหลือ ≤ 20 องศา ด้วย Goldmann I/4) จะเลื่อนระดับความรุนแรงขึ้นหนึ่งขั้น ระดับ III ขึ้นไปมีสิทธิ์ได้รับเงินอุดหนุนค่ารักษาพยาบาล 7).
การวินิจฉัยทางคลินิกทำได้ง่ายหากยืนยันการไม่มีหรือการเจริญไม่สมบูรณ์ของม่านตาด้วยกล้องจุลทรรศน์ชนิดกรีดแสง ประเมินเนื้อเยื่อม่านตาที่เหลือด้วย gonioscopy หรือกล้องจุลทรรศน์อัลตราซาวนด์ชีวภาพ ตรวจสอบความผิดปกติของพัฒนาการของมุมช่องหน้าม่านตาด้วย
ประเมินภาวะแทรกซ้อนทางตาต่อไปนี้อย่างเป็นระบบ:
เป้าหมายที่สำคัญที่สุดในการประเมินทางพันธุกรรมของภาวะไม่มีม่านตาคือการยืนยันว่าการขาดหายของ PAX6 ขยายไปถึงยีน WT1 หรือไม่1) การกลายพันธุ์และการขาดหายในบริเวณ PAX6 และ WT1 ได้รับการประเมินโดยการหาลำดับเอ็กโซมทั้งหมดหรือ MLPA1)2)
ในภาวะไม่มีม่านตาที่เกิดขึ้นประปราย การประเมินความเสี่ยงของเนื้องอกวิล์มส์จากการขาดหายของยีน WT1 สัมพันธ์โดยตรงกับการพยากรณ์โรคเพื่อการอยู่รอด1) แม้ในกรณีที่เกิดในครอบครัว เนื่องจากความหลากหลายของฟีโนไทป์ จึงแนะนำให้วินิจฉัยยืนยันด้วยการตรวจทางพันธุกรรมและการให้คำปรึกษาทางพันธุกรรม
ไม่มีการรักษาที่หายขาดสำหรับภาวะไม่มีม่านตา การรักษามุ่งเน้นไปที่การดูแลสายตาเลือนรางเพื่อใช้การมองเห็นที่เหลืออยู่ให้เกิดประโยชน์สูงสุด และการรักษาเฉพาะสำหรับภาวะแทรกซ้อนแต่ละอย่าง แนวทางปฏิบัติทางคลินิก (ปี 2021) ให้คำแนะนำตามคำถามทางคลินิก 6 ข้อ8)
CQ1: แนะนำอย่างอ่อนไม่ให้ทำการปลูกถ่ายกระจกตาสำหรับความขุ่นของสโตรมากระจกตา8)
การปลูกถ่ายกระจกตาอาจช่วยให้การมองเห็นดีขึ้นในระยะสั้น แต่การปรับปรุงมีจำกัดเนื่องจากภาวะแทรกซ้อน เช่น ภาวะจอประสาทตาพัฒนาน้อย ในระยะยาว การพยากรณ์การมองเห็นไม่ดีเนื่องจากโรคต้อหินที่ดำเนินไปและความล้มเหลวของเนื้อเยื่อปลูกถ่าย
CQ2: แนะนำอย่างอ่อนให้ทำการผ่าตัดรักษาภาวะพร่องเซลล์ต้นกำเนิดเยื่อบุกระจกตา 8).
CQ3: แนะนำอย่างอ่อนให้ทำการผ่าตัดต้อกระจก 8).
ต้อกระจกเกิดขึ้นใน 50-85% ของผู้ป่วยก่อนอายุ 20 ปี การผ่าตัดวางแผนตามความรุนแรงของความขุ่นและอาการกลัวแสง มีรายงานการมองเห็นดีขึ้นใน 66-100% ของกรณีผ่าตัด แต่ต้องระวังประเด็นต่อไปนี้
เนื่องจากเส้นใยซินน์ (Zinn) เปราะบาง การใส่เลนส์แก้วตาเทียมจึงต้องมีข้อบ่งชี้อย่างระมัดระวัง
Hu และคณะ (2024) ได้ทำการผ่าตัดสลายต้อกระจกด้วยคลื่นเสียงความถี่สูงโดยใช้แสงส่องจากด้านหลังแบบโคมระย้าช่วยในผู้ป่วยภาวะไร้ม่านตาตั้งแต่กำเนิด 2 รายที่มี AAK รุนแรง การมองเห็นระหว่างผ่าตัดตามปกติทำได้ยากเนื่องจากกระจกตาขุ่น แต่การส่องแสงจากด้านหลังทำให้มองเห็นเลนส์แก้วตาและแคปซูลด้านหน้าได้ชัดเจน และค่าสายตาที่แก้ไขแล้วดีขึ้นเป็น 20/200 และ 20/1000 ที่ 3 สัปดาห์หลังผ่าตัด 4).
CQ4: แนะนำอย่างยิ่งให้ทำการรักษาโรคต้อหิน 8).
หลังจากเริ่มมีโรคต้อหิน ให้จัดการตามขั้นตอนวิธี 5 ขั้นตอนต่อไปนี้
การรักษาด้วยยา: ยาปิดกั้นเบตา ยากระตุ้นซิมพาเทติก และยาที่เกี่ยวข้องกับพรอสตาแกลนดินได้ผลดี บริโมนิดีน (ยากระตุ้นตัวรับแอลฟา-อะดรีเนอร์จิก) ห้ามใช้ในเด็กอายุต่ำกว่า 2 ปีเนื่องจากเสี่ยงต่อการกดระบบประสาทส่วนกลาง หากกังวลเกี่ยวกับความเสียหายต่อเยื่อบุกระจกตา ให้ใช้ยาที่ไม่มีสารกันเสีย
การผ่าตัดสร้างทางระบายน้ำใหม่ (โกนิโอโตมี, ทราบีคิวโลโตมี): แนะนำให้เป็นการผ่าตัดครั้งแรก 16) มีรายงานการทำโกนิโอโตมีเพื่อป้องกัน อย่างไรก็ตาม อาจไม่ได้ผลในกรณีที่ม่านตาที่เหลือปกคลุมทราบีคิวลัม
การผ่าตัดกรอง (ทราบีคิวเลกโตมี): มีรายงานจำกัดเฉพาะบางกรณีและระยะสั้นถึงปานกลาง ผลลัพธ์มักไม่ดีในเด็ก และการรั่วของลูกตาหลังผ่าตัดสูงถึงประมาณ 25% 13) นอกจากนี้ยังมีรายงานโรคต้อหินชนิดร้ายหลังผ่าตัด
การผ่าตัดปลูกถ่ายชันต์ต้อหิน (การผ่าตัดชันต์แบบท่อ): สามารถใช้อุปกรณ์ชนิด Baerveldt และ Ahmed ได้ ในตาที่ยังมีเลนส์ธรรมชาติ แนะนำให้ใส่ท่อในแนวสัมผัส ไม่ใช่เข้าหาศูนย์กลางกระจกตา สามารถคาดหวังการควบคุมความดันลูกตาที่ดี
การจี้ทำลายซิลิอารีบอดี: ทางเลือกสุดท้าย มีรายงานว่าการจี้เย็นซิลิอารีบอดีทำให้เกิดการรั่วของลูกตาในหลายกรณี เนื่องจากมีภาวะซิลิอารีบอดีเจริญไม่เต็มที่ ความเสี่ยงต่อการรั่วของลูกตาจึงสูงกว่าตาปกติ
เนื่องจากมีความผิดปกติของพัฒนาการของมุมตา จึงจำเป็นต้องใช้แนวทางที่แตกต่างจากโรคต้อหินมุมเปิดปกติ ในครั้งแรกให้เลือกการผ่าตัดสร้างทางระบายน้ำใหม่ จากนั้นการผ่าตัดชันท์แบบท่อเป็นทางเลือกที่ดี บริโมนิดีนห้ามใช้ในเด็กอายุต่ำกว่า 2 ปี และการใช้ยาต้านเมตาบอไลต์อาจทำให้ AAK แย่ลง จึงต้องพิจารณาอย่างรอบคอบ 8)
CQ5: แนะนำอย่างยิ่งให้ดำเนินการดูแลผู้มีสายตาเลือนราง 8)
การแก้ไขค่าสายตาเป็นพื้นฐาน อัตราการเกิดภาวะแทรกซ้อนสายตาสั้นรายงานว่ามากกว่า 64%
CQ6: แนะนำอย่างยิ่งให้รักษาอาการกลัวแสง 8)
ผู้ป่วยส่วนใหญ่สามารถเรียนในโรงเรียนปกติได้ แต่จำเป็นต้องได้รับการสนับสนุน เช่น หนังสือเรียนขยายใหญ่ แท็บเล็ต และที่วางหนังสือ ทางเลือกอื่นๆ ได้แก่ การเรียนในชั้นเรียนสำหรับผู้บกพร่องทางการมองเห็น หรือการใช้บริการให้คำปรึกษาด้านการเลี้ยงดูและการศึกษาจากโรงเรียนคนตาบอดและโรงเรียนสนับสนุนการมองเห็นเฉพาะทาง
ตั้งแต่เดือนเมษายน 2017 เป็นต้นมา โรคนี้ได้รับการกำหนดให้เป็นโรคหายากที่ระบุ ดังนั้นแม้ว่าผู้ป่วยจะยังไม่มีบัตรประจำตัวคนพิการทางร่างกาย หากมีความรุนแรงระดับ III ขึ้นไป ก็จะมีสิทธิ์ได้รับเงินอุดหนุนค่ารักษาพยาบาลและการจัดหาอุปกรณ์เทียม 7) อุปกรณ์เทียมที่มีสิทธิ์ ได้แก่ แว่นสายตา แว่นกันแสง คอนแทคเลนส์ (รวมถึงชนิดที่มีม่านตาเทียม) แว่นตาสำหรับผู้บกพร่องทางการมองเห็น ไม้เท้านิรภัยสำหรับผู้พิการทางสายตา และตาเทียม
ยีน PAX6 ครอบคลุมดีเอ็นเอจีโนม 22 kb ซึ่งประกอบด้วย 14 เอ็กซอน และเข้ารหัสกรดอะมิโน 422 ตัว 1) ยีนนี้มีโดเมนจับดีเอ็นเอสองโดเมน (paired domain และ paired-type homeodomain) และโดเมน PST (ที่อุดมด้วยโพรลีน ซีรีน และทรีโอนีน) ที่ปลาย C ทำหน้าที่เป็นตัวกระตุ้นการถอดรหัส
PAX6 ควบคุมการเพิ่มจำนวน การแยกตัว การเคลื่อนที่ และการยึดเกาะของเซลล์ และเป้าหมายของมันรวมถึง PAX6 เอง รวมถึงยีนที่เข้ารหัสคริสตัลลินของเลนส์และเคราตินของกระจกตา การแสดงออกยังคงดำเนินต่อไปในจอประสาทตา เลนส์ และกระจกตาของผู้ใหญ่ ยีน PAX6 เป็นหนึ่งในยีนควบคุมหลักที่ควบคุมการแยกตัวของอวัยวะในช่วงตัวอ่อน
การกลายพันธุ์ของ PAX6 ส่วนใหญ่ทำให้เกิด haploinsufficiency ผ่านการย่อยสลาย mRNA ที่ขึ้นกับ nonsense-mediated decay (NMD) 1) การกลายพันธุ์ที่ทำให้เกิดรหัสหยุดก่อนกำหนด (PTC) (การกลายพันธุ์แบบ nonsense, frameshift และการกลายพันธุ์แบบ splice ส่วนใหญ่) ส่งผลให้เกิดฟีโนไทป์ aniridia ทั่วไป
ในทางกลับกัน หาก PTC อยู่ในเอ็กซอนสุดท้ายหรือภายใน 50 bp จากปลายของเอ็กซอนรองสุดท้าย การกลายพันธุ์อาจหลบหนี NMD และสร้างโปรตีนที่ถูกตัดทอนซึ่งอาจทำให้เกิดฟีโนไทป์ที่รุนแรง 1)
มีรายงานกรณีที่หายากของการกลายพันธุ์แบบ nonsense ของ PAX6 c.282C>A (p.Cys94*) ร่วมกับ trisomy 21 ในผู้ป่วยรายเดียวกัน การกลายพันธุ์ PAX6 เกิดขึ้นแบบ de novo และทำให้เกิด aniridia สมบูรณ์ทั้งสองข้าง ต้อหินแต่กำเนิด AAK และ foveal hypoplasia 2)
แม้ว่าจะยังไม่มีการกำหนดความสัมพันธ์ระหว่างจีโนไทป์และฟีโนไทป์ที่ชัดเจน แต่ก็ทราบแนวโน้มบางประการ 1)
ในชุดการศึกษา gonioscopy ของ Grant และ Walton แสดงให้เห็นว่า stroma ของม่านตายื่นไปข้างหน้าบน trabecular meshwork เกิดการยึดเกาะคล้าย synechia ค่อยๆ กลายเป็นแผ่นและในที่สุดนำไปสู่การอุดตันของมุม 14) กลไกนี้เป็นปัจจัยหลักในการเกิดต้อหิน ทางพยาธิวิทยาพื้นฐานคือความบกพร่องของกล้ามเนื้อเรียบโดยมีรากม่านตาคงเหลือและความผิดปกติของมุม
AAK เกิดจากภาวะพร่องเซลล์ต้นกำเนิดลิมบัส (LSCD) เป็นหลัก แต่ยังเกี่ยวข้องกับการแบ่งตัวผิดปกติของเยื่อบุกระจกตา การยึดเกาะผิดปกติ การแทรกซึมของเซลล์เยื่อบุตาขาว และการผลิตน้ำตาไม่เพียงพอ การขาด matrix metalloproteinase 9 (MMP-9) ซึ่งควบคุมโดย PAX6 ทำให้เกิดการสะสมของ fibrin และการแทรกซึมของเซลล์อักเสบ ส่งผลให้การจัดเรียงคอลลาเจนใน stroma ผิดปกติและสูญเสียความใส
AAK แบ่งเป็น 5 ระยะ ระยะที่ I: ความผิดปกติของเยื่อบุส่วนปลายเท่านั้น ระยะที่ II: การเปลี่ยนแปลงของเยื่อบุแบบเข้าสู่ศูนย์กลาง (ยังไม่ถึงศูนย์กลาง) ระยะที่ III: การเปลี่ยนแปลงของเยื่อบุกระจกตาส่วนกลางและเส้นเลือดใหม่ผิวเผินส่วนปลาย ระยะที่ IV: เส้นเลือดใหม่ผิวเผินทั่วทั้งกระจกตา ระยะที่ V: ความผิดปกติของเยื่อบุทั่วทั้งกระจกตาและแผลเป็นใน stroma ชั้นลึก 10)
มีความสัมพันธ์ระหว่างสถานะการกลายพันธุ์ของ PAX6 กับการดำเนินโรคของ AAK ในผู้ป่วยที่มีการกลายพันธุ์แบบ PTC หรือต่อปลาย C-terminal AAK จะดำเนินโรคตามอายุ ในขณะที่การกลายพันธุ์ชนิดอื่นอาจทำให้เกิดโรคกระจกตาที่ไม่ดำเนินโรค 11)
กลุ่มอาการ Gillespie เกิดจากการกลายพันธุ์ของยีน ITPR1 3) ITPR1 เป็นสมาชิกของครอบครัวตัวรับ IP3 ซึ่งสร้างช่องปล่อย Ca²⁺ และอยู่ที่เอนโดพลาสมิกเรติคูลัม การกลายพันธุ์แบบเด่นเชิงลบส่งผลต่อการสร้างและคงสภาพของกล้ามเนื้อหูรูดม่านตา ทำให้เกิดภาวะม่านตาพร่องเฉพาะบริเวณรอบรูม่านตาและม่านตาขยายคงที่
ในการทบทวนวรรณกรรมกลุ่มอาการ Gillespie โดย Ciaccio และคณะ (2024) จากการวิเคราะห์ 33 รายที่ยืนยันระดับโมเลกุล พบว่าพัฒนาการด้านการเคลื่อนไหวล่าช้าแต่ดีขึ้นตามเวลา ภาวะบกพร่องทางสติปัญญาไม่พบในทุกราย (17% มีสติปัญญาปกติ) และอาการทางระบบประสาทไม่ดำเนินโรค 3)
ด้วยการแพร่หลายของเทคโนโลยีการวิเคราะห์เอ็กโซมทั้งหมด การระบุการกลายพันธุ์ PAX6 ใหม่ยังคงดำเนินต่อไป ในฐานข้อมูลการกลายพันธุ์ PAX6 ของมนุษย์ มีการบันทึกการกลายพันธุ์ 491 รายการในปี 2018 และมีการรายงานการกลายพันธุ์ใหม่ประมาณ 250 รายการตั้งแต่นั้นมา 1) การกลายพันธุ์ในบริเวณที่ไม่เข้ารหัสก็เริ่มถูกระบุว่าเป็นสาเหตุของภาวะไม่มีม่านตา ซึ่งหวังว่าจะช่วยอธิบายกรณีที่ไม่ได้รับการวินิจฉัยด้วยการตรวจแบบเดิม 9)
ในการผ่าตัดต้อกระจกในผู้ป่วยที่มี AAK รุนแรง เทคนิคการมองเห็นโดยใช้แสงย้อนแบบโคมระย้ามีประโยชน์ 4) เทคนิคนี้ช่วยให้การสลายต้อกระจกด้วยคลื่นเสียงความถี่สูงปลอดภัยแม้ในผู้ป่วยที่มี AAK ระดับ 3-4 และมีการปรับปรุงการมองเห็นหลังผ่าตัด
เริ่มชัดเจนว่ารูปแบบการดำเนินของ AAK แตกต่างกันตามชนิดของการกลายพันธุ์ PAX6 ด้วยต้นทุนการตรวจทางพันธุกรรมที่ลดลง การทำนายแนวทางทางคลินิกตามชนิดของการกลายพันธุ์และการแทรกแซงตั้งแต่เนิ่นๆ จึงกลายเป็นทางเลือกที่สมจริง
ในกรณีของภาวะไม่มีม่านตาร่วมกับกลุ่มอาการดาวน์ มีรายงานแนวทางที่ค่อนข้างไม่รุนแรงแม้จะมีโรคทั้งสองอยู่ร่วมกัน 2) การทำความเข้าใจผลกระทบของการอยู่ร่วมกันของความผิดปกติทางพันธุกรรมหลายอย่างต่อฟีโนไทป์อาจให้ข้อมูลเชิงลึกที่สำคัญสำหรับการแพทย์เฉพาะบุคคลในอนาคต
กำลังมีการศึกษาการประยุกต์ใช้ยา read-through (ataluren) สำหรับการกลายพันธุ์ชนิด PTC ในภาวะไม่มีม่านตาในระดับการวิจัยพื้นฐาน 8) สำหรับการบำบัดด้วยยีน PAX6 การวิจัยพื้นฐานเกี่ยวกับการแทนที่ยีนโดยใช้เวกเตอร์ AAV-PAX6 ในแบบจำลองหนูกลายพันธุ์ Sey กำลังดำเนินอยู่ คาดว่าจะพัฒนาไปสู่การทดลองทางคลินิกในอนาคต
การทดลองทางคลินิกเกี่ยวกับการปลูกถ่ายแผ่นเซลล์เยื่อบุกระจกตาที่ได้จากเซลล์ iPS กำลังดำเนินการทั้งในและต่างประเทศ และได้รับความสนใจในฐานะการรักษาใหม่สำหรับ AAK 8) สำหรับม่านตาเทียม (เช่น CustomFlex Artificial Iris) ประสบการณ์การใช้งานในต่างประเทศกำลังสะสมมากขึ้น คอนแทคเลนส์ที่มีม่านตาเทียมเป็นอุปกรณ์ช่วยเหลืออยู่ภายใต้การคุ้มครองของประกัน
ในแนวทางปฏิบัติทางคลินิก (ปี 2021) การสะสมข้อมูลทะเบียนขนาดใหญ่ในญี่ปุ่นเพื่อทำความเข้าใจสถานการณ์จริง และการปรับปรุงแนวทางตามการปรับปรุงคุณภาพของหลักฐาน ถูกระบุว่าเป็นประเด็นสำคัญในอนาคต 8) คาดว่าจะมีการปรับปรุงการทำนายการดำเนินของ AAK ตามการกลายพันธุ์ของยีนแต่ละบุคคลและการแทรกแซงตั้งแต่เนิ่นๆ