孤立性无虹膜症
频率:约占全部病例的2/3。
遗传方式:常染色体显性遗传(AD)。
特征:由PAX6基因突变引起。不伴有全身症状。外显率完全,但表现度多样。

无虹膜症是一种罕见的先天性疾病,特征为虹膜不同程度的发育不全或缺损。“无虹膜症”这一名称并不准确,因为通过房角镜或超声生物显微镜(UBM)几乎总能检测到虹膜组织碎片。
患病率约为1/40,000至1/100,000,未见显著的种族或性别差异 1)。ICD-10中归类为Q13.1。
无虹膜症是一种全眼球疾病,不仅影响虹膜,还影响角膜、晶状体、房角、中心凹和视神经 1),呈现多种威胁视力的眼部并发症。视力预后通常较差,矫正视力常约为0.1。瞳孔对光反射消失,但调节功能保留。60-90%的病例为双眼发病。
已确认以下三种表型。
孤立性无虹膜症
频率:约占全部病例的2/3。
遗传方式:常染色体显性遗传(AD)。
特征:由PAX6基因突变引起。不伴有全身症状。外显率完全,但表现度多样。
WAGR综合征
频率:部分散发病例。
遗传方式:PAX6和WT1的相邻缺失。
特征:合并Wilms瘤、泌尿生殖器异常和智力障碍。肿瘤风险高达50%。
Gillespie综合征
频率:约占全部病例的2%。
遗传方式:ITPR1基因突变。
特征:伴有小脑性共济失调和智力障碍。特征性虹膜异常表现为固定性瞳孔散大3)。
散发性无虹膜症约占全部病例的1/3,由包含PAX6的11p13新生缺失引起。如果缺失波及相邻的WT1基因,则导致WAGR综合征1)。散发性无虹膜症患者中25-30%发生Wilms瘤,相对风险为67。
PAX6是眼形成的master control基因,参与眼、神经管、嗅球、胰腺朗格汉斯岛和嗅上皮的发育。单等位基因功能丧失(单倍剂量不足)即可发病,双等位基因异常则导致胚胎致死。2017年被指定为《难病法》规定的指定难病,重症度Ⅲ度以上(详见诊断与检查项)可享受医疗费补助7)。
散发性(新发突变)约占全部病例的1/3,即使没有家族史也会发病。散发病例可能提示WAGR综合征,因此基因检测和腹部超声筛查Wilms肿瘤非常重要。
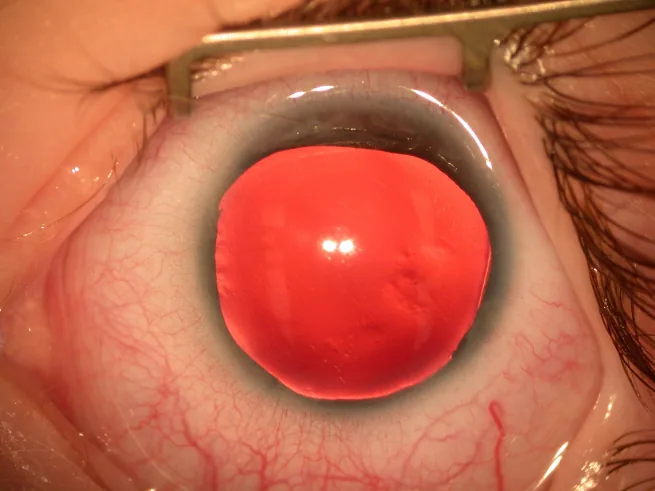
大多数无虹膜症在出生时因虹膜、瞳孔异常或在婴儿期因眼球震颤而被发现。
表型在家族间和家族内有所不同,但左右眼差异通常较小。
主要由于中心凹发育不全,矫正视力通常在0.1至0.2左右。合并黄斑发育不良时视力预后尤其差。从婴儿期开始的屈光矫正和低视力护理对视觉发育很重要。
PAX6不仅在眼组织中表达,还在中枢神经系统、胰腺朗格汉斯岛和嗅上皮中表达,因此可能出现以下眼外并发症8)。
决定视功能的重要因素是青光眼、黄斑发育不良、眼球震颤、角膜病变、白内障和虹膜发育不良。由于青光眼导致的视野和视力损害是不可逆的,因此在随访中眼压管理最为重要。8)
大多数先天性无虹膜症是由位于第11号染色体短臂(11p13)上的PAX6基因杂合突变引起的。单倍体不足是PAX6相关疾病的主要发病机制。1)
PAX6基因是眼睛形成的master control基因,在眼睛、神经管、嗅球和胰腺的发育中起重要作用。正常眼睛发育需要两个拷贝的PAX6,仅一个拷贝的功能丧失即可导致无虹膜症。1)
在一项中国患者的队列研究中,96.9%的病例发现了PAX6基因的致病突变。1)在典型无虹膜症中,诱导无义介导的mRNA降解(NMD)的突变或大片段缺失在96%的病例中被检测到。1)
病理学上,除虹膜根部外平滑肌缺失,房角发育不全。角膜上皮干细胞功能异常,导致上皮和Bowman膜异常,形成富含血管的角膜血管翳。
导致无虹膜症表型的PAX6突变分类如下。
| 突变类型 | 频率 |
|---|---|
| 无义突变 | 约39% |
| 移码突变 | 约25% |
| 剪接突变 | 约13% |
| 错义突变 | 约12% |
通读突变(C末端延伸突变)约占5%,由于终止密码子转变为翻译密码子,产生异常延长的PAX6蛋白6)。C末端延伸突变常伴有严重的虹膜发育不全和高度视力障碍1)6)。
基因突变多为PTC型突变,也有错义突变的报道7)。关于基因检测的实用性,Sanger测序或NGS可在近85%的孤立性无虹膜症患者中检测到突变。此外,MLPA或CMA可在近15%的患者中检测到PAX6基因内或顺式调控区域的缺失8)。
Wang(2023)新鉴定了一个移码突变c.640_646del(p.R214Pfs*28),并报告了一例表现为完全虹膜缺损、中心凹发育不全、晶状体偏位和视网膜脱离的病例1)。
Ratna等人(2022)在一个印度家系中鉴定出通读突变c.1268A>T(p.*423L)。患者表现为完全无虹膜、眼球震颤、中心凹发育不全、AAK、晶状体向上半脱位、高度近视和视神经萎缩,显示出C末端延伸突变导致的严重表型6)。
在散发性无虹膜症中,涉及PAX6和WT1的大片段缺失是WAGR综合征的原因。存在WT1缺失时,Wilms肿瘤风险高达50%1)。若怀疑WAGR综合征,可通过基因检测确认PAX6和WT1缺失,从而进行Wilms肿瘤风险评估和发育迟缓的随访8)。基因检测对WT1区域的评估至关重要,散发性病例中30%在5岁前发生Wilms肿瘤。由于WT1基因位于PAX6附近,两者同时缺失的11号染色体短臂缺失(11p13缺失)导致无虹膜症合并Wilms肿瘤。
Gillespie综合征由ITPR1基因的杂合显性负性突变或双等位基因突变引起3)。迄今为止,已有37例通过分子诊断确诊,Gly2554残基被认为是热点3)。
根据无虹膜症的诊断标准(2020年),依据以下标准确诊7)。
A. 症状
B. 检查所见
C. 需鉴别的疾病
E. 遗传学检查:PAX6基因致病性变异或11p13区域缺失
诊断类别7):
用于难病认定的严重程度分类规定如下四个等级7)。
| 严重程度 | 定义 |
|---|---|
| Ⅰ度 | 单眼受累,对侧眼正常 |
| Ⅱ度 | 双眼患病,较好眼矫正视力≥0.3 |
| Ⅲ度 | 双眼患病,较好眼矫正视力≥0.1且<0.3 |
| Ⅳ度 | 双眼患病,较好眼矫正视力<0.1 |
即使为Ⅰ~Ⅲ度,若伴有青光眼等导致的视野狭窄(Goldmann I/4视标中心残存视野20度以内),则严重程度上升一级。严重程度Ⅲ度及以上为医疗费补助对象7)。
通过裂隙灯显微镜确认虹膜缺损或发育不全即可轻松做出临床诊断。使用房角镜和超声生物显微镜评估残留虹膜组织。同时检查前房角发育异常的有无。
系统评估以下眼部并发症:
无虹膜症遗传评估最重要的目标是确认PAX6缺失是否延伸至WT1基因1)。通过全外显子组测序或MLPA法评估PAX6和WT1区域的突变和缺失1)2)。
散发性无虹膜症中,因WT1基因缺失导致的Wilms肿瘤风险评估直接关系到生命预后1)。即使是家族性病例,由于表型多样性,也建议进行基因检测以确诊并提供遗传咨询。
无虹膜症尚无根治性治疗方法。管理核心是低视力康复以最大限度利用残余视力,以及针对各并发症的个体化治疗。临床指南(2021年)基于6个临床问题提出了建议8)。
CQ1:弱推荐不进行角膜移植治疗角膜基质混浊8)。
角膜移植可能在短期内改善视力,但由于黄斑发育不全等合并症,改善有限。长期来看,由于青光眼进展和移植片功能不全,视力预后不良。
CQ2:弱推荐对角膜上皮干细胞缺乏症进行手术治疗。 8)
CQ3:弱推荐实施白内障手术。 8)
白内障在20岁前发病率为50–85%。根据混浊和畏光程度计划手术。据报道66–100%的手术病例视力改善,但需注意以下几点。
由于Zinn小带脆弱,人工晶状体植入需谨慎适应。
Hu等人(2024)对两例伴有严重AAK的先天性无虹膜症患者实施了吊灯式后照明辅助下的超声乳化白内障吸除术。由于角膜混浊,常规术中可视化困难,但后方照明使晶状体和前囊清晰可见,术后3周矫正视力分别改善至20/200和20/10004)。
CQ4:强烈推荐进行青光眼治疗8)。
青光眼发病后,根据以下五步算法进行管理。
药物治疗:β受体阻滞剂、交感神经兴奋剂和前列腺素(PG)相关药物有效。溴莫尼定(α肾上腺素受体激动剂)因有中枢神经抑制风险,禁用于2岁以下儿童。若担心角膜上皮损伤,应使用不含防腐剂的制剂。
流出道重建术(房角切开术/小梁切开术):推荐作为初次手术16)。也有预防性房角切开术的报道。但在残留虹膜覆盖小梁网的病例中可能无效。
滤过手术(小梁切除术):仅有少数中短期报道。在儿童眼中效果往往较差,术后低眼压发生率约25%13)。也有术后恶性青光眼的报道。
青光眼植入物手术(引流阀植入术):可使用Baerveldt和Ahmed型装置。在有晶状体眼中植入引流管时,建议采用切线方向而非角膜中央方向。可望获得良好的眼压控制。
睫状体破坏手术:最后手段。睫状体冷冻术据报道常导致低眼压。由于睫状体发育不全,低眼压风险高于健康眼。
由于存在房角发育异常,需要采取与通常的开角型青光眼不同的方法。初次选择流出道重建术,其次,管分流手术是良好的选择。溴莫尼定禁用于2岁以下儿童,使用抗代谢药物可能加重AAK,因此需要谨慎判断8)。
CQ5:强烈推荐进行低视力康复8)。
屈光矫正是基础,近视的合并率据报道为64%以上。
CQ6:强烈推荐进行畏光治疗8)。
大多数患者可以进入普通学校学习,但需要放大课本、平板电脑、阅读架等支持。也可以选择进入弱视班,或利用盲校/视觉特别支援学校的育儿咨询和教育咨询。
自2017年4月起,该病被认定为指定疑难病,因此即使未取得残疾人手册,重症度Ⅲ度以上的患者也可享受医疗费补助和辅助器具的提供7)。适用的辅助器具包括矫正眼镜、遮光眼镜、隐形眼镜(含人工虹膜型)、弱视眼镜、视觉障碍者安全拐杖和义眼。
PAX6基因跨越22 kb的基因组DNA,包含14个外显子,编码422个氨基酸1)。它具有两个DNA结合结构域(配对结构域和配对型同源结构域),C端的PST(富含脯氨酸、丝氨酸、苏氨酸)结构域作为转录激活因子发挥作用。
PAX6调控细胞的增殖、分化、迁移和粘附,其靶点包括PAX6自身以及编码晶状体蛋白和角膜角蛋白的基因。在成人的视网膜、晶状体和角膜中持续表达。PAX6是调控胚胎期器官分化的主控基因之一。
大多数PAX6突变通过无义介导的mRNA降解(NMD)导致单倍剂量不足1)。引入提前终止密码子(PTC)的突变(无义突变、移码突变和大多数剪接突变)会导致典型的无虹膜症表型。
另一方面,如果PTC位于最后一个外显子或倒数第二个外显子的末端50 bp以内,则可能逃逸NMD,翻译出截短蛋白,可能导致严重表型1)。
曾有罕见病例报道,同一患者同时存在PAX6无义突变c.282C>A(p.Cys94*)和21三体综合征。PAX6突变是新发突变,表现为完全双眼无虹膜、先天性青光眼、AAK和中心凹发育不全2)。
虽然尚未建立明确的基因型-表型相关性,但已知一些趋势1)。
Grant和Walton的房角镜检查系列显示,早期虹膜基质向前延伸至小梁网上形成粘连样附着,逐渐呈片状并最终导致房角关闭14)。该机制是青光眼发生的主要原因。病理学基础是虹膜根部保留的平滑肌缺损和房角发育不全。
AAK主要由角膜缘干细胞缺乏(LSCD)引起,但角膜上皮异常分化和黏附异常、结膜细胞浸润以及泪液分泌不足也参与其中。由PAX6调节的基质金属蛋白酶9(MMP-9)缺乏导致纤维蛋白积聚和炎症细胞浸润,基质胶原排列紊乱导致透明性丧失。
AAK分为5期。I期仅周边上皮异常,II期向心性上皮改变(未达中央),III期中央角膜上皮改变和周边浅层新生血管,IV期全角膜浅层新生血管,V期全角膜上皮异常和深层基质瘢痕10)。
PAX6突变状态与AAK进展相关。携带PTC或C末端延长突变的患者AAK呈年龄依赖性进展,而其他突变类型可能表现为非进行性角膜病变11)。
Gillespie综合征由ITPR1基因突变引起3)。ITPR1是IP3受体家族成员,形成Ca²⁺释放通道并定位于内质网。显性负性突变影响虹膜括约肌的形成和维持,导致瞳孔周围特异性虹膜发育不全和固定性瞳孔散大。
Ciaccio等人(2024)的Gillespie综合征文献综述中,对33例分子确诊病例的分析证实,运动发育延迟但随时间改善,并非所有病例均有智力障碍(17%智力正常),神经系统体征为非进行性3)。
随着全外显子组测序技术的普及,新的PAX6突变不断被鉴定。截至2018年,人类PAX6突变数据库已登记491个突变,此后又报告了约250个新突变1)。非编码区的突变也被确定为无虹膜症的原因,有望阐明传统检测无法诊断的病例9)。
对于伴有严重AAK的病例,使用吊灯式逆照明辅助的可视化技术在白内障手术中很有用4)。该技术即使在3~4级高度AAK患者中也能安全进行超声乳化吸除术,并已获得术后视力改善。
PAX6突变的类型不同,AAK的进展模式也有所不同。随着基因检测成本的降低,基于突变类型的临床病程预测和早期干预正成为现实的选择。
在无虹膜症合并21三体综合征的病例中,尽管两种疾病共存,但已有报告显示病程相对较轻2)。理解多种遗传障碍在同一患者中共存时对表型的影响,可能为未来的个体化医疗提供重要见解。
针对PTC型突变的通读药物(ataluren)在无虹膜症中的应用正在基础研究层面进行探讨8)。关于PAX6基因治疗,使用AAV-PAX6载体对Sey突变小鼠模型进行基因补充的基础研究正在进行中。期待未来向临床试验的转化。
iPS细胞来源的角膜上皮细胞片移植的临床试验正在国内外进行,作为AAK的新疗法备受关注8)。人工虹膜(如CustomFlex Artificial Iris等)在海外已有使用经验积累。作为辅助器具,带人工虹膜的隐形眼镜属于保险适用范围。
根据诊疗指南(2021年),通过积累日本国内大规模注册数据来掌握实际情况,并基于证据质量的提高修订指南,被定位为未来的重要课题8)。期待基于个体基因突变的AAK进展预测和早期干预的优化。