Aniridia isolata
Frequenza: circa 2/3 del totale.
Modalità di trasmissione: autosomica dominante (AD).
Caratteristiche: causata da mutazione del gene PAX6. Nessun sintomo sistemico. Penetranza completa ma espressività variabile.

L’aniridia è una rara malattia congenita caratterizzata da un diverso grado di sottosviluppo o assenza dell’iride. Il termine ‘aniridia’ è un termine improprio, poiché alla gonioscopia o all’ecografia biomicroscopica (UBM) sono quasi sempre visibili frammenti di tessuto irideo.
La prevalenza è di circa 1/40.000-1/100.000 e non sono state riportate differenze significative di razza o sesso 1). Nell’ICD-10 è classificata come Q13.1.
Si tratta di una malattia panoculare che colpisce non solo l’iride, ma anche cornea, cristallino, angolo, fovea e nervo ottico 1), presentandosi con varie complicanze oculari che minacciano la vista. La prognosi visiva è generalmente sfavorevole, con l’acuità visiva corretta che spesso rimane intorno a 0,1. Il riflesso pupillare è assente ma l’accomodazione è preservata e il 60-90% dei casi è bilaterale.
Sono riconosciuti i seguenti tre fenotipi.
Aniridia isolata
Frequenza: circa 2/3 del totale.
Modalità di trasmissione: autosomica dominante (AD).
Caratteristiche: causata da mutazione del gene PAX6. Nessun sintomo sistemico. Penetranza completa ma espressività variabile.
Sindrome WAGR
Frequenza: una parte dei casi sporadici.
Modalità di trasmissione: delezione contigua di PAX6 e WT1.
Caratteristiche: associata a tumore di Wilms, anomalie genitourinarie e ritardo mentale. Rischio tumorale fino al 50%.
Sindrome di Gillespie
Frequenza: circa il 2% del totale.
Modalità di trasmissione: mutazione del gene ITPR1.
Caratteristiche: associata ad atassia cerebellare e disabilità intellettiva. Caratteristica è un’anomalia iridea specifica con midriasi fissa3).
L’aniridia sporadica rappresenta circa 1/3 del totale ed è causata da una delezione de novo di 11p13 che include PAX6. Se la delezione si estende al gene WT1 adiacente, causa la sindrome WAGR1). Il 25-30% delle aniridie sporadiche sviluppa un tumore di Wilms, con un rischio relativo riportato di 67.
PAX6 è un gene maestro del controllo della formazione dell’occhio, coinvolto nello sviluppo dell’occhio, del tubo neurale, del bulbo olfattivo, delle isole di Langerhans del pancreas e dell’epitelio olfattivo. La perdita di funzione di un allele (aploinsufficienza) causa la malattia; l’anomalia di entrambi gli alleli è letale in utero. Nel 2017 è stata designata come malattia rara specificata dalla legge sulle malattie rare, e i casi con gravità di grado III o superiore (per i dettagli, vedere la sezione Diagnosi ed esami) hanno diritto a un contributo per le spese mediche7).
I casi sporadici (nuova mutazione) rappresentano circa un terzo di tutti i casi e possono verificarsi senza una storia familiare. Nei casi sporadici esiste la possibilità di una sindrome WAGR, pertanto sono importanti il test genetico e lo screening ecografico addominale per il tumore di Wilms.
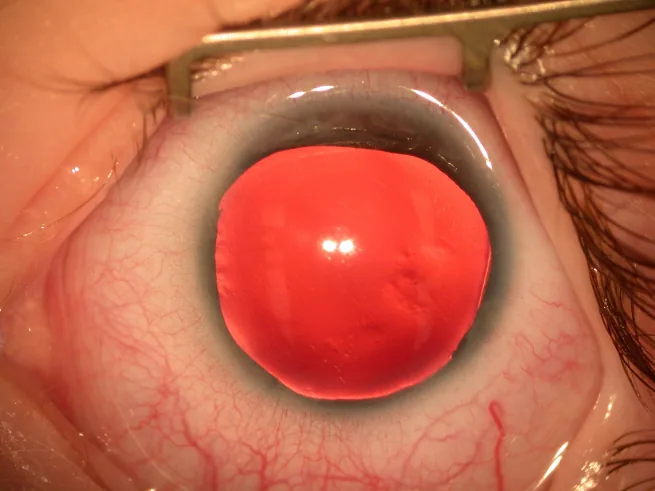
La maggior parte dei casi di aniridia viene scoperta alla nascita a causa di un’anomalia dell’iride o della pupilla, oppure durante l’infanzia a causa del nistagmo.
Il fenotipo varia tra le famiglie e all’interno della stessa famiglia, ma le differenze tra i due occhi sono generalmente piccole.
Principalmente a causa dell’ipoplasia foveale, l’acuità visiva corretta è spesso di circa 0,1–0,2. In caso di ipoplasia maculare associata, la prognosi visiva è particolarmente sfavorevole. La correzione refrattiva e la cura dell’ipovisione fin dalla prima infanzia sono importanti per lo sviluppo visivo.
PAX6 è espresso non solo nei tessuti oculari ma anche nel sistema nervoso centrale, nelle isole di Langerhans del pancreas e nell’epitelio olfattivo, pertanto possono essere osservate le seguenti complicanze extraoculari 8).
I fattori determinanti della funzione visiva sono il glaucoma, l’ipoplasia maculare, il nistagmo, la cheratopatia, la cataratta e l’anomalia dell’iride. I danni al campo visivo e all’acuità visiva causati dal glaucoma sono irreversibili, quindi la gestione della pressione intraoculare è fondamentale nel follow-up.8)
La maggior parte delle aniridie congenite è causata da mutazioni eterozigoti del gene PAX6 situato sul braccio corto del cromosoma 11 (11p13). L’aploinsufficienza di PAX6 è il principale meccanismo patogenetico.1)
Il gene PAX6 è un gene maestro del controllo dello sviluppo oculare e svolge un ruolo cruciale nello sviluppo dell’occhio, del tubo neurale, del bulbo olfattivo e del pancreas. Per il normale sviluppo dell’occhio sono necessarie due copie di PAX6 e la perdita di funzione di una sola copia è sufficiente a causare l’aniridia.1)
In uno studio di coorte su pazienti cinesi, mutazioni causative nel gene PAX6 sono state identificate nel 96,9% dei casi.1) Nell’aniridia tipica, mutazioni che inducono la degradazione dell’mRNA mediata da codoni di stop prematuri (NMD) o delezioni di grandi dimensioni vengono rilevate nel 96% dei casi.1)
Dal punto di vista patologico, la muscolatura liscia è assente tranne che alla radice dell’iride e si osserva un sottosviluppo dell’angolo iridocorneale. È presente una disfunzione delle cellule staminali dell’epitelio corneale, che porta ad anomalie dell’epitelio e della membrana di Bowman, con formazione di un panno riccamente vascolarizzato.
La distribuzione delle mutazioni di PAX6 che causano il fenotipo dell’aniridia è mostrata di seguito.
| Tipo di mutazione | Frequenza |
|---|---|
| Mutazione nonsenso | Circa 39% |
| Mutazione con scorrimento della finestra di lettura | Circa 25% |
| Mutazione di splicing | Circa 13% |
| Mutazione missenso | Circa il 12% |
Le mutazioni run-on (mutazioni di estensione C-terminale) rappresentano circa il 5% dei casi. Esse derivano dalla conversione di un codone di stop in un codone di traduzione, producendo una proteina PAX6 anormalmente allungata 6). Le mutazioni di estensione C-terminale sono spesso associate a grave ipoplasia dell’iride e grave deficit visivo 1)6).
Le mutazioni genetiche sono per lo più di tipo PTC (codone di stop prematuro), ma sono state riportate anche mutazioni missenso 7). Per quanto riguarda l’utilità dei test genetici, il sequenziamento Sanger o NGS rileva mutazioni in quasi l’85% dei casi di aniridia isolata. Inoltre, MLPA o CMA rilevano delezioni nel gene PAX6 o nella regione cis-regolatoria in quasi il 15% dei casi 8).
Wang (2023) ha identificato una nuova mutazione frameshift c.640_646del (p.R214Pfs*28) e ha riportato un caso con assenza completa dell’iride, ipoplasia foveale, ectopia lentis e distacco di retina 1).
Ratna et al. (2022) hanno identificato una mutazione run-on c.1268A>T (p.*423L) in una famiglia indiana. Gli individui affetti presentavano aniridia completa, nistagmo, ipoplasia foveale, AAK, sublussazione superiore del cristallino, miopia elevata e atrofia ottica, dimostrando il fenotipo grave associato alle mutazioni di estensione C-terminale 6).
Nell’aniridia sporadica, grandi delezioni che includono il gene WT1 oltre a PAX6 causano la sindrome WAGR. In caso di delezione di WT1, il rischio di tumore di Wilms arriva fino al 50% 1). In caso di sospetta sindrome WAGR, il test genetico può confermare le delezioni di PAX6 e WT1, consentendo la valutazione del rischio di tumore di Wilms e il monitoraggio del ritardo dello sviluppo 8). La valutazione della regione WT1 tramite test genetico è essenziale; si stima che il 30% dei casi sporadici sviluppi un tumore di Wilms entro i 5 anni di età. A causa della vicinanza dei geni WT1 e PAX6, la delezione del braccio corto del cromosoma 11 (delezione 11p13) provoca aniridia in combinazione con tumore di Wilms.
La sindrome di Gillespie è causata da mutazioni eterozigoti dominanti negative o bialleliche nel gene ITPR1 3). Ad oggi, sono stati riportati 37 casi confermati molecolarmente, e il residuo Gly2554 è noto come hot spot 3).
Secondo i criteri diagnostici per l’aniridia (2020), la diagnosi viene confermata sulla base dei seguenti criteri 7).
A. Sintomi
B. Reperti strumentali
C. Diagnosi differenziale
E. Test genetici : Mutazione patogena del gene PAX6 o delezione della regione 11p13
Categorie diagnostiche7) :
La classificazione della gravità per il riconoscimento come malattia rara è definita in quattro stadi7).
| Gravità | Definizione |
|---|---|
| Grado I | Coinvolgimento unilaterale, occhio controlaterale sano |
| Grado II | Coinvolgimento bilaterale, migliore acuità visiva corretta ≥ 0,3 |
| Grado III | Coinvolgimento bilaterale, migliore acuità visiva corretta ≥ 0,1 e < 0,3 |
| Grado IV | Coinvolgimento bilaterale, migliore acuità visiva corretta < 0,1 |
Anche per i gradi I–III, in presenza di restringimento del campo visivo dovuto a glaucoma (campo visivo centrale residuo ≤ 20° con bersaglio Goldmann I/4), la gravità aumenta di un livello. La gravità di grado III o superiore dà diritto all’assistenza medica 7).
La diagnosi clinica è semplice se si conferma l’assenza o l’ipoplasia dell’iride con la lampada a fessura. La valutazione del tessuto irideo residuo viene effettuata mediante gonioscopia o microscopia ultrasonica biomicroscopica. Verificare anche la presenza di anomalie dello sviluppo dell’angolo della camera anteriore.
Valutare sistematicamente le seguenti complicanze oculari:
L’obiettivo più importante della valutazione genetica dell’aniridia è determinare se la delezione di PAX6 si estende al gene WT11). Il sequenziamento dell’intero esoma o la tecnica MLPA consentono di valutare mutazioni/delezioni nelle regioni PAX6 e WT11)2).
Nell’aniridia sporadica, la valutazione del rischio di tumore di Wilms da delezione del gene WT1 è direttamente correlata alla prognosi vitale1). Anche nelle forme familiari, a causa della diversità fenotipica, si raccomandano la diagnosi genetica e la consulenza genetica.
Non esiste un trattamento curativo per l’aniridia. La gestione si basa sulla riabilitazione visiva per massimizzare l’acuità visiva residua e sul trattamento individuale di ogni complicanza. Le linee guida cliniche (2021) presentano raccomandazioni basate su 6 quesiti clinici8).
CQ1: Si raccomanda debolmente di non eseguire il trapianto di cornea per l’opacità stromale corneale8).
Il trapianto di cornea può migliorare l’acuità visiva a breve termine, ma il miglioramento è limitato a causa di comorbidità come l’ipoplasia maculare. A lungo termine, la progressione del glaucoma e il fallimento del trapianto portano a una prognosi visiva sfavorevole.
CQ2: Si raccomanda debolmente di eseguire un trattamento chirurgico per l’insufficienza delle cellule staminali epiteliali corneali. 8)
CQ3: Si raccomanda debolmente di eseguire un intervento di cataratta. 8)
La cataratta si sviluppa nel 50–85% dei pazienti entro i 20 anni. L’intervento viene pianificato in base all’intensità dell’opacità e della fotofobia. È stato riportato un miglioramento visivo nel 66–100% dei casi operati, ma è necessario prestare attenzione ai seguenti punti.
A causa della fragilità delle zonule di Zinn, l’inserimento di un impianto intraoculare richiede un’attenta indicazione.
Hu et al. (2024) hanno eseguito la facoemulsificazione assistita da illuminazione retrograda a lampadario in due pazienti con aniridia congenita e AAK grave. A causa dell’opacità corneale, la visualizzazione intraoperatoria abituale era difficile, ma l’illuminazione posteriore ha permesso una chiara visualizzazione del cristallino e della capsula anteriore, e l’acuità visiva corretta è migliorata rispettivamente a 20/200 e 20/1000 a 3 settimane dall’intervento 4).
CQ4: Si raccomanda vivamente di trattare il glaucoma 8).
Dopo l’insorgenza del glaucoma, la gestione segue il seguente algoritmo in 5 fasi.
Terapia farmacologica: Beta-bloccanti, simpaticomimetici e farmaci correlati alle prostaglandine (PG) sono efficaci. La brimonidina (agonista alfa-adrenergico) è controindicata nei bambini di età inferiore a 2 anni a causa del rischio di depressione del SNC. In caso di rischio di danno epiteliale corneale, utilizzare preparati senza conservanti.
Chirurgia ricostruttiva del deflusso (goniotomia, trabeculotomia): Raccomandata come primo intervento 16). Sono state riportate anche goniotomie profilattiche. Tuttavia, può essere inefficace nei casi in cui l’iride residua copre il trabecolato.
Chirurgia filtrante (trabeculectomia): Solo pochi report a breve e medio termine. Negli occhi pediatrici i risultati tendono a essere scadenti e la fistola bulbare postoperatoria si verifica in circa il 25% dei casi 13). Sono stati riportati anche casi di glaucoma maligno postoperatorio.
Chirurgia con impianto per glaucoma (chirurgia di shunt tubulare): Sono disponibili dispositivi di tipo Baerveldt e Ahmed. Per l’inserimento del tubo in un occhio fachico, si raccomanda una direzione tangenziale piuttosto che verso il centro della cornea. Ci si aspetta un buon controllo della pressione intraoculare.
Ciclocoagulazione: Ultima risorsa. La criocoagulazione del corpo ciliare ha spesso portato a fistola bulbare. A causa dell’ipoplasia del corpo ciliare, il rischio di fistola bulbare è più elevato rispetto a un occhio sano.
A causa dell’anomalia dello sviluppo dell’angolo, è necessario un approccio diverso rispetto al glaucoma ad angolo aperto comune. Come prima scelta si opta per la ricostruzione delle vie di deflusso, seguita dall’intervento di shunt tubulare come buona opzione. La brimonidina è controindicata nei bambini di età inferiore a 2 anni e l’uso di antimetaboliti può peggiorare l’AAK, pertanto è necessaria una decisione attenta 8).
CQ5: Si raccomanda vivamente di attuare la cura per ipovisione 8).
La correzione refrattiva è fondamentale e il tasso di complicanze della miopia è stimato superiore al 64%.
CQ6: Si raccomanda vivamente di trattare la fotofobia 8).
La maggior parte dei pazienti può frequentare classi normali, ma necessita di supporti come libri di testo ingranditi, tablet e leggii. Sono opzioni anche la frequenza di classi per ipovedenti o l’utilizzo di consulenze educative e per la cura dei bambini offerte da scuole per ciechi o scuole speciali per la vista.
Da aprile 2017, questa malattia è riconosciuta come malattia rara designata. Pertanto, anche senza certificato di disabilità, i pazienti con gravità di grado III o superiore hanno diritto a contributi per le spese mediche e alla fornitura di ausili 7). Gli ausili ammissibili includono occhiali correttivi, occhiali schermanti, lenti a contatto (incluse quelle con iride artificiale), occhiali per ipovedenti, bastone di sicurezza per non vedenti e protesi oculare.
PAX6 si estende su 22 kb di DNA genomico contenente 14 esoni e codifica per 422 amminoacidi 1). Possiede due domini di legame al DNA (dominio paired e omeodominio paired) e un dominio PST C-terminale (ricco di prolina, serina e treonina) che funge da attivatore trascrizionale.
PAX6 regola la proliferazione, differenziazione, migrazione e adesione cellulare. I suoi bersagli includono lo stesso PAX6, nonché i geni che codificano per le cristalline del cristallino e le cheratine corneali. L’espressione continua nella retina, nel cristallino e nella cornea adulti. PAX6 è uno dei geni di controllo master che governano la differenziazione degli organi durante il periodo embrionale.
La maggior parte delle mutazioni di PAX6 causa aploinsufficienza attraverso la degradazione dell’mRNA mediata da codoni di stop non senso (NMD) 1). Le mutazioni che introducono un codone di stop prematuro (PTC) (mutazioni non senso, frameshift e la maggior parte delle mutazioni di splicing) portano al fenotipo tipico di aniridia.
D’altra parte, se il PTC si trova nell’ultimo esone o entro 50 bp terminali del penultimo esone, può sfuggire al NMD e una proteina tronca può essere tradotta, portando a un fenotipo grave 1).
È stato riportato un raro caso di mutazione non senso PAX6 c.282C>A (p.Cys94*) associata a trisomia 21 nello stesso paziente. La mutazione PAX6 è insorta de novo, causando aniridia bilaterale completa, glaucoma congenito, AAK e ipoplasia foveale 2).
Sebbene non sia stata stabilita una chiara correlazione genotipo-fenotipo, sono note alcune tendenze 1).
Nella serie di gonioscopie di Grant e Walton, è stato dimostrato che inizialmente lo stroma irideo si estende anteriormente sul trabecolato, formando aderenze, poi gradualmente diventa a lamina e infine porta all’occlusione angolare 14). Questo meccanismo è il principale fattore nello sviluppo del glaucoma. Patologicamente, alla base vi sono un difetto della muscolatura liscia con risparmio della radice dell’iride e una disgenesia dell’angolo.
L’AAK è causata principalmente da una deficienza di cellule staminali limbari (LSCD), ma sono coinvolti anche una differenziazione anomala dell’epitelio corneale, un’adesione anomala, l’infiltrazione di cellule congiuntivali e una produzione lacrimale insufficiente. Una carenza di metalloproteinasi di matrice 9 (MMP-9), regolata da PAX6, porta all’accumulo di fibrina e all’infiltrazione di cellule infiammatorie, alterando l’organizzazione del collagene stromale e causando perdita di trasparenza.
L’AAK è classificata in 5 stadi. Lo stadio I presenta solo anomalie epiteliali periferiche, lo stadio II un cambiamento epiteliale centripeto (non raggiunge il centro), lo stadio III un cambiamento epiteliale centrale e neovascolarizzazione superficiale periferica, lo stadio IV una neovascolarizzazione superficiale di tutta la cornea, e lo stadio V un’anomalia epiteliale totale e una cicatrice stromale profonda 10).
Esiste una correlazione tra lo stato mutazionale di PAX6 e la progressione dell’AAK. Nei pazienti con mutazioni PTC o di estensione C-terminale, l’AAK progredisce in modo dipendente dall’età, mentre altri tipi di mutazioni possono causare una cheratopatia non progressiva 11).
La sindrome di Gillespie è causata da mutazioni nel gene ITPR1 3). ITPR1 appartiene alla famiglia dei recettori IP3, forma canali di rilascio di Ca²⁺ ed è localizzato nel reticolo endoplasmatico. Le mutazioni dominanti negative influenzano la formazione e il mantenimento dello sfintere dell’iride, portando a un’ipoplasia iridea specifica intorno alla pupilla e a midriasi fissa.
In una revisione della letteratura sulla sindrome di Gillespie di Ciaccio et al. (2024), l’analisi di 33 casi confermati molecolarmente ha mostrato che lo sviluppo motorio è ritardato ma migliora nel tempo, il deficit intellettivo non è presente in tutti i casi (17% ha intelligenza normale) e i segni neurologici sono non progressivi 3).
Con la diffusione del sequenziamento dell’intero esoma, continuano a essere identificate nuove mutazioni di PAX6. Nel 2018, l’Human PAX6 Mutation Database contava 491 mutazioni, e da allora sono state riportate circa 250 nuove mutazioni 1). Mutazioni nelle regioni non codificanti vengono anche identificate come causa di aniridia, il che dovrebbe chiarire i casi non diagnosticati con i test convenzionali 9).
Per la chirurgia della cataratta in casi di AAK grave, è utile la tecnica di visualizzazione con illuminazione retrograda a candelabro 4). Questa tecnica consente una facoemulsificazione sicura anche in pazienti con AAK di grado 3-4, con miglioramento della vista post-operatorio.
Sta diventando chiaro che il tipo di mutazione di PAX6 influenza il pattern di progressione dell’AAK. Con la riduzione dei costi dei test genetici, la predizione del decorso clinico basata sul tipo di mutazione e l’intervento precoce diventano opzioni realistiche.
In casi di aniridia associata a trisomia 21, sono stati riportati esempi di decorso relativamente lieve nonostante la coesistenza di entrambe le malattie 2). Comprendere l’impatto della coesistenza di più disturbi genetici in uno stesso paziente sul fenotipo potrebbe fornire importanti conoscenze per la medicina personalizzata futura.
L’applicazione dell’ataluren, un farmaco read-through per mutazioni di tipo PTC, all’aniridia è studiata a livello di ricerca di base 8). Per quanto riguarda la terapia genica di PAX6, sono in corso ricerche di base sulla sostituzione genica tramite vettore AAV-PAX6 in un modello murino con mutazione Sey. Ci si aspetta uno sviluppo verso studi clinici futuri.
Studi clinici sul trapianto di foglietti epiteliali corneali derivati da cellule iPS sono condotti in Giappone e all’estero, attirando attenzione come nuova terapia per l’AAK 8). Per le iridi artificiali (come CustomFlex Artificial Iris), l’esperienza d’uso all’estero si accumula. Le lenti a contatto con iride artificiale sono coperte dall’assicurazione come dispositivi di assistenza.
Secondo le linee guida cliniche (2021), l’accumulo di dati di registro su larga scala in Giappone per comprendere la situazione reale e la revisione delle linee guida basata sul miglioramento della qualità delle evidenze sono considerati compiti importanti per il futuro 8). Ci si aspetta l’ottimizzazione della predizione della progressione dell’AAK e dell’intervento precoce basata sulle singole mutazioni genetiche.