آنیریدی ایزوله
فراوانی: حدود دو سوم کل موارد.
الگوی توارث: اتوزومال غالب (AD).
ویژگیها: ناشی از جهش در ژن PAX6. بدون علائم سیستمیک. نفوذ کامل اما بیان متغیر.

آنیریدیا (Aniridia) یک بیماری مادرزادی نادر است که با هیپوپلازی یا فقدان عنبیه به درجات مختلف مشخص میشود. نام «آنیریدیا» اشتباه است و با گونیوسکوپی یا میکروسکوپ اولتراسوند (UBM) تقریباً همیشه قطعاتی از بافت عنبیه دیده میشود.
شیوع حدود ۱ در ۴۰٬۰۰۰ تا ۱ در ۱۰۰٬۰۰۰ است و تفاوت نژادی یا جنسی قابل توجهی گزارش نشده است 1). در ICD-10 با کد Q13.1 طبقهبندی میشود.
این بیماری نه تنها عنبیه، بلکه قرنیه، عدسی، زاویه، فووآ و عصب بینایی را نیز تحت تأثیر قرار میدهد 1) و عوارض چشمی متعددی را ایجاد میکند که بینایی را تهدید میکنند. پیشآگهی بینایی عموماً ضعیف است و اغلب دید اصلاحشده حدود ۰.۱ است. واکنش مردمک از بین رفته اما تطابق حفظ میشود و ۶۰ تا ۹۰٪ موارد دوطرفه هستند.
سه فنوتیپ زیر شناخته شده است.
آنیریدی ایزوله
فراوانی: حدود دو سوم کل موارد.
الگوی توارث: اتوزومال غالب (AD).
ویژگیها: ناشی از جهش در ژن PAX6. بدون علائم سیستمیک. نفوذ کامل اما بیان متغیر.
سندرم WAGR
فراوانی: بخشی از موارد پراکنده.
الگوی توارث: حذف مجاور ژنهای PAX6 و WT1.
ویژگیها: همراه با تومور ویلمز، ناهنجاریهای دستگاه تناسلی-ادراری و عقبماندگی ذهنی. خطر تومور تا ۵۰٪.
سندرم گیلسپی
فراوانی: حدود ۲٪ از کل موارد.
الگوی توارث: جهش در ژن ITPR1.
ویژگیها: همراه با آتاکسی مخچهای و ناتوانی ذهنی. ناهنجاری مشخص عنبیه با میدریاز ثابت مشخصه است3).
آنیریدی پراکنده حدود یک سوم کل موارد را تشکیل میدهد و ناشی از حذف de novo در ناحیه 11p13 شامل PAX6 است. اگر حذف به ژن مجاور WT1 گسترش یابد، باعث سندرم WAGR میشود1). ۲۵ تا ۳۰٪ از موارد آنیریدی پراکنده به تومور ویلمز مبتلا میشوند و خطر نسبی ۶۷ گزارش شده است.
PAX6 یک ژن کنترل کننده اصلی در تشکیل چشم است و در رشد چشم، لوله عصبی، پیاز بویایی، جزایر لانگرهانس پانکراس و اپیتلیوم بویایی نقش دارد. بیماری با از دست دادن عملکرد یک آلل (هاپلوناکافی) ایجاد میشود و ناهنجاری در هر دو آلل منجر به مرگ جنینی میشود. از سال ۲۰۱۷ به عنوان یک بیماری نادر تحت قانون بیماریهای نادر تعیین شده است و موارد با شدت درجه III یا بالاتر (برای جزئیات به بخش تشخیص و آزمایش مراجعه کنید) واجد شرایط کمک هزینه پزشکی هستند7).
موارد پراکنده (جهش جدید) حدود یک سوم موارد را تشکیل میدهند و بدون سابقه خانوادگی نیز رخ میدهند. در موارد پراکنده، احتمال سندرم WAGR وجود دارد، بنابراین آزمایش ژنتیک و غربالگری تومور ویلمز با سونوگرافی شکم مهم است.
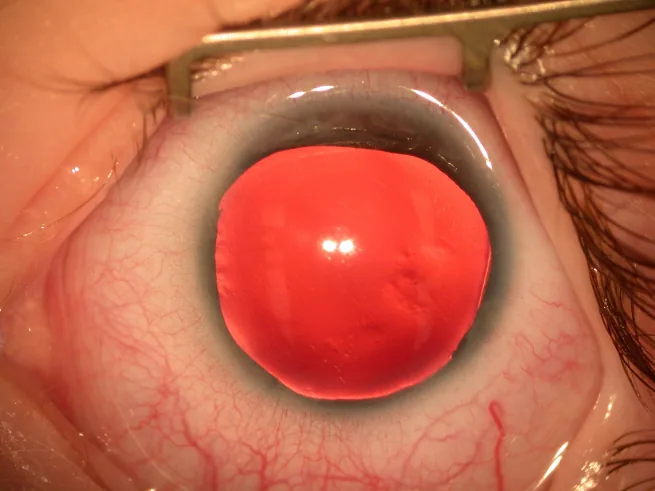
بیشتر موارد آنیریدیا در بدو تولد با ناهنجاری عنبیه و مردمک یا در دوران نوزادی با نیستاگموس تشخیص داده میشوند.
فنوتیپ بین خانوادهها و حتی درون یک خانواده متفاوت است، اما تفاوت بین چشم راست و چپ معمولاً اندک است.
علت اصلی هیپوپلازی فووئا است و حدت بینایی اصلاحشده اغلب حدود 0.1 تا 0.2 است. در صورت همراهی با هیپوپلازی ماکولا، پیشآگهی بینایی به ویژه ضعیف است. اصلاح عیوب انکساری و مراقبتهای کمبینایی از دوران نوزادی برای رشد بینایی مهم است.
PAX6 علاوه بر بافت چشم در سیستم عصبی مرکزی، جزایر لانگرهانس پانکراس و اپیتلیوم بویایی نیز بیان میشود، بنابراین ممکن است عوارض خارج چشمی زیر دیده شود 8).
عوامل مهم تعیینکننده بینایی عبارتند از: گلوکوم، هیپوپلازی ماکولا، نیستاگموس، کراتوپاتی، آب مروارید و ناهنجاری عنبیه. از آنجایی که آسیب میدان بینایی و کاهش بینایی ناشی از گلوکوم غیرقابل برگشت است، مدیریت فشار داخل چشم در پیگیری از اهمیت بالایی برخوردار است8).
اکثر موارد آنیریدی مادرزادی ناشی از جهشهای هتروزیگوت در ژن PAX6 واقع در بازوی کوتاه کروموزوم ۱۱ (11p13) است. مکانیسم اصلی بیماری، هاپلوناکافی PAX6 میباشد1).
ژن PAX6 یک ژن کنترلکننده اصلی در تشکیل چشم است و نقش مهمی در رشد چشم، لوله عصبی، پیاز بویایی و پانکراس ایفا میکند. برای رشد طبیعی چشم دو نسخه از PAX6 مورد نیاز است و از دست دادن عملکرد یک نسخه به تنهایی باعث بروز آنیریدی میشود1).
در یک مطالعه کوهورت بر روی بیماران چینی، جهشهای عامل بیماری در ۹۶.۹٪ موارد در ژن PAX6 شناسایی شده است1). در آنیریدی کلاسیک، جهشهایی که باعث تخریب mRNA وابسته به کدون بیمعنی (NMD) میشوند یا حذفهای بزرگ در ۹۶٪ موارد یافت میشوند1).
از نظر آسیبشناسی، عضلات صاف به جز ریشه عنبیه از بین رفته و زاویه اتاق قدامی دچار ناهنجاری رشدی میشود. ناهنجاری عملکردی سلولهای بنیادی اپیتلیوم قرنیه مشاهده میشود که منجر به ناهنجاری در اپیتلیوم و غشای بومن و تشکیل پانوس عروقی میگردد.
توزیع جهشهای PAX6 که باعث فنوتیپ آنیریدی میشوند در زیر نشان داده شده است.
| نوع جهش | فراوانی |
|---|---|
| جهش بیمعنی | حدود ۳۹٪ |
| جهش تغییر چارچوب | حدود ۲۵٪ |
| جهش پیرایش | حدود ۱۳٪ |
| جهش نادرست (میسنس) | حدود ۱۲٪ |
جهشهای ران-آن (جهشهای طویلکننده C-ترمینال) حدود ۵٪ را تشکیل میدهند و در آن کدون پایان به یک کدون ترجمه تبدیل میشود و پروتئین PAX6 به طور غیرطبیعی طویل تولید میشود 6). جهشهای طویلکننده C-ترمینال اغلب با هیپوپلازی شدید عنبیه و اختلال شدید بینایی همراه هستند 1)6).
جهشهای ژنی عمدتاً از نوع جهشهای PTC هستند و جهشهای نادرست (میسنس) نیز گزارش شدهاند 7). در مورد usefulness آزمایش ژنتیکی، با توالییابی سنگر یا NGS، نزدیک به ۸۵٪ از موارد آنیریدیای ایزوله دارای جهش تشخیص داده میشوند. علاوه بر این، با MLPA یا CMA، حذفهای درون ژنی PAX6 یا ناحیه تنظیمی سیس نزدیک به ۱۵٪ موارد تشخیص داده میشود 8).
Wang (2023) یک جهش جدید تغییر چارچوب c.640_646del (p.R214Pfs*28) را شناسایی کرد و موردی را گزارش داد که با فقدان کامل عنبیه، هیپوپلازی فووئا، جابجایی عدسی و جداشدگی شبکیه همراه بود 1).
Ratna و همکاران (2022) در یک خانواده هندی جهش ران-آن c.1268A>T (p.*423L) را شناسایی کردند. افراد مبتلا آنیریدی کامل، نیستاگموس، هیپوپلازی فووئا، AAK، سابلوکساسیون فوقانی عدسی، نزدیکبینی شدید و آتروفی عصب بینایی را نشان دادند که یک فنوتیپ شدید ناشی از جهش طویلکننده C-ترمینال است 6).
در آنیریدیای پراکنده، حذف بزرگ شامل ژن WT1 علاوه بر PAX6 باعث سندرم WAGR میشود. خطر تومور ویلمز در صورت حذف WT1 تا ۵۰٪ است 1). در صورت مشکوک بودن به سندرم WAGR، آزمایش ژنتیکی برای تأیید حذف PAX6 و WT1 انجام میشود که امکان ارزیابی خطر تومور ویلمز و پیگیری تأخیر رشدی را فراهم میکند 8). ارزیابی ناحیه WT1 با آزمایش ژنتیکی ضروری است و ۳۰٪ موارد پراکنده تا سن ۵ سالگی به تومور ویلمز مبتلا میشوند. از آنجا که ژن WT1 در نزدیکی PAX6 قرار دارد، حذف بازوی کوتاه کروموزوم ۱۱ (حذف 11p13) که هر دو را شامل میشود، باعث همراهی آنیریدیا با تومور ویلمز میشود.
سندرم گیلسپی در اثر جهشهای هتروزیگوت غالب منفی یا جهشهای دو آللی در ژن ITPR1 ایجاد میشود 3). تاکنون ۳۷ مورد با تشخیص مولکولی تأیید شده گزارش شده است و باقیمانده Gly2554 به عنوان یک نقطه داغ شناخته میشود 3).
بر اساس معیارهای تشخیص آنیریدیا (2020)، تشخیص با معیارهای زیر تأیید میشود7).
A. علائم
B. یافتههای آزمایشگاهی
C. بیماریهای قابل افتراق
E. آزمایش ژنتیکی: جهش بیماریزا در ژن PAX6 یا حذف ناحیه 11p13
ردهبندی تشخیصی7):
طبقهبندی شدت برای تأیید بیماری نادر به چهار درجه زیر تعریف شده است7).
| شدت | تعریف |
|---|---|
| درجه I | درگیری یک چشم، چشم دیگر سالم |
| درجه II | درگیری هر دو چشم، بهترین دید اصلاحشده 0.3 یا بیشتر |
| درجه III | درگیری هر دو چشم، بهترین دید اصلاحشده 0.1 یا بیشتر و کمتر از 0.3 |
| درجه IV | درگیری هر دو چشم، بهترین دید اصلاحشده کمتر از 0.1 |
حتی در درجه I تا III، در صورت وجود تنگی میدان بینایی ناشی از گلوکوم و غیره (میدان بینایی باقیمانده مرکزی 20 درجه یا کمتر با هدف Goldmann I/4)، شدت یک درجه افزایش مییابد. شدت درجه III یا بالاتر واجد شرایط دریافت کمک هزینه پزشکی است7).
تشخیص بالینی با تأیید فقدان یا ناقصبودن عنبیه با استفاده از میکروسکوپ اسلیت لامپ آسان است. ارزیابی بافت باقیمانده عنبیه با گونیوسکوپی و میکروسکوپ اولتراسوند بیومیکروسکوپی انجام میشود. همچنین ناهنجاریهای رشدی زاویه اتاق قدامی بررسی میشود.
عوارض چشمی زیر به طور سیستماتیک ارزیابی میشوند:
مهمترین هدف در ارزیابی ژنتیکی آنیریدیا، تأیید این است که آیا حذف PAX6 تا ژن WT1 گسترش یافته است یا خیر 1). با استفاده از توالییابی کامل اگزوم یا روش MLPA، جهشها و حذفهای ناحیه PAX6 و WT1 ارزیابی میشوند 1)2).
در آنیریدیای پراکنده، ارزیابی خطر تومور ویلمز ناشی از حذف ژن WT1 مستقیماً با پیشآگهی حیاتی مرتبط است 1). حتی در موارد خانوادگی نیز به دلیل تنوع فنوتیپی، تشخیص قطعی با آزمایش ژنتیکی و مشاوره ژنتیک توصیه میشود.
درمان قطعی برای آنیریدیا وجود ندارد. مراقبت از دید کم برای استفاده حداکثری از بینایی باقیمانده و درمان جداگانه هر عارضه، محور مدیریت است. در راهنمای بالینی (2021)، توصیههایی بر اساس 6 سؤال بالینی ارائه شده است 8).
CQ1: پیوند قرنیه برای کدورت پارانشیم قرنیه بهطور ضعیف توصیه نمیشود 8).
اگرچه پیوند قرنیه ممکن است در کوتاهمدت بهبود بینایی ایجاد کند، اما به دلیل عوارضی مانند هیپوپلازی ماکولا، بهبود محدود است. در بلندمدت، پیشرفت گلوکوم و نارسایی پیوند منجر به پیشآگهی ضعیف بینایی میشود.
CQ2: درمان جراحی برای نارسایی سلولهای بنیادی اپیتلیال قرنیه به طور ضعیف توصیه میشود 8).
CQ3: جراحی آب مروارید به طور ضعیف توصیه میشود 8).
آب مروارید در 50-85% موارد تا سن 20 سالگی ایجاد میشود. جراحی بر اساس شدت کدورت و فوتوفوبیا برنامهریزی میشود. گزارش شده است که در 66-100% موارد جراحی، بینایی بهبود مییابد، اما نکات زیر باید مورد توجه قرار گیرند:
به دلیل ضعف زینول، کاشت لنز داخل چشمی با احتیاط انجام میشود.
هو و همکاران (۲۰۲۴) در دو مورد آنیریدی مادرزادی همراه با AAK شدید، فیکوامولسیفیکاسیون با کمک روشنایی معکوس لوستر انجام دادند. با وجود کدورت قرنیه که تجسم حین عمل را دشوار میکرد، روشنایی از پشت امکان تجسم واضح عدسی و کپسول قدامی را فراهم کرد و دید اصلاحشده سه هفته پس از عمل به ترتیب به ۲۰/۲۰۰ و ۲۰/۱۰۰۰ بهبود یافت 4).
CQ4: درمان گلوکوم به شدت توصیه میشود 8).
پس از شروع گلوکوم، مدیریت بر اساس الگوریتم پنج مرحلهای زیر انجام میشود.
درمان دارویی: بتا بلوکرها، محرکهای سمپاتیک و داروهای مرتبط با پروستاگلاندین (PG) مؤثر هستند. بریمونیدین (محرک گیرنده آلفا آدرنرژیک) در نوزادان به دلیل خطر سرکوب سیستم عصبی مرکزی در کودکان زیر ۲ سال منع مصرف دارد. در صورت نگرانی از آسیب اپیتلیال قرنیه، از فرآوردههای بدون مواد نگهدارنده استفاده شود.
جراحی بازسازی مسیر خروجی (گونیوتومی/ترابکولوتومی): به عنوان جراحی اولیه توصیه میشود 16). گزارشهایی از گونیوتومی پیشگیرانه نیز وجود دارد. با این حال، در مواردی که عنبیه باقیمانده ترابکولوم را پوشانده است، ممکن است بیاثر باشد.
جراحی فیلتراسیون (ترابکولکتومی): تنها گزارشهای محدود و کوتاهمدت وجود دارد. نتایج در چشم کودکان معمولاً ضعیف است و فیستول پس از عمل در حدود ۲۵٪ موارد رخ میدهد 13). همچنین گزارشهایی از گلوکوم بدخیم پس از عمل وجود دارد.
جراحی ایمپلنت گلوکوم (جراحی شانت لولهای): دستگاههای Baerveldt و Ahmed قابل استفاده هستند. در چشمهای دارای عدسی طبیعی، قرار دادن لوله به صورت مماسی به جای جهت مرکزی قرنیه توصیه میشود. کنترل خوب فشار داخل چشم قابل انتظار است.
سیکلوکواگولاسیون: آخرین راهکار. گزارش شده است که کرایوکواگولاسیون جسم مژگانی در بسیاری از موارد منجر به فیستول میشود. به دلیل هیپوپلازی جسم مژگانی، خطر فیستول نسبت به چشم سالم بیشتر است.
از آنجایی که ناهنجاریهای رشدی زاویه در پسزمینه وجود دارد، رویکرد متفاوتی نسبت به گلوکوم زاویه باز معمولی لازم است. در مرحله اول، جراحی بازسازی مسیر خروجی انتخاب میشود و سپس جراحی شنت لوله گزینه مناسبی است. بریمونیدین در کودکان زیر ۲ سال منع مصرف دارد و استفاده از داروهای ضد متابولیت ممکن است AAK را تشدید کند، بنابراین قضاوت دقیق لازم است 8).
CQ5: انجام مراقبت از کمبینایی به شدت توصیه میشود 8).
اصلاح عیوب انکساری اساسی است و میزان همراهی نزدیکبینی ۶۴٪ یا بیشتر گزارش شده است.
CQ6: درمان حساسیت به نور به شدت توصیه میشود 8).
بیشتر بیماران میتوانند در مدارس عادی تحصیل کنند، اما به کمکهایی مانند کتابهای درسی بزرگنما، تبلت و پایه کتاب نیاز دارند. گزینههای دیگر شامل حضور در کلاسهای کمبینایان، مشاوره تربیتی و تحصیلی در مدارس نابینایان یا مدارس ویژه بینایی است.
از آوریل 2017، این بیماری به عنوان یک بیماری نادر تعیین شده است، بنابراین حتی اگر فرد کارت معلولیت نداشته باشد، در صورت شدت درجه III یا بالاتر، مشمول کمک هزینه پزشکی و کمک هزینه وسایل کمکی میشود 7). وسایل کمکی شامل عینک طبی، عینک ضد نور، لنز تماسی (از جمله با عنبیه مصنوعی)، عینک کمبینایی، عصای ایمنی برای نابینایان و چشم مصنوعی است.
PAX6 یک DNA ژنومی 22 کیلوبازی شامل 14 اگزون است و 422 اسید آمینه را کد میکند 1). دارای دو دامنه اتصال به DNA (دامنه جفتی و هومئودومین جفتی) است و دامنه PST (غنی از پرولین، سرین و ترئونین) در انتهای C به عنوان فعالکننده رونویسی عمل میکند.
PAX6 تکثیر، تمایز، مهاجرت و چسبندگی سلولها را تنظیم میکند و اهداف آن شامل خود PAX6 و همچنین ژنهای کدکننده کریستالین عدسی و کراتین قرنیه است. بیان آن در شبکیه، عدسی و قرنیه بزرگسالان ادامه مییابد. ژن PAX6 یکی از ژنهای کنترل اصلی است که تمایز اندامها را در دوره جنینی هدایت میکند.
بیشتر جهشهای PAX6 از طریق تخریب mRNA وابسته به جهش بیمعنی (NMD) باعث نارسایی هاپلوئیدی میشوند 1). جهشهایی که کدون توقف زودرس (PTC) ایجاد میکنند (جهشهای بیمعنی، جهشهای تغییر چارچوب و بیشتر جهشهای پیرایشی) منجر به فنوتیپ کلاسیک آنیریدیا میشوند.
از سوی دیگر، اگر PTC در اگزون نهایی یا در 50 جفت باز انتهایی اگزون ماقبل آخر قرار گیرد، از NMD فرار کرده و پروتئین کوتاه شده ترجمه میشود که ممکن است منجر به فنوتیپ شدید شود 1).
یک مورد نادر از همراهی جهش بیمعنی PAX6 c.282C>A (p.Cys94*) و تریزومی 21 در یک بیمار گزارش شده است. جهش PAX6 به صورت de novo رخ داده و منجر به آنیریدیا کامل دوطرفه، گلوکوم مادرزادی، AAK و هیپوپلازی فووئا شده است 2).
اگرچه همبستگی واضح ژنوتیپ-فنوتیپ ثابت نشده است، برخی تمایلات شناخته شده است 1).
در سری گونیوسکوپی گرانت و والتون نشان داده شد که در مراحل اولیه، استرومای عنبیه به سمت جلو روی ترابکولوم کشیده شده و اتصالات چسبندهای ایجاد میکند، سپس به تدریج به صورت ورقهای درآمده و نهایتاً منجر به انسداد زاویه میشود 14). این مکانیسم عامل اصلی ایجاد گلوکوم است. از نظر پاتولوژیک، فقدان عضله صاف با حفظ ریشه عنبیه و ناهنجاری رشدی زاویه زمینهساز است.
AAK عمدتاً ناشی از کمبود سلولهای بنیادی لیمبوس (LSCD) است، اما تمایز غیرطبیعی اپیتلیوم قرنیه، چسبندگی غیرطبیعی، نفوذ سلولهای ملتحمه و تولید ناکافی اشک نیز نقش دارند. کمبود ماتریکس متالوپروتئیناز ۹ (MMP-9) که توسط PAX6 تنظیم میشود، منجر به تجمع فیبرین و نفوذ سلولهای التهابی میشود و به دلیل اختلال در آرایش کلاژن استروما، شفافیت از بین میرود.
AAK به ۵ مرحله تقسیم میشود. در مرحله I فقط اپیتلیوم محیطی غیرطبیعی است، در مرحله II تغییرات اپیتلیال گریز از مرکز (بدون رسیدن به مرکز) دیده میشود، در مرحله III تغییرات اپیتلیال قرنیه مرکزی و عروق جدید سطحی محیطی، در مرحله IV عروق جدید سطحی تمام قرنیه، و در مرحله V ناهنجاری اپیتلیال تمام قرنیه و اسکار عمقی استروما مشاهده میشود 10).
بین وضعیت جهش PAX6 و پیشرفت AAK ارتباط وجود دارد. در بیماران دارای جهشهای PTC و طویلکننده C ترمینال، AAK با افزایش سن پیشرفت میکند، در حالی که در سایر انواع جهش ممکن است کراتوپاتی غیرپیشرونده دیده شود 11).
سندرم گیلزپی ناشی از جهش در ژن ITPR1 است 3). ITPR1 عضوی از خانواده گیرندههای IP3 است که کانالهای آزادکننده Ca²⁺ را تشکیل میدهد و در شبکه آندوپلاسمی موضعی دارد. جهشهای غالب منفی بر تشکیل و نگهداری عضله اسفنکتر عنبیه تأثیر میگذارند و منجر به هیپوپلازی اختصاصی عنبیه اطراف مردمک و میدریاز ثابت میشوند.
در مرور ادبیات سندرم گیلزپی توسط Ciaccio و همکاران (۲۰۲۴)، تجزیه و تحلیل ۳۳ مورد تأیید شده مولکولی نشان داد که تأخیر حرکتی وجود دارد اما با گذشت زمان بهبود مییابد، ناتوانی ذهنی در همه موارد دیده نمیشود و ۱۷٪ هوش طبیعی دارند، و علائم عصبی غیرپیشرونده هستند 3).
با گسترش تکنیک توالییابی کامل اگزوم، شناسایی جهشهای جدید PAX6 ادامه دارد. تا سال ۲۰۱۸، ۴۹۱ جهش در پایگاه داده جهشهای انسانی PAX6 ثبت شده بود و از آن زمان تاکنون حدود ۲۵۰ جهش جدید گزارش شده است 1). جهشهای ناحیه غیرکدکننده نیز به عنوان علت آنیریدیا شناسایی میشوند و انتظار میرود مواردی که با آزمایشهای قبلی قابل تشخیص نبودند، روشن شوند 9).
در جراحی آب مروارید در موارد همراه با AAK شدید، تکنیک تجسم با کمک نور پسزمینه لوستر (Chandelier retroillumination) مفید است 4). این روش امکان فیکوامولسیفیکاسیون ایمن را حتی در بیماران با AAK درجه ۳ تا ۴ فراهم کرده و بهبود بینایی پس از عمل حاصل میشود.
مشخص شده است که الگوی پیشرفت AAK بسته به نوع جهش PAX6 متفاوت است. با کاهش هزینه آزمایش ژنتیک، پیشبینی سیر بالینی بر اساس نوع جهش و مداخله زودهنگام به گزینهای عملی تبدیل شده است.
در موارد همراهی آنیریدیا و تریزومی ۲۱، مواردی با سیر نسبتاً خفیف علی رغم وجود هر دو بیماری گزارش شده است 2). درک تأثیر همزمانی چند اختلال ژنتیکی در یک بیمار بر فنوتیپ، میتواند دانش مهمی برای پزشکی فردمحور در آینده فراهم کند.
کاربرد داروی read-through (آتالورن) برای جهشهای نوع PTC در آنیریدیا در سطح تحقیقات پایه بررسی میشود 8). در مورد ژن درمانی PAX6، تحقیقات پایه با استفاده از ناقل AAV-PAX6 برای جایگزینی ژن در مدل موش با جهش Sey در حال انجام است. انتظار میرود این تحقیقات به کارآزمایی بالینی منجر شود.
کارآزمایی بالینی پیوند ورقه سلولهای اپیتلیال قرنیه مشتق از سلولهای iPS در داخل و خارج از کشور در حال انجام است و به عنوان یک درمان جدید برای AAK مورد توجه است 8). در مورد عنبیه مصنوعی (مانند CustomFlex Artificial Iris)، تجربه استفاده در خارج از کشور انباشته شده است. لنزهای تماسی با عنبیه مصنوعی به عنوان وسیله کمکی تحت پوشش بیمه هستند.
در راهنمای بالینی (۲۰۲۱)، جمعآوری دادههای رجیستری در مقیاس بزرگ در ژاپن برای درک وضعیت واقعی و بازبینی راهنما بر اساس بهبود کیفیت شواهد، به عنوان وظایف مهم آینده تعیین شده است 8). پیشبینی پیشرفت AAK بر اساس جهش ژنتیکی فردی و بهینهسازی مداخله زودهنگام مورد انتظار است.