هورمون رشد
شیوع: حدود ۷۰٪ از بیماران ONH به آن نیاز دارند.
اندیکاسیون: در صورت تأیید کمبود هورمون رشد شروع میشود.

هیپوپلازی عصب بینایی (ONH) شایعترین ناهنجاری مادرزادی عصب بینایی است که با کاهش تعداد آکسونهای عصب بینایی مشخص میشود. میتواند یکطرفه یا دوطرفه باشد و ممکن است با نقص ساختارهای خط وسط مغز همراه باشد.
در سال 1877، بریر اولین توصیف بافتشناسی را ارائه داد و در سال 1941، ریوز توصیف بالینی را انجام داد. در سال 1956، د مورسیه همراهی با فقدان سپتوم پلوسیدوم را گزارش کرد که به سندرم د مورسیه (دیسپلازی سپتو-اپتیک، SOD) معروف شد. در سال 1970، هویت و همکاران تصویر بالینی دقیقی را گزارش کردند و آگاهی از این بیماری گسترش یافت.
SOD زمانی تشخیص داده میشود که دو یا بیشتر از سه علامت زیر وجود داشته باشد3)6):
شیوع SOD حدود 1 در 10,000 تولد تخمین زده میشود2)6). از نظر اپیدمیولوژیک، سومین علت شایع اختلال بینایی در کودکان زیر 3 سال است. در انگلستان 10.9 در 100,000 نفر و در سوئد 17.3 در 100,000 نفر گزارش شده است.
در یک مطالعه از ۱۶ مورد در دانشگاه نیگاتا ژاپن، میانگین سن در اولین مراجعه ۲.۴ سال، ۱۲ نفر از ۱۶ مورد (۷۵٪) زن و ۱۱ نفر از ۱۶ مورد (۶۹٪) دوطرفه بودند1).
نوع شدید آن آپلازی عصب بینایی (optic nerve aplasia) نام دارد. در این حالت، پاپی و عروق شبکیه به طور کامل وجود ندارند و بیمار درک نور ندارد.
هیپوپلازی سگمان فوقانی عصب بینایی (superior segmental optic hypoplasia; SSOH) نوع خاصی است که در آن فقط فیبرهای عصبی فوقانی هیپوپلاستیک هستند و ارتباط آن با دیابت مادری ذکر شده است. شیوع آن در ژاپن حدود ۰.۳٪ گزارش شده است. تفاوت جنسیتی ندارد.
ONH به ناهنجاری مورفولوژیک مجزای عصب بینایی اشاره دارد. SOD سندرمی است که حداقل دو مورد از سه علامت ONH، نارسایی هیپوفیز و ناهنجاری ساختاری مغز میانی را شامل میشود و ONH یکی از اجزای تشکیلدهنده SOD است. گزارش شده است که حدود ۳۷.۵٪ از بیماران ONH معیارهای تشخیصی SOD را دارند1).
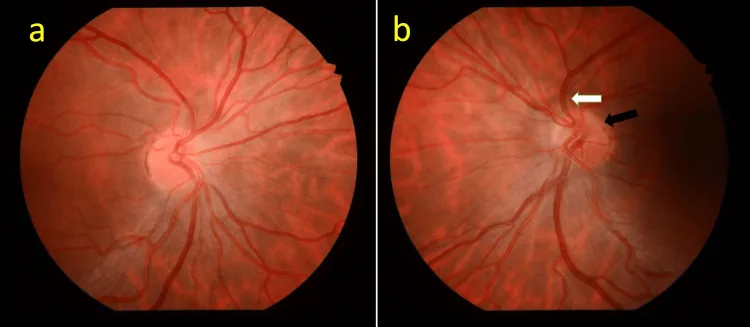
دید در ONH از طبیعی تا عدم درک نور متغیر است. بسیاری از موارد دید کمتر از ۰.۱ دارند و دید به تراکم دسته پاپیلوماکولار بستگی دارد. هیپوپلازی عصب بینایی از این نظر با سایر ناهنجاریهای مادرزادی پاپی متفاوت است؛ حتی اگر ماکولا تشکیل شده باشد، درجه توسعه دسته عصبی پاپیلوماکولار متغیر است، بنابراین مواردی از دید ۱.۰ تا دید بسیار پایین دیده میشود.
بر اساس دادههای ژاپنی، ضعف بینایی در 11 مورد از 16 مورد (69٪)، استرابیسم در 8 مورد از 16 مورد (50٪) و نیستاگموس در 5 مورد از 16 مورد (31٪) مشاهده شد1).
یافتههای مشخصی با افتالموسکوپی مشاهده میشود.
فراوانی یافتههای اصلی چشمی و عوارض سیستمیک در زیر نشان داده شده است.
| یافته | فراوانی |
|---|---|
| ناهنجاریهای ساختاری CNS | حدود 90٪ |
| اختلالات رشد عصبی | حدود 70٪ |
| اختلال عملکرد هیپوتالاموس (دوچشمی) | 81% |
| اختلال عملکرد هیپوتالاموس (یکچشمی) | 69% |
| تأخیر رشد (دوچشمی) | 78% |
حتی در موارد یکچشمی، اختلال عملکرد هیپوتالاموس در 69% موارد دیده میشود و در 18.2% از بیماران بدون علامت نیز ناهنجاری مغزی وجود دارد1). در موارد یکچشنی نیز MRI و غربالگری غدد درونریز ضروری است.
پاتولوژی ONH ناهنجاری در رشد سلولهای گانگلیونی شبکیه (RGC) و رشتههای عصبی است. دو فرضیه وجود دارد: فرضیه ناهنجاری رشدی و فرضیه دژنراسیون رتروگرید. همچنین فرضیه ایسکمی کیاسمای بینایی و عصب بینایی ناشی از آسیب عروقی شریان مغزی قدامی مطرح شده است.
اکثر موارد پراکنده هستند2)3).
جهشهای ژنتیکی زیر ممکن است دخیل باشند.
تشخیص ONH بر اساس یافتههای افتالموسکوپی است و با تصویربرداری تشخیصی و غربالگری غدد درونریز ترکیب میشود.
تشخیص علامت حلقه دوتایی اولین گام در تشخیص است. نسبت DM/DD 3 یا بیشتر (3.2 یا بیشتر برای پاپیل کوچک) به عنوان معیار در نظر گرفته میشود.
در بررسی بیماران ژاپنی، ناهنجاری مغزی در 43.8% و SOD در 37.5% مشاهده شد. قابل توجه این است که حتی در افراد بدون علامت، 18.2% ناهنجاری مغزی داشتند1). علاوه بر این، در 2 مورد از 3 موردی که کم کاری هیپوفیز نشان دادند، MRI مورفولوژی هیپوفیز طبیعی بود1).
آزمایشات زیر برای همه بیماران ONH توصیه می شود:
تشخیص افتراقی با بیماری های زیر ضروری است:
بله، ممکن است. در مطالعهای بر روی بیماران ژاپنی، از ۳ مورد با کاهش عملکرد هیپوفیز، ۲ مورد MRI طبیعی داشتند1). صرفنظر از نتیجه MRI، غربالگری غدد درونریز باید برای همه بیماران انجام شود.
هیچ درمان قطعی برای خود ONH وجود ندارد. مدیریت اصلی بر بهینهسازی عملکرد بینایی و رسیدگی به عوارض سیستمیک (بهویژه اختلالات غدد درونریز) متمرکز است. همکاری یک تیم چندتخصصی (چشمپزشکی، غدد، اطفال، نورولوژی، توانبخشی) ضروری است. ارزیابی رشد هر شش ماه و ارزیابی بینایی سالیانه توصیه میشود.
هورمون رشد
شیوع: حدود ۷۰٪ از بیماران ONH به آن نیاز دارند.
اندیکاسیون: در صورت تأیید کمبود هورمون رشد شروع میشود.
هورمون تیروئید
شیوع: حدود ۴۳٪ نیاز دارند.
اندیکاسیون: در صورت غیرطبیعی بودن TSH و FT4 شروع میشود.
هورمون کورتیکواستروئید
فراوانی: در حدود 27% موارد نیاز است.
توجه: نارسایی آدرنال میتواند در زمان استرس کشنده باشد. آموزش دوز استرس (افزایش دوز در هنگام تب یا جراحی) ضروری است5).
هورمون ضدادراری
فراوانی: حدود 5% با دیابت بیمزه عارضه دارند.
توجه: اصلاح سریع سدیم میتواند باعث تشنج شود. سرعت اصلاح باید کمتر از 0.5 mEq/L در ساعت باشد4).
در موارد مدیریت بزرگسالان، رژیمهای جایگزینی مانند لووتیروکسین 137 میکروگرم، دسموپرسین، و هیدروکورتیزون 10 میلیگرم (صبح) / 7.5 میلیگرم (عصر) گزارش شده است2).
هیپوپلازی عصب بینایی به خودی خود، در صورت عدم ابتلا به گلوکوم، غیرپیشرونده است. در صورت عدم وجود گلوکوم، باید از تجویز بیمورد قطرههای چشمی یا جراحی برای کاهش فشار چشم خودداری کرد. با این حال، اختلالات غدد درونریز ممکن است به مرور زمان ظاهر یا بدتر شوند و پیگیری طولانیمدت ضروری است1). تشخیص زودهنگام و شروع درمان جایگزینی هورمونی تا سن 3 سالگی در موارد لازم میتواند از عوارض جلوگیری کند، بنابراین حتی در موارد یکطرفه نیز مهم است که این بیماری را در نظر داشت و از دست نداد.
هیپوپلازی عصب بینایی به خودی خود غیرپیشرونده است و در صورت عدم ابتلا به گلوکوم، بینایی معمولاً پایدار است. با این حال، اختلالات غدد درونریز ممکن است در سالهای بعد ظاهر شوند، بنابراین ادامه ارزیابی دورهای سیستمیک مهم است.
ماهیت ONH کاهش لایه فیبرهای عصبی شبکیه (RNFL) و سلولهای گانگلیونی است و تأثیر کمی بر لایههای خارجی شبکیه دارد. دو فرضیه اصلی برای مکانیسم بروز آن وجود دارد.
همچنین فرضیهای وجود دارد که ایسکمی ناحیه کیاسمای بینایی و عصب بینایی ناشی از اختلال عروقی شریان مغزی قدامی در این امر نقش دارد.
اختلال عملکرد هیپوتالاموس در ۶۹٪ موارد ONH یکطرفه و ۸۱٪ موارد دوطرفه مشاهده میشود. غده هیپوفیز و عصب بینایی از نظر جنینشناسی نزدیک به هم هستند و تصور میشود که یک اختلال رشدی یکسان بر هر دو تأثیر میگذارد.
تأخیر رشدی در ۷۵٪ کل موارد مشاهده میشود و در موارد دوطرفه (۷۸٪) بیشتر از یکطرفه (۳۹٪) است.
SOD plus وضعیتی است که علاوه بر SOD کلاسیک، ناهنجاریهای قشر مغز (مانند پلیمیکروژیری، شیارنگاری مغز) را نیز شامل میشود و گزارش شده است که بیشتر از SOD کلاسیک دیده میشود7). پیشآگهی رشد عصبی بدتر است و خطر تشنج نیز بالاتر است.
کارآزمایی بالینی (NCT06760546) برای setmelanotide، آگونیست گیرنده ملانوکورتین ۴ (MC4R)، به عنوان درمان دارویی برای چاقی مرتبط با SOD در حال انجام است2). چاقی هیپوتالاموسی به طور قابل توجهی کیفیت زندگی بیماران SOD را کاهش میدهد، بنابراین این دارو به عنوان یک گزینه درمانی جدید مورد توجه است.
در نوزادان مبتلا به SOD که با قند خون طبیعی تشخیص داده شدهاند، درمان با تستوسترون (25 میلیگرم تزریق عضلانی، ماهی یک بار به مدت 3 ماه) برای مدیریت میکروپنیس و کریپتورکیدیسم و همچنین درمان با FSH نوترکیب گزارش شده است5). این موارد نشاندهنده امکان مداخله زودهنگام جایگزینی هورمونی هستند، اما اثربخشی و ایمنی طولانیمدت هنوز ثابت نشده است.