視神經發育不全(ONH)是最常見的先天性視神經 異常,其特徵是視神經 軸突數量減少。
可為單眼或雙眼,常伴隨結構性中樞神經系統異常(約90%)和神經發育障礙(約70%)。
中隔視神經發育不全(SOD,德莫西症候群)的診斷需滿足以下三項中的至少兩項:ONH、垂體功能低下、透明中隔缺損 。
檢眼鏡下的雙環徵是診斷線索,MRI腦結構評估和內分泌篩查必不可少。
視力 範圍從正常到無光感,取決於乳頭黃斑 束的密度。內分泌異常可能在後期顯現,需要長期補充生長激素、甲狀腺激素、腎上腺皮質激素等。
視神經發育不全本身在未併發青光眼 時是非進行性的,但多學科協作的長期追蹤很重要。
視神經發育不全(ONH)是最常見的先天性視神經 異常,其特徵是視神經 軸突數量減少。可為單眼或雙眼,可能伴有中線腦結構缺陷。
Briere於1877年首次進行組織學描述,Reeves於1941年進行臨床描述。1956年,de Morsier報告了其與透明中隔缺損 的關聯,從而稱為德莫西症候群(中隔視神經發育不全,SOD)。1970年,Hoyt等人報告了詳細的臨床特徵,提高了對該病的認識。
SOD的診斷需滿足以下三項中的至少兩項3) 6) :
ONH(單眼或雙眼)
垂體功能低下
中線腦結構異常(透明中隔缺損 、胼胝體發育不全等)
SOD的盛行率估計約為每10,000名新生兒中1例2) 6) 。流行病學上,它是3歲以下兒童視力 障礙的第三大常見原因。據報導,英格蘭為每10萬人10.9例,瑞典為17.3例。
在日本新潟大學對16例病例的研究中,初診年齡中位數為2.4歲,女性佔12/16例(75%),雙側性佔11/16例(69%)1) 。
重症型為視神經 缺如(optic nerve aplasia)。視乳頭和視網膜 血管完全缺失,無光感。
上方節段性視神經發育不全 (superior segmental optic hypoplasia; SSOH)是一種特殊類型,僅上方視神經 纖維發育不全,與母體糖尿病有關。日本報告的患病率約為0.3%。無性別差異。
Q
ONH和SOD有什麼不同?
A
ONH指視神經 單獨的形態異常。SOD是滿足ONH、垂體功能低下和正中腦結構異常三聯徵中兩項或以上的症候群,ONH是SOD的組成部分之一。據報告,約37.5%的ONH患者符合SOD的診斷標準1) 。
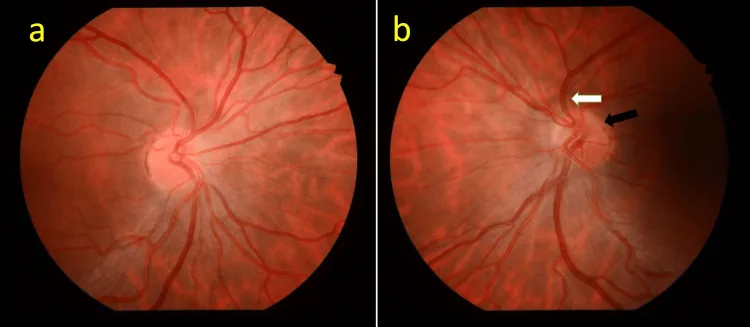
視神經發育不全的眼底照片。左眼顯示小視乳頭和乳頭周圍的雙環樣暈輪。 Mujahid M, et al. Superior Segmental Optic Nerve Hypoplasia: A Case Report and Literature Review. Cureus. 2026. Figure 1. PM
CI D: PMC12906824. License: CC BY.
眼底照片對比圖像,左面板顯示視乳頭較小,乳頭周圍有雙環樣暈輪。顯示了視神經發育不全,尤其是節段型中出現的乳頭縮小和雙環樣暈輪。
ONH的視力 範圍從正常到無光感。多數在0.1以下,視力 取決於乳頭黃斑 束的密度。視神經發育不全在這點上與其他乳頭先天異常不同,即使黃斑 形成,乳頭黃斑 神經纖維束的發育程度也有差異,因此視力 從保持1.0的病例到極低的病例範圍廣泛。
視力 下降視力 的病例。視野缺損 缺損 。在視力 相對較好的單眼或雙眼病例中,有時可檢測出雙顳側偏盲傾向。RAPD (相對性傳入性瞳孔 反應缺陷)眼球震顫 眼球震顫 或蹺蹺板樣眼球震顫 。斜視
在日本資料中,視力 不良佔11/16例(69%),斜視 佔8/16例(50%),眼震 佔5/16例(31%)1) 。
檢眼鏡檢查可見特徵性表現。
視神經 盤雙環徵 :在小視盤周圍可見淡色內環(鞏膜 篩板 )和色素外環(脈絡膜 色素層)的雙重環狀表現。這是本病的特徵性表現。由於神經纖維束減少導致視盤變小,原本應為視盤的區域呈環狀可見。DM/DD比值 :視盤中心凹距離(DM)與視盤直徑(DD)的比值。≥3可疑,≥4高度提示。≥3.2判定為小視盤。DD/DM比值<0.35為參考標準。視網膜 靜脈迂曲OCT 表現視網膜神經纖維層 (RNFL )、神經節細胞層(GCL)和內叢狀層(IPL)變薄。視網膜 血管
主要眼部表現和全身併發症的頻率如下所示。
表現 頻率 結構性中樞神經系統異常 約90% 神經發育障礙 約70% 下視丘功能障礙(雙眼) 81% 下視丘功能障礙(單眼) 69% 發展遲緩(雙眼) 78%
Q
單眼ONH也需要全身檢查嗎?
A
即使是單眼病例,下視丘功能障礙的發生率也達69%,無症狀患者中18.2%存在腦部異常1) 。單眼病例也必須進行MRI和內分泌篩查。
ONH的病理是視網膜神經節細胞 (RGC )和神經纖維的發育不全。存在兩種假說:發育異常假說和逆行性變性假說。也有假說認為前腦動脈血管障礙導致的視交叉 和視神經 缺血是病因。
大多數病例是散發的2) 3) 。
以下基因突變可能與之相關。
HESX1 :參與前腦和垂體發育。突變攜帶者佔所有SOD病例的不到1%7) 。PAX6 、SOX2 、OTX2 :參與眼和腦發育的轉錄因子。
年輕分娩(尤其是初產年齡較小)
母體糖尿病 :與SSOH關聯尤為密切早產
藥物暴露:苯妥英、奎寧、LSD、酒精
ONH的診斷基於檢眼鏡檢查結果,並結合影像學檢查和內分泌篩查。
確認雙環徵是診斷的第一步。DM/DD比值≥3(≥3.2為小視盤)可作為參考標準。
MRI :建議所有ONH患者進行。評估透明隔缺損 、胼胝體形態以及腦下垂體的大小和形態。
指向下徵 :視交叉 向下偏移的表現。是SOD的特徵性表現3) 。視交叉 的正常寬度為11.13–16.92 mm,視神經 橫截面積≤4.0 mm²判定為萎縮3) 。
OCT RNFL 厚度(視乳頭周圍視網膜神經纖維層 厚度)。可客觀定量變薄程度。
在日本患者的研究中,腦異常佔43.8%,SOD佔37.5%。值得注意的是,即使無症狀,仍有18.2%存在腦異常1) 。此外,在3例腦下垂體功能低下患者中,有2例MRI顯示腦下垂體形態正常1) 。
建議對所有ONH患者進行以下檢查:
皮質醇
TSH(甲狀腺刺激激素)、FT4(游離甲狀腺素)
IGF-1(胰島素樣生長因子-1)、IGFBP-3
LH(黃體生成激素)、FSH(濾泡刺激激素)
需要與以下疾病進行鑑別:
視神經萎縮 視神經 缺損 視盤凹陷 。牽牛花症候群 傾斜視 盤症候群 :視盤不對稱傾斜。青光眼 性視神經病變 RNFL 缺損 模式不同。如有可能,定期用OCT 測量RNFL 厚度以確認有無變化。
Q
即使MRI正常,也可能有內分泌異常嗎?
A
有可能。在日本患者的研究中,3例腦下垂體功能低下患者中有2例MRI表現正常1) 。無論MRI結果如何,所有患者都應進行內分泌篩檢。
ONH本身沒有根治性治療方法。管理的核心是優化視覺功能並處理全身併發症(尤其是內分泌異常)。多專科團隊(眼科、內分泌科、小兒科、神經科、復健科)的合作至關重要,建議每半年評估生長情況,每年評估視覺功能。
屈光 矯正屈光 不正很重要。如果存在眼球震顫 ,嘗試透過眼鏡或隱形眼鏡進行屈光 矯正。斜視手術 斜視 ,進行以後退術為主的斜視手術 。也可考慮針對眼球震顫 的眼外肌 手術。
生長激素
頻率 :約70%的ONH患者需要。
適應症 :確診生長激素分泌不足時開始。
甲狀腺激素
頻率 :約43%需要。
適應症 :TSH/FT4異常時開始補充。
腎上腺皮質激素
頻率 :約27%需要。
注意 :腎上腺功能不全在壓力時可能致命。必須指導壓力劑量(發燒或手術時增加劑量)5) 。
抗利尿激素
頻率 :約5%合併尿崩症。
注意 :快速矯正鈉可能導致抽搐。矯正速度應低於0.5 mEq/L/小時4) 。
在成人管理案例中,有報告使用甲狀腺素137 μg、去氨加壓素和氫化可的松10 mg(早上)/7.5 mg(傍晚)的補充方案2) 。
內分泌異常在嬰幼兒期可能無症狀,但隨著成長可能在以後顯現。長期定期評估是必需的1) 。
合併腎上腺功能不全時,在感染、外傷、手術等壓力情況下增加氫化可的松劑量(壓力劑量)可挽救生命5) 。
在尿崩症管理中,嚴格遵守高鈉血症的矯正速度。快速矯正可能導致抽搐和腦水腫4) 。
視神經發育不全本身是非進行性的,除非合併青光眼 。不合併青光眼 時,應避免為降低眼壓 而輕易使用眼藥水或手術治療。然而,內分泌異常可能隨時間出現或惡化,因此長期追蹤是必不可少的1) 。早期診斷並在必要時於3歲前開始激素替代治療可避免後遺症,因此即使是單眼病例,也應考慮本病並避免漏診。
Q
視力將來會惡化嗎?
A
視神經發育不全本身是非進行性的,不合併青光眼 時視力 通常穩定。但內分泌異常可能在以後出現,因此定期全身評估的持續進行很重要。
ONH的本質是視網膜神經纖維層 (RNFL )和神經節細胞的減少,對視網膜 外層影響較小。其發生機制主要有兩種假說。
發育異常假說 :胚胎期視網膜神經節細胞 的分化和遷移障礙導致視神經 軸突形成不足。逆行性變性假說 :中樞神經系統結構異常(如透明中隔缺損 、胼胝體缺損 等)引起的逆行性軸索變性。
也有假說認為前大腦動脈血管障礙導致的視交叉 和視神經 區域缺血可能參與其中。
下視丘功能障礙在單眼ONH中佔69%,雙眼ONH中佔81%。垂體和視神經 在發育上鄰近,同一發育障礙可能影響兩者。
發展遲緩在所有病例中佔75%,雙眼(78%)高於單眼(39%)。
SOD plus是指在典型SOD基礎上伴有皮質發育異常(如多小腦迴、裂腦症等)的病理狀態,有報告指出其比典型SOD更常見7) 。神經發育預後更差,癲癇合併風險也更高。
針對SOD相關肥胖的藥物療法,黑皮質素4受體(MC4R)促效劑setmelanotide的臨床試驗(NCT 06760546)正在進行中2) 。下視丘性肥胖顯著降低SOD患者的生活品質,因此作為一種新的治療選擇備受關注。
在診斷為正常血糖的SOD新生兒中,已有報告使用睪固酮療法(25mg肌肉注射,每月1次,共3個月)治療小陰莖和隱睪,以及嘗試重組FSH療法5) 。這些顯示早期內分泌介入的可能性,但長期有效性與安全性尚未確定。
Kiyokawa M, Ueki S, Hatase T, Hanyu T, Fukuchi T. The Prevalence of Brain Abnormalities in Japanese Patients with Optic Nerve Hypoplasia. Neuro-Ophthalmology. 2021;45(4):265-270.
Swami A, Sharma M, VanDyke L. Hypopituitarism and Other Endocrinopathies as a Consequence of Septo-Optic Dysplasia. Cureus. 2025;17(4):e82329.
Suwal S, Khatiwada A, Lamichhane S, Ghimire P, KC S. Exploring the diverse imaging spectrum of Septo-optic dysplasia: A case series. Radiol Case Rep. 2025;20:384-390.
Oyadiran OO, Gonzalez N, Khiami A. Hypernatremia in an Infant: A Case of Septo-Optic Dysplasia. Cureus. 2021;13(1):e12450.
Palorath A, Kharode I. Septo-Optic Dysplasia Diagnosed in a Newborn Infant with Normoglycemia. Case Rep Pediatr. 2021;2021:4836030.
Aliu E, Musa J, Parisapogu A, et al. Septo-optic dysplasia in an infant. Radiol Case Rep. 2022;17:3147-3150.
Reyes A, Galvis J, Estupinan Y. Septo-optic dysplasia plus: A case report. Biomedica. 2024;44:451-459.
開啟下方的 AI 助手,並將複製的內容貼到聊天欄。