视神经发育不全(ONH)是最常见的先天性视神经 异常,其特征是视神经 轴突数量减少。
可为单眼或双眼,常伴有结构性中枢神经系统异常(约90%)和神经发育障碍(约70%)。
视中隔发育不全(SOD,德莫西综合征)的诊断需满足以下三项中的至少两项:ONH、垂体功能减退、透明隔缺如。
检眼镜下的双环征是诊断线索,MRI脑结构评估和内分泌筛查必不可少。
视力 范围从正常到无光感,取决于乳头黄斑 束的密度。内分泌异常可能在后期显现,需要长期补充生长激素、甲状腺激素、肾上腺皮质激素 等。
视神经发育不全本身在未并发青光眼 时是非进行性的,但多学科协作的长期随访很重要。
视神经发育不全(ONH)是最常见的先天性视神经 异常,其特征是视神经 轴突数量减少。可为单眼或双眼,可能伴有中线脑结构缺陷。
Briere于1877年首次进行组织学描述,Reeves于1941年进行临床描述。1956年,de Morsier报告了其与透明隔缺如的关联,从而被称为德莫西综合征(视中隔发育不全,SOD)。1970年,Hoyt等人报告了详细的临床特征,提高了对该病的认识。
SOD的诊断需满足以下三项中的至少两项3) 6) :
ONH(单眼或双眼)
垂体功能减退
中线脑结构异常(透明隔缺如、胼胝体发育不全等)
SOD的患病率估计约为每10,000名新生儿中1例2) 6) 。流行病学上,它是3岁以下儿童视力 障碍的第三大常见原因。据报道,英格兰为每10万人10.9例,瑞典为17.3例。
在日本新潟大学对16例病例的研究中,初诊年龄中位数为2.4岁,女性占12/16例(75%),双侧性占11/16例(69%)1) 。
重症型为视神经 缺如(optic nerve aplasia)。视乳头和视网膜 血管完全缺失,无光感。
上方节段性视神经发育不全 (superior segmental optic hypoplasia; SSOH)是一种特殊类型,仅上方视神经 纤维发育不全,与母体糖尿病有关。日本报道的患病率约为0.3%。无性别差异。
Q
ONH和SOD有什么区别?
A
ONH指视神经 单独的形态异常。SOD是满足ONH、垂体功能低下和正中脑结构异常三联征中两项或以上的综合征,ONH是SOD的组成部分之一。据报道,约37.5%的ONH患者符合SOD的诊断标准1) 。
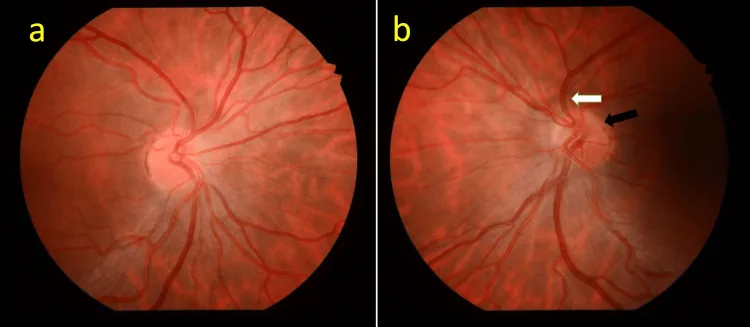
视神经发育不全的眼底照片。左眼显示小视乳头和乳头周围的双环样晕轮。 Mujahid M, et al. Superior Segmental Optic Nerve Hypoplasia: A Case Report and Literature Review. Cureus. 2026. Figure 1. PM
CI D: PMC12906824. License: CC BY.
眼底照片对比图像,左面板显示视乳头较小,乳头周围有双环样晕轮。显示了视神经发育不全,尤其是节段型中出现的乳头缩小和双环样晕轮。
ONH的视力 范围从正常到无光感。多数在0.1以下,视力 取决于乳头黄斑 束的密度。视神经发育不全在这一点上与其他乳头先天异常不同,即使黄斑 形成,乳头黄斑 神经纤维束的发育程度也有差异,因此视力 从保持1.0的病例到极低的病例范围广泛。
视力 下降视力 的病例。视野缺损 缺损 。在视力 相对较好的单眼或双眼病例中,有时可检测出双颞侧偏盲 倾向。RAPD (相对性传入性瞳孔 反应缺陷)眼球震颤 眼球震颤 或跷跷板样眼球震颤 。斜视
在日本的数据中,视力 不良占11/16例(69%),斜视 占8/16例(50%),眼球震颤 占5/16例(31%)1) 。
检眼镜检查可见特征性表现。
视神经乳头 双环征 :在小乳头周围可见淡色内环(巩膜 筛板 )和色素外环(脉络膜 色素层)的双重环状表现。这是本病的特征性表现。由于神经纤维束减少导致乳头变小,原本应为乳头的区域呈环状可见。DM/DD比值 :乳头中心凹 距离(DM)与乳头直径(DD)的比值。≥3可疑,≥4高度提示。≥3.2判定为小乳头。DD/DM比值<0.35为参考标准。视网膜 静脉迂曲OCT 表现视网膜神经纤维层 (RNFL )、神经节细胞层(GCL)和内丛状层(IPL)变薄。视网膜 血管
主要眼部表现和全身并发症的频率如下所示。
表现 频率 结构性中枢神经系统异常 约90% 神经发育障碍 约70% 下丘脑功能障碍(双眼) 81% 下丘脑功能障碍(单眼) 69% 发育迟缓(双眼) 78%
Q
单眼ONH也需要全身检查吗?
A
即使是单眼病例,下丘脑功能障碍的发生率也达69%,无症状患者中18.2%存在脑部异常1) 。单眼病例也必须进行MRI和内分泌筛查。
ONH的病理是视网膜神经节细胞 (RGC )和神经纤维的发育不全。存在两种假说:发育异常假说和逆行性变性假说。也有假说认为前脑动脉血管障碍导致的视交叉 和视神经 缺血是病因。
大多数病例是散发的2) 3) 。
以下基因突变可能与之相关。
HESX1 :参与前脑和垂体发育。突变携带者占所有SOD病例的不到1%7) 。PAX6 、SOX2 、OTX2 :参与眼和脑发育的转录因子。
年轻分娩(尤其是初产年龄较小)
母体糖尿病 :与SSOH关联尤为密切早产
药物暴露:苯妥英、奎宁、LSD、酒精
ONH的诊断基于检眼镜检查结果,并结合影像学检查和内分泌筛查。
确认双环征是诊断的第一步。DM/DD比值≥3(≥3.2为小视盘)可作为参考标准。
MRI :推荐所有ONH患者进行。评估透明隔缺如、胼胝体形态以及垂体的大小和形态。
指向下征 :视交叉 向下偏移的表现。是SOD的特征性表现3) 。视交叉 的正常宽度为11.13–16.92 mm,视神经 横截面积≤4.0 mm²判定为萎缩3) 。
OCT RNFL 厚度(视乳头周围视网膜神经纤维层 厚度)。可客观定量变薄程度。
在日本患者的研究中,脑异常占43.8%,SOD占37.5%。值得注意的是,即使无症状,仍有18.2%存在脑异常1) 。此外,在3例垂体功能低下患者中,有2例MRI显示垂体形态正常1) 。
建议对所有ONH患者进行以下检查:
皮质醇
TSH(促甲状腺激素)、FT4(游离甲状腺素)
IGF-1(胰岛素样生长因子-1)、IGFBP-3
LH(黄体生成素)、FSH(卵泡刺激素)
需要与以下疾病进行鉴别:
视神经萎缩 视神经 缺损 视盘凹陷 。牵牛花综合征 倾斜视 盘综合征 :视盘不对称倾斜。青光眼 性视神经病变 RNFL 缺损 模式不同。如有可能,定期用OCT 测量RNFL 厚度以确认有无变化。
Q
即使MRI正常,也可能存在内分泌异常吗?
A
有可能。在日本患者的研究中,3例垂体功能低下患者中有2例MRI表现正常1) 。无论MRI结果如何,所有患者都应进行内分泌筛查。
ONH本身没有根治性治疗方法。管理的核心是优化视功能和应对全身并发症(尤其是内分泌异常)。多学科团队(眼科、内分泌科、儿科、神经科、康复科)的协作至关重要,建议每半年评估生长情况,每年评估视功能。
屈光 矫正屈光 不正很重要。如果存在眼球震颤 ,尝试通过眼镜或隐形眼镜进行屈光 矫正。斜视手术 斜视 ,进行以后退术为主的斜视手术 。也可考虑针对眼球震颤 的眼外肌 手术。
生长激素
频率 :约70%的ONH患者需要。
适应症 :确诊生长激素分泌不足时开始。
甲状腺激素
频率 :约43%需要。
适应症 :TSH/FT4异常时开始补充。
肾上腺皮质激素
频率 :约27%的患者需要。
注意 :肾上腺功能不全在应激时可能致命。必须指导应激剂量(发热或手术时增加剂量)5) 。
抗利尿激素
频率 :约5%合并尿崩症。
注意 :快速纠正钠可能导致抽搐。纠正速度应低于0.5 mEq/L/小时4) 。
在成人管理病例中,有报道使用左甲状腺素137 μg、去氨加压素和氢化可的松10 mg(早晨)/7.5 mg(傍晚)的补充方案2) 。
内分泌异常在婴幼儿期可能无症状,但随着成长可能在以后显现。长期定期评估是必需的1) 。
合并肾上腺功能不全时,在感染、外伤、手术等应激情况下增加氢化可的松剂量(应激剂量)可挽救生命5) 。
在尿崩症管理中,严格遵守高钠血症的纠正速度。快速纠正可能导致抽搐和脑水肿4) 。
视神经发育不全本身是非进行性的,除非合并青光眼 。不合并青光眼 时,应避免为降低眼压 而轻易使用眼药水或手术治疗。然而,内分泌异常可能随时间出现或恶化,因此长期随访是必不可少的1) 。早期诊断并在必要时于3岁前开始激素替代治疗可避免后遗症,因此即使是单眼病例,也应考虑本病并避免漏诊。
Q
视力将来会恶化吗?
A
视神经发育不全本身是非进行性的,不合并青光眼 时视力 通常稳定。但内分泌异常可能在以后出现,因此定期全身评估的持续进行很重要。
ONH的本质是视网膜神经纤维层 (RNFL )和神经节细胞的减少,对外层视网膜 影响较小。其发生机制主要有两种假说。
发育异常假说 :胚胎期视网膜神经节细胞 的分化和迁移障碍导致视神经 轴突形成不足。逆行性变性假说 :中枢神经系统结构异常(如透明隔缺如、胼胝体缺如等)引起的逆行性轴索变性。
也有假说认为前大脑动脉血管障碍导致的视交叉 和视神经 区域缺血可能参与其中。
下丘脑功能障碍在单眼ONH中占69%,双眼ONH中占81%。垂体和视神经 在发育上邻近,同一发育障碍可能影响两者。
发育迟缓在所有病例中占75%,双眼(78%)高于单眼(39%)。
SOD plus是指在经典SOD基础上伴有皮质发育异常(如多小脑回、裂脑症等)的病理状态,有报道称其比经典SOD更常见7) 。神经发育预后更差,癫痫合并风险也更高。
针对SOD相关肥胖的药物疗法,黑皮质素4受体(MC4R)激动剂setmelanotide的临床试验(NCT 06760546)正在进行中2) 。下丘脑性肥胖显著降低SOD患者的生活质量,因此作为一种新的治疗选择备受关注。
在诊断为正常血糖的SOD新生儿中,已有报道使用睾酮疗法(25mg肌肉注射,每月1次,共3个月)治疗小阴茎和隐睾,以及尝试重组FSH疗法5) 。这些表明早期内分泌干预的可能性,但长期有效性和安全性尚未确定。
Kiyokawa M, Ueki S, Hatase T, Hanyu T, Fukuchi T. The Prevalence of Brain Abnormalities in Japanese Patients with Optic Nerve Hypoplasia. Neuro-Ophthalmology. 2021;45(4):265-270.
Swami A, Sharma M, VanDyke L. Hypopituitarism and Other Endocrinopathies as a Consequence of Septo-Optic Dysplasia. Cureus. 2025;17(4):e82329.
Suwal S, Khatiwada A, Lamichhane S, Ghimire P, KC S. Exploring the diverse imaging spectrum of Septo-optic dysplasia: A case series. Radiol Case Rep. 2025;20:384-390.
Oyadiran OO, Gonzalez N, Khiami A. Hypernatremia in an Infant: A Case of Septo-Optic Dysplasia. Cureus. 2021;13(1):e12450.
Palorath A, Kharode I. Septo-Optic Dysplasia Diagnosed in a Newborn Infant with Normoglycemia. Case Rep Pediatr. 2021;2021:4836030.
Aliu E, Musa J, Parisapogu A, et al. Septo-optic dysplasia in an infant. Radiol Case Rep. 2022;17:3147-3150.
Reyes A, Galvis J, Estupinan Y. Septo-optic dysplasia plus: A case report. Biomedica. 2024;44:451-459.
复制全文后,可以粘贴到你常用的 AI 助手中提问。
打开下面的 AI 助手,并把复制的内容粘贴到聊天框。