هرمون النمو
التكرار: يحتاجه حوالي 70% من مرضى ONH.
المؤشرات: يبدأ عند تأكيد نقص هرمون النمو.

نقص تنسج العصب البصري (ONH) هو أكثر اضطرابات العصب البصري الخلقية شيوعًا، ويتميز بانخفاض عدد محاور العصب البصري. قد يكون أحادي أو ثنائي الجانب، وقد يصاحبه عيوب في البنى الدماغية الوسطى.
وصف بريير (Briere) المرض تشريحيًا لأول مرة عام 1877، وسجله ريفز (Reeves) سريريًا عام 1941. في عام 1956، أبلغ دي مورسييه (de Morsier) عن ارتباطه بغياب الحاجز الشفاف، وأصبح يُعرف بمتلازمة دي مورسييه (خلل تنسج الحاجز البصري). في عام 1970، أبلغ هويت (Hoyt) وزملاؤه عن الصورة السريرية التفصيلية، مما وسع نطاق التعرف على المرض.
تُشخص متلازمة خلل تنسج الحاجز البصري (SOD) بوجود اثنين أو أكثر من الثلاثي التالي3)6):
يقدر معدل انتشار متلازمة خلل تنسج الحاجز البصري بحوالي 1 لكل 10,000 ولادة2)6). وبائيًا، هو ثالث سبب شائع لضعف البصر لدى الأطفال دون سن الثالثة. في إنجلترا، يُبلغ عنه بمعدل 10.9 لكل 100,000 نسمة، وفي السويد 17.3.
في دراسة أجريت على 16 حالة في جامعة نيغاتا باليابان، كان متوسط عمر التشخيص الأولي 2.4 سنة، وكانت الإناث 12/16 (75%)، وكانت الحالات الثنائية 11/16 (69%) 1).
هناك نوع شديد يسمى عدم تنسج العصب البصري (optic nerve aplasia). حيث لا توجد حليمة بصرية أو أوعية شبكية على الإطلاق، ويفقد المريض الإحساس بالضوء.
نقص تنسج العصب البصري القطاعي العلوي (superior segmental optic hypoplasia; SSOH) هو نوع خاص يحدث فيه نقص تنسج ألياف العصب البصري في الجزء العلوي فقط، وقد ارتبط بداء السكري لدى الأم. يُقدر معدل الانتشار في اليابان بحوالي 0.3%. لا يوجد فرق بين الجنسين.
ONH يشير إلى شذوذ شكل العصب البصري وحده. SOD هي متلازمة تتطلب وجود اثنين أو أكثر من ثلاث علامات: ONH، قصور الغدة النخامية، وشذوذ بنية الدماغ المتوسط. ONH هو أحد مكونات SOD. تشير التقارير إلى أن حوالي 37.5% من مرضى ONH يستوفون معايير تشخيص SOD 1).
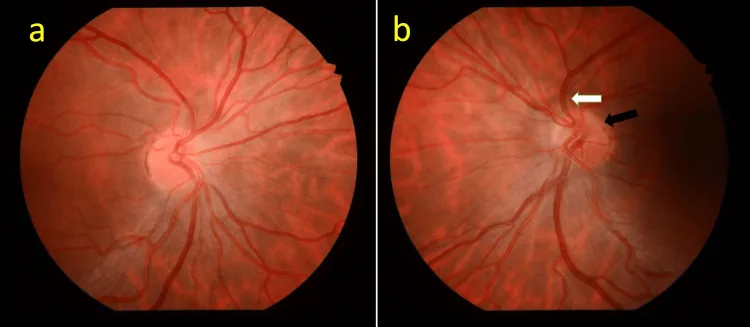
تتراوح حدة البصر في ONH من طبيعية إلى عدم الإحساس بالضوء. غالبًا ما تكون أقل من 0.1، وتعتمد حدة البصر على كثافة حزمة الألياف العصبية البقعية الحليمية. يختلف نقص تنسج العصب البصري عن غيره من شذوذات الحليمة الخلقية في هذه النقطة، فحتى مع وجود بقعة طبيعية، هناك تباين في درجة تطور حزمة الألياف العصبية البقعية الحليمية، مما يؤدي إلى نطاق واسع من حدة البصر من 1.0 إلى منخفضة جدًا.
في بيانات يابانية، كان ضعف البصر موجودًا في 11/16 حالة (69%)، والحول في 8/16 حالة (50%)، والرأرأة في 5/16 حالة (31%)1).
توجد علامات مميزة بمنظار العين.
فيما يلي العلامات العينية الرئيسية وتواتر المضاعفات الجهازية.
| العلامة | التواتر |
|---|---|
| تشوهات هيكلية في الجهاز العصبي المركزي | حوالي 90% |
| اضطرابات النمو العصبي | حوالي 70% |
| خلل في وظائف تحت المهاد (ثنائي العينين) | 81% |
| خلل في وظائف تحت المهاد (أحادي العين) | 69% |
| تأخر النمو (ثنائي العينين) | 78% |
حتى في الحالات أحادية العين، يُلاحظ خلل في وظائف تحت المهاد بنسبة 69%، ويوجد تشوه دماغي في 18.2% من المرضى حتى بدون أعراض1). التصوير بالرنين المغناطيسي والفحص الهرموني ضروريان حتى في الحالات أحادية العين.
أصل ONH هو عدم اكتمال نمو الخلايا العقدية الشبكية (RGC) والألياف العصبية. هناك فرضيتان: فرضية الشذوذ التطوري وفرضية التنكس الرجعي. كما طُرحت فرضية أن نقص تروية التصالب البصري والعصب البصري الناتج عن اضطراب وعائي في الشريان الدماغي الأمامي هو السبب.
معظم الحالات تكون متفرقة2)3).
قد تشارك الطفرات الجينية التالية.
يعتمد تشخيص ONH على نتائج تنظير العين، ويتم دمجه مع التصوير التشخيصي وفحص الغدد الصماء.
تأكيد علامة الحلقة المزدوجة هو الخطوة الأولى في التشخيص. نسبة DM/DD ≥ 3 (≥ 3.2 تشير إلى حليمة صغيرة) هي معيار إرشادي.
في دراسة على المرضى اليابانيين، وُجدت تشوهات دماغية في 43.8%، ومتلازمة خلل التنسج الحاجز البصري (SOD) في 37.5%. الجدير بالذكر أنه حتى في حالة عدم وجود أعراض، كانت التشوهات الدماغية موجودة في 18.2% من الحالات1). بالإضافة إلى ذلك، في 2 من 3 حالات أظهرت قصورًا في الغدة النخامية، كان شكل الغدة النخامية طبيعيًا في التصوير بالرنين المغناطيسي1).
يوصى بإجراء الفحوصات التالية لجميع مرضى نقص تنسج العصب البصري (ONH):
من الضروري التفريق بين الأمراض التالية:
نعم، يمكن. في دراسة على مرضى يابانيين، كانت نتائج الرنين المغناطيسي طبيعية في 2 من 3 حالات أظهرت قصورًا في الغدة النخامية1). يجب إجراء فحص هرموني لجميع المرضى بغض النظر عن نتائج الرنين المغناطيسي.
لا يوجد علاج جذري لـ ONH بحد ذاته. يركز العلاج على تحسين الوظيفة البصرية ومعالجة المضاعفات الجهازية (خاصة الاضطرابات الهرمونية). التعاون بين فريق متعدد التخصصات (طب العيون، الغدد الصماء، طب الأطفال، طب الأعصاب، إعادة التأهيل) ضروري، ويوصى بتقييم النمو كل ستة أشهر والوظيفة البصرية سنويًا.
هرمون النمو
التكرار: يحتاجه حوالي 70% من مرضى ONH.
المؤشرات: يبدأ عند تأكيد نقص هرمون النمو.
هرمون الغدة الدرقية
التكرار: يحتاجه حوالي 43%.
المؤشرات: يبدأ التعويض عند وجود خلل في TSH و FT4.
هرمون قشرة الغدة الكظرية
التكرار: مطلوب في حوالي 27%.
تنبيه: قصور الغدة الكظرية يمكن أن يكون مميتًا عند الإجهاد. التوجيه بشأن جرعات الإجهاد (زيادة الجرعة عند الحمى أو الجراحة) ضروري 5).
الهرمون المضاد لإدرار البول
التكرار: حوالي 5% يعانون من مرض السكري الكاذب.
تنبيه: التصحيح السريع للصوديوم قد يسبب تشنجات. يجب أن يكون معدل التصحيح أقل من 0.5 ملي مكافئ/لتر/ساعة 4).
في حالات إدارة البالغين، تم الإبلاغ عن أنظمة تعويضية مثل ليفوثيروكسين 137 ميكروغرام، ديزموبريسين، وهيدروكورتيزون 10 ملغ (صباحًا)/7.5 ملغ (مساءً) 2).
نقص تنسج العصب البصري نفسه غير تقدمي إذا لم يترافق مع الجلوكوما. في حالة عدم وجود الجلوكوما، يجب تجنب قطرات العين أو الجراحة غير الضرورية لخفض ضغط العين. ومع ذلك، قد تظهر الاضطرابات الهرمونية أو تتفاقم بمرور الوقت، مما يستلزم متابعة طويلة الأمد 1). التشخيص المبكر وبدء العلاج الهرموني قبل سن 3 سنوات في الحالات الضرورية يمكن أن يمنع المضاعفات، لذلك من المهم مراعاة هذا المرض حتى في الحالات أحادية العين.
نقص تنسج العصب البصري نفسه غير تقدمي، وغالبًا ما تكون الرؤية مستقرة إذا لم يترافق مع الجلوكوما. ومع ذلك، قد تظهر الاضطرابات الهرمونية في وقت لاحق، لذا فإن التقييم الدوري المنتظم مهم.
جوهر ONH هو انخفاض في طبقة الألياف العصبية الشبكية (RNFL) والخلايا العقدية، مع تأثير ضئيل على الطبقات الخارجية للشبكية. هناك فرضيتان رئيسيتان لآلية الحدوث.
هناك أيضًا فرضية تشير إلى أن نقص التروية في منطقة التصالب البصري والعصب البصري بسبب اضطراب وعائي في الشريان الدماغي الأمامي قد يلعب دورًا.
يُلاحظ خلل وظيفي في منطقة تحت المهاد في 69% من حالات ONH أحادية العين و81% من حالات ثنائية العين. تقع الغدة النخامية والعصب البصري بالقرب من بعضهما تطوريًا، ويُعتقد أن نفس الاضطراب التطوري يؤثر على كليهما.
يُلاحظ تأخر النمو في 75% من الحالات الكلية، وهو أعلى في الحالات ثنائية العين (78%) مقارنة بأحادية العين (39%).
SOD plus هو حالة تتميز بوجود تشوهات قشرية (مثل تعدد التلافيف الصغيرة، انشقاق الدماغ) بالإضافة إلى SOD الكلاسيكي، وقد تم الإبلاغ عن حدوثه بتواتر أعلى من SOD الكلاسيكي 7). يكون التشخيص العصبي النمائي أسوأ، وخطر الإصابة بالصرع أعلى.
تجري حاليًا تجربة سريرية (NCT06760546) لعقار setmelanotide، وهو ناهض لمستقبل الميلانوكورتين 4 (MC4R)، كعلاج دوائي للسمنة المرتبطة بـ SOD 2). نظرًا لأن السمنة تحت المهاد تقلل بشكل كبير من جودة حياة مرضى SOD، فإن هذا يمثل خيارًا علاجيًا جديدًا واعدًا.
تم الإبلاغ عن محاولات إدارة القضيب الصغير والخصية المعلقة باستخدام العلاج بالتستوستيرون (25 ملغ عضليًا، مرة واحدة شهريًا لمدة 3 أشهر) والعلاج بـ FSH المؤتلف لدى الأطفال حديثي الولادة المصابين بـ SOD والذين تم تشخيصهم بسكر الدم الطبيعي 5). تشير هذه إلى إمكانية التدخل المبكر بالتعويض الهرموني، لكن الفعالية والسلامة على المدى الطويل لم يتم تأكيدها بعد.