Hormone de croissance
Fréquence : Nécessaire chez environ 70 % des patients atteints d’ONH.
Indication : Débuter en cas de déficit confirmé en hormone de croissance.

L’hypoplasie du nerf optique (HNO) est l’anomalie congénitale du nerf optique la plus fréquente, caractérisée par une réduction du nombre d’axones optiques. Elle peut être unilatérale ou bilatérale et s’accompagner de défauts des structures cérébrales médianes.
Décrite histologiquement pour la première fois par Briere en 1877, la clinique a été rapportée par Reeves en 1941. En 1956, de Morsier a décrit l’association avec l’agénésie du septum pellucidum, connue sous le nom de syndrome de de Morsier (dysplasie septo-optique, DSO). En 1970, Hoyt et al. ont rapporté des descriptions cliniques détaillées, élargissant la reconnaissance de cette maladie.
La DSO est diagnostiquée lorsque au moins deux des trois éléments suivants sont présents3)6) :
La prévalence de la DSO est estimée à environ 1/10 000 naissances2)6). Sur le plan épidémiologique, c’est la troisième cause de déficience visuelle chez les enfants de moins de 3 ans. En Angleterre, elle est de 10,9 pour 100 000 habitants, et en Suède de 17,3.
Dans une étude de 16 cas à l’Université de Niigata au Japon, l’âge médian au premier diagnostic était de 2,4 ans, 12/16 (75 %) étaient des femmes et 11/16 (69 %) étaient bilatéraux 1).
Une forme sévère est l’aplasie du nerf optique (optic nerve aplasia). La papille et les vaisseaux rétiniens sont totalement absents, et il n’y a pas de perception lumineuse.
L’hypoplasie segmentaire supérieure du nerf optique (superior segmental optic hypoplasia ; SSOH) est une forme particulière où seules les fibres nerveuses optiques supérieures sont hypoplasiques, et une association avec le diabète maternel a été signalée. La prévalence au Japon est d’environ 0,3 %. Il n’y a pas de différence de sexe.
L’ONH désigne une anomalie morphologique isolée du nerf optique. La SOD est un syndrome qui répond à au moins deux des trois critères suivants : ONH, insuffisance hypophysaire et anomalies cérébrales de la ligne médiane. L’ONH est l’un des composants de la SOD. Selon un rapport, environ 37,5 % des patients atteints d’ONH répondent aux critères diagnostiques de la SOD 1).
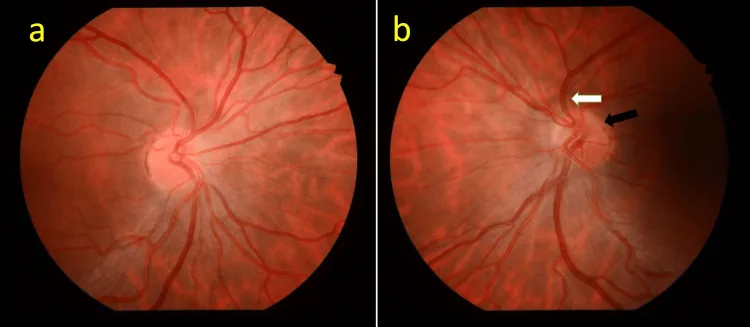
L’acuité visuelle dans l’ONH varie de normale à absence de perception lumineuse. Dans la plupart des cas, elle est inférieure à 0,1 et dépend de la densité du faisceau papillo-maculaire. L’hypoplasie du nerf optique diffère des autres anomalies congénitales de la papille sur ce point : même si la macula est formée, le développement du faisceau de fibres nerveuses papillo-maculaires varie, ce qui entraîne une large gamme d’acuité visuelle, allant de 1,0 à très faible.
Selon les données japonaises, une mauvaise vision a été observée dans 11/16 cas (69 %), un strabisme dans 8/16 cas (50 %) et un nystagmus dans 5/16 cas (31 %)1).
Des signes caractéristiques sont observés à l’ophtalmoscopie.
Les principales observations oculaires et la fréquence des complications systémiques sont présentées ci-dessous.
| Observation | Fréquence |
|---|---|
| Anomalies structurelles du SNC | Environ 90 % |
| Troubles neurodéveloppementaux | Environ 70 % |
| Dysfonction hypothalamique (bilatérale) | 81% |
| Dysfonction hypothalamique (unilatérale) | 69% |
| Retard de développement (bilatéral) | 78% |
Même en cas d’atteinte unilatérale, une dysfonction hypothalamique est observée dans 69% des cas, et des anomalies cérébrales sont présentes chez 18,2% des patients asymptomatiques1). L’IRM et le dépistage endocrinien sont indispensables même en cas d’atteinte unilatérale.
La pathologie de l’ONH est une dysgénésie des cellules ganglionnaires rétiniennes (CGR) et des fibres nerveuses. Deux hypothèses existent : la théorie de la dysgénésie et celle de la dégénérescence rétrograde. Une hypothèse impliquant une ischémie du chiasma et du nerf optique due à des troubles vasculaires de l’artère cérébrale antérieure a également été proposée.
La majorité des cas sont sporadiques2)3).
Les mutations génétiques suivantes peuvent être impliquées.
Le diagnostic de l’ONH repose sur l’examen ophtalmoscopique, combiné à l’imagerie et au dépistage endocrinien.
La confirmation du signe du double anneau est la première étape du diagnostic. Un rapport DM/DD ≥ 3 (≥ 3,2 pour une papille petite) est un indicateur.
Dans une étude portant sur des patients japonais, des anomalies cérébrales ont été observées dans 43,8 % des cas et un SOD dans 37,5 % des cas. Il est à noter que des anomalies cérébrales étaient présentes chez 18,2 % des patients asymptomatiques 1). De plus, chez 2 des 3 patients présentant une insuffisance hypophysaire, l’IRM montrait une morphologie hypophysaire normale 1).
Les examens suivants sont recommandés pour tous les patients atteints de NOH.
Un diagnostic différentiel avec les maladies suivantes est nécessaire.
Oui, c’est possible. Dans une étude portant sur des patients japonais, 2 des 3 patients présentant une insuffisance hypophysaire avaient une IRM normale 1). Un dépistage endocrinien doit être effectué chez tous les patients, indépendamment des résultats de l’IRM.
Il n’existe pas de traitement curatif pour l’ONH elle-même. La prise en charge se concentre sur l’optimisation de la fonction visuelle et la gestion des complications systémiques (en particulier les anomalies endocriniennes). Une collaboration multidisciplinaire (ophtalmologie, endocrinologie, pédiatrie, neurologie, réadaptation) est essentielle. Une évaluation de la croissance tous les six mois et de la fonction visuelle une fois par an est recommandée.
Hormone de croissance
Fréquence : Nécessaire chez environ 70 % des patients atteints d’ONH.
Indication : Débuter en cas de déficit confirmé en hormone de croissance.
Hormone thyroïdienne
Fréquence : Nécessaire chez environ 43 % des patients.
Indication : Débuter en cas d’anomalie de la TSH et de la FT4.
Cortisol (hormone corticostéroïde)
Fréquence : nécessaire dans environ 27 % des cas.
Attention : l’insuffisance surrénalienne peut être mortelle en période de stress. L’enseignement du stress-dosing (augmentation des doses en cas de fièvre ou de chirurgie) est indispensable 5).
Hormone antidiurétique
Fréquence : environ 5 % développent un diabète insipide.
Attention : une correction rapide du sodium peut provoquer des convulsions. La vitesse de correction doit être inférieure à 0,5 mEq/L/h 4).
Chez les adultes, des schémas de substitution tels que lévothyroxine 137 µg, desmopressine, hydrocortisone 10 mg (matin) / 7,5 mg (soir) ont été rapportés 2).
L’hypoplasie du nerf optique elle-même est non progressive en l’absence de glaucome associé. En l’absence de glaucome, il faut éviter les collyres ou la chirurgie visant à abaisser la pression intraoculaire. Cependant, les anomalies endocriniennes peuvent apparaître ou s’aggraver avec le temps, d’où la nécessité d’un suivi à long terme 1). Un diagnostic précoce et un traitement hormonal substitutif avant l’âge de 3 ans dans les cas nécessaires permettent d’éviter des séquelles, il est donc important de ne pas méconnaître cette maladie même en cas d’atteinte unilatérale.
L’hypoplasie du nerf optique elle-même est non progressive et, en l’absence de glaucome, la vision reste souvent stable. Cependant, des anomalies endocriniennes peuvent apparaître plus tard, d’où l’importance d’une évaluation systémique régulière.
L’essence de l’ONH est une diminution de la couche de fibres nerveuses rétiniennes (RNFL) et des cellules ganglionnaires, avec peu d’effet sur les couches externes de la rétine. Deux hypothèses principales existent quant au mécanisme de développement.
Il existe également une hypothèse selon laquelle l’ischémie de la région du chiasma optique et du nerf optique due à des troubles vasculaires de l’artère cérébrale antérieure serait impliquée.
Un dysfonctionnement hypothalamique est observé dans 69 % des cas d’ONH unilatérale et dans 81 % des cas bilatéraux. L’hypophyse et le nerf optique sont proches sur le plan développemental, et on pense que le même trouble du développement affecte les deux.
Un retard de développement est observé dans 75 % de l’ensemble des cas, avec une fréquence plus élevée dans les cas bilatéraux (78 %) que dans les cas unilatéraux (39 %).
Le SOD plus est une condition qui associe, en plus du SOD classique, des anomalies de la formation corticale (polymicrogyrie, schizencéphalie, etc.) et serait plus fréquent que le SOD classique selon certains rapports7). Le pronostic neurodéveloppemental est plus défavorable et le risque d’épilepsie est également plus élevé.
Un essai clinique (NCT06760546) du setmelanotide, un agoniste du récepteur de la mélanocortine 4 (MC4R), est en cours comme traitement médicamenteux de l’obésité associée au SOD2). L’obésité hypothalamique réduit considérablement la qualité de vie des patients atteints de SOD, ce qui en fait une nouvelle option thérapeutique prometteuse.
Chez les nouveau-nés SOD diagnostiqués avec une glycémie normale, la gestion du micropénis et de la cryptorchidie par un traitement à la testostérone (25 mg IM, une fois par mois pendant 3 mois) et des tentatives de thérapie par FSH recombinante ont été rapportées 5). Ces approches montrent le potentiel d’une intervention précoce de supplémentation endocrinienne, mais leur efficacité et sécurité à long terme ne sont pas encore établies.