孤立性無虹膜症
頻率:約佔全部病例的2/3。
遺傳形式:體染色體顯性遺傳(AD)。
特徵:由PAX6基因突變引起。不伴隨全身症狀。外顯率完全,但表現度多樣。

無虹膜症是一種罕見的先天性疾病,特徵為虹膜不同程度的發育不全或缺損。「無虹膜症」這一名稱並不準確,因為透過隅角鏡或超音波生物顯微鏡(UBM)幾乎總能檢測到虹膜組織碎片。
盛行率約為1/40,000至1/100,000,未報告顯著的種族或性別差異 1)。ICD-10中歸類為Q13.1。
無虹膜症是一種泛眼球疾病,不僅影響虹膜,還影響角膜、水晶體、隅角、中心凹和視神經 1),呈現多種威脅視力的眼部併發症。視力預後通常不佳,矯正視力常約為0.1。瞳孔對光反射消失,但調節功能保留。60-90%的病例為雙眼發病。
已確認以下三種表現型。
孤立性無虹膜症
頻率:約佔全部病例的2/3。
遺傳形式:體染色體顯性遺傳(AD)。
特徵:由PAX6基因突變引起。不伴隨全身症狀。外顯率完全,但表現度多樣。
WAGR症候群
頻率:部分散發病例。
遺傳形式:PAX6和WT1的相鄰缺失。
特徵:合併Wilms腫瘤、泌尿生殖器異常和智能障礙。腫瘤風險高達50%。
Gillespie症候群
頻率:約佔全部病例的2%。
遺傳形式:ITPR1基因突變。
特徵:伴隨小腦性共濟失調和智能障礙。特徵性虹膜異常表現為固定性瞳孔散大3)。
散發性無虹膜症約佔全部病例的1/3,由包含PAX6的11p13新生缺失引起。如果缺失波及相鄰的WT1基因,則導致WAGR症候群1)。散發性無虹膜症患者中25-30%發生Wilms腫瘤,相對風險為67。
PAX6是眼形成的master control基因,參與眼、神經管、嗅球、胰臟蘭氏小島和嗅上皮的發育。單一對偶基因功能喪失(單倍劑量不足)即可發病,雙對偶基因異常則導致胚胎致死。2017年被指定為《難病法》規定的指定難病,重症度Ⅲ度以上(詳見診斷與檢查項)可享受醫療費補助7)。
散發性(新發突變)約占全部病例的1/3,即使沒有家族史也會發病。散發病例可能提示WAGR症候群,因此基因檢測和腹部超音波篩檢Wilms腫瘤非常重要。
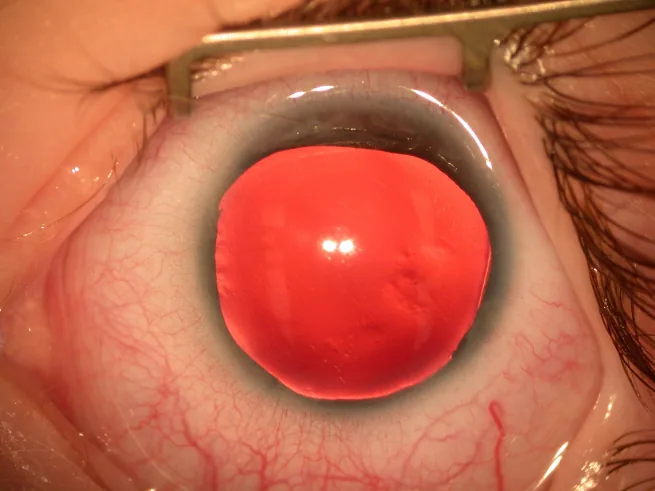
大多數無虹膜症在出生時因虹膜、瞳孔異常或在嬰兒期因眼球震顫而被發現。
表現在家族間和家族內有所不同,但左右眼差異通常較小。
主要由於中心凹發育不全,矯正視力通常在0.1至0.2左右。合併黃斑發育不良時視力預後尤其差。從嬰兒期開始的屈光矯正和低視力護理對視覺發育很重要。
PAX6不僅在眼組織中表現,還在中樞神經系統、胰臟蘭氏小島和嗅上皮中表現,因此可能出現以下眼外併發症8)。
決定視功能的關鍵因素是青光眼、黃斑部發育不全、眼球震顫、角膜病變、白內障和虹膜發育異常。由於青光眼導致的視野和視力損害是不可逆的,因此在追蹤觀察中眼壓管理最為重要。8)
大多數先天性無虹膜症是由位於第11號染色體短臂(11p13)上的PAX6基因異合子突變所引起。單套基因不足(haploinsufficiency)是PAX6相關疾病的主要致病機制。1)
PAX6基因是眼睛形成的master control基因,在眼睛、神經管、嗅球和胰臟的發育中扮演重要角色。正常的眼睛發育需要兩個PAX6基因拷貝,僅一個拷貝的功能喪失即可導致無虹膜症。1)
在一項中國患者的世代研究中,96.9%的病例發現PAX6基因的致病突變。1)在典型無虹膜症中,誘發無義突變依賴性mRNA降解(NMD)的突變或大片段缺失在96%的病例中被檢測到。1)
病理學上,除虹膜根部外平滑肌缺損,隅角發育不全。角膜上皮幹細胞功能異常,導致上皮和Bowman氏膜異常,形成富含血管的角膜血管翳。
導致無虹膜症表現型的PAX6突變分類如下。
| 突變類型 | 頻率 |
|---|---|
| 無義突變 | 約39% |
| 框架位移突變 | 約25% |
| 剪接突變 | 約13% |
| 錯義突變 | 約12% |
通讀突變(C端延伸突變)約佔5%,由於終止密碼子轉變為翻譯密碼子,產生異常延長的PAX6蛋白6)。C端延伸突變常伴有嚴重的虹膜發育不全和高度視力障礙1)6)。
基因突變多為PTC型突變,也有錯義突變的報導7)。關於基因檢測的實用性,Sanger定序或NGS可在近85%的孤立性無虹膜症患者中檢測到突變。此外,MLPA或CMA可在近15%的患者中檢測到PAX6基因內或順式調控區域的缺失8)。
Wang(2023)新鑑定了一個移碼突變c.640_646del(p.R214Pfs*28),並報告了一例表現為完全虹膜缺損、中心凹發育不全、水晶體偏位和視網膜剝離的病例1)。
Ratna等人(2022)在一個印度家系中鑑定出通讀突變c.1268A>T(p.*423L)。患者表現為完全無虹膜、眼球震顫、中心凹發育不全、AAK、水晶體向上半脫位、高度近視和視神經萎縮,顯示出C端延伸突變導致的嚴重表型6)。
在散發性無虹膜症中,涉及PAX6和WT1的大片段缺失是WAGR症候群的原因。存在WT1缺失時,Wilms腫瘤風險高達50%1)。若懷疑WAGR症候群,可透過基因檢測確認PAX6和WT1缺失,從而進行Wilms腫瘤風險評估和發展遲緩的追蹤8)。基因檢測對WT1區域的評估至關重要,散發性病例中30%在5歲前發生Wilms腫瘤。由於WT1基因位於PAX6附近,兩者同時缺失的第11號染色體短臂缺失(11p13缺失)導致無虹膜症合併Wilms腫瘤。
Gillespie症候群由ITPR1基因的雜合顯性負性突變或雙等位基因突變引起3)。迄今為止,已有37例通過分子診斷確診,Gly2554殘基被認為是熱點3)。
根據無虹膜症的診斷標準(2020年),依以下標準確診7)。
A. 症狀
B. 檢查所見
C. 需鑑別的疾病
E. 遺傳學檢查:PAX6基因致病性變異或11p13區域缺失
診斷類別7):
用於難病認定的嚴重程度分類規定如下四個等級7)。
| 嚴重程度 | 定義 |
|---|---|
| Ⅰ度 | 單眼受累,對側眼正常 |
| Ⅱ度 | 雙眼罹病,較好眼矯正視力≥0.3 |
| Ⅲ度 | 雙眼罹病,較好眼矯正視力≥0.1且<0.3 |
| Ⅳ度 | 雙眼罹病,較好眼矯正視力<0.1 |
即使為Ⅰ~Ⅲ度,若伴有青光眼等導致的視野狹窄(Goldmann I/4視標中心殘存視野20度以內),則嚴重程度上升一級。嚴重程度Ⅲ度以上為醫療費補助對象7)。
透過裂隙燈顯微鏡確認虹膜缺損或發育不全即可輕鬆做出臨床診斷。使用隅角鏡和超音波生物顯微鏡評估殘留虹膜組織。同時檢查前房隅角發育異常的有無。
系統評估以下眼部併發症:
無虹膜症遺傳評估最重要的目標是確認PAX6缺失是否延伸至WT1基因1)。透過全外顯子組定序或MLPA法評估PAX6和WT1區域的突變和缺失1)2)。
散發性無虹膜症中,因WT1基因缺失導致的Wilms腫瘤風險評估直接關係到生命預後1)。即使是家族性病例,由於表型多樣性,也建議進行基因檢測以確診並提供遺傳諮詢。
無虹膜症尚無根治性治療方法。管理核心是低視力復健以最大限度利用殘餘視力,以及針對各併發症的個別化治療。臨床指南(2021年)基於6個臨床問題提出了建議8)。
CQ1:弱推薦不進行角膜移植治療角膜基質混濁8)。
角膜移植可能在短期內改善視力,但由於黃斑發育不全等合併症,改善有限。長期來看,由於青光眼進展和移植片功能不全,視力預後不良。
CQ2:弱建議對角膜上皮幹細胞缺乏症進行手術治療。 8)
CQ3:弱建議實施白內障手術。 8)
白內障在20歲前發生率為50–85%。根據混濁和畏光程度計畫手術。據報告66–100%的手術病例視力改善,但需注意以下幾點。
由於Zinn小帶脆弱,人工水晶體植入需謹慎適應。
Hu等人(2024)對兩例伴有嚴重AAK的先天性無虹膜症患者實施了吊燈式後照明輔助下的超聲乳化白內障吸除術。由於角膜混濁,常規術中可視化困難,但後方照明使水晶體和前囊清晰可見,術後3週矯正視力分別改善至20/200和20/10004)。
CQ4:強烈建議進行青光眼治療8)。
青光眼發病後,根據以下五步演算法進行管理。
藥物治療:β受體阻斷劑、交感神經興奮劑和前列腺素(PG)相關藥物有效。溴莫尼定(α腎上腺素受體激動劑)因有中樞神經抑制風險,禁用於2歲以下兒童。若擔心角膜上皮損傷,應使用不含防腐劑的製劑。
流出道重建術(隅角切開術/小樑切開術):建議作為初次手術16)。也有預防性隅角切開術的報告。但在殘留虹膜覆蓋小樑網的病例中可能無效。
濾過手術(小樑切除術):僅有少數中短期報告。在兒童眼中效果往往較差,術後低眼壓發生率約25%13)。也有術後惡性青光眼的報告。
青光眼植入物手術(引流閥植入術):可使用Baerveldt和Ahmed型裝置。在有水晶體眼中植入引流管時,建議採用切線方向而非角膜中央方向。可望獲得良好的眼壓控制。
睫狀體破壞手術:最後手段。睫狀體冷凍術據報告常導致低眼壓。由於睫狀體發育不全,低眼壓風險高於健康眼。
由於隅角發育異常為背景,需要與一般開放隅角青光眼不同的處理方式。初次選擇流出道重建術,其次,導管分流手術是良好的選擇。Brimonidine禁用於2歲以下兒童,使用抗代謝藥物可能惡化AAK,因此需謹慎判斷8)。
CQ5:強烈建議實施低視力照護8)。
屈光矯正是基本,近視的合併率據報導為64%以上。
CQ6:強烈建議進行畏光治療8)。
大多數患者可以進入普通班級就讀,但需要放大教科書、平板電腦、書架等輔助。也可以選擇進入弱視班,或利用盲校/視覺特別支援學校的育兒諮詢和教育諮詢。
自2017年4月起,該病被認定為指定難病,因此即使未取得身心障礙手冊,重症度Ⅲ度以上的患者也可享受醫療費補助和輔具提供7)。適用的輔具包括矯正眼鏡、遮光眼鏡、隱形眼鏡(含人工虹膜型)、弱視眼鏡、視覺障礙者安全手杖和義眼。
PAX6跨越22 kb的基因組DNA,包含14個外顯子,編碼422個胺基酸1)。它具有兩個DNA結合結構域(配對結構域和配對型同源結構域),C端的PST(富含脯胺酸、絲胺酸、蘇胺酸)結構域作為轉錄活化因子發揮作用。
PAX6調控細胞的增殖、分化、遷移和黏附,其標靶包括PAX6自身以及編碼晶狀體蛋白和角膜角蛋白的基因。在成人的視網膜、晶狀體和角膜中持續表現。PAX6是調控胚胎期器官分化的主控基因之一。
大多數PAX6突變通過無義介導的mRNA降解(NMD)導致單倍劑量不足1)。引入提前終止密碼子(PTC)的突變(無義突變、框移突變和大多數剪接突變)會導致典型的無虹膜症表型。
另一方面,如果PTC位於最後一個外顯子或倒數第二個外顯子的末端50 bp以內,則可能逃逸NMD,轉譯出截短蛋白,可能導致嚴重表型1)。
曾有罕見病例報導,同一患者同時存在PAX6無義突變c.282C>A(p.Cys94*)和21三體症。PAX6突變是新發突變,表現為完全雙眼無虹膜、先天性青光眼、AAK和中心凹發育不全2)。
雖然尚未建立明確的基因型-表型相關性,但已知一些趨勢1)。
Grant和Walton的隅角鏡檢查系列顯示,早期虹膜基質向前延伸至小樑網上形成沾黏樣附著,逐漸呈片狀並最終導致隅角閉塞14)。此機制是青光眼發生的主要原因。病理學基礎是虹膜根部保留的平滑肌缺損和隅角發育不全。
AAK主要由角膜緣幹細胞缺乏(LSCD)引起,但角膜上皮異常分化和黏附異常、結膜細胞浸潤以及淚液分泌不足也參與其中。由PAX6調節的基質金屬蛋白酶9(MMP-9)缺乏導致纖維蛋白積聚和發炎細胞浸潤,基質膠原排列紊亂導致透明性喪失。
AAK分為5期。I期僅周邊上皮異常,II期向心性上皮改變(未達中央),III期中央角膜上皮改變和周邊淺層新生血管,IV期全角膜淺層新生血管,V期全角膜上皮異常和深層基質疤痕10)。
PAX6突變狀態與AAK進展相關。攜帶PTC或C末端延長突變的患者AAK呈年齡依賴性進展,而其他突變類型可能表現為非進行性角膜病變11)。
Gillespie症候群由ITPR1基因突變引起3)。ITPR1是IP3受體家族成員,形成Ca²⁺釋放通道並定位於內質網。顯性負性突變影響虹膜括約肌的形成和維持,導致瞳孔周圍特異性虹膜發育不全和固定性瞳孔散大。
Ciaccio等人(2024)的Gillespie症候群文獻回顧中,對33例分子確診病例的分析證實,運動發育延遲但隨時間改善,並非所有病例均有智力障礙(17%智力正常),神經學徵象為非進行性3)。
隨著全外顯子組定序技術的普及,新的PAX6突變持續被鑑定。截至2018年,人類PAX6突變資料庫已登記491個突變,此後又報告了約250個新突變1)。非編碼區的突變也被確定為無虹膜症的原因,有望闡明傳統檢測無法診斷的病例9)。
對於伴有嚴重AAK的病例,使用吊燈式逆照明輔助的可視化技術在白內障手術中很有用4)。該技術即使在3~4級高度AAK患者中也能安全進行超聲乳化吸除術,並已獲得術後視力改善。
PAX6突變的類型不同,AAK的進展模式也有所不同。隨著基因檢測成本的降低,基於突變類型的臨床病程預測和早期干預正成為現實的選擇。
在無虹膜症合併21三體症候群的病例中,儘管兩種疾病共存,但已有報告顯示病程相對較輕2)。理解多種遺傳障礙在同一患者中共存時對表型的影響,可能為未來的個人化醫療提供重要見解。
針對PTC型突變的通讀藥物(ataluren)在無虹膜症中的應用正在基礎研究層面進行探討8)。關於PAX6基因治療,使用AAV-PAX6載體對Sey突變小鼠模型進行基因補充的基礎研究正在進行中。期待未來向臨床試驗的轉化。
iPS細胞來源的角膜上皮細胞片移植的臨床試驗正在國內外進行,作為AAK的新療法備受關注8)。人工虹膜(如CustomFlex Artificial Iris等)在海外已有使用經驗累積。作為輔助器具,帶人工虹膜的隱形眼鏡屬於保險給付範圍。
根據診療指引(2021年),透過累積日本國內大規模註冊數據來掌握實際情況,並基於證據品質的提高修訂指引,被定位為未來的重要課題8)。期待基於個體基因突變的AAK進展預測和早期干預的最佳化。