Aniridia Isolada
Frequência: Cerca de 2/3 do total.
Padrão de herança: Autossômico dominante (AD).
Características: Causada por mutação no gene PAX6. Sem sintomas sistêmicos. Penetrância completa, mas expressividade variável.

Aniridia é uma doença congênita rara caracterizada por hipoplasia ou defeito da íris em vários graus. O nome “aniridia” é um equívoco, pois fragmentos de tecido da íris são quase sempre observáveis por gonioscopia ou microscopia ultrassônica (UBM).
A prevalência é de aproximadamente 1/40.000 a 1/100.000, sem diferenças raciais ou de gênero significativas relatadas 1). Na CID-10, é classificada como Q13.1.
É uma doença pan-ocular que afeta não apenas a íris, mas também a córnea, o cristalino, o ângulo da câmara anterior, a fóvea e o nervo óptico 1), apresentando múltiplas complicações oculares que ameaçam a visão. O prognóstico visual é geralmente ruim, com acuidade corrigida em torno de 0,1. O reflexo pupilar está ausente, mas o reflexo de acomodação é preservado, e 60-90% dos casos são bilaterais.
Os três fenótipos a seguir são reconhecidos.
Aniridia Isolada
Frequência: Cerca de 2/3 do total.
Padrão de herança: Autossômico dominante (AD).
Características: Causada por mutação no gene PAX6. Sem sintomas sistêmicos. Penetrância completa, mas expressividade variável.
Síndrome de WAGR
Frequência: Parte dos casos esporádicos.
Padrão de herança: Deleção contígua de PAX6 e WT1.
Características: Associada a tumor de Wilms, anomalias geniturinárias e retardo mental. Risco de tumor de até 50%.
Síndrome de Gillespie
Frequência: Cerca de 2% do total.
Padrão de herança: Mutação no gene ITPR1.
Características: Associada a ataxia cerebelar e deficiência intelectual. Apresenta uma anomalia iriana característica com pupila fixa e dilatada 3).
A aniridia esporádica representa cerca de 1/3 do total de casos, causada por deleção de novo em 11p13 envolvendo PAX6. Se a deleção se estender ao gene WT1 adjacente, causa a síndrome de WAGR 1). 25-30% dos casos de aniridia esporádica desenvolvem tumor de Wilms, com risco relativo de 67.
PAX6 é o gene mestre controlador da formação ocular, envolvido no desenvolvimento do olho, tubo neural, bulbo olfatório, ilhotas de Langerhans do pâncreas e epitélio olfatório. A doença ocorre por perda de função de um alelo (haploinsuficiência), e a anormalidade em ambos os alelos é letal embrionária. Em 2017, foi designada como doença rara específica pela Lei de Doenças Raras, e casos com gravidade grau III ou superior (veja a seção de diagnóstico e exames para detalhes) são elegíveis para subsídio de custos médicos 7).
Casos esporádicos (mutações novas) representam cerca de um terço de todos os casos e podem ocorrer sem histórico familiar. Em casos esporádicos, há possibilidade de síndrome de WAGR, portanto, o teste genético e a triagem de tumor de Wilms com ultrassom abdominal são importantes.
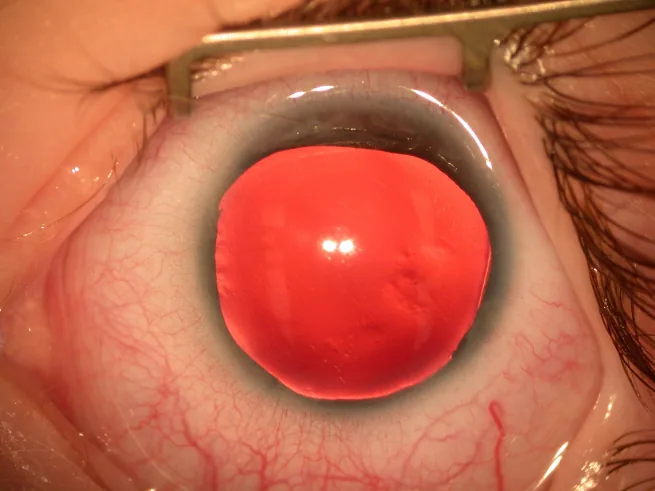
A maioria dos casos de aniridia é descoberta ao nascimento devido a anormalidades da íris/pupila, ou na infância devido ao nistagmo.
O fenótipo varia entre famílias e dentro de uma mesma família, mas a diferença entre os olhos direito e esquerdo geralmente é pequena.
Devido principalmente à hipoplasia foveal, a acuidade visual corrigida é frequentemente em torno de 0,1 a 0,2. O prognóstico visual é particularmente ruim quando há hipoplasia macular. A correção refrativa e os cuidados com baixa visão desde a primeira infância são importantes para o desenvolvimento visual.
Como o PAX6 também é expresso no sistema nervoso central, nas ilhotas de Langerhans do pâncreas e no epitélio olfatório, as seguintes complicações extraoculares podem ocorrer 8).
Os fatores determinantes da função visual são glaucoma, hipoplasia macular, nistagmo, ceratopatia, catarata e anomalias da íris. Como o dano ao campo visual e a perda de visão causados pelo glaucoma são irreversíveis, o manejo da pressão intraocular é o mais importante no acompanhamento8).
A maioria dos casos de aniridia congênita é causada por mutações heterozigóticas no gene PAX6 localizado no braço curto do cromossomo 11 (11p13). O principal mecanismo da doença é a haploinsuficiência1).
O gene PAX6 é um gene mestre controlador da formação ocular, desempenhando um papel importante no desenvolvimento do olho, tubo neural, bulbo olfatório e pâncreas. O desenvolvimento ocular normal requer duas cópias do PAX6, e a perda de função de apenas uma cópia já causa aniridia1).
Em um estudo de coorte de pacientes chineses, mutações causadoras no gene PAX6 foram identificadas em 96,9% dos casos1). Na aniridia típica, mutações que induzem degradação de mRNA dependente de mutação sem sentido (NMD) ou deleções grandes são detectadas em 96% dos casos1).
Patologicamente, há deficiência de músculo liso com preservação da raiz da íris, e observa-se disgenesia do ângulo. Há disfunção das células-tronco epiteliais da córnea, causando anormalidades no epitélio e na membrana de Bowman, e formação de pannus rico em vasos.
Abaixo está a distribuição das mutações do PAX6 que causam o fenótipo de aniridia.
| Tipo de mutação | Frequência |
|---|---|
| Mutação sem sentido (nonsense) | Cerca de 39% |
| Mutação de deslocamento de quadro (frameshift) | Cerca de 25% |
| Mutação de sítio de splicing | Cerca de 13% |
| Mutação de sentido trocado (missense) | Cerca de 12% |
Mutações run-on (mutações de extensão C-terminal) representam cerca de 5%, nas quais o códon de parada é convertido em um códon de tradução, resultando em uma proteína PAX6 anormalmente estendida 6). Mutações de extensão C-terminal frequentemente estão associadas a hipoplasia grave da íris e comprometimento visual severo 1)6).
As mutações genéticas são predominantemente do tipo PTC, e também há relatos de mutações missense 7). Quanto à utilidade do teste genético, o sequenciamento Sanger ou NGS detecta mutações em quase 85% dos casos de aniridia isolada. Além disso, MLPA ou CMA detectam deleções dentro do gene PAX6 ou na região cis-regulatória em quase 15% dos casos 8).
Wang (2023) identificou uma nova mutação de deslocamento de quadro c.640_646del (p.R214Pfs*28) e relatou um caso apresentando ausência total da íris, hipoplasia foveal, deslocamento do cristalino e descolamento de retina 1).
Ratna et al. (2022) identificaram uma mutação run-on c.1268A>T (p.*423L) em uma família indiana. Os indivíduos afetados apresentaram aniridia total, nistagmo, hipoplasia foveal, AAK, subluxação superior do cristalino, miopia alta e atrofia do nervo óptico, indicando um fenótipo grave devido à mutação de extensão C-terminal 6).
Na aniridia esporádica, uma grande deleção que inclui o gene WT1 além do PAX6 causa a síndrome de WAGR. O risco de tumor de Wilms é de até 50% na presença de deleção do WT1 1). Se houver suspeita de síndrome de WAGR, o teste genético pode confirmar a deficiência de PAX6 e WT1, permitindo a avaliação do risco de tumor de Wilms e o acompanhamento do atraso no desenvolvimento 8). A avaliação da região WT1 por teste genético é essencial, e 30% dos casos esporádicos desenvolvem tumor de Wilms antes dos 5 anos de idade. Como o gene WT1 está localizado próximo ao PAX6, a deleção do braço curto do cromossomo 11 (deleção 11p13) que inclui ambos os genes causa aniridia associada a tumor de Wilms.
A síndrome de Gillespie é causada por mutações heterozigóticas dominantes negativas ou mutações bialélicas no gene ITPR1 3). Até o momento, 37 casos foram confirmados molecularmente, e o resíduo Gly2554 é conhecido como um ponto crítico 3).
Com base nos critérios diagnósticos de aniridia (2020), o diagnóstico é confirmado pelos seguintes critérios7).
A. Sintomas
B. Achados de Exame
C. Doenças a serem diferenciadas
E. Exame genético: Mutação patogênica no gene PAX6 ou deleção na região 11p13
Categorias de diagnóstico7):
A classificação de gravidade para designação de doença rara é definida em quatro níveis conforme abaixo7).
| Gravidade | Definição |
|---|---|
| Grau I | Um olho afetado, o outro olho normal |
| Grau II | Ambos os olhos afetados, melhor acuidade visual corrigida ≥ 0,3 |
| Grau III | Ambos os olhos afetados, melhor acuidade visual corrigida ≥ 0,1 e < 0,3 |
| Grau IV | Ambos os olhos afetados, melhor acuidade visual corrigida < 0,1 |
Mesmo nos graus I a III, se houver estreitamento do campo visual devido a glaucoma ou outra condição (campo visual central remanescente ≤ 20 graus com o alvo Goldmann I/4), a gravidade é elevada em um grau. Grau III ou superior é elegível para subsídio de custos médicos 7).
O diagnóstico clínico é fácil se a ausência ou hipoplasia da íris for confirmada por lâmpada de fenda. O tecido iriano remanescente é avaliado por gonioscopia ou microscopia ultrassônica biomicroscópica. Anomalias de desenvolvimento do ângulo da câmara anterior também são verificadas.
As seguintes complicações oculares são avaliadas sistematicamente:
O objetivo mais importante na avaliação genética da aniridia é confirmar se a deleção do PAX6 se estende ao gene WT11). Mutações e deleções nas regiões PAX6 e WT1 são avaliadas por sequenciamento do exoma completo ou MLPA1)2).
Na aniridia esporádica, a avaliação do risco de tumor de Wilms devido à deleção do gene WT1 está diretamente ligada ao prognóstico de vida1). Mesmo nos casos familiares, devido à variabilidade fenotípica, recomenda-se diagnóstico definitivo por teste genético e aconselhamento genético.
Não existe terapia curativa para aniridia. O tratamento concentra-se em cuidados de baixa visão para maximizar a visão residual e tratamento individualizado para cada complicação. As diretrizes clínicas (2021) fornecem recomendações com base em 6 questões clínicas8).
CQ1: Recomenda-se fracamente não realizar transplante de córnea para opacidade do estroma corneano8).
O transplante de córnea pode proporcionar melhora visual em curto prazo, mas a melhora é limitada devido a complicações como hipoplasia macular. A longo prazo, o prognóstico visual é ruim devido à progressão do glaucoma e falência do enxerto.
CQ2: A cirurgia para deficiência de células-tronco epiteliais da córnea é fracamente recomendada 8).
CQ3: A cirurgia de catarata é fracamente recomendada 8).
A catarata ocorre em 50-85% dos casos antes dos 20 anos. A cirurgia é planejada com base na intensidade da opacidade e fotofobia. Relata-se melhora visual em 66-100% dos casos operados, mas os seguintes pontos requerem atenção.
Devido à fragilidade das zônulas de Zinn, a inserção de lente intraocular requer indicação cautelosa.
Hu et al. (2024) realizaram facoemulsificação assistida por iluminação posterior tipo candelabro em dois casos de aniridia congênita com AAK grave. A visualização intraoperatória usual era difícil devido à opacidade corneana, mas a iluminação posterior permitiu visualização clara do cristalino e da cápsula anterior, e a acuidade visual corrigida melhorou para 20/200 e 20/1000 em 3 semanas de pós-operatório 4).
CQ4: Recomenda-se fortemente a realização do tratamento do glaucoma 8).
Após o início do glaucoma, o manejo é baseado no algoritmo de 5 etapas a seguir.
Terapia medicamentosa: Betabloqueadores, estimulantes simpáticos e medicamentos relacionados à prostaglandina são eficazes. Brimonidina (estimulante do receptor alfa-adrenérgico) é contraindicada em menores de 2 anos devido ao risco de depressão do sistema nervoso central. Se houver preocupação com dano ao epitélio corneano, use preparações sem conservantes.
Cirurgia de reconstrução da via de drenagem (goniotomia, trabeculotomia): Recomendada como cirurgia inicial 16). Há relatos de goniotomia profilática. No entanto, pode ser ineficaz em casos onde a íris residual cobre o trabéculo.
Cirurgia de filtração (trabeculectomia): Relatos limitados a poucos casos e médio-curto prazo. Os resultados tendem a ser ruins em olhos pediátricos, e a fístula ocular pós-operatória atinge cerca de 25% 13). Há também relatos de glaucoma maligno pós-operatório.
Cirurgia de implante de glaucoma (cirurgia de shunt tubular): Dispositivos tipo Baerveldt e Ahmed podem ser usados. Em olhos fáquicos, recomenda-se inserir o tubo tangencialmente, não em direção ao centro da córnea. Pode-se esperar bom controle da pressão intraocular.
Ciclofotocoagulação: Último recurso. Há relatos de que a criocoagulação do corpo ciliar levou a fístula ocular em muitos casos. Devido à hipoplasia do corpo ciliar, o risco de fístula ocular é maior do que em olhos normais.
Devido a anormalidades no desenvolvimento do ângulo, é necessária uma abordagem diferente do glaucoma de ângulo aberto usual. Inicialmente, opta-se pela cirurgia de reconstrução da via de drenagem, e em seguida a cirurgia de derivação tubular é uma boa opção. A brimonidina é contraindicada em menores de 2 anos, e o uso de antimetabólitos pode piorar a AAK, exigindo julgamento cuidadoso 8).
CQ5: Recomenda-se fortemente a realização de cuidados com baixa visão 8).
A correção refrativa é básica, e a taxa de complicação de miopia é relatada em mais de 64%.
CQ6: Recomenda-se fortemente o tratamento da fotofobia 8).
A maioria dos pacientes pode frequentar escolas regulares, mas necessita de suporte como livros didáticos ampliados, tablets e estantes para leitura. Alternativas incluem frequentar classes para baixa visão ou utilizar consultas de educação e cuidados infantis de escolas para cegos e escolas de apoio visual especializado.
Desde abril de 2017, esta doença foi designada como doença rara especificada, portanto, mesmo que o paciente não possua carteira de deficiência física, se a gravidade for grau III ou superior, ele se torna elegível para subsídio de custos médicos e fornecimento de órteses e próteses 7). As órteses e próteses elegíveis incluem óculos corretivos, óculos de proteção contra luz, lentes de contato (incluindo as com íris artificial), óculos para baixa visão, bengala de segurança para deficientes visuais e olho artificial.
O gene PAX6 abrange 22 kb de DNA genômico contendo 14 éxons e codifica 422 aminoácidos 1). Possui dois domínios de ligação ao DNA (domínio pareado e homeodomínio pareado), e o domínio PST (rico em prolina, serina e treonina) na extremidade C funciona como ativador da transcrição.
PAX6 regula a proliferação, diferenciação, migração e adesão celular, e seus alvos incluem o próprio PAX6, bem como genes que codificam cristalinas do cristalino e queratinas da córnea. A expressão continua na retina, cristalino e córnea de adultos. O gene PAX6 é um dos genes mestres de controle que governam a diferenciação de órgãos durante o período embrionário.
A maioria das mutações no PAX6 causa haploinsuficiência através da degradação do mRNA dependente de nonsense-mediated decay (NMD) 1). Mutações que introduzem um códon de parada prematuro (PTC) (mutações nonsense, mutações de deslocamento de quadro e a maioria das mutações de splicing) resultam no fenótipo típico de aniridia.
Por outro lado, se o PTC estiver localizado no último éxon ou dentro de 50 bp do final do penúltimo éxon, pode escapar do NMD e produzir uma proteína truncada que pode causar um fenótipo grave 1).
Foi relatado um caso raro de mutação nonsense no PAX6 c.282C>A (p.Cys94*) concomitante com trissomia do 21 no mesmo paciente. A mutação PAX6 ocorreu de novo e resultou em aniridia bilateral completa, glaucoma congênito, AAK e hipoplasia foveal 2).
Embora não haja uma correlação genótipo-fenótipo clara estabelecida, algumas tendências são conhecidas 1).
Na série de gonioscopia de Grant e Walton, foi demonstrado que o estroma da íris se estende anteriormente sobre a malha trabecular formando uma aderência semelhante a sinéquia, que gradualmente se torna em forma de folha e eventualmente leva à oclusão angular 14). Esse mecanismo é o principal fator para o desenvolvimento do glaucoma. Patologicamente, a base é um defeito do músculo liso com raiz da íris remanescente e disgenesia angular.
AAK é causada principalmente por deficiência de células-tronco do limbo (LSCD), mas também envolve diferenciação anormal do epitélio corneano, adesão anormal, infiltração de células conjuntivais e produção insuficiente de lágrimas. A deficiência de metaloproteinase de matriz 9 (MMP-9) regulada por PAX6 causa acúmulo de fibrina e infiltração de células inflamatórias, resultando em desarranjo da disposição do colágeno estromal e perda de transparência.
AAK é classificada em 5 estágios. Estágio I: anormalidade epitelial apenas periférica. Estágio II: alterações epiteliais centrípetas (ainda não atingindo o centro). Estágio III: alterações epiteliais na córnea central e neovascularização superficial periférica. Estágio IV: neovascularização superficial de toda a córnea. Estágio V: anormalidade epitelial de toda a córnea e cicatriz estromal profunda 10).
Há uma relação entre o status da mutação PAX6 e a progressão da AAK. Em pacientes com mutações PTC ou extensão C-terminal, a AAK progride de forma dependente da idade, enquanto em outros tipos de mutação, pode ocorrer ceratopatia não progressiva 11).
A síndrome de Gillespie é causada por mutações no gene ITPR1 3). ITPR1 é um membro da família de receptores IP3 que forma canais de liberação de Ca²⁺ e está localizado no retículo endoplasmático. Mutações dominantes negativas afetam a formação e manutenção do esfíncter da pupila, resultando em hipoplasia da íris específica ao redor da pupila e midríase fixa.
Na revisão da literatura sobre síndrome de Gillespie por Ciaccio et al. (2024), a análise de 33 casos confirmados molecularmente revelou que o desenvolvimento motor é atrasado, mas melhora com o tempo, a deficiência intelectual não está presente em todos os casos (17% têm inteligência normal) e os sinais neurológicos são não progressivos 3).
Com a disseminação da tecnologia de sequenciamento completo do exoma, a identificação de novas mutações no PAX6 continua. No Banco de Dados de Mutações PAX6 Humanas, 491 mutações foram registradas em 2018, e cerca de 250 novas mutações foram relatadas desde então 1). Mutações em regiões não codificantes também estão sendo identificadas como causa de aniridia, o que se espera que esclareça casos não diagnosticados por exames convencionais 9).
Em casos de cirurgia de catarata com AAK grave, a técnica de visualização assistida por iluminação retrógrada tipo candelabro é útil 4). Essa técnica permite facoemulsificação segura mesmo em pacientes com AAK grau 3-4, e a melhora da acuidade visual pós-operatória tem sido obtida.
Torna-se claro que os padrões de progressão da AAK diferem conforme o tipo de mutação no PAX6. Com a redução do custo dos testes genéticos, a predição do curso clínico com base no tipo de mutação e a intervenção precoce tornam-se opções realistas.
Em casos de aniridia coexistindo com trissomia do 21, foram relatados cursos relativamente leves apesar da presença de ambas as doenças 2). Compreender o impacto da coexistência de múltiplos distúrbios genéticos no fenótipo pode fornecer insights importantes para a medicina personalizada no futuro.
A aplicação do fármaco read-through (atalureno) para mutações do tipo PTC na aniridia está sendo investigada em nível de pesquisa básica 8). Quanto à terapia gênica do PAX6, pesquisas básicas sobre reposição gênica usando vetor AAV-PAX6 em modelo de camundongo mutante Sey estão em andamento. Espera-se que avance para ensaios clínicos no futuro.
Ensaios clínicos de transplante de folhas de células epiteliais da córnea derivadas de iPS estão sendo realizados nacional e internacionalmente, atraindo atenção como nova terapia para AAK 8). Quanto à íris artificial (como CustomFlex Artificial Iris), a experiência de uso no exterior está se acumulando. Lentes de contato com íris artificial como órtese são cobertas pelo seguro.
Nas diretrizes de prática clínica (2021), o acúmulo de dados de registro em larga escala no Japão para compreender a situação real e a revisão das diretrizes com base na melhoria da qualidade das evidências foram identificados como questões importantes para o futuro 8). Espera-se a otimização da predição da progressão da AAK com base em mutações genéticas individuais e da intervenção precoce.