Bệnh vô mống mắt đơn độc
Tần suất: Khoảng 2/3 tổng số.
Kiểu di truyền: Trội trên nhiễm sắc thể thường (AD).
Đặc điểm: Do đột biến gen PAX6. Không kèm triệu chứng toàn thân. Tính thâm nhập hoàn toàn nhưng biểu hiện đa dạng.

Vô mống mắt (Aniridia) là một bệnh bẩm sinh hiếm gặp, đặc trưng bởi thiểu sản hoặc khiếm khuyết mống mắt ở nhiều mức độ. Tên gọi “vô mống mắt” là một cách gọi sai, vì các mảnh mô mống mắt hầu như luôn có thể quan sát được bằng kính soi góc tiền phòng (gonioscopy) hoặc kính hiển vi siêu âm (UBM).
Tỷ lệ mắc khoảng 1/40.000 đến 1/100.000, không có sự khác biệt đáng kể về chủng tộc hoặc giới tính được báo cáo 1). Trong ICD-10, được phân loại là Q13.1.
Đây là một bệnh toàn nhãn cầu (pan-ocular) không chỉ ảnh hưởng đến mống mắt mà còn đến giác mạc, thủy tinh thể, góc tiền phòng, hố trung tâm và thần kinh thị giác 1), biểu hiện với nhiều biến chứng mắt đe dọa thị lực. Tiên lượng thị lực nhìn chung xấu, thị lực điều chỉnh thường khoảng 0,1. Phản xạ đồng tử biến mất nhưng phản xạ điều tiết (accommodation) được bảo tồn, và 60-90% trường hợp là hai bên.
Ba kiểu hình sau đây đã được xác nhận.
Bệnh vô mống mắt đơn độc
Tần suất: Khoảng 2/3 tổng số.
Kiểu di truyền: Trội trên nhiễm sắc thể thường (AD).
Đặc điểm: Do đột biến gen PAX6. Không kèm triệu chứng toàn thân. Tính thâm nhập hoàn toàn nhưng biểu hiện đa dạng.
Hội chứng WAGR
Tần suất: Một phần trong các ca lẻ tẻ.
Kiểu di truyền: Mất đoạn liền kề của PAX6 và WT1.
Đặc điểm: Kèm u Wilms, bất thường sinh dục niệu và chậm phát triển tâm thần. Nguy cơ u lên tới 50%.
Hội chứng Gillespie
Tần suất: Khoảng 2% tổng số.
Kiểu di truyền: Đột biến gen ITPR1.
Đặc điểm: Kèm mất điều hòa tiểu não và khuyết tật trí tuệ. Biểu hiện bất thường mống mắt đặc trưng với đồng tử cố định và giãn 3).
Vô mống mắt lẻ tẻ chiếm khoảng 1/3 tổng số ca, do mất đoạn de novo trên 11p13 bao gồm PAX6. Nếu mất đoạn mở rộng đến gen WT1 lân cận, sẽ gây hội chứng WAGR 1). 25-30% ca vô mống mắt lẻ tẻ phát triển u Wilms, với nguy cơ tương đối là 67.
PAX6 là gen kiểm soát chính của sự hình thành mắt, tham gia vào phát triển mắt, ống thần kinh, hành khứu giác, đảo Langerhans tụy và biểu mô khứu giác. Bệnh xảy ra do mất chức năng một alen (haploinsufficiency), và nếu cả hai alen bất thường sẽ gây chết phôi. Năm 2017, bệnh được chỉ định là bệnh hiếm gặp cụ thể theo Luật Bệnh Hiếm, và các trường hợp có mức độ nặng từ độ III trở lên (xem phần chẩn đoán và xét nghiệm để biết chi tiết) đủ điều kiện nhận hỗ trợ chi phí y tế 7).
Các trường hợp lẻ tẻ (đột biến mới) chiếm khoảng 1/3 tổng số ca và có thể xảy ra mà không có tiền sử gia đình. Ở các trường hợp lẻ tẻ, có khả năng mắc hội chứng WAGR, do đó xét nghiệm di truyền và siêu âm bụng để tầm soát u Wilms là rất quan trọng.
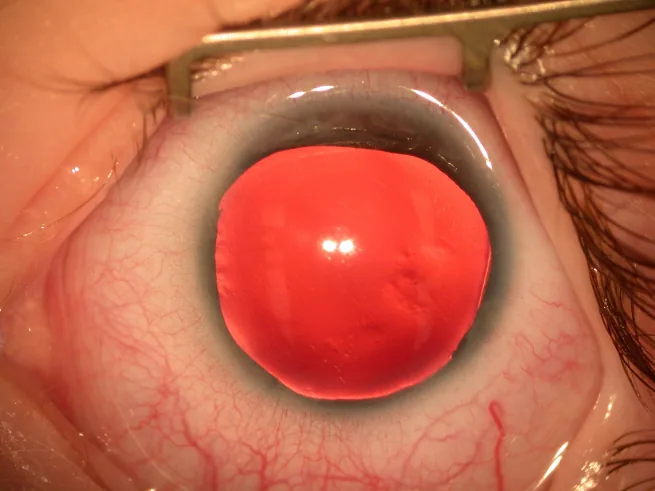
Hầu hết các trường hợp vô mống mắt được phát hiện khi sinh do bất thường mống mắt/đồng tử, hoặc ở giai đoạn trẻ sơ sinh do rung giật nhãn cầu.
Kiểu hình khác nhau giữa các gia đình và trong cùng một gia đình, nhưng sự khác biệt giữa mắt phải và mắt trái thường nhỏ.
Chủ yếu do bất sản hố trung tâm, thị lực sau chỉnh kính thường khoảng 0,1-0,2. Tiên lượng thị lực đặc biệt xấu nếu có bất sản hoàng điểm. Chỉnh tật khúc xạ và chăm sóc thị lực kém từ giai đoạn sơ sinh rất quan trọng cho sự phát triển thị giác.
Vì PAX6 cũng được biểu hiện ở hệ thần kinh trung ương, đảo tụy Langerhans và biểu mô khứu giác, các biến chứng ngoài mắt sau đây có thể xảy ra 8).
Các yếu tố quyết định chức năng thị giác là glôcôm, bất sản hoàng điểm, rung giật nhãn cầu, bệnh lý giác mạc, đục thủy tinh thể và bất thường mống mắt. Vì tổn thương thị trường và suy giảm thị lực do glôcôm gây ra là không hồi phục, nên quản lý nhãn áp là quan trọng nhất trong theo dõi8).
Hầu hết các trường hợp vô mống mắt bẩm sinh là do đột biến dị hợp tử trên gen PAX6 nằm ở nhánh ngắn nhiễm sắc thể 11 (11p13). Cơ chế bệnh chính là bất hoạt một alen (haploinsufficiency)1).
Gen PAX6 là gen kiểm soát chính của sự hình thành mắt, đóng vai trò quan trọng trong sự phát triển của mắt, ống thần kinh, hành khứu giác và tuyến tụy. Sự phát triển bình thường của mắt cần hai bản sao của PAX6, và chỉ mất chức năng một bản sao đã gây ra vô mống mắt1).
Trong một nghiên cứu đoàn hệ bệnh nhân Trung Quốc, đột biến gây bệnh trên gen PAX6 được xác định ở 96,9% trường hợp1). Trong vô mống mắt điển hình, đột biến gây phân hủy mRNA phụ thuộc đột biến vô nghĩa (NMD) hoặc mất đoạn lớn được phát hiện ở 96% trường hợp1).
Về mặt bệnh lý, có sự thiếu hụt cơ trơn với phần gốc mống mắt còn lại, và quan sát thấy loạn sản góc. Có rối loạn chức năng tế bào gốc biểu mô giác mạc, gây bất thường ở biểu mô và màng Bowman, và hình thành màng tân mạch (pannus) giàu mạch máu.
Dưới đây là phân bố các đột biến PAX6 gây ra kiểu hình vô mống mắt.
| Loại đột biến | Tần suất |
|---|---|
| Đột biến vô nghĩa (nonsense) | Khoảng 39% |
| Đột biến dịch khung (frameshift) | Khoảng 25% |
| Đột biến vị trí nối (splice site) | Khoảng 13% |
| Đột biến sai nghĩa (missense) | Khoảng 12% |
Đột biến run-on (đột biến kéo dài đầu C) chiếm khoảng 5%, trong đó codon kết thúc được chuyển đổi thành codon dịch mã, dẫn đến sản xuất protein PAX6 kéo dài bất thường 6). Đột biến kéo dài đầu C thường đi kèm với thiểu sản mống mắt nặng và suy giảm thị lực nghiêm trọng 1)6).
Các đột biến gen chủ yếu là loại PTC, và cũng có báo cáo về đột biến sai nghĩa 7). Về tính hữu ích của xét nghiệm di truyền, giải trình tự Sanger hoặc NGS phát hiện đột biến ở gần 85% trường hợp vô mống mắt đơn độc. Ngoài ra, MLPA hoặc CMA phát hiện mất đoạn trong gen PAX6 hoặc vùng điều hòa cis ở gần 15% trường hợp 8).
Wang (2023) đã xác định một đột biến dịch khung mới c.640_646del (p.R214Pfs*28) và báo cáo một trường hợp biểu hiện mất hoàn toàn mống mắt, thiểu sản hố trung tâm, lệch thủy tinh thể và bong võng mạc 1).
Ratna và cộng sự (2022) đã xác định đột biến run-on c.1268A>T (p.*423L) trong một gia đình người Ấn Độ. Những người bị ảnh hưởng biểu hiện vô mống mắt hoàn toàn, rung giật nhãn cầu, thiểu sản hố trung tâm, AAK, bán trật thủy tinh thể lên trên, cận thị nặng và teo thần kinh thị giác, cho thấy kiểu hình nặng do đột biến kéo dài đầu C 6).
Trong vô mống mắt lẻ tẻ, mất đoạn lớn bao gồm gen WT1 ngoài PAX6 gây ra hội chứng WAGR. Nguy cơ u Wilms lên tới 50% nếu có mất đoạn WT1 1). Nếu nghi ngờ hội chứng WAGR, xét nghiệm di truyền có thể xác nhận sự thiếu hụt PAX6 và WT1, cho phép đánh giá nguy cơ u Wilms và theo dõi chậm phát triển 8). Đánh giá vùng WT1 bằng xét nghiệm di truyền là rất cần thiết, và 30% trường hợp lẻ tẻ phát triển u Wilms trước 5 tuổi. Do gen WT1 nằm gần PAX6, mất đoạn nhánh ngắn nhiễm sắc thể 11 (mất đoạn 11p13) bao gồm cả hai gen gây ra vô mống mắt kèm u Wilms.
Hội chứng Gillespie gây ra bởi các đột biến trội âm tính dị hợp tử hoặc đột biến hai alen trên gen ITPR1 3). Cho đến nay, 37 trường hợp đã được xác nhận về mặt phân tử, và gốc Gly2554 được biết đến như một điểm nóng 3).
Dựa trên tiêu chuẩn chẩn đoán bệnh vô mống mắt (2020), chẩn đoán được xác định theo các tiêu chí sau7).
A. Triệu chứng
B. Kết quả xét nghiệm
C. Các bệnh cần phân biệt
E. Xét nghiệm di truyền: Đột biến bệnh lý ở gen PAX6 hoặc mất đoạn vùng 11p13
Phân loại chẩn đoán7):
Phân loại mức độ nặng để xác nhận bệnh hiếm được quy định thành bốn mức như sau7).
| Mức độ nặng | Định nghĩa |
|---|---|
| Độ I | Một mắt bị ảnh hưởng, mắt kia bình thường |
| Độ II | Cả hai mắt bị ảnh hưởng, thị lực điều chỉnh tốt nhất ≥ 0,3 |
| Độ III | Cả hai mắt bị ảnh hưởng, thị lực điều chỉnh tốt nhất ≥ 0,1 và < 0,3 |
| Độ IV | Cả hai mắt bị ảnh hưởng, thị lực điều chỉnh tốt nhất < 0,1 |
Ngay cả ở độ I–III, nếu có hẹp thị trường do glôcôm hoặc bệnh khác (thị trường trung tâm còn lại ≤ 20 độ với thị kích Goldmann I/4), mức độ nặng sẽ tăng lên một bậc. Độ III trở lên đủ điều kiện nhận hỗ trợ chi phí y tế 7).
Chẩn đoán lâm sàng dễ dàng nếu xác nhận mống mắt thiếu hoặc bất sản bằng đèn khe. Mô mống mắt còn lại được đánh giá bằng soi góc tiền phòng hoặc kính hiển vi siêu âm sinh học. Các bất thường phát triển của góc tiền phòng cũng được kiểm tra.
Các biến chứng mắt sau đây được đánh giá một cách có hệ thống:
Mục tiêu quan trọng nhất trong đánh giá di truyền của bệnh vô mống mắt là xác nhận xem sự mất đoạn PAX6 có mở rộng đến gen WT1 hay không1). Các đột biến và mất đoạn ở vùng PAX6 và WT1 được đánh giá bằng giải trình tự toàn bộ exome hoặc MLPA1)2).
Trong bệnh vô mống mắt lẻ tẻ, đánh giá nguy cơ u Wilms do mất đoạn gen WT1 liên quan trực tiếp đến tiên lượng sống1). Ngay cả ở các trường hợp gia đình, do tính đa dạng kiểu hình, khuyến cáo chẩn đoán xác định bằng xét nghiệm di truyền và tư vấn di truyền.
Không có liệu pháp chữa khỏi cho bệnh vô mống mắt. Điều trị tập trung vào chăm sóc thị lực thấp để tận dụng tối đa thị lực còn lại và điều trị riêng cho từng biến chứng. Hướng dẫn lâm sàng (2021) đưa ra khuyến cáo dựa trên 6 câu hỏi lâm sàng8).
CQ1: Khuyến cáo yếu không thực hiện ghép giác mạc cho đục nhu mô giác mạc8).
Ghép giác mạc có thể cải thiện thị lực trong ngắn hạn, nhưng sự cải thiện bị hạn chế do các biến chứng như thiểu sản điểm vàng. Về lâu dài, tiên lượng thị lực kém do tiến triển của glôcôm và suy mảnh ghép.
CQ2: Phẫu thuật điều trị suy tế bào gốc biểu mô giác mạc được khuyến cáo yếu 8).
CQ3: Phẫu thuật đục thủy tinh thể được khuyến cáo yếu 8).
Đục thủy tinh thể xảy ra ở 50-85% trường hợp trước 20 tuổi. Phẫu thuật được lên kế hoạch dựa trên mức độ đục và sợ ánh sáng. Có báo cáo cải thiện thị lực ở 66-100% ca phẫu thuật, nhưng cần lưu ý các điểm sau.
Do dây chằng Zinn yếu, việc đặt thủy tinh thể nhân tạo cần chỉ định thận trọng.
Hu và cộng sự (2024) đã thực hiện phẫu thuật tán nhuyễn thủy tinh thể có hỗ trợ chiếu sáng ngược dạng đèn chùm trên hai trường hợp vô mống mắt bẩm sinh kèm AAK nặng. Việc quan sát trong phẫu thuật thông thường khó khăn do đục giác mạc, nhưng chiếu sáng từ phía sau giúp quan sát rõ thủy tinh thể và bao trước, và thị lực chỉnh kính cải thiện lên 20/200 và 20/1000 sau 3 tuần phẫu thuật 4).
CQ4: Khuyến cáo mạnh mẽ thực hiện điều trị glôcôm 8).
Sau khi khởi phát glôcôm, việc quản lý dựa trên thuật toán 5 bước sau đây.
Điều trị bằng thuốc: Thuốc chẹn beta, thuốc kích thích giao cảm và thuốc liên quan đến prostaglandin có hiệu quả. Brimonidine (thuốc kích thích thụ thể alpha-adrenergic) chống chỉ định ở trẻ dưới 2 tuổi do nguy cơ ức chế hệ thần kinh trung ương. Nếu lo ngại tổn thương biểu mô giác mạc, sử dụng chế phẩm không chứa chất bảo quản.
Phẫu thuật tái tạo đường dẫn lưu (mở góc tiền phòng, mở bè củng mạc): Được khuyến cáo là phẫu thuật đầu tay 16). Có báo cáo về mở góc tiền phòng dự phòng. Tuy nhiên, có thể không hiệu quả trong trường hợp mống mắt tồn dư che phủ vùng bè.
Phẫu thuật lọc (cắt bè củng mạc): Chỉ có báo cáo hạn chế trên một số ít trường hợp và trung hạn. Kết quả có xu hướng kém ở mắt trẻ em, và rò nhãn cầu sau phẫu thuật lên tới khoảng 25% 13). Cũng có báo cáo về glôcôm ác tính sau phẫu thuật.
Phẫu thuật cấy ghép glôcôm (phẫu thuật shunt ống): Có thể sử dụng thiết bị loại Baerveldt và Ahmed. Ở mắt còn thủy tinh thể, khuyến cáo đặt ống theo hướng tiếp tuyến, không hướng về trung tâm giác mạc. Có thể kỳ vọng kiểm soát nhãn áp tốt.
Đông lạnh thể mi: Biện pháp cuối cùng. Có báo cáo rằng đông lạnh thể mi dẫn đến rò nhãn cầu trong nhiều trường hợp. Do có giảm sản thể mi, nguy cơ rò nhãn cầu cao hơn mắt bình thường.
Do có bất thường phát triển góc tiền phòng, cần cách tiếp cận khác với glôcôm góc mở thông thường. Lúc đầu, chọn phẫu thuật tái tạo đường dẫn lưu, sau đó phẫu thuật shunt ống là lựa chọn tốt. Brimonidine chống chỉ định cho trẻ dưới 2 tuổi, và sử dụng thuốc kháng chuyển hóa có thể làm nặng thêm AAK, do đó cần cân nhắc thận trọng 8).
CQ5: Khuyến cáo mạnh mẽ thực hiện chăm sóc thị lực kém 8).
Chỉnh khúc xạ là cơ bản, tỷ lệ biến chứng cận thị được báo cáo trên 64%.
CQ6: Khuyến cáo mạnh mẽ điều trị chứng sợ ánh sáng 8).
Hầu hết bệnh nhân có thể học ở trường phổ thông, nhưng cần được hỗ trợ như sách giáo khoa phóng to, máy tính bảng và giá đọc sách. Các lựa chọn khác bao gồm học tại lớp dành cho người khiếm thị hoặc sử dụng dịch vụ tư vấn nuôi dạy trẻ và giáo dục từ trường dành cho người mù và trường hỗ trợ thị giác đặc biệt.
Kể từ tháng 4 năm 2017, bệnh này đã được chỉ định là bệnh hiếm, do đó ngay cả khi bệnh nhân chưa có thẻ khuyết tật thể chất, nếu mức độ nghiêm trọng từ độ III trở lên, họ sẽ đủ điều kiện nhận trợ cấp chi phí y tế và cung cấp dụng cụ chỉnh hình 7). Các dụng cụ chỉnh hình đủ điều kiện bao gồm kính điều chỉnh, kính chống ánh sáng, kính áp tròng (bao gồm loại có mống mắt nhân tạo), kính cho người khiếm thị, gậy an toàn cho người khiếm thị và mắt giả.
Gen PAX6 trải dài trên 22 kb DNA bộ gen bao gồm 14 exon và mã hóa 422 axit amin 1). Nó có hai vùng liên kết DNA (vùng ghép đôi và vùng homeo ghép đôi), và vùng PST (giàu proline, serine và threonine) ở đầu C hoạt động như một yếu tố hoạt hóa phiên mã.
PAX6 điều chỉnh sự tăng sinh, biệt hóa, di chuyển và kết dính của tế bào, và các mục tiêu của nó bao gồm chính PAX6 cũng như các gen mã hóa crystallin của thủy tinh thể và keratin của giác mạc. Sự biểu hiện tiếp tục ở võng mạc, thủy tinh thể và giác mạc của người trưởng thành. Gen PAX6 là một trong những gen kiểm soát chính điều phối sự biệt hóa cơ quan trong thời kỳ phôi thai.
Hầu hết các đột biến PAX6 gây ra bất hoạt đơn bội thông qua sự phân hủy mRNA phụ thuộc vào quá trình phân hủy qua trung gian vô nghĩa (NMD) 1). Các đột biến tạo ra mã kết thúc sớm (PTC) (đột biến vô nghĩa, đột biến dịch khung và hầu hết các đột biến nối) dẫn đến kiểu hình vô mống mắt điển hình.
Mặt khác, nếu PTC nằm ở exon cuối cùng hoặc trong vòng 50 bp tính từ cuối exon áp chót, nó có thể thoát khỏi NMD và tạo ra protein bị cắt ngắn có thể gây ra kiểu hình nghiêm trọng 1).
Một trường hợp hiếm gặp đã được báo cáo về đột biến vô nghĩa PAX6 c.282C>A (p.Cys94*) kết hợp với hội chứng tam nhiễm 21 trên cùng một bệnh nhân. Đột biến PAX6 xảy ra de novo và dẫn đến vô mống mắt hoàn toàn hai bên, glôcôm bẩm sinh, AAK và giảm sản hố trung tâm 2).
Mặc dù chưa thiết lập được mối tương quan kiểu gen – kiểu hình rõ ràng, nhưng một số xu hướng đã được biết đến 1).
Trong loạt nghiên cứu soi góc tiền phòng của Grant và Walton, cho thấy mô đệm mống mắt mở rộng ra phía trước trên lưới bè tạo thành sự bám dính giống như dính, dần dần trở thành dạng tấm và cuối cùng dẫn đến tắc góc 14). Cơ chế này là yếu tố chính gây ra bệnh tăng nhãn áp. Về mặt bệnh lý, nền tảng là khiếm khuyết cơ trơn với gốc mống mắt còn sót lại và loạn sản góc.
AAK chủ yếu do thiếu hụt tế bào gốc vùng rìa (LSCD), nhưng cũng liên quan đến biệt hóa biểu mô giác mạc bất thường, kết dính bất thường, xâm nhập tế bào kết mạc và sản xuất nước mắt không đủ. Sự thiếu hụt matrix metalloproteinase 9 (MMP-9) do PAX6 điều hòa gây tích tụ fibrin và xâm nhập tế bào viêm, dẫn đến rối loạn sắp xếp collagen nhu mô và mất độ trong suốt.
AAK được phân loại thành 5 giai đoạn. Giai đoạn I: chỉ bất thường biểu mô ngoại vi. Giai đoạn II: thay đổi biểu mô hướng tâm (chưa đến trung tâm). Giai đoạn III: thay đổi biểu mô giác mạc trung tâm và tân mạch nông ngoại vi. Giai đoạn IV: tân mạch nông toàn bộ giác mạc. Giai đoạn V: bất thường biểu mô toàn bộ giác mạc và sẹo nhu mô sâu 10).
Có mối liên quan giữa tình trạng đột biến PAX6 và sự tiến triển của AAK. Ở bệnh nhân có đột biến PTC hoặc kéo dài đầu C, AAK tiến triển phụ thuộc vào tuổi, trong khi ở các loại đột biến khác, có thể xuất hiện bệnh lý giác mạc không tiến triển 11).
Hội chứng Gillespie do đột biến gen ITPR1 gây ra 3). ITPR1 là thành viên của họ thụ thể IP3 hình thành kênh giải phóng Ca²⁺ và khu trú ở lưới nội chất. Đột biến trội âm ảnh hưởng đến sự hình thành và duy trì cơ thắt đồng tử, gây thiểu sản mống mắt đặc hiệu quanh đồng tử và giãn đồng tử cố định.
Trong bài tổng quan y văn về hội chứng Gillespie của Ciaccio và cộng sự (2024), từ phân tích 33 trường hợp được xác nhận phân tử, cho thấy sự phát triển vận động bị chậm nhưng cải thiện theo thời gian, khuyết tật trí tuệ không xảy ra ở tất cả các trường hợp (17% có trí thông minh bình thường), và các dấu hiệu thần kinh không tiến triển 3).
Với sự phổ biến của công nghệ giải trình tự toàn bộ exome, việc xác định các đột biến PAX6 mới vẫn tiếp tục. Trong Cơ sở dữ liệu đột biến PAX6 ở người, 491 đột biến đã được đăng ký vào năm 2018 và khoảng 250 đột biến mới đã được báo cáo kể từ đó 1). Các đột biến ở vùng không mã hóa cũng đang được xác định là nguyên nhân gây ra bệnh vô mống mắt, do đó hy vọng sẽ làm sáng tỏ các trường hợp không được chẩn đoán bằng xét nghiệm thông thường 9).
Trong phẫu thuật đục thủy tinh thể ở bệnh nhân có AAK nặng, kỹ thuật hình ảnh hỗ trợ chiếu sáng ngược dạng đèn chùm rất hữu ích 4). Kỹ thuật này cho phép tán nhuyễn thủy tinh thể an toàn ngay cả ở bệnh nhân có AAK độ 3-4, và cải thiện thị lực sau phẫu thuật đã đạt được.
Ngày càng rõ ràng rằng các mô hình tiến triển của AAK khác nhau tùy theo loại đột biến PAX6. Với chi phí xét nghiệm di truyền giảm, việc dự đoán diễn tiến lâm sàng dựa trên loại đột biến và can thiệp sớm đang trở thành những lựa chọn thực tế.
Trong các trường hợp vô mống mắt kết hợp với hội chứng Down, đã có báo cáo về diễn tiến tương đối nhẹ mặc dù có sự hiện diện của cả hai bệnh 2). Hiểu được tác động của sự cùng tồn tại của nhiều rối loạn di truyền lên kiểu hình có thể cung cấp những hiểu biết quan trọng cho y học cá thể hóa trong tương lai.
Việc ứng dụng thuốc đọc xuyên (ataluren) cho các đột biến loại PTC trong bệnh vô mống mắt đang được nghiên cứu ở cấp độ nghiên cứu cơ bản 8). Về liệu pháp gen PAX6, nghiên cứu cơ bản về thay thế gen bằng vector AAV-PAX6 trên mô hình chuột đột biến Sey đang được tiến hành. Hy vọng sẽ phát triển thành các thử nghiệm lâm sàng trong tương lai.
Các thử nghiệm lâm sàng về ghép tấm tế bào biểu mô giác mạc có nguồn gốc từ tế bào iPS đang được tiến hành trong và ngoài nước, thu hút sự chú ý như một liệu pháp mới cho AAK 8). Đối với mống mắt nhân tạo (như CustomFlex Artificial Iris), kinh nghiệm sử dụng ở nước ngoài đang được tích lũy. Kính áp tròng có mống mắt nhân tạo như một thiết bị hỗ trợ được bảo hiểm chi trả.
Trong hướng dẫn thực hành lâm sàng (2021), việc tích lũy dữ liệu đăng ký quy mô lớn tại Nhật Bản để hiểu thực trạng và sửa đổi hướng dẫn dựa trên cải thiện chất lượng bằng chứng được xác định là các vấn đề quan trọng trong tương lai 8). Dự kiến sẽ tối ưu hóa dự đoán tiến triển AAK dựa trên các đột biến gen riêng lẻ và can thiệp sớm.