Isolierte Aniridie
Häufigkeit: etwa 2/3 aller Fälle.
Erbgang: autosomal-dominant (AD).
Merkmale: verursacht durch PAX6-Genmutation. Keine systemischen Symptome. Penetranz vollständig, aber Expressivität variabel.

Aniridie ist eine seltene angeborene Erkrankung, die durch eine unterschiedlich ausgeprägte Unterentwicklung oder das Fehlen der Iris gekennzeichnet ist. Der Begriff „Aniridie“ ist eine Fehlbezeichnung, da bei der Gonioskopie oder Ultraschallbiomikroskopie (UBM) fast immer Irisgewebefragmente nachweisbar sind.
Die Prävalenz liegt bei etwa 1/40.000 bis 1/100.000, es wurden keine signifikanten Unterschiede bezüglich Rasse oder Geschlecht berichtet 1). In der ICD-10 wird sie unter Q13.1 klassifiziert.
Es handelt sich um eine panokuläre Erkrankung, die nicht nur die Iris, sondern auch Hornhaut, Linse, Kammerwinkel, Fovea und Sehnerv betrifft 1) und mit verschiedenen das Sehvermögen bedrohenden Augenkomplikationen einhergeht. Die Sehprognose ist im Allgemeinen schlecht, die korrigierte Sehschärfe bleibt oft bei etwa 0,1. Der Pupillenreflex fehlt, aber die Akkommodation ist erhalten, und 60–90 % der Fälle sind bilateral.
Die folgenden drei Phänotypen werden anerkannt.
Isolierte Aniridie
Häufigkeit: etwa 2/3 aller Fälle.
Erbgang: autosomal-dominant (AD).
Merkmale: verursacht durch PAX6-Genmutation. Keine systemischen Symptome. Penetranz vollständig, aber Expressivität variabel.
WAGR-Syndrom
Häufigkeit: ein Teil der sporadischen Fälle.
Erbgang: kontinuierliche Deletion von PAX6 und WT1.
Merkmale: assoziiert mit Wilms-Tumor, Urogenitalanomalien und geistiger Behinderung. Tumorrisiko bis zu 50%.
Gillespie-Syndrom
Häufigkeit: etwa 2% aller Fälle.
Erbgang: ITPR1-Genmutation.
Merkmale: assoziiert mit zerebellärer Ataxie und geistiger Behinderung. Charakteristisch ist eine spezifische Irisanomalie mit fixierter Mydriasis3).
Sporadische Aniridie macht etwa 1/3 aller Fälle aus und wird durch eine De-novo-Deletion von 11p13 einschließlich PAX6 verursacht. Wenn die Deletion das benachbarte WT1-Gen betrifft, führt dies zum WAGR-Syndrom1). 25–30% der sporadischen Aniridie entwickeln einen Wilms-Tumor, das relative Risiko wird mit 67 angegeben.
PAX6 ist ein Master-Kontrollgen der Augenbildung und an der Entwicklung von Auge, Neuralrohr, Riechkolben, Langerhans-Inseln der Bauchspeicheldrüse und Riechepithel beteiligt. Ein Funktionsverlust eines Allels (Haploinsuffizienz) führt zur Erkrankung; eine Anomalie beider Allele ist embryonal letal. 2017 wurde es als spezifizierte seltene Krankheit nach dem Seltene-Krankheiten-Gesetz eingestuft, und Fälle mit Schweregrad III oder höher (Einzelheiten siehe Abschnitt Diagnose und Untersuchungen) haben Anspruch auf Kostenübernahme für medizinische Behandlungen7).
Sporadische Fälle (Neumutationen) machen etwa ein Drittel aller Fälle aus und können ohne Familienanamnese auftreten. Bei sporadischen Fällen besteht die Möglichkeit eines WAGR-Syndroms, daher sind Gentests und ein abdominales Ultraschall-Screening auf Wilms-Tumor wichtig.
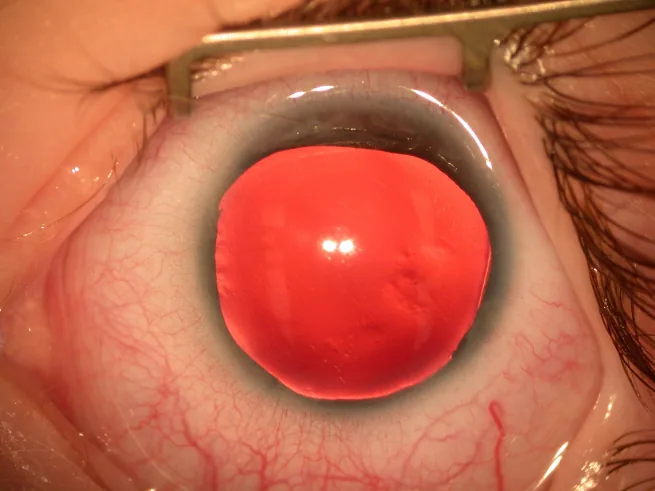
Die meisten Fälle von Aniridie werden bei der Geburt aufgrund einer Iris-/Pupillenanomalie oder im Säuglingsalter aufgrund von Nystagmus entdeckt.
Der Phänotyp variiert zwischen und innerhalb von Familien, aber die Unterschiede zwischen beiden Augen sind in der Regel gering.
Hauptsächlich aufgrund der fovealen Hypoplasie liegt die korrigierte Sehschärfe oft bei etwa 0,1–0,2. Bei gleichzeitiger Makulahypoplasie ist die Sehprognose besonders schlecht. Refraktionskorrektur und Sehbehindertenversorgung ab dem Säuglingsalter sind für die Sehentwicklung wichtig.
PAX6 wird nicht nur im Augengewebe, sondern auch im Zentralnervensystem, in den Langerhans-Inseln der Bauchspeicheldrüse und im Riechepithel exprimiert, daher können folgende extraokuläre Komplikationen auftreten 8).
Die entscheidenden Faktoren für die Sehfunktion sind Glaukom, Makulahypoplasie, Nystagmus, Hornhauterkrankung, Katarakt und Irisanomalie. Die durch Glaukom verursachten Gesichtsfeld- und Sehschärfenschäden sind irreversibel, daher ist das Augeninnendruckmanagement bei der Nachsorge von größter Bedeutung.8)
Die meisten angeborenen Aniridien werden durch heterozygote Mutationen im PAX6-Gen auf dem kurzen Arm von Chromosom 11 (11p13) verursacht. Haploinsuffizienz von PAX6 ist der Hauptmechanismus der Erkrankung.1)
Das PAX6-Gen ist ein Master-Kontrollgen für die Augenentwicklung und spielt eine wichtige Rolle bei der Entwicklung von Auge, Neuralrohr, Riechkolben und Bauchspeicheldrüse. Für die normale Augenentwicklung sind zwei Kopien von PAX6 erforderlich, und der Funktionsverlust einer einzigen Kopie reicht aus, um eine Aniridie zu verursachen.1)
In einer Kohortenstudie mit chinesischen Patienten wurden bei 96,9 % der Fälle ursächliche Mutationen im PAX6-Gen identifiziert.1) Bei typischer Aniridie werden in 96 % der Fälle Mutationen, die einen Nonsense-vermittelten mRNA-Abbau (NMD) induzieren, oder große Deletionen nachgewiesen.1)
Pathologisch fehlt die glatte Muskulatur mit Ausnahme der Iriswurzel, und es liegt eine Fehlentwicklung des Kammerwinkels vor. Es besteht eine Funktionsstörung der Hornhautepithel-Stammzellen, die zu Anomalien des Epithels und der Bowman-Membran führt, und es bildet sich ein gefäßreicher Pannus.
Die Verteilung der PAX6-Mutationen, die den Aniridie-Phänotyp verursachen, ist unten dargestellt.
| Mutationstyp | Häufigkeit |
|---|---|
| Nonsense-Mutation | Etwa 39 % |
| Rasterschubmutation | Etwa 25 % |
| Spleißmutation | Etwa 13 % |
| Missense-Mutation | Etwa 12 % |
Run-on-Mutationen (C-terminale Verlängerungsmutationen) machen etwa 5 % aus. Sie entstehen, wenn ein Stoppcodon in ein Translationscodon umgewandelt wird, wodurch ein abnormal verlängertes PAX6-Protein produziert wird 6). C-terminale Verlängerungsmutationen gehen häufig mit schwerer Iris-Hypoplasie und hochgradiger Sehbehinderung einher 1)6).
Genmutationen sind meist vom PTC-Typ, es wurden aber auch Missense-Mutationen berichtet 7). Zur Nützlichkeit von Gentests: Mittels Sanger-Sequenzierung oder NGS werden bei fast 85 % der isolierten Aniridie-Fälle Mutationen nachgewiesen. Zusätzlich werden mit MLPA oder CMA Deletionen im PAX6-Gen oder in der cis-regulatorischen Region bei fast 15 % der Fälle gefunden 8).
Wang (2023) identifizierte eine neue Frameshift-Mutation c.640_646del (p.R214Pfs*28) und berichtete über einen Fall mit vollständigem Irisdefekt, Foveahypoplasie, Linsenluxation und Netzhautablösung 1).
Ratna et al. (2022) identifizierten in einer indischen Familie eine Run-on-Mutation c.1268A>T (p.*423L). Die Betroffenen zeigten vollständige Aniridie, Nystagmus, Foveahypoplasie, AAK, Linsensubluxation nach oben, starke Myopie und Optikusatrophie, was den schweren Phänotyp bei C-terminalen Verlängerungsmutationen verdeutlicht 6).
Bei sporadischer Aniridie verursachen große Deletionen, die neben PAX6 auch das WT1-Gen umfassen, das WAGR-Syndrom. Bei WT1-Deletion beträgt das Wilms-Tumor-Risiko bis zu 50 % 1). Bei Verdacht auf WAGR-Syndrom kann ein Gentest die Deletionen von PAX6 und WT1 bestätigen, die Wilms-Tumor-Risikobewertung und die Überwachung von Entwicklungsverzögerungen ermöglichen 8). Die Bewertung der WT1-Region durch Gentests ist unerlässlich; 30 % der sporadischen Fälle entwickeln bis zum Alter von 5 Jahren einen Wilms-Tumor. Da das WT1-Gen in der Nähe von PAX6 liegt, führt eine Deletion des kurzen Arms von Chromosom 11 (11p13-Deletion) zu Aniridie in Kombination mit Wilms-Tumor.
Das Gillespie-Syndrom wird durch heterozygote dominant-negative oder biallelische Mutationen im ITPR1-Gen verursacht 3). Bisher wurden 37 molekulargenetisch bestätigte Fälle berichtet, und das Gly2554-Rest ist als Hotspot bekannt 3).
Gemäß den Diagnosekriterien für Aniridie (2020) wird die Diagnose anhand der folgenden Kriterien bestätigt 7).
A. Symptome
B. Untersuchungsbefunde
C. Differenzialdiagnosen
E. Genetische Tests : Pathogene Mutation im PAX6-Gen oder Deletion der Region 11p13
Diagnosekategorien7) :
Die Schweregradeinteilung für die Anerkennung als seltene Erkrankung ist in vier Stufen definiert7).
| Schweregrad | Definition |
|---|---|
| Grad I | Einseitige Erkrankung, das andere Auge gesund |
| Grad II | Beidseitige Erkrankung, korrigierter Visus des besseren Auges ≥ 0,3 |
| Grad III | Beidseitige Erkrankung, korrigierter Visus des besseren Auges ≥ 0,1 und < 0,3 |
| Grad IV | Beidseitige Erkrankung, korrigierter Visus des besseren Auges < 0,1 |
Auch bei Grad I–III wird der Schweregrad um eine Stufe erhöht, wenn eine Gesichtsfeldeinschränkung durch Glaukom vorliegt (zentrales Restgesichtsfeld ≤ 20° mit Goldmann I/4-Marke). Ab Schweregrad III besteht Anspruch auf medizinische Kostenunterstützung 7).
Die klinische Diagnose ist einfach, wenn mit der Spaltlampe ein Fehlen oder eine Hypoplasie der Iris bestätigt wird. Die Beurteilung des verbleibenden Irisgewebes erfolgt mittels Gonioskopie oder Ultraschallbiomikroskopie. Auch auf Entwicklungsanomalien des Kammerwinkels wird geprüft.
Systematische Beurteilung der folgenden Augenkomplikationen:
Das wichtigste Ziel der genetischen Beurteilung der Aniridie ist die Feststellung, ob die PAX6-Deletion bis zum WT1-Gen reicht1). Mittels Exom-Sequenzierung oder MLPA werden Mutationen/Deletionen in den PAX6- und WT1-Regionen bewertet1)2).
Bei sporadischer Aniridie ist die Beurteilung des Wilms-Tumor-Risikos durch WT1-Gendeletion direkt mit der Lebensprognose verbunden1). Auch bei familiären Fällen wird aufgrund der phänotypischen Vielfalt eine genetische Diagnose und genetische Beratung empfohlen.
Es gibt keine kausale Behandlung der Aniridie. Der Schwerpunkt der Behandlung liegt auf der Low-Vision-Versorgung zur bestmöglichen Nutzung des Restsehvermögens und der individuellen Behandlung jeder Komplikation. Die klinische Leitlinie (2021) enthält Empfehlungen basierend auf 6 klinischen Fragen8).
CQ1: Es wird schwach empfohlen, bei Hornhautstromatrübung keine Hornhauttransplantation durchzuführen8).
Eine Hornhauttransplantation kann kurzfristig die Sehschärfe verbessern, aber die Verbesserung ist aufgrund von Begleiterkrankungen wie Makulahypoplasie begrenzt. Langfristig führen das Fortschreiten des Glaukoms und Transplantatversagen zu einer schlechten Sehprognose.
CQ2: Eine chirurgische Behandlung bei Limbusstammzellinsuffizienz wird schwach empfohlen. 8)
CQ3: Eine Kataraktoperation wird schwach empfohlen. 8)
Katarakt entwickelt sich bei 50–85 % der Patienten bis zum 20. Lebensjahr. Die Operation wird je nach Trübungsgrad und Photophobie geplant. Eine Sehverbesserung wird bei 66–100 % der operierten Fälle berichtet, jedoch sind folgende Punkte zu beachten.
Aufgrund der Fragilität der Zinn-Zonula ist die Implantation einer Intraokularlinse nur mit Vorsicht indiziert.
Hu et al. (2024) führten bei zwei Patienten mit angeborener Aniridie und schwerer AAK eine Phakoemulsifikation unter Unterstützung einer Kronleuchter-Rückbeleuchtung durch. Aufgrund der Hornhauttrübung war die übliche intraoperative Visualisierung schwierig, aber die Beleuchtung von hinten ermöglichte eine klare Visualisierung der Linse und der Vorderkapsel, und die korrigierte Sehschärfe verbesserte sich 3 Wochen postoperativ auf 20/200 bzw. 20/1000 4).
CQ4: Eine Glaukombehandlung wird stark empfohlen 8).
Nach Auftreten des Glaukoms erfolgt die Behandlung nach folgendem 5-Stufen-Algorithmus.
Medikamentöse Therapie: Betablocker, Sympathomimetika und Prostaglandin (PG)-verwandte Medikamente sind wirksam. Brimonidin (Alpha-Adrenozeptor-Agonist) ist bei Säuglingen unter 2 Jahren aufgrund des Risikos einer ZNS-Depression kontraindiziert. Bei Bedenken hinsichtlich einer Hornhautepithelschädigung konservierungsmittelfreie Präparate verwenden.
Abflussrekonstruktion (Goniotomie, Trabekulotomie): Als Ersteingriff empfohlen 16). Es gibt auch Berichte über prophylaktische Goniotomie. Allerdings kann sie bei Fällen, in denen das restliche Irisgewebe das Trabekelwerk bedeckt, unwirksam sein.
Fistulierende Operation (Trabekulektomie): Nur wenige Kurz- und mittelfristige Berichte. Bei kindlichen Augen sind die Ergebnisse tendenziell schlecht, und postoperative Bulbusfisteln treten in etwa 25 % der Fälle auf 13). Es gibt auch Berichte über postoperatives malignes Glaukom.
Glaukom-Implantat-Operation (Tube-Shunt-Operation): Baerveldt- und Ahmed-Typ-Implantate sind verfügbar. Bei der Tubusinsertion in ein phakes Auge wird eine tangentiale statt einer zentralen Richtung zur Hornhaut empfohlen. Eine gute Augeninnendruckkontrolle ist zu erwarten.
Zyklokoagulation: Letzte Maßnahme. Bei der Kryokoagulation des Ziliarkörpers wurde häufig eine Bulbusfistel berichtet. Aufgrund der Ziliarkörperhypoplasie ist das Risiko einer Bulbusfistel höher als bei gesunden Augen.
Aufgrund der abnormalen Entwicklung des Kammerwinkels ist ein anderer Ansatz als beim normalen Offenwinkelglaukom erforderlich. Zunächst wird eine Abflusswegs-Rekonstruktion gewählt, anschließend ist die Tube-Shunt-Operation eine gute Option. Brimonidin ist bei Kindern unter 2 Jahren kontraindiziert, und die Verwendung von Antimetaboliten kann die AAK verschlechtern, daher ist eine sorgfältige Entscheidung erforderlich 8).
CQ5: Die Durchführung einer Low-Vision-Versorgung wird stark empfohlen 8).
Die Refraktionskorrektur ist grundlegend, und die Komplikationsrate der Myopie wird auf über 64 % geschätzt.
CQ6: Die Behandlung von Photophobie wird stark empfohlen 8).
Die meisten Patienten können eine Regelschule besuchen, benötigen jedoch Hilfsmittel wie vergrößerte Schulbücher, Tablets und Buchständer. Auch der Besuch einer Sehbehindertenklasse oder die Nutzung von Erziehungs- und Bildungsberatung durch Blindenschulen oder spezielle Sehförderschulen sind Optionen.
Seit April 2017 ist die Erkrankung als designierte seltene Krankheit anerkannt. Daher haben Patienten ab Schweregrad III auch ohne Schwerbehindertenausweis Anspruch auf Kostenübernahme für medizinische Behandlungen und Hilfsmittel 7). Zu den förderfähigen Hilfsmitteln gehören Korrekturbrillen, Sonnenschutzbrillen, Kontaktlinsen (einschließlich solcher mit künstlicher Iris), Sehbehindertenbrillen, Langstöcke für Sehbehinderte und Augenprothesen.
PAX6 erstreckt sich über 22 kb genomischer DNA mit 14 Exons und kodiert für 422 Aminosäuren 1). Es besitzt zwei DNA-Bindungsdomänen (Paired-Domäne und Paired-Homöodomäne) und eine C-terminale PST-Domäne (reich an Prolin, Serin und Threonin), die als Transkriptionsaktivator fungiert.
PAX6 reguliert Zellproliferation, -differenzierung, -migration und -adhäsion. Zu seinen Zielgenen gehören neben PAX6 selbst die Gene für Linsen-Crystalline und Hornhaut-Keratine. Die Expression bleibt in der adulten Netzhaut, Linse und Hornhaut bestehen. PAX6 ist eines der Master-Kontrollgene, die die embryonale Organentwicklung steuern.
Die meisten PAX6-Mutationen verursachen eine Haploinsuffizienz über den Nonsense-vermittelten mRNA-Abbau (NMD) 1). Mutationen, die ein vorzeitiges Stopcodon (PTC) einführen (Nonsense-, Frameshift- und die meisten Spleißmutationen), führen zum typischen Aniridie-Phänotyp.
Liegt das PTC hingegen im letzten Exon oder innerhalb der letzten 50 bp des vorletzten Exons, kann es dem NMD entgehen, und ein verkürztes Protein wird translatiert, was zu einem schweren Phänotyp führen kann 1).
Ein seltener Fall einer PAX6-Nonsense-Mutation c.282C>A (p.Cys94*) in Kombination mit einer Trisomie 21 bei einem Patienten wurde berichtet. Die PAX6-Mutation trat de novo auf und führte zu vollständiger bilateraler Aniridie, angeborenem Glaukom, AAK und Foveahypoplasie 2).
Obwohl keine eindeutige Genotyp-Phänotyp-Korrelation etabliert ist, sind einige Tendenzen bekannt 1).
In der Gonioskopie-Serie von Grant und Walton zeigte sich, dass das Irisstroma frühzeitig nach vorne auf das Trabekelwerk ausläuft und adhäsionsartige Anlagerungen bildet, die allmählich blattartig werden und schließlich zum Kammerwinkelverschluss führen 14). Dieser Mechanismus ist der Hauptfaktor für die Glaukomentstehung. Pathologisch liegen ein Defekt der glatten Muskulatur unter Erhalt der Iriswurzel und eine Kammerwinkeldysgenesie zugrunde.
AAK wird hauptsächlich durch einen Limbusstammzellmangel (LSCD) verursacht, aber auch abnorme Differenzierung des Hornhautepithels, Adhäsionsstörungen, Infiltration von Bindehautzellen und unzureichende Tränenproduktion sind beteiligt. Ein Mangel an Matrix-Metalloproteinase 9 (MMP-9), die durch PAX6 reguliert wird, führt zu Fibrinablagerung und Entzündungszellinfiltration, was die Kollagenanordnung im Stroma stört und zur Transparenzminderung führt.
AAK wird in 5 Stadien eingeteilt. Stadium I zeigt nur periphere Epithelanomalien, Stadium II zentripetale Epithelveränderungen (Zentrum nicht erreicht), Stadium III zentrale Epithelveränderungen und periphere oberflächliche Neovaskularisation, Stadium IV oberflächliche Neovaskularisation der gesamten Hornhaut, Stadium V totale Epithelanomalie und tiefe Stromanarbe 10).
Es besteht ein Zusammenhang zwischen dem PAX6-Mutationsstatus und dem Fortschreiten der AAK. Bei Patienten mit PTC- oder C-terminalen Verlängerungsmutationen schreitet die AAK altersabhängig fort, während andere Mutationstypen eine nicht-progressive Keratopathie verursachen können 11).
Das Gillespie-Syndrom wird durch Mutationen im ITPR1-Gen verursacht 3). ITPR1 gehört zur IP3-Rezeptorfamilie, bildet Ca²⁺-Freisetzungskanäle und ist im endoplasmatischen Retikulum lokalisiert. Dominant-negative Mutationen beeinträchtigen die Bildung und Aufrechterhaltung des Irissphinkters, was zu einer spezifischen Iris-Hypoplasie um die Pupille und einer fixierten Mydriasis führt.
In einer Literaturübersicht zum Gillespie-Syndrom von Ciaccio et al. (2024) zeigte die Analyse von 33 molekular bestätigten Fällen, dass die motorische Entwicklung verzögert ist, sich aber im Laufe der Zeit verbessert, eine geistige Behinderung nicht in allen Fällen vorliegt (17% haben normale Intelligenz) und die neurologischen Zeichen nicht progressiv sind 3).
Durch die Verbreitung der Ganzexom-Sequenzierung werden weiterhin neue PAX6-Mutationen identifiziert. Die Human PAX6 Mutation Database verzeichnete 2018 491 Mutationen, und seitdem wurden etwa 250 neue Mutationen berichtet 1). Auch Mutationen in nicht-kodierenden Regionen werden als Ursache für Aniridie identifiziert, was zur Aufklärung von Fällen beitragen könnte, die mit herkömmlichen Tests nicht diagnostiziert werden konnten 9).
Bei Kataraktoperationen in Fällen mit schwerer AAK ist die Visualisierungstechnik mit Hilfe einer Kronleuchter-Rückbeleuchtung nützlich 4). Diese Technik ermöglicht eine sichere Phakoemulsifikation auch bei Patienten mit hochgradiger AAK (Grad 3–4) und führt zu einer postoperativen Sehverbesserung.
Es wird zunehmend deutlich, dass die Art der PAX6-Mutation das Fortschreiten der AAK beeinflusst. Mit sinkenden Kosten für Gentests werden die Vorhersage des klinischen Verlaufs auf Basis des Mutationstyps und eine frühzeitige Intervention zu realistischen Optionen.
Bei Fällen mit gleichzeitigem Auftreten von Aniridie und Trisomie 21 wurden trotz des Vorliegens beider Erkrankungen relativ milde Verläufe berichtet 2). Das Verständnis der Auswirkungen des gleichzeitigen Vorliegens mehrerer genetischer Störungen bei einem Patienten auf den Phänotyp könnte wichtige Erkenntnisse für die zukünftige personalisierte Medizin liefern.
Die Anwendung des Read-through-Medikaments Ataluren bei PTC-Mutationen für die Aniridie wird auf Ebene der Grundlagenforschung untersucht 8). Für die PAX6-Gentherapie laufen Grundlagenforschungen zum Genersatz durch AAV-PAX6-Vektoren im Sey-Mausmodell. Eine Entwicklung hin zu klinischen Studien wird erwartet.
Klinische Studien zur Transplantation von aus iPS-Zellen gewonnenen Hornhautepithelzellschichten werden im In- und Ausland durchgeführt und als neue Therapie für AAK beachtet 8). Für künstliche Iris (z. B. CustomFlex Artificial Iris) sammelt sich im Ausland Erfahrung an. Kontaktlinsen mit künstlicher Iris sind als Hilfsmittel erstattungsfähig.
Laut der klinischen Leitlinie (2021) werden die Erfassung der tatsächlichen Situation durch die Sammlung großer Registerdaten in Japan und die Überarbeitung der Leitlinie auf Basis einer verbesserten Evidenzqualität als wichtige zukünftige Aufgaben angesehen 8). Die Optimierung der Vorhersage des AAK-Verlaufs und der frühzeitigen Intervention auf Basis individueller Genmutationen wird erwartet.