İzole Aniridi
Sıklık: Toplamın yaklaşık 2/3’ü.
Kalıtım şekli: Otozomal dominant (AD).
Özellikler: PAX6 gen mutasyonuna bağlıdır. Sistemik bulgu yoktur. Penetrans tamdır ancak ekspresyon değişkendir.

Aniridi, irisin değişen derecelerde hipoplazisi veya yokluğu ile karakterize nadir bir konjenital hastalıktır. “Aniridi” adı yanlış bir adlandırmadır; gonyoskopi veya ultrason biyomikroskopi (UBM) ile hemen her zaman iris doku parçaları görülür.
Prevalansı yaklaşık 1/40.000 ila 1/100.000’dir ve belirgin bir ırk veya cinsiyet farkı bildirilmemiştir 1). ICD-10’da Q13.1 olarak sınıflandırılır.
Sadece irisi değil, aynı zamanda kornea, lens, açı, fovea ve optik siniri de etkileyen pan-oküler bir hastalıktır 1) ve görmeyi tehdit eden çeşitli oküler komplikasyonlara yol açar. Görme prognozu genellikle kötüdür ve düzeltilmiş görme keskinliği çoğunlukla 0.1 civarındadır. Pupil refleksi kaybolmuştur ancak akomodasyon korunur ve vakaların %60-90’ı bilateraldir.
Aşağıdaki üç fenotip tanınmaktadır.
İzole Aniridi
Sıklık: Toplamın yaklaşık 2/3’ü.
Kalıtım şekli: Otozomal dominant (AD).
Özellikler: PAX6 gen mutasyonuna bağlıdır. Sistemik bulgu yoktur. Penetrans tamdır ancak ekspresyon değişkendir.
WAGR Sendromu
Sıklık: Sporadik vakaların bir kısmı.
Kalıtım şekli: PAX6 ve WT1’in bitişik delesyonu.
Özellikler: Wilms tümörü, genitoüriner anomali ve mental retardasyon eşlik eder. Tümör riski en fazla %50’dir.
Gillespie Sendromu
Sıklık: Toplamın yaklaşık %2’si.
Kalıtım şekli: ITPR1 gen mutasyonu.
Özellikler: Serebellar ataksi ve zihinsel engellilik eşlik eder. Fiks midriyazis ile karakterize spesifik iris anomalisi tipiktir3).
Sporadik aniridi toplamın yaklaşık 1/3’ünü oluşturur ve PAX6 dahil 11p13’te de novo delesyon sonucu oluşur. Bitişik WT1 genine kadar uzanan delesyon WAGR sendromuna neden olur1). Sporadik aniridinin %25-30’unda Wilms tümörü gelişir ve rölatif risk 67 olarak bildirilmiştir.
PAX6, göz oluşumunun ana kontrol genidir ve göz, nöral tüp, olfaktör bulb, pankreas Langerhans adacıkları ve olfaktör epitelin gelişiminde rol oynar. Tek alelin fonksiyon kaybı (haploinsufficiency) ile ortaya çıkar ve her iki alel anormal olduğunda embriyonik ölümle sonuçlanır. 2017 yılında Nadir Hastalıklar Yasası kapsamında belirlenmiş nadir hastalık haline gelmiştir ve şiddet derecesi III ve üzeri (detaylar için tanı ve test bölümüne bakınız) tıbbi masraf desteğine hak kazanır7).
Sporadik (yeni mutasyon) vakalar toplamın yaklaşık 1/3’ünü oluşturur ve aile öyküsü olmadan da ortaya çıkar. Sporadik vakalarda WAGR sendromu olasılığı nedeniyle genetik test ve abdominal ultrason ile Wilms tümörü taraması önemlidir.
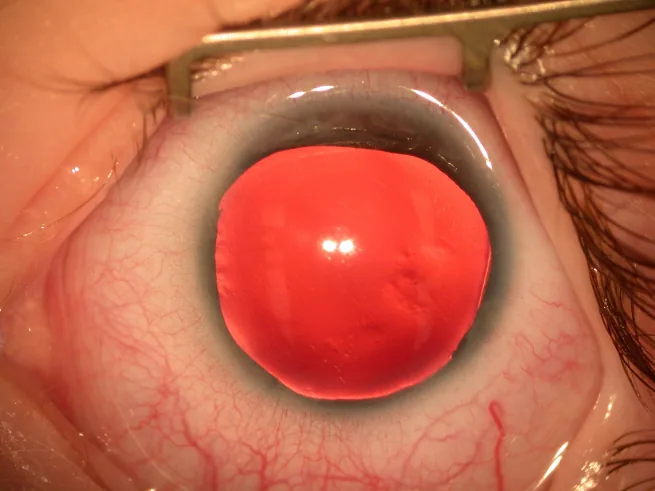
Aniridinin çoğu doğumda iris/pupilla anomalisi veya bebeklik döneminde nistagmus ile tespit edilir.
Fenotip aileler arasında ve aile içinde farklılık gösterebilir, ancak sağ ve sol göz arasındaki fark genellikle küçüktür.
Ana neden fovea hipoplazisidir ve düzeltilmiş görme keskinliği genellikle 0.1-0.2 civarındadır. Makula hipoplazisi eşlik ettiğinde görme prognozu özellikle kötüdür. Bebeklikten itibaren refraksiyon düzeltmesi ve az görme rehabilitasyonu görsel gelişim için önemlidir.
PAX6, göz dokusunun yanı sıra merkezi sinir sistemi, pankreas Langerhans adacıkları ve koku epitelinde de eksprese edildiğinden, aşağıdaki göz dışı komplikasyonlar görülebilir 8).
Görme keskinliğini belirleyen önemli faktörler glokom, makula hipoplazisi, nistagmus, keratopati, katarakt ve iris anomalileridir. Glokoma bağlı görme alanı ve görme keskinliği kaybı geri dönüşümsüz olduğundan, takipte göz içi basıncı yönetimi en önemli unsurdur8).
Konjenital aniridi vakalarının çoğu, kromozom 11’in kısa kolunda (11p13) yer alan PAX6 genindeki heterozigot mutasyonlardan kaynaklanır. Ana patojenik mekanizma PAX6 haplo-yetersizliğidir1).
PAX6 geni, göz gelişiminin ana kontrol genidir ve göz, nöral tüp, koku soğanı ve pankreas gelişiminde önemli rol oynar. Normal göz gelişimi için iki kopya PAX6 gereklidir ve tek bir kopyanın işlev kaybı bile aniridiye neden olur1).
Çinli hastalar üzerinde yapılan bir kohort çalışmasında, vakaların %96.9’unda PAX6 geninde nedensel mutasyonlar tespit edilmiştir1). Klasik aniridide, anlamsız mutasyon aracılı mRNA bozunmasını (NMD) indükleyen mutasyonlar veya büyük delesyonlar %96 oranında saptanır1).
Patolojik olarak, iris kökü dışında düz kas kaybı ve açı gelişim bozukluğu görülür. Kornea epitel kök hücre fonksiyon bozukluğu mevcuttur, epitel ve Bowman membranında anormalliklere ve vasküler pannus oluşumuna yol açar.
Aniridi fenotipine neden olan PAX6 mutasyonlarının dağılımı aşağıda gösterilmiştir.
| Mutasyon Tipi | Sıklık |
|---|---|
| Anlamsız mutasyon | Yaklaşık %39 |
| Çerçeve kayması mutasyonu | Yaklaşık %25 |
| Splice bölgesi mutasyonu | Yaklaşık %13 |
| Yanlış anlamlı mutasyon (missense) | Yaklaşık %12 |
Run-on mutasyonları (C-terminal uzama mutasyonları) yaklaşık %5’ini oluşturur ve durdurma kodonunun bir translasyon kodonuna dönüşmesiyle anormal şekilde uzamış PAX6 proteini üretilir 6). C-terminal uzama mutasyonları sıklıkla şiddetli iris hipoplazisi ve ileri düzeyde görme bozukluğu ile ilişkilidir 1)6).
Gen mutasyonları çoğunlukla PTC tipi mutasyonlardır ve missense mutasyonları da rapor edilmiştir 7). Genetik testin yararlılığı açısından, izole aniridinin yaklaşık %85’inde Sanger dizileme veya NGS ile mutasyon saptanır. Ayrıca, MLPA veya CMA ile PAX6 geni içi veya sis-düzenleyici bölge delesyonları yaklaşık %15’inde saptanır 8).
Wang (2023) yeni bir çerçeve kayması mutasyonu c.640_646del (p.R214Pfs*28) tanımlamış ve tam iris yokluğu, fovea hipoplazisi, lens subluksasyonu ve retina dekolmanı ile seyreden bir olgu bildirmiştir 1).
Ratna ve ark. (2022) bir Hint ailesinde run-on mutasyonu c.1268A>T (p.*423L) tanımlamıştır. Etkilenen bireylerde tam aniridi, nistagmus, fovea hipoplazisi, AAK, lensin yukarı subluksasyonu, yüksek miyopi ve optik atrofi görülmüş olup, C-terminal uzama mutasyonuna bağlı şiddetli bir fenotip sergilemiştir 6).
Sporadik aniridide, PAX6’ya ek olarak WT1 genini de içeren büyük delesyonlar WAGR sendromuna neden olur. WT1 delesyonu varlığında Wilms tümörü riski %50’ye kadardır 1). WAGR sendromu şüphesi varsa genetik test ile PAX6 ve WT1 delesyonu doğrulanabilir, böylece Wilms tümörü risk değerlendirmesi ve gelişimsel gecikme takibi mümkün olur 8). WT1 bölgesinin genetik test ile değerlendirilmesi zorunludur; sporadik olguların %30’unda 5 yaşına kadar Wilms tümörü gelişir. WT1 geninin PAX6’ya yakın konumlanması nedeniyle, her ikisini de içeren kromozom 11 kısa kol delesyonu (11p13 delesyonu) aniridiye Wilms tümörünün eşlik etmesine yol açar.
Gillespie sendromu, ITPR1 genindeki heterozigot dominant negatif mutasyonlar veya biallelik mutasyonlar sonucu oluşur 3). Bugüne kadar moleküler tanısı doğrulanmış 37 olgu bildirilmiştir ve Gly2554 kalıntısı bir sıcak nokta olarak bilinir 3).
Aniridi tanı kriterlerine (2020) göre, aşağıdaki kriterlerle kesin tanı konur7).
A. Belirtiler
B. Muayene Bulguları
C. Ayırıcı Tanıda Düşünülmesi Gereken Hastalıklar
E. Genetik test: PAX6 geninde patojenik mutasyon veya 11p13 bölgesinde delesyon
Tanı kategorileri7):
Nadir hastalık onayı için şiddet sınıflandırması aşağıdaki dört aşamada tanımlanmıştır7).
| Şiddet | Tanım |
|---|---|
| Derece I | Tek gözde hastalık, diğer göz sağlıklı |
| Derece II | Her iki gözde hastalık, iyi olan gözde düzeltilmiş görme keskinliği 0.3 veya üzeri |
| Derece III | Her iki gözde hastalık, iyi olan gözde düzeltilmiş görme keskinliği 0.1 veya üzeri ancak 0.3’ten az |
| Derece IV | Her iki gözde hastalık, iyi olan gözde düzeltilmiş görme keskinliği 0.1’den az |
Derece I-III’te bile, glokom vb. nedeniyle görme alanı daralması (Goldmann I/4 hedefi ile merkezi rezidüel görme alanı 20 derece veya daha az) varsa, şiddet bir derece artar. Derece III ve üzeri tıbbi mali yardım için uygundur7).
Yarık lamba mikroskobu ile irisin yokluğu veya az gelişmişliği doğrulanarak klinik tanı kolaydır. Kalan iris dokusunun değerlendirilmesi gonyoskopi ve ultrason biyomikroskopisi ile yapılır. Ön kamara açısının gelişimsel anomalileri de kontrol edilir.
Aşağıdaki oküler komplikasyonlar sistematik olarak değerlendirilir:
Aniridinin genetik değerlendirmesinde en önemli hedef, PAX6 delesyonunun WT1 genine kadar uzanıp uzanmadığının doğrulanmasıdır 1). Tüm ekzom dizileme veya MLPA yöntemi ile PAX6 ve WT1 bölgelerindeki mutasyon ve delesyonlar değerlendirilir 1)2).
Sporadik aniridide, WT1 gen delesyonuna bağlı Wilms tümörü riskinin değerlendirilmesi hayati prognozla doğrudan ilişkilidir 1). Ailesel olgularda bile fenotipik çeşitlilik nedeniyle genetik test ile kesin tanı ve genetik danışmanlık önerilir.
Aniridi için kesin bir tedavi yoktur. Kalan görmeyi en üst düzeyde kullanmak için az görme rehabilitasyonu ve her bir komplikasyon için ayrı ayrı tedavi, yönetimin temelini oluşturur. Klinik kılavuzda (2021) 6 klinik soruya dayalı öneriler sunulmuştur 8).
CQ1: Korneal parankimal opasite için kornea nakli zayıf bir şekilde önerilmez 8).
Kornea nakli kısa vadede görme iyileşmesi sağlayabilse de, maküler hipoplazi gibi eşlik eden durumlar nedeniyle iyileşme sınırlıdır. Uzun vadede glokom ilerlemesi ve greft yetmezliği nedeniyle görme prognozu kötüdür.
CQ2: Kornea epitel kök hücre yetmezliğinde cerrahi tedavi zayıf önerilir 8).
CQ3: Katarakt cerrahisi zayıf önerilir 8).
Katarakt 20 yaşına kadar %50-85 oranında gelişir. Cerrahi, opasite ve fotofobi şiddetine göre planlanır. Cerrahi vakaların %66-100’ünde görme iyileşmesi bildirilmiştir, ancak aşağıdaki noktalara dikkat edilmelidir:
Zinn zonüllerinin zayıf olması nedeniyle göz içi lens implantasyonu dikkatli bir şekilde endikedir.
Hu ve ark. (2024), şiddetli AAK ile birlikte konjenital aniridili iki olguda avize ters aydınlatma yardımıyla fakoemülsifikasyon uyguladı. Kornea bulanıklığı nedeniyle normal intraoperatif görüntüleme zordu, ancak arkadan aydınlatma lens ve ön kapsülün net görüntülenmesini sağladı ve postoperatif 3. haftada düzeltilmiş görme keskinliği sırasıyla 20/200 ve 20/1000’e yükseldi 4).
CQ4: Glokom tedavisi güçlü bir şekilde önerilir 8).
Glokom başlangıcından sonra aşağıdaki 5 aşamalı algoritmaya göre yönetilir.
İlaç tedavisi: Beta blokerler, sempatomimetikler ve prostaglandin (PG) ilişkili ilaçlar etkilidir. Bebeklerde brimonidin (alfa adrenerjik reseptör agonisti) santral sinir sistemi depresyonu riski nedeniyle 2 yaş altında kontrendikedir. Kornea epitel hasarı endişesi varsa koruyucu içermeyen preparatlar kullanılır.
Dışa akım yolu rekonstrüksiyonu (goniyotomi/trabekülotomi): İlk cerrahi olarak önerilir 16). Profilaktik goniyotomi raporları da vardır. Ancak kalan iris trabekülumu örten olgularda etkisiz olabilir.
Filtrasyon cerrahisi (trabekülektomi): Sadece az sayıda ve orta-kısa dönemli raporlar mevcuttur. Çocuk gözlerinde sonuçlar kötü olma eğilimindedir ve postoperatif göz fistülü yaklaşık %25 oranında görülür 13). Postoperatif malign glokom raporları da vardır.
Glokom implant cerrahisi (tüp şant cerrahisi): Baerveldt ve Ahmed tipi cihazlar kullanılabilir. Doğal lensli gözlerde tüp yerleşimi kornea merkezine doğru değil, teğetsel yönde önerilir. İyi göz içi basınç kontrolü beklenebilir.
Siklokoagülasyon: Son çare. Siliyer cisim kriyokoagülasyonunun çoğu olguda göz fistülüne yol açtığı bildirilmiştir. Siliyer cisim hipoplazisi nedeniyle sağlıklı göze göre fistül riski daha yüksektir.
Açı gelişim anomalileri altta yattığından, normal açık açılı glokomdan farklı bir yaklaşım gereklidir. İlk olarak dışa akım yolu rekonstrüksiyonu seçilir, ardından tüp şant cerrahisi iyi bir seçenektir. Brimonidin 2 yaş altında kontrendikedir ve antimetabolit kullanımı AAK’yi kötüleştirebileceğinden dikkatli karar verilmelidir 8).
CQ5: Az görme bakımının uygulanması güçlü bir şekilde önerilir 8).
Refraksiyon düzeltmesi temeldir ve miyopi birliktelik oranı %64 ve üzerindedir.
CQ6: Fotofobi tedavisinin uygulanması güçlü bir şekilde önerilir 8).
Hastaların çoğu normal okullara gidebilir, ancak büyük puntolu ders kitapları, tablet, kitap sehpası gibi yardımlara ihtiyaç duyarlar. Az görme sınıflarına katılmak veya körler okulu/görme engelliler özel eğitim okulundan ebeveyn danışmanlığı ve eğitim danışmanlığı almak da seçenekler arasındadır.
Nisan 2017’den itibaren belirlenmiş nadir hastalık olarak kabul edildiğinden, engelli kimlik kartı olmasa bile, şiddet derecesi III ve üzeri olanlar tıbbi yardım ve ortez-protez desteğinden yararlanabilir 7). Destek kapsamındaki ortez-protezler arasında düzeltici gözlük, güneş gözlüğü, kontakt lens (yapay irisli dahil), az görme gözlüğü, görme engelli beyaz bastonu ve protez göz bulunur.
PAX6, 14 ekzon içeren 22 kb’lik bir genomik DNA’ya uzanır ve 422 amino asit kodlar 1). İki DNA bağlanma alanına (paired domain ve paired-type homeodomain) sahiptir ve C-terminalindeki PST (prolin, serin, treonin açısından zengin) alanı transkripsiyon aktivatörü olarak işlev görür.
PAX6, hücre çoğalmasını, farklılaşmasını, göçünü ve yapışmasını düzenler; hedefleri arasında PAX6’nın kendisi ve lens kristalini ile kornea keratinini kodlayan genler bulunur. Erişkin retina, lens ve korneasında ifadesi devam eder. PAX6 geni, embriyonik dönemde organ farklılaşmasını yöneten ana kontrol genlerinden biridir.
PAX6 mutasyonlarının çoğu, anlamsız mutasyona bağlı mRNA yıkımı (NMD) yoluyla haplo-yetersizliğe neden olur 1). Erken durdurma kodonu (PTC) oluşturan mutasyonlar (anlamsız mutasyonlar, çerçeve kayması mutasyonları ve çoğu splice mutasyonu) tipik aniridi fenotipine yol açar.
Öte yandan, PTC son ekzonda veya sondan bir önceki ekzonun terminal 50 bp’si içinde yer alıyorsa NMD’den kaçar ve kesilmiş protein sentezlenerek şiddetli fenotipe neden olabilir 1).
PAX6 anlamsız mutasyonu c.282C>A (p.Cys94*) ile trizomi 21’in aynı hastada birlikte görüldüğü nadir bir vaka bildirilmiştir. PAX6 mutasyonu de novo oluşmuş ve tam bilateral aniridi, konjenital glokom, AAK ve foveal hipoplazi ile sonuçlanmıştır 2).
Kesin bir genotip-fenotip korelasyonu kurulmamış olmakla birlikte, bazı eğilimler bilinmektedir 1).
Grant ve Walton’ın gonioskopi serilerinde, erken dönemde iris stromasının trabeküler ağ üzerinde öne doğru uzanarak yapışıklık benzeri bağlantılar oluşturduğu, giderek tabaka haline gelip sonunda açı tıkanıklığına yol açtığı gösterilmiştir 14). Bu mekanizma glokom gelişiminin ana nedenidir. Patolojik olarak, iris kökünün korunduğu düz kas defekti ve açının gelişimsel yetersizliği temel oluşturur.
AAK esas olarak limbal kök hücre yetmezliği (LSCD) nedeniyle oluşur, ancak kornea epitelinin anormal farklılaşması, yapışma bozukluğu, konjonktiva hücre infiltrasyonu ve yetersiz gözyaşı üretimi de rol oynar. PAX6 tarafından düzenlenen matriks metalloproteinaz 9 (MMP-9) eksikliği, fibrin birikimi ve inflamatuar hücre infiltrasyonuna yol açar; stromadaki kolajen diziliminin bozulmasıyla saydamlık kaybolur.
AAK 5 evreye ayrılır. Evre I’de sadece periferik epitel anormalliği, Evre II’de santrale ulaşmayan santripetal epitel değişiklikleri, Evre III’te santral korneada epitel değişiklikleri ve periferik yüzeyel neovaskülarizasyon, Evre IV’te tüm korneada yüzeyel neovaskülarizasyon, Evre V’de tüm korneada epitel anormalliği ve derin stromal skar görülür 10).
PAX6 mutasyon durumu ile AAK’nin ilerlemesi arasında ilişki vardır. PTC ve C-terminal uzama mutasyonları olan hastalarda AAK yaşa bağlı olarak ilerlerken, diğer mutasyon tiplerinde ilerleyici olmayan keratopati görülebilir 11).
Gillespie sendromu, ITPR1 genindeki mutasyonlar sonucu oluşur 3). ITPR1, IP3 reseptör ailesinin bir üyesidir ve Ca²⁺ salınım kanallarını oluşturarak endoplazmik retikulumda lokalize olur. Dominant negatif mutasyonlar, iris sfinkter kasının oluşumu ve devamlılığını etkileyerek pupil çevresinde spesifik iris hipoplazisi ve fiks midriyazise yol açar.
Ciaccio ve ark. (2024) Gillespie sendromu literatür taramasında, moleküler olarak doğrulanmış 33 vakanın analizinde motor gelişimin geciktiği ancak zamanla düzeldiği, zihinsel engelin tüm vakalarda görülmediği ve %17’sinde normal zeka olduğu, nörolojik bulguların ilerleyici olmadığı doğrulanmıştır 3).
Tüm ekzom dizileme teknolojisinin yaygınlaşmasıyla yeni PAX6 mutasyonlarının tanımlanması devam etmektedir. İnsan PAX6 Mutasyon Veritabanı’nda 2018 itibarıyla 491 mutasyon kayıtlıydı ve o zamandan beri yaklaşık 250 yeni mutasyon rapor edilmiştir 1). Kodlama yapmayan bölgelerdeki mutasyonların da aniridiye neden olduğu vakalar tespit edilmekte olup, geleneksel testlerle teşhis edilemeyen vakaların aydınlatılması beklenmektedir 9).
Şiddetli AAK eşlik eden vakalarda katarakt cerrahisi için, avizeli ters aydınlatma destekli görselleştirme tekniği faydalıdır 4). Bu teknik, Grade 3-4 yüksek AAK’sı olan hastalarda bile güvenli fakoemülsifikasyona olanak sağlar ve ameliyat sonrası görme iyileşmesi elde edilir.
PAX6 mutasyonunun türüne göre AAK’nin ilerleme paterninin farklı olduğu giderek daha net anlaşılmaktadır. Genetik test maliyetlerinin düşmesiyle, mutasyon tipine dayalı klinik seyir tahmini ve erken müdahale gerçekçi bir seçenek haline gelmektedir.
Aniridi ve trizomi 21 birlikteliği olan vakalarda, her iki hastalığın varlığına rağmen nispeten hafif seyir gösteren örnekler bildirilmiştir 2). Aynı hastada birden fazla genetik bozukluğun bir arada bulunmasının fenotip üzerindeki etkisini anlamak, gelecekteki kişiselleştirilmiş tıp için önemli bilgiler sağlayabilir.
PTC tipi mutasyonlara karşı read-through ilacı (ataluren) aniridiye yönelik temel araştırma düzeyinde incelenmektedir 8). PAX6 gen tedavisi için, Sey mutant fare modelinde AAV-PAX6 vektörü ile gen yerine koyma konusunda temel araştırmalar devam etmektedir. Gelecekte klinik çalışmalara geçilmesi beklenmektedir.
iPS hücresi kaynaklı kornea epitel hücre tabakası nakli ile ilgili klinik çalışmalar yurt içinde ve yurt dışında yürütülmekte olup, AAK için yeni bir tedavi yöntemi olarak dikkat çekmektedir 8). Yapay iris (CustomFlex Artificial Iris vb.) konusunda yurt dışında kullanım deneyimi birikmiştir. Yardımcı cihaz olarak yapay irisli kontakt lensler sigorta kapsamındadır.
Klinik kılavuzda (2021), Japonya’da büyük ölçekli kayıt verilerinin biriktirilmesiyle gerçek durumun anlaşılması ve kanıt kalitesinin iyileştirilmesine dayalı kılavuz revizyonu, gelecekteki önemli görevler olarak belirlenmiştir 8). Bireysel gen mutasyonuna dayalı AAK ilerlemesinin tahmini ve erken müdahalenin optimize edilmesi beklenmektedir.