Изолированная аниридия
Частота: около 2/3 от общего числа.
Тип наследования: аутосомно-доминантный (АД).
Особенности: вызвана мутацией гена PAX6. Без системных проявлений. Пенетрантность полная, но экспрессивность вариабельна.

Аниридия — редкое врожденное заболевание, характеризующееся различной степенью недоразвития или отсутствия радужной оболочки. Термин «аниридия» является неправильным, поскольку при гониоскопии или ультразвуковой биомикроскопии (УБМ) почти всегда обнаруживаются фрагменты ткани радужки.
Распространенность составляет около 1/40 000–1/100 000, значительных различий по расе или полу не сообщалось 1). В МКБ-10 она классифицируется как Q13.1.
Это панокулярное заболевание, поражающее не только радужку, но и роговицу, хрусталик, угол передней камеры, фовеа и зрительный нерв 1), проявляющееся различными угрожающими зрению глазными осложнениями. Прогноз по зрению в целом неблагоприятный, корригированная острота зрения часто остается на уровне около 0,1. Зрачковый рефлекс отсутствует, но аккомодация сохранена, и 60–90% случаев являются двусторонними.
Признаются следующие три фенотипа.
Изолированная аниридия
Частота: около 2/3 от общего числа.
Тип наследования: аутосомно-доминантный (АД).
Особенности: вызвана мутацией гена PAX6. Без системных проявлений. Пенетрантность полная, но экспрессивность вариабельна.
Синдром WAGR
Частота: часть спорадических случаев.
Тип наследования: смежная делеция PAX6 и WT1.
Особенности: сочетается с опухолью Вильмса, аномалиями мочеполовой системы и умственной отсталостью. Риск опухоли до 50%.
Синдром Гиллеспи
Частота: около 2% от общего числа.
Тип наследования: мутация гена ITPR1.
Особенности: сопровождается мозжечковой атаксией и умственной отсталостью. Характерна специфическая аномалия радужки с фиксированным мидриазом3).
Спорадическая аниридия составляет около 1/3 всех случаев и вызывается делецией de novo в 11p13, включающей PAX6. Если делеция распространяется на соседний ген WT1, это приводит к синдрому WAGR1). У 25–30% пациентов со спорадической аниридией развивается опухоль Вильмса, относительный риск составляет 67.
PAX6 является главным контролирующим геном формирования глаза и участвует в развитии глаза, нервной трубки, обонятельной луковицы, островков Лангерганса поджелудочной железы и обонятельного эпителия. Потеря функции одной аллели (гаплонедостаточность) вызывает заболевание; аномалия обеих аллелей приводит к внутриутробной гибели. В 2017 году заболевание было включено в перечень редких заболеваний по закону о редких болезнях, и случаи с тяжестью III степени и выше (подробнее см. раздел Диагностика и обследования) имеют право на финансовую поддержку медицинских расходов7).
Спорадические случаи (новые мутации) составляют около трети всех случаев и могут возникать без семейного анамнеза. При спорадических случаях существует риск синдрома WAGR, поэтому важны генетическое тестирование и ультразвуковой скрининг брюшной полости на опухоль Вильмса.
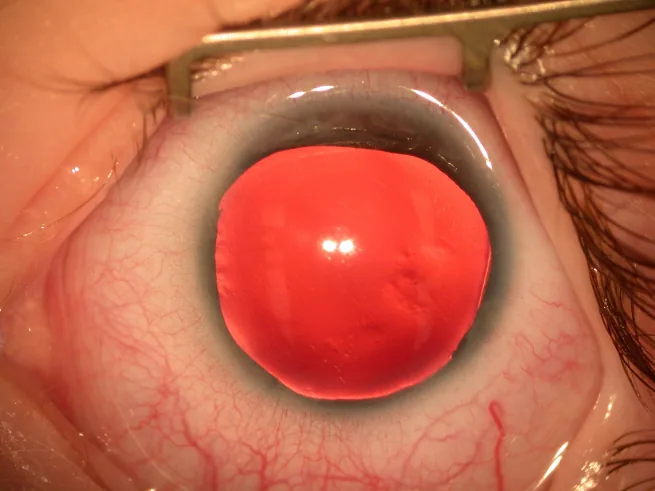
Большинство случаев аниридии выявляются при рождении из-за аномалии радужки/зрачка или в младенчестве из-за нистагма.
Фенотип варьирует между семьями и внутри одной семьи, но различия между правым и левым глазом обычно невелики.
В основном из-за гипоплазии фовеа корригированная острота зрения часто составляет около 0,1–0,2. При сопутствующей гипоплазии макулы прогноз зрения особенно плохой. Коррекция рефракции и помощь слабовидящим с младенчества важны для зрительного развития.
PAX6 экспрессируется не только в тканях глаза, но также в центральной нервной системе, островках Лангерганса поджелудочной железы и обонятельном эпителии, поэтому могут наблюдаться следующие внеглазные осложнения 8).
Ключевыми факторами, определяющими зрительную функцию, являются глаукома, гипоплазия макулы, нистагм, кератопатия, катаракта и аномалии радужки. Повреждения поля зрения и остроты зрения, вызванные глаукомой, необратимы, поэтому контроль внутриглазного давления имеет первостепенное значение при наблюдении.8)
Большинство случаев врожденной аниридии вызваны гетерозиготными мутациями в гене PAX6, расположенном на коротком плече хромосомы 11 (11p13). Основным механизмом заболевания является гаплонедостаточность PAX6.1)
Ген PAX6 является главным контролирующим геном развития глаза и играет важную роль в развитии глаза, нервной трубки, обонятельной луковицы и поджелудочной железы. Для нормального развития глаза необходимы две копии PAX6, и потеря функции одной копии достаточна для развития аниридии.1)
В когортном исследовании китайских пациентов причинные мутации в гене PAX6 были идентифицированы в 96,9% случаев.1) При типичной аниридии в 96% случаев обнаруживаются мутации, индуцирующие нонсенс-опосредованный распад мРНК (NMD), или крупные делеции.1)
Патологически гладкая мышца отсутствует, за исключением корня радужки, и наблюдается недоразвитие угла передней камеры. Имеется дисфункция стволовых клеток эпителия роговицы, приводящая к аномалиям эпителия и мембраны Боумена, и образуется богатый сосудами паннус.
Распределение мутаций PAX6, вызывающих фенотип аниридии, представлено ниже.
| Тип мутации | Частота |
|---|---|
| Нонсенс-мутация | Около 39% |
| Мутация со сдвигом рамки считывания | Около 25% |
| Сплайсинг-мутация | Около 13% |
| Миссенс-мутация | Около 12% |
Мутации типа run-on (мутации с удлинением C-конца) составляют около 5% случаев. Они возникают, когда стоп-кодон преобразуется в кодон трансляции, что приводит к продукции аномально удлиненного белка PAX6 6). Мутации с удлинением C-конца часто связаны с тяжелой гипоплазией радужки и глубокими нарушениями зрения 1)6).
Генетические мутации чаще всего относятся к типу PTC (преждевременный стоп-кодон), но также сообщается о миссенс-мутациях 7). Что касается полезности генетического тестирования, секвенирование по Сэнгеру или NGS выявляет мутации почти у 85% пациентов с изолированной аниридией. Кроме того, с помощью MLPA или CMA обнаруживаются делеции в гене PAX6 или цис-регуляторной области почти у 15% пациентов 8).
Wang (2023) идентифицировал новую мутацию со сдвигом рамки считывания c.640_646del (p.R214Pfs*28) и сообщил о случае с полным отсутствием радужки, гипоплазией фовеа, смещением хрусталика и отслойкой сетчатки 1).
Ratna и соавт. (2022) идентифицировали мутацию run-on c.1268A>T (p.*423L) в индийской семье. Пораженные лица имели полную аниридию, нистагм, гипоплазию фовеа, AAK, верхний подвывих хрусталика, сильную миопию и атрофию зрительного нерва, что демонстрирует тяжелый фенотип, связанный с мутациями удлинения C-конца 6).
При спорадической аниридии крупные делеции, включающие ген WT1 помимо PAX6, вызывают синдром WAGR. При делеции WT1 риск опухоли Вильмса составляет до 50% 1). При подозрении на синдром WAGR генетическое тестирование может подтвердить делеции PAX6 и WT1, что позволяет оценить риск опухоли Вильмса и наблюдать за задержкой развития 8). Оценка области WT1 с помощью генетического тестирования необходима; считается, что у 30% спорадических случаев развивается опухоль Вильмса к 5 годам. Из-за близкого расположения генов WT1 и PAX6 делеция короткого плеча хромосомы 11 (делеция 11p13) приводит к аниридии в сочетании с опухолью Вильмса.
Синдром Гиллеспи вызывается гетерозиготными доминантно-негативными или биаллельными мутациями в гене ITPR1 3). На сегодняшний день сообщается о 37 молекулярно подтвержденных случаях, и остаток Gly2554 известен как горячая точка 3).
Согласно диагностическим критериям аниридии (2020 г.), диагноз подтверждается на основании следующих критериев 7).
A. Симптомы
B. Результаты обследования
C. Дифференциальный диагноз
E. Генетическое тестирование : Патогенная мутация в гене PAX6 или делеция области 11p13
Диагностические категории7) :
Классификация степени тяжести для признания редким заболеванием определена в четыре стадии7).
| Степень тяжести | Определение |
|---|---|
| I степень | Одностороннее поражение, другой глаз здоров |
| II степень | Двустороннее поражение, корригированная острота зрения лучшего глаза 0,3 и выше |
| III степень | Двустороннее поражение, корригированная острота зрения лучшего глаза 0,1 и выше, но менее 0,3 |
| IV степень | Двустороннее поражение, корригированная острота зрения лучшего глаза менее 0,1 |
Даже при I–III степени, если имеется сужение поля зрения из-за глаукомы (центральное остаточное поле зрения ≤ 20° с меткой Goldmann I/4), степень тяжести повышается на один уровень. Степень тяжести III и выше является основанием для получения медицинской помощи 7).
Клинический диагноз легко поставить при подтверждении отсутствия или гипоплазии радужки с помощью щелевой лампы. Оценка остаточной ткани радужки проводится с помощью гониоскопии или ультразвуковой биомикроскопии. Также проверяется наличие аномалий развития угла передней камеры.
Систематически оцениваются следующие глазные осложнения:
Наиболее важной целью генетической оценки аниридии является определение того, распространяется ли делеция PAX6 на ген WT11). Полноэкзомное секвенирование или метод MLPA используются для оценки мутаций/делеций в областях PAX6 и WT11)2).
При спорадической аниридии оценка риска опухоли Вильмса из-за делеции гена WT1 напрямую связана с жизненным прогнозом1). Даже при семейных формах из-за фенотипического разнообразия рекомендуется генетическая диагностика и генетическое консультирование.
Этиотропного лечения аниридии не существует. Основой ведения является слабовидение для максимального использования остаточного зрения и индивидуальное лечение каждого осложнения. Клинические рекомендации (2021) содержат рекомендации, основанные на 6 клинических вопросах8).
CQ1: Слабо рекомендуется не проводить трансплантацию роговицы при помутнении стромы роговицы8).
Трансплантация роговицы может краткосрочно улучшить остроту зрения, но улучшение ограничено из-за сопутствующих заболеваний, таких как гипоплазия макулы. В долгосрочной перспективе прогрессирование глаукомы и недостаточность трансплантата приводят к плохому зрительному прогнозу.
CQ2: Хирургическое лечение недостаточности лимбальных эпителиальных стволовых клеток рекомендуется с низкой степенью убедительности. 8)
CQ3: Хирургия катаракты рекомендуется с низкой степенью убедительности. 8)
Катаракта развивается у 50–85% пациентов к 20 годам. Операция планируется в зависимости от интенсивности помутнения и светобоязни. Сообщается об улучшении зрения в 66–100% прооперированных случаев, однако необходимо обратить внимание на следующие моменты.
Из-за слабости цинновых связок имплантация интраокулярной линзы требует осторожного подхода.
Hu и соавт. (2024) выполнили факоэмульсификацию с помощью ретро-освещения люстрой у двух пациентов с врожденной аниридией и тяжелой ААК. Из-за помутнения роговицы обычная интраоперационная визуализация была затруднена, но заднее освещение позволило четко визуализировать хрусталик и переднюю капсулу, и через 3 недели после операции корригированная острота зрения улучшилась до 20/200 и 20/1000 соответственно 4).
CQ4: Настоятельно рекомендуется проводить лечение глаукомы 8).
После развития глаукомы ведение осуществляется по следующему 5-этапному алгоритму.
Медикаментозная терапия: Бета-блокаторы, симпатомиметики и препараты, связанные с простагландинами (PG), эффективны. Бримонидин (альфа-адренергический агонист) противопоказан детям младше 2 лет из-за риска угнетения ЦНС. При опасении повреждения эпителия роговицы использовать препараты без консервантов.
Реконструкция путей оттока (гониотомия, трабекулотомия): Рекомендуется в качестве первой операции 16). Имеются сообщения о профилактической гониотомии. Однако она может быть неэффективна в случаях, когда остаточная радужка покрывает трабекулу.
Фистулизирующая операция (трабекулэктомия): Имеются лишь немногочисленные кратко- и среднесрочные сообщения. В детских глазах результаты, как правило, плохие, послеоперационная фистула глазного яблока возникает примерно в 25% случаев 13). Также сообщалось о послеоперационной злокачественной глаукоме.
Операция с имплантатом для глаукомы (шунтирующая операция с трубкой): Доступны устройства типа Baerveldt и Ahmed. При введении трубки в факичный глаз рекомендуется направлять ее тангенциально, а не к центру роговицы. Ожидается хороший контроль внутриглазного давления.
Цилиарная коагуляция: Крайняя мера. Сообщается, что криокоагуляция цилиарного тела часто приводила к фистуле глазного яблока. Из-за гипоплазии цилиарного тела риск фистулы выше, чем в здоровом глазу.
Из-за аномалии развития угла передней камеры требуется иной подход, чем при обычной открытоугольной глаукоме. Первым выбором является реконструкция путей оттока, затем хорошим вариантом становится трубчатое шунтирование. Бримонидин противопоказан детям младше 2 лет, а применение антиметаболитов может ухудшить ААК, поэтому требуется осторожное решение 8).
CQ5: Настоятельно рекомендуется проводить помощь при слабовидении 8).
Коррекция рефракции является основой, частота осложнений миопии составляет более 64%.
CQ6: Настоятельно рекомендуется проводить лечение светобоязни 8).
Большинство пациентов могут посещать обычные классы, но им требуются вспомогательные средства, такие как увеличенные учебники, планшеты и подставки для книг. Также возможны посещение классов для слабовидящих или использование консультаций по уходу за детьми и образовательных консультаций, предоставляемых школами для слепых или специализированными школами для слабовидящих.
С апреля 2017 года это заболевание признано редким заболеванием, поэтому даже без удостоверения инвалидности пациенты с тяжестью III степени и выше имеют право на финансовую помощь на медицинские расходы и предоставление вспомогательных устройств 7). К таким устройствам относятся корректирующие очки, солнцезащитные очки, контактные линзы (в том числе с искусственной радужкой), очки для слабовидящих, трость безопасности для слабовидящих и глазной протез.
PAX6 охватывает 22 kb геномной ДНК, содержащей 14 экзонов, и кодирует 422 аминокислоты 1). Он имеет два ДНК-связывающих домена (парный домен и парный гомеодомен) и C-концевой PST-домен (богатый пролином, серином и треонином), который функционирует как активатор транскрипции.
PAX6 регулирует пролиферацию, дифференцировку, миграцию и адгезию клеток. Его мишени включают сам PAX6, а также гены, кодирующие кристаллины хрусталика и кератины роговицы. Экспрессия продолжается в сетчатке, хрусталике и роговице взрослого человека. PAX6 является одним из главных контрольных генов, управляющих органной дифференцировкой в эмбриональном периоде.
Большинство мутаций PAX6 вызывают гаплонедостаточность через нонсенс-опосредованный распад мРНК (NMD) 1). Мутации, вводящие преждевременный стоп-кодон (PTC) (нонсенс-мутации, сдвиг рамки считывания и большинство сплайсинговых мутаций), приводят к типичному фенотипу аниридии.
С другой стороны, если PTC расположен в последнем экзоне или в пределах последних 50 п.н. предпоследнего экзона, он может избежать NMD, и может быть транслирован усеченный белок, что приводит к тяжелому фенотипу 1).
Сообщается о редком случае сочетания нонсенс-мутации PAX6 c.282C>A (p.Cys94*) и трисомии 21 у одного пациента. Мутация PAX6 возникла de novo, что привело к полной двусторонней аниридии, врожденной глаукоме, AAK и гипоплазии фовеа 2).
Хотя четкой корреляции генотип-фенотип не установлено, известны некоторые тенденции 1).
В серии гониоскопических исследований Grant и Walton было показано, что на ранних стадиях строма радужки распространяется кпереди на трабекулу, образуя спаечные прикрепления, которые постепенно становятся листовидными и в конечном итоге приводят к закрытию угла 14). Этот механизм является основным фактором развития глаукомы. Патологически в основе лежат дефект гладкой мышцы с сохранением корня радужки и дисплазия угла.
ААК в основном вызывается дефицитом лимбальных стволовых клеток (LSCD), но также участвуют аномальная дифференцировка эпителия роговицы, нарушение адгезии, инфильтрация конъюнктивальных клеток и недостаточная продукция слезы. Дефицит матриксной металлопротеиназы 9 (MMP-9), регулируемой PAX6, приводит к накоплению фибрина и инфильтрации воспалительных клеток, нарушая коллагеновую организацию стромы и вызывая потерю прозрачности.
ААК классифицируется на 5 стадий. Стадия I: только периферические эпителиальные аномалии; стадия II: центростремительные эпителиальные изменения (центр не достигнут); стадия III: центральные эпителиальные изменения и периферическая поверхностная неоваскуляризация; стадия IV: поверхностная неоваскуляризация всей роговицы; стадия V: тотальная эпителиальная аномалия и глубокий стромальный рубец 10).
Существует связь между статусом мутации PAX6 и прогрессированием ААК. У пациентов с PTC или C-концевыми мутациями удлинения ААК прогрессирует с возрастом, тогда как другие типы мутаций могут вызывать непрогрессирующую кератопатию 11).
Синдром Гиллеспи вызывается мутациями в гене ITPR1 3). ITPR1 принадлежит к семейству рецепторов IP3, образует каналы высвобождения Ca²⁺ и локализуется в эндоплазматическом ретикулуме. Доминантно-негативные мутации влияют на формирование и поддержание сфинктера радужки, вызывая специфическую гипоплазию радужки вокруг зрачка и фиксированный мидриаз.
В обзоре литературы по синдрому Гиллеспи Ciaccio и соавт. (2024) анализ 33 молекулярно подтвержденных случаев показал, что моторное развитие задерживается, но со временем улучшается, умственная отсталость присутствует не во всех случаях (17% имеют нормальный интеллект), а неврологические признаки являются непрогрессирующими 3).
Благодаря распространению технологии полного экзомного секвенирования продолжается идентификация новых мутаций PAX6. В Human PAX6 Mutation Database по состоянию на 2018 год было зарегистрировано 491 мутация, и с тех пор сообщалось еще о примерно 250 новых мутациях 1). Также выявляются мутации в некодирующих областях, вызывающие аниридию, что позволяет надеяться на выяснение случаев, которые не удавалось диагностировать с помощью традиционных тестов 9).
При хирургии катаракты в случаях с тяжелой ААК полезна техника визуализации с помощью ретро-освещения типа «люстра» 4). Этот метод позволяет безопасно выполнить факоэмульсификацию даже у пациентов с высокой ААК 3–4 степени, что приводит к послеоперационному улучшению зрения.
Становится очевидным, что тип мутации PAX6 влияет на характер прогрессирования ААК. Снижение стоимости генетического тестирования делает прогнозирование клинического течения на основе типа мутации и раннее вмешательство реалистичными вариантами.
В случаях сочетания аниридии и трисомии 21 сообщалось о примерах относительно легкого течения, несмотря на сосуществование обоих заболеваний 2). Понимание влияния сосуществования нескольких генетических нарушений у одного пациента на фенотип может дать важные знания для будущей персонализированной медицины.
Применение препарата для «прочитывания» преждевременных стоп-кодонов (аталурен) при мутациях PTC-типа для лечения аниридии изучается на уровне фундаментальных исследований 8). Что касается генной терапии PAX6, ведутся фундаментальные исследования по замещению гена с помощью вектора AAV-PAX6 на мышиной модели с мутацией Sey. Ожидается переход к клиническим испытаниям в будущем.
Клинические испытания трансплантации листов эпителиальных клеток роговицы, полученных из iPS-клеток, проводятся в Японии и за рубежом, привлекая внимание как новый метод лечения ААК 8). Что касается искусственной радужки (например, CustomFlex Artificial Iris), за рубежом накоплен опыт использования. Контактные линзы с искусственной радужкой покрываются страховкой как вспомогательные средства.
Согласно клиническим рекомендациям (2021 г.), накопление крупномасштабных регистровых данных в Японии для понимания реальной ситуации и пересмотр рекомендаций на основе повышения качества доказательств рассматриваются как важные будущие задачи 8). Ожидается оптимизация прогнозирования прогрессирования ААК и раннего вмешательства на основе индивидуальных генетических мутаций.