Aniridia Aislada
Frecuencia: Aproximadamente 2/3 del total.
Herencia: Autosómica dominante (AD).
Características: Causada por mutación del gen PAX6. Sin síntomas sistémicos. Penetrancia completa pero expresividad variable.

La aniridia es un trastorno congénito raro caracterizado por diversos grados de hipoplasia o ausencia del iris. El término “aniridia” es un nombre inapropiado, ya que mediante gonioscopia o microscopía ultrasónica biomicroscópica (UBM) casi siempre se detectan fragmentos de tejido del iris.
La prevalencia es de aproximadamente 1/40,000 a 1/100,000, sin diferencias raciales o de sexo significativas reportadas 1). Se clasifica como Q13.1 en la CIE-10.
La aniridia es una enfermedad panocular que afecta no solo al iris sino también a la córnea, el cristalino, el ángulo, la fóvea y el nervio óptico 1), presentando diversas complicaciones oculares que amenazan la visión. El pronóstico visual es generalmente malo, con una agudeza visual corregida a menudo alrededor de 0.1. El reflejo pupilar a la luz está ausente, pero la acomodación se conserva. El 60-90% de los casos son bilaterales.
Se reconocen los siguientes tres fenotipos.
Aniridia Aislada
Frecuencia: Aproximadamente 2/3 del total.
Herencia: Autosómica dominante (AD).
Características: Causada por mutación del gen PAX6. Sin síntomas sistémicos. Penetrancia completa pero expresividad variable.
Síndrome de WAGR
Frecuencia: Una parte de los casos esporádicos.
Herencia: Deleción contigua de PAX6 y WT1.
Características: Asociado con tumor de Wilms, anomalías genitourinarias y discapacidad intelectual. Riesgo de tumor de hasta el 50%.
Síndrome de Gillespie
Frecuencia: Aproximadamente el 2% del total.
Herencia: Mutación del gen ITPR1.
Características: Acompañado de ataxia cerebelosa y discapacidad intelectual. Es característica una anomalía del iris con midriasis fija3).
La aniridia esporádica representa aproximadamente 1/3 del total y es causada por una deleción de novo de 11p13 que incluye PAX6. Si la deleción se extiende al gen WT1 adyacente, causa el síndrome de WAGR1). El 25-30% de los pacientes con aniridia esporádica desarrollan tumor de Wilms, con un riesgo relativo de 67.
PAX6 es un gen maestro de control para la formación del ojo y participa en el desarrollo del ojo, tubo neural, bulbo olfatorio, islotes de Langerhans del páncreas y epitelio olfatorio. Se manifiesta con pérdida de función de un alelo (haploinsuficiencia), y las anomalías bialélicas son letales embrionarias. Fue designada como enfermedad intratable especificada bajo la Ley de Enfermedades Intratables en 2017, y los pacientes con grado de severidad III o superior (ver sección de Diagnóstico y Pruebas para detalles) son elegibles para subsidios de gastos médicos7).
Los casos esporádicos (mutaciones de novo) representan aproximadamente un tercio del total y pueden ocurrir sin antecedentes familiares. En los casos esporádicos existe la posibilidad de síndrome de WAGR, por lo que son importantes las pruebas genéticas y la ecografía abdominal para la detección del tumor de Wilms.
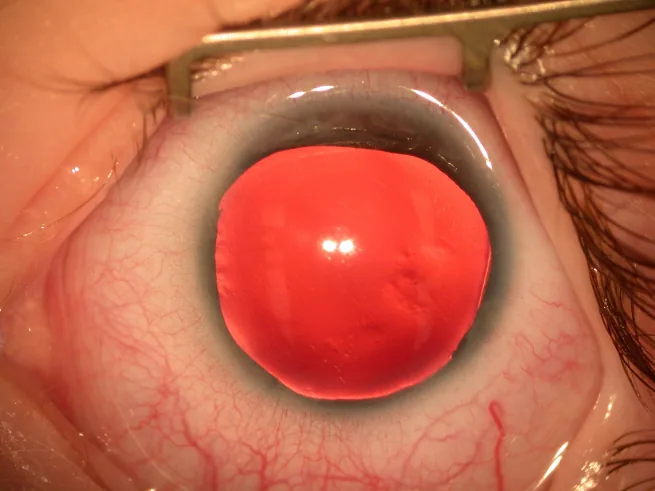
La mayoría de los casos de aniridia se descubren al nacer debido a anomalías del iris y la pupila, o en la infancia debido a nistagmo.
El fenotipo varía entre familias y dentro de una misma familia, pero las diferencias entre el ojo derecho e izquierdo suelen ser pequeñas.
Debido principalmente a la hipoplasia foveal, la agudeza visual corregida suele ser de alrededor de 0.1 a 0.2. El pronóstico visual es particularmente malo cuando hay hipoplasia macular. La corrección refractiva y el cuidado de baja visión desde la infancia son importantes para el desarrollo visual.
PAX6 se expresa no solo en los tejidos oculares sino también en el sistema nervioso central, los islotes de Langerhans del páncreas y el epitelio olfatorio, por lo que pueden observarse las siguientes complicaciones extraoculares 8).
Los factores importantes que determinan la función visual son el glaucoma, la hipoplasia macular, el nistagmo, la queratopatía, la catarata y la hipoplasia del iris. Dado que el daño del campo visual y la agudeza visual causado por el glaucoma es irreversible, el manejo de la presión intraocular es lo más importante en el seguimiento.8)
La mayoría de los casos de aniridia congénita son causados por mutaciones heterocigotas en el gen PAX6 ubicado en el brazo corto del cromosoma 11 (11p13). La haploinsuficiencia es el principal mecanismo de la enfermedad relacionada con PAX6.1)
El gen PAX6 es un gen maestro de control para la formación del ojo y desempeña un papel importante en el desarrollo del ojo, el tubo neural, el bulbo olfatorio y el páncreas. Se requieren dos copias de PAX6 para el desarrollo normal del ojo, y la pérdida de función de una sola copia conduce a aniridia.1)
En un estudio de cohorte de pacientes chinos, se identificaron mutaciones causales en el gen PAX6 en el 96.9% de los casos.1) En la aniridia típica, las mutaciones que inducen la degradación del ARNm dependiente de mutaciones sin sentido (NMD) o deleciones grandes se detectan en el 96% de los casos.1)
Patológicamente, el músculo liso está ausente excepto en la raíz del iris, y se observa un desarrollo anormal del ángulo. Se observan anomalías funcionales de las células madre del epitelio corneal, lo que lleva a anomalías en el epitelio y la membrana de Bowman, y formación de un paño vascularizado.
El desglose de las mutaciones de PAX6 que causan el fenotipo de aniridia se muestra a continuación.
| Tipo de mutación | Frecuencia |
|---|---|
| Mutación sin sentido | Aproximadamente 39% |
| Mutación de cambio de marco | Aproximadamente 25% |
| Mutación de empalme | Aproximadamente 13% |
| Mutación de cambio de sentido | Aproximadamente 12% |
Las mutaciones de tipo run-on (mutaciones de extensión del extremo C) representan aproximadamente el 5% y producen una proteína PAX6 anormalmente extendida debido a la conversión de un codón de parada en un codón de traducción 6). Las mutaciones de extensión del extremo C a menudo se asocian con hipoplasia grave del iris y deterioro visual profundo 1)6).
Las mutaciones genéticas son a menudo del tipo PTC, pero también se han reportado mutaciones de cambio de sentido 7). En cuanto a la utilidad de las pruebas genéticas, la secuenciación Sanger o NGS detecta mutaciones en casi el 85% de los casos de aniridia aislada. Además, MLPA o CMA detectan deleciones dentro del gen PAX6 o su región cis-reguladora en casi el 15% de los casos 8).
Wang (2023) identificó una nueva mutación de cambio de marco c.640_646del (p.R214Pfs*28) y reportó un caso que presentaba ausencia completa de iris, hipoplasia foveal, subluxación del cristalino y desprendimiento de retina 1).
Ratna et al. (2022) identificaron una mutación run-on c.1268A>T (p.*423L) en una familia india. Los individuos afectados presentaban aniridia completa, nistagmo, hipoplasia foveal, AAK, subluxación superior del cristalino, miopía alta y atrofia óptica, indicando un fenotipo grave debido a la mutación de extensión del extremo C 6).
En la aniridia esporádica, las deleciones grandes que involucran tanto a PAX6 como a WT1 causan el síndrome de WAGR. El riesgo de tumor de Wilms en casos con deleción de WT1 es de hasta el 50% 1). Si se sospecha síndrome de WAGR, las pruebas genéticas pueden confirmar las deleciones de PAX6 y WT1, permitiendo la evaluación del riesgo de tumor de Wilms y el seguimiento del retraso del desarrollo 8). La evaluación de la región WT1 mediante pruebas genéticas es esencial, y el 30% de los casos esporádicos desarrollan tumor de Wilms a los 5 años. Debido a que WT1 se encuentra cerca de PAX6, las deleciones del brazo corto del cromosoma 11 (deleción 11p13) que involucran ambos genes resultan en aniridia con tumor de Wilms.
El síndrome de Gillespie es causado por mutaciones heterocigotas dominantes negativas o mutaciones bialélicas en el gen ITPR1 3). Hasta la fecha, se han confirmado 37 casos mediante diagnóstico molecular, y el residuo Gly2554 se conoce como un punto caliente 3).
Según los criterios diagnósticos de aniridia (2020), se confirma con los siguientes criterios7).
A. Síntomas
B. Hallazgos de Exploración
C. Enfermedades a Diferenciar
E. Pruebas genéticas: Mutación patogénica en el gen PAX6 o deleción de la región 11p13
Categorías diagnósticas7):
La clasificación de gravedad para la designación de enfermedad intratable se define en los siguientes cuatro niveles7).
| Gravedad | Definición |
|---|---|
| Grado I | Afectación unilateral, ojo contralateral normal |
| Grado II | Afectación de ambos ojos, mejor agudeza visual corregida en el ojo mejor ≥ 0.3 |
| Grado III | Afectación de ambos ojos, mejor agudeza visual corregida en el ojo mejor ≥ 0.1 y < 0.3 |
| Grado IV | Afectación de ambos ojos, mejor agudeza visual corregida en el ojo mejor < 0.1 |
Incluso para los grados I a III, si se acompaña de estrechamiento del campo visual debido a glaucoma, etc. (campo visual residual central dentro de 20 grados con el objetivo Goldmann I/4), la gravedad aumenta un grado. La gravedad de grado III o superior es elegible para subsidios de gastos médicos 7).
El diagnóstico clínico es fácil si se confirman defectos o hipoplasia del iris mediante microscopía de lámpara de hendidura. Se utilizan gonioscopia y microscopía ultrasónica biomicroscópica para evaluar el tejido residual del iris. También se verifica la presencia de anomalías del desarrollo del ángulo de la cámara anterior.
Se evalúan sistemáticamente las siguientes complicaciones oculares:
El objetivo más importante en la evaluación genética de la aniridia es determinar si la deleción de PAX6 se extiende al gen WT1 1). La secuenciación del exoma completo o MLPA se utilizan para evaluar mutaciones y deleciones en las regiones PAX6 y WT1 1)2).
En la aniridia esporádica, la evaluación del riesgo de tumor de Wilms debido a la deleción del gen WT1 está directamente relacionada con el pronóstico vital 1). Incluso en casos familiares, debido a la variabilidad fenotípica, se recomiendan las pruebas genéticas para el diagnóstico definitivo y el asesoramiento genético.
No existe un tratamiento curativo para la aniridia. El manejo se centra en la atención de baja visión para maximizar la visión residual y el tratamiento individualizado de cada complicación. Las guías clínicas (2021) proporcionan recomendaciones basadas en seis preguntas clínicas 8).
CQ1: Se recomienda débilmente no realizar trasplante de córnea para la opacidad del estroma corneal 8).
El trasplante de córnea puede proporcionar una mejora visual a corto plazo, pero la mejora es limitada debido a comorbilidades como la hipoplasia macular. A largo plazo, el pronóstico visual es malo debido a la progresión del glaucoma y al fracaso del injerto.
CQ2: Recomendamos débilmente realizar tratamiento quirúrgico para la deficiencia de células madre del epitelio corneal. 8)
CQ3: Recomendamos débilmente realizar cirugía de cataratas. 8)
Las cataratas se desarrollan en el 50–85% de los pacientes a los 20 años. La cirugía se planifica según la gravedad de la opacidad y la fotofobia. Se ha informado mejoría visual en el 66–100% de los casos quirúrgicos, pero se deben tener en cuenta los siguientes puntos.
Debido a que las zónulas de Zinn son frágiles, la inserción de lentes intraoculares requiere una indicación cuidadosa.
Hu y cols. (2024) realizaron facoemulsificación asistida por retroiluminación con candelabro en dos casos de aniridia congénita con AAK grave. Aunque la visualización intraoperatoria convencional era difícil debido a la opacidad corneal, la iluminación posterior permitió una visualización clara del cristalino y la cápsula anterior, y la agudeza visual corregida mejoró a 20/200 y 20/1000 respectivamente a las 3 semanas postoperatorias 4).
CQ4: Se recomienda firmemente realizar tratamiento para el glaucoma 8).
Después del inicio del glaucoma, el manejo se basa en el siguiente algoritmo de cinco pasos.
Farmacoterapia: Los betabloqueantes, simpaticomiméticos y fármacos relacionados con prostaglandinas (PG) son efectivos. La brimonidina (agonista del receptor adrenérgico alfa) está contraindicada en menores de 2 años debido al riesgo de depresión del sistema nervioso central. Si se teme daño epitelial corneal, use formulaciones sin conservantes.
Cirugía de reconstrucción de la vía de salida (goniotomía/trabeculotomía): Recomendada como cirugía inicial 16). También se ha reportado goniotomía profiláctica. Sin embargo, puede ser ineficaz en casos donde el iris residual cubre la malla trabecular.
Cirugía filtrante (trabeculectomía): Solo existen reportes a corto y mediano plazo en pocos casos. Los resultados tienden a ser pobres en ojos pediátricos, con hipotonía ocular postoperatoria en aproximadamente el 25% 13). También se ha reportado glaucoma maligno postoperatorio.
Cirugía de implante para glaucoma (cirugía de derivación con tubo): Están disponibles los dispositivos Baerveldt y Ahmed. Para la inserción del tubo en ojos fáquicos, se recomienda una dirección tangencial en lugar de central hacia la córnea. Se puede esperar un buen control de la presión intraocular.
Procedimientos ciclodestructivos: Último recurso. Se ha reportado que la ciclocrioterapia resulta en hipotonía ocular en muchos casos. Debido a la hipoplasia del cuerpo ciliar, el riesgo de hipotonía es mayor que en ojos sanos.
Debido a que la causa subyacente es un desarrollo anormal del ángulo, se necesita un enfoque diferente al del glaucoma de ángulo abierto primario. El tratamiento inicial es la cirugía de reconstrucción de la vía de salida, seguida de la cirugía de derivación con tubo como una buena opción. La brimonidina está contraindicada en niños menores de 2 años, y el uso de antimetabolitos puede empeorar la AAK, por lo que se requiere un juicio cuidadoso 8).
CQ5: Se recomienda firmemente realizar atención de baja visión 8).
La corrección refractiva es fundamental; la tasa de complicación de miopía se reporta en un 64% o más.
CQ6: Se recomienda firmemente el tratamiento de la fotofobia 8).
La mayoría de los pacientes pueden asistir a escuelas regulares, pero necesitan apoyo como libros de texto ampliados, tabletas y atriles. También es posible asistir a clases para personas con baja visión o utilizar consultas de crianza y educativas proporcionadas por escuelas para ciegos o escuelas de apoyo especial para discapacidad visual.
Desde abril de 2017, esta condición ha sido designada como una enfermedad intratable especificada. Por lo tanto, incluso si los pacientes no tienen un certificado de discapacidad física, aquellos con grado de severidad III o superior son elegibles para subsidios de gastos médicos y provisión de dispositivos de asistencia 7). Los dispositivos de asistencia elegibles incluyen gafas correctivas, gafas de sol, lentes de contacto (incluyendo aquellos con iris artificial), gafas para baja visión, bastones blancos para discapacitados visuales y ojos artificiales.
PAX6 abarca 22 kb de ADN genómico que contiene 14 exones y codifica 422 aminoácidos 1). Tiene dos dominios de unión al ADN (dominio pareado y homeodominio de tipo pareado), y el dominio PST (rico en prolina, serina y treonina) en el extremo C-terminal funciona como un activador transcripcional.
PAX6 regula la proliferación, diferenciación, migración y adhesión celular. Sus dianas incluyen el propio PAX6, así como genes que codifican cristalinas del cristalino y queratinas corneales. La expresión continúa en la retina, el cristalino y la córnea del adulto. PAX6 es uno de los genes maestros que gobiernan la diferenciación de órganos durante el período embrionario.
La mayoría de las mutaciones de PAX6 causan haploinsuficiencia a través de la degradación del ARNm mediada por codones de terminación prematura (NMD) 1). Las mutaciones que introducen un codón de terminación prematura (PTC) (mutaciones sin sentido, mutaciones de cambio de marco y la mayoría de las mutaciones de empalme) dan como resultado el fenotipo típico de aniridia.
Por otro lado, si el PTC se encuentra en el exón final o dentro de los últimos 50 pb del penúltimo exón, puede escapar de la NMD y traducirse una proteína truncada, lo que potencialmente conduce a un fenotipo grave 1).
Se ha informado un caso raro en el que una mutación sin sentido de PAX6 c.282C>A (p.Cys94*) y trisomía 21 coexistieron en el mismo paciente. La mutación de PAX6 surgió de novo y resultó en aniridia bilateral completa, glaucoma congénito, AAK e hipoplasia foveal 2).
Aunque no se ha establecido una correlación clara genotipo-fenotipo, se conocen varias tendencias 1).
En la serie de gonioscopia de Grant y Walton, se demostró que en etapas tempranas el estroma del iris se extiende anteriormente sobre la malla trabecular formando adherencias, que gradualmente se vuelven laminares y finalmente conducen al cierre angular14). Este mecanismo es la causa principal del desarrollo del glaucoma. Patológicamente, se basa en un defecto del músculo liso que respeta la raíz del iris y en la disgenesia del ángulo.
La AAK es causada principalmente por deficiencia de células madre limbares (LSCD), pero también contribuyen la diferenciación y adhesión anormales del epitelio corneal, la invasión de células conjuntivales y la producción insuficiente de lágrimas. La deficiencia de metaloproteinasa de matriz 9 (MMP-9), regulada por PAX6, conduce a la acumulación de fibrina e infiltración de células inflamatorias, y pérdida de transparencia debido a la desorganización del colágeno estromal.
La AAK se clasifica en 5 etapas. La etapa I muestra solo anomalías epiteliales periféricas, la etapa II muestra cambios epiteliales centrípetos (sin alcanzar el centro), la etapa III muestra cambios epiteliales corneales centrales y neovascularización superficial periférica, la etapa IV muestra neovascularización superficial de toda la córnea, y la etapa V muestra anomalías epiteliales y cicatrización estromal profunda de toda la córnea10).
Existe una asociación entre el estado de mutación de PAX6 y la progresión de la AAK. En pacientes con mutaciones PTC o de extensión del extremo C, la AAK progresa de manera dependiente de la edad, mientras que otros tipos de mutaciones pueden presentar queratopatía no progresiva11).
El síndrome de Gillespie es causado por mutaciones en el gen ITPR13). ITPR1 es miembro de la familia de receptores de IP3, forma canales de liberación de Ca²⁺ y se localiza en el retículo endoplásmico. Las mutaciones dominantes negativas afectan la formación y el mantenimiento del músculo esfínter del iris, lo que lleva a hipoplasia del iris específica alrededor de la pupila y midriasis fija.
En la revisión bibliográfica del síndrome de Gillespie por Ciaccio et al. (2024), el análisis de 33 casos confirmados molecularmente confirmó que el desarrollo motor se retrasa pero mejora con el tiempo, la discapacidad intelectual no está presente en todos los casos (17% tienen inteligencia normal) y los signos neurológicos son no progresivos3).
Con la difusión de la secuenciación del exoma completo, se continúan identificando nuevas mutaciones de PAX6. Hasta 2018, se registraron 491 mutaciones en la Base de Datos de Mutaciones de PAX6 Humano, y desde entonces se han reportado aproximadamente 250 nuevas mutaciones 1). También se están identificando mutaciones en regiones no codificantes como causa de aniridia, lo que se espera que aclare casos que no pudieron diagnosticarse con las pruebas convencionales 9).
Para la cirugía de cataratas en casos con AAK grave, las técnicas de visualización con retroiluminación tipo candelabro son útiles 4). Esta técnica permite una facoemulsificación segura incluso en pacientes con AAK de grado 3 a 4, y se ha logrado una mejora visual postoperatoria.
Se está aclarando que el patrón de progresión de la AAK difiere según el tipo de mutación de PAX6. Con la disminución de los costos de las pruebas genéticas, la predicción del curso clínico y la intervención temprana basadas en el tipo de mutación se están convirtiendo en opciones realistas.
En casos de aniridia combinada con trisomía 21, se han reportado cursos relativamente leves a pesar de la coexistencia de ambas enfermedades 2). Comprender el impacto de múltiples trastornos genéticos coexistiendo en el mismo paciente sobre el fenotipo puede proporcionar información importante para la medicina personalizada futura.
La aplicación de fármacos de lectura continua (ataluren) para mutaciones de tipo PTC en la aniridia se está investigando a nivel de investigación básica 8). En cuanto a la terapia génica de PAX6, se está llevando a cabo investigación básica de suplementación génica con vectores AAV-PAX6 en modelos de ratón con mutación Sey. Se espera su desarrollo hacia ensayos clínicos futuros.
Se están realizando ensayos clínicos de trasplante de láminas de células epiteliales corneales derivadas de iPS tanto a nivel nacional como internacional, atrayendo la atención como un nuevo tratamiento para la AAK 8). En cuanto a los iris artificiales (como CustomFlex Artificial Iris), se ha acumulado experiencia de uso en el extranjero. Como dispositivos protésicos, los lentes de contacto con iris artificial están cubiertos por el seguro.
Según las guías de práctica clínica (2021), la acumulación de datos de registro a gran escala en Japón para comprender la situación real y la revisión de las guías basada en la mejora de la calidad de la evidencia se consideran tareas importantes para el futuro 8). Se espera la optimización de la predicción de la progresión de la AAK y la intervención temprana basada en mutaciones genéticas individuales.