晶状体前囊所见
中央盘:前囊中央白色颗粒状物质积聚。
中间透明带:瞳孔缘与虹膜摩擦导致物质被清除而形成的透明环状区域。
周边颗粒带(peripheral band):位于中间透明带外侧的颗粒状物质沉积带。所有病例均存在,有时仅在散瞳后才能确认。
上述三个区域的同心圆模式是典型表现。散瞳后观察最佳。

假性剥脱综合征(Pseudoexfoliation Syndrome; XFS、PEX)是一种纤维性异常物质(假性剥脱物质)在眼内各部位(如晶状体、虹膜、睫状体、小梁网等)沉积的疾病。1917年由Linberg首次描述1)。
“假性剥脱”这一名称是为了与高温作业者发生的真性晶状体前囊剥脱(玻璃工剥脱)相区别。虽然看似眼部局部疾病,但剥脱物质也存在于皮肤、心脏、肺、肝脏、血管壁等全身组织,因此被理解为一种全身性疾病2)。
全球患病率在约60岁以上人群中为10–20%,但在斯堪的纳维亚和中东地区尤其高,而在东亚地区相对较低2)。在日本,70岁以上人群中约4%患有假性剥脱综合征,PEX合并眼中20–40%合并青光眼。
基于人群的数据显示,约15–26%的XFS眼在5年内发展为假性剥脱性青光眼4)。假性剥脱性青光眼是全球最常见的可确定病因的开角型青光眼2)。
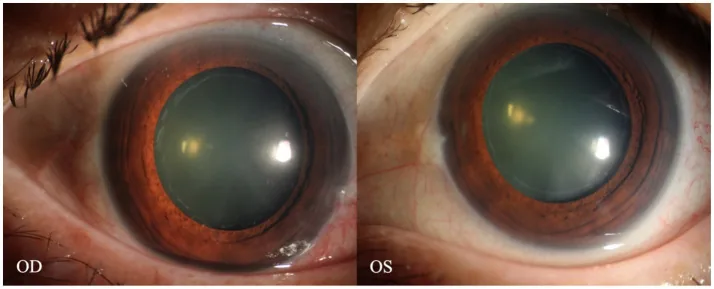
XFS本身通常缺乏自觉症状。常在以下情况中被发现。
裂隙灯显微镜检查可见以下特征性表现。
晶状体前囊所见
中央盘:前囊中央白色颗粒状物质积聚。
中间透明带:瞳孔缘与虹膜摩擦导致物质被清除而形成的透明环状区域。
周边颗粒带(peripheral band):位于中间透明带外侧的颗粒状物质沉积带。所有病例均存在,有时仅在散瞳后才能确认。
上述三个区域的同心圆模式是典型表现。散瞳后观察最佳。
其他眼部表现
瞳孔缘的假性剥脱物质:缩瞳时容易看到的白色物质沉积。
瞳孔散大不良(虫蚀状瞳孔):由于虹膜括约肌上的剥脱物质沉积导致虹膜硬化和瞳孔缘色素脱落4)。
Zinn小带脆弱:表现为晶状体震颤(phacodonesis)。
Sampaolesi线:越过Schwalbe线的波浪状色素沉着。伴有下方小梁网重度色素沉着。
眼压升高和日内波动增大:眼压水平高于POAG,日内波动也更大4)。
初期常作为单眼性疾病被发现。但长期来看,许多患者对侧眼也会发病,最终双眼性的比例很高4)。单眼发现时对侧眼的定期观察很重要。
XFS是一种年龄相关疾病,60岁以上患病率急剧增加。虽为多因素,但遗传因素最为重要。
假性剥脱物质产生的核心机制是细胞外基质代谢异常和弹性纤维积累。该物质包含原纤维蛋白、玻连蛋白、层粘连蛋白等2)。剥脱物质沉积在Zinn小带上,促进基质金属蛋白酶(MMP)的降解,导致支持结构脆弱化8)。
XFS的诊断主要基于裂隙灯显微镜的临床检查。重要的是在缩瞳和散瞳两种状态下进行检查:缩瞳时评估瞳孔缘的白色剥脱物质,散瞳时评估晶状体表面的三区模式和Zinn小带的状态。
散瞳后观察晶状体前囊是基础。确认三区模式:中央盘、中间透明带和周边颗粒带。周边带在所有病例中都存在,有时仅在散瞳后才能看到。还需检查瞳孔缘、虹膜和晶状体赤道部的物质沉积2)。
Sampaolesi线(越过Schwalbe线的波浪状色素沉着)是XFS的特征4)。确认房角开放,评估小梁网的严重色素沉着。
建议在不同时间多次测量眼压。XFS的日内波动较大,单次测量可能漏诊4)。
怀疑假性剥脱性青光眼时进行。评估视网膜神经纤维层(RNFL)变薄。根据青光眼诊疗指南第5版定期进行检查6)。
作为术前评估,确认有无晶状体震颤及其程度。前房深度小于2.5mm提示Zinn小带脆弱,并发症风险增加约5倍5)。前房深度不对称和晶状体偏位也很重要。术前还需通过镜面显微镜评估角膜内皮细胞密度5)。
真性剥脱(True exfoliation)是高温作业者或玻璃工人发生的晶状体前囊层状剥离,由红外线暴露引起。与假性剥脱综合征(XFS)是不同疾病。XFS是细胞来源的纤维性物质沉积,病理不同。近年来玻璃工人减少,真性剥脱病例几乎不再见到。
目前尚无治愈XFS本身的治疗方法。并发症(青光眼、白内障)的管理是治疗的核心。
假性剥脱性青光眼是继发性开角型青光眼最常见的原因,其进展速度约为POAG的3倍2)4)。眼压波动幅度大,建议积极降低眼压(证据级别1B)6)。考虑到约15-26%的XFS眼在5年内发展为假性剥脱性青光眼,定期随访很重要4)。
药物治疗:参照POAG,设定目标眼压并降低眼压。前列腺素(PG)制剂为一线选择。根据情况联合使用β受体阻滞剂滴眼液、碳酸酐酶抑制剂(CAI)滴眼液或口服药物6)。
手术治疗6):
XFS患者在白内障手术中需要特殊处理。散瞳不良和Zinn小带脆弱并存,术中并发症风险据报道约为2.68倍5)。基于术前评估的风险分层是最重要的步骤5)。
| 风险项目 | XFS患者中的情况 |
|---|---|
| Zinn小带断裂 | 低风险病例最高2.0%,高风险病例最高9.0%5) |
| 晶状体囊破裂/玻璃体脱出 | XFS眼风险显著增高5) |
| 瞳孔散大不良 | 即使最大散瞳,瞳孔直径常小于6毫米5) |
| IOL偏位/脱位 | 囊袋内固定的长期稳定性降低。晚期可能发生IOL-囊袋复合体脱位 |
前房深度小于2.5毫米提示悬韧带脆弱,并发症风险增加约5倍5)。通过镜面显微镜评估角膜内皮细胞密度也有助于判断术后角膜内皮功能不全的风险。
确保散瞳:
前囊切开和核处理:
Zinn小带和晶状体囊的支持:
房角冲洗:手术结束时冲洗前房角,去除假性剥脱物质和OVD。改善经小梁网的房水流出,预防术后眼压升高。
大型研究报告显示,在校正年龄和核混浊度后,PXF组与对照组术后1年的最佳矫正视力相当(P=0.09),1年后的并发症率也无显著差异(PXF组2.7% vs 对照组2.5%)5)。平均角膜内皮细胞减少率PXF组为14.7%,对照组为12.7%(P=0.066)。这表明在适当的术前评估和风险管理下,PXF眼白内障手术可获得良好效果5)。
假性剥脱物质是由变性的弹性纤维微原纤维和细胞外基质成分组成的复合物。在电子显微镜下,它显示出直径50-60纳米的细纤维呈束状和放射状排列的特征性结构2)。
假性剥脱物质的产生部位有多处。晶状体上皮细胞、虹膜色素上皮和非色素上皮、睫状体非色素上皮已被确定为主要来源。在眼外,血管内皮细胞和成纤维细胞中也证实有产生,支持XFS是一种全身性疾病2)。
LOXL1的作用:LOXL1属于赖氨酰氧化酶家族,是一种催化胶原蛋白和弹性蛋白交联形成的酶3)。LOXL1功能下降导致弹性纤维稳态破坏,异常纤维性物质积累。
眼压升高的机制:剥脱物质和色素颗粒积聚在小梁网和Schlemm管中,增加房水流出阻力。小梁细胞产生剥脱物质、色素颗粒被小梁细胞吞噬、以及弹性纤维生成抑制导致的细胞外基质异常沉积也参与其中2)。
Zinn小带脆弱的机制:Zinn小带主要由含有fibrillin-1的微纤维构成。在XFS中,假性剥脱物质沿小带沉积,溶酶体酶(MMP)促进其降解。这导致支持功能随时间逐渐下降8)。
据报道,XFS患者白内障手术中Zinn小带断裂的频率是对照组的4倍8)。这一发现表明术中机械操作暴露了小带的脆弱性。
罕见合并病例:有报道称,在MRCS综合征(小角膜-视杆视锥细胞营养不良-白内障-后巩膜葡萄肿)合并XFS的病例中,XFS特征的纤维性物质沉积与严重的眼轴延长(眼轴长30.9 mm)相结合,导致Zinn小带显著脆弱化8)。
白内障手术以外的晶状体脱位风险:XFS患者存在潜在的Zinn小带脆弱性,在白内障手术以外的眼内手术中也有晶状体脱位的风险。Yamamoto等人(2025)报告了一例78岁男性假性剥脱性青光眼患者,在玻璃体手术中套管针插入后立即发生晶状体自发性后脱位9)。术前未确认晶状体晃动,但术中观察到Zinn小带上纤维状假性剥脱物质沉积和脆弱性。该病例表明,在XFS患者的任何眼内手术中都需要考虑晶状体脱位。
XFS的研究在基因治疗、药物治疗和生物标志物开发领域正在进展。
全基因组关联分析(GWAS)已鉴定出除LOXL1之外的多个易感基因位点。已报道的有CACNA1A、POMP、AGPAT1、RBMS3、SEMA6A等。阐明这些基因产物的功能将加深对病理的理解,并可能成为未来的治疗靶点。血管张力通路的基因多态性与POAG的关联也有报道3)。
目前正在探索调节LOXL1表达的小分子化合物。此外,TGF-β1已被证明可促进XFS中纤维物质的产生,抑制TGF-β信号通路作为治疗策略正在研究中。
房水和血清中假性剥脱物质及相关蛋白的定量可能用于监测疾病活动性。有望应用于发病前诊断和风险分层。
与POAG相比,眼压水平更高,进展倾向更强,预后不良的病例不少。即使早期发现和治疗,视野损害也可能进展。眼压波动大的病例尤其需要注意,早期青光眼试验(EMGT)的分析也证实了假性剥脱性青光眼的快速进展速度7)。早期开始积极治疗很重要。